注射用蜂毒制劑中蜂毒肽和蜂毒明肽的HPLC檢測方法建立及驗證
陳若塵 王麗娜 李麗紅 任鳳芝
摘要:目的:對注射用蜂毒制劑中蜂毒肽及蜂毒明肽的含量HPLC檢測方法的建立及驗證。方法:采用高效液相色譜法,以C8色譜柱,進行不同液相條件洗脫檢測,確定方法后進行方法學研究。結果:建立了適宜的HPLC檢測方法,并完成了方法驗證。結論:本研究結果確定了注射用蜂毒制劑中蜂毒肽及蜂毒明肽的含量HPLC檢測方法。
關鍵詞:蜂毒肽;蜂毒明肽;HPLC檢測方法
Abstract: Objective:To establish and verify an HPLC method for the determination of melittin andapamin in bee venom preparations for injection. Methods:High Performance Liquid Chromatography with C8 column was used for elution detection under different liquid conditions. After the method was determined, the methodology was studied. Results: A suitable HPLC method was established and verified. Conclusion:The results of this study determined the HPLC method for the determination of melittin andapamin in bee venom preparations for injection.
Key words: Melittin; Apamin; HPLC method
【中圖分類號】R97 ? ? ? ? ? ? 【文獻標識碼】A ? ? ? ? ? ? 【文章編號】2107-2306(2021)07--02
蜜蜂毒是蜜蜂科昆蟲中華蜜蜂或意大利蜜蜂尾部蟄刺腺內的有毒液體,性味辛苦,平,功效祛風濕,止疼痛。主治風濕性關節炎,腰肌酸痛,坐骨神經痛[1]。蜜蜂毒中含有多種不同化學結構的生物活性物質,主要有:蜂毒素(Melittin),蜂毒明肽(apamin),MCD-肽(mast cell degranulating peptide),心臟肽(cardiopeptide),含組胺肽(histapeptide),賽卡平(secapin),托肽平(tertiapin)、阿度拉平(adolapin)等,此外還含有組胺,磷脂酶 A2及透明質酸酶等[2]。
以 HPLC 法測定提取物中蜂毒素的含量,方法準確、簡便、重現性好、靈敏度高,可為蜂毒素產品質量標準制定提供可靠的依據,因此建立了注射用蜂毒制劑中蜂毒肽、蜂毒明肽含量測定的方法。注射用蜂毒一般使用指紋圖譜方法進行質量研究,使用該方法用于定量測定時,蜂毒肽及蜂毒明肽與其周圍雜質分離較差,故需重新確定檢測方法。液相方法檢測注射用蜂毒時,噪音較大,使得蜂毒肽及蜂毒明肽的定量限較高,因此需要提高樣品溶液的濃度進行檢測。
1、儀器及試劑
2、HPLC分析方法的確定
通過查閱相關文獻[3],現有HPLC方法確定為:照高效液相色譜法(中國藥典2015年版四部通則0512)試驗,色譜柱為Zorbax 300 SB C8(250mm×4.6mm,5μm);柱溫35℃;以0.1%三氟乙酸(TFA)水溶液為流動相A,以乙腈為流動相B;流速為每分鐘1mL;按下表進行梯度洗脫;檢測波長為220nm;進樣量10μl。,梯度程序如下:
2.1三氟乙酸(TFA)用量
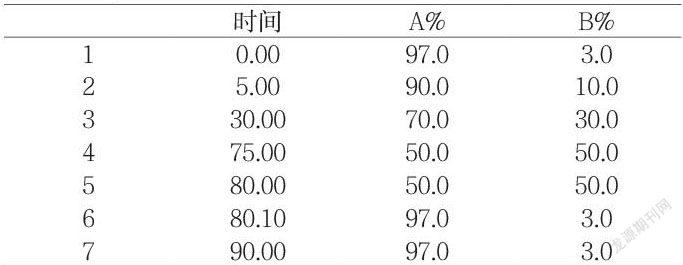
在現有方法的基礎上修改流動相中TFA的比例,分別以0.05%、0.10%、0.15%、0.20%的TFA水溶液作為流動相A,以乙腈為流動相B,注射用蜂毒樣品進行HPLC檢測。結果如圖所示:
結果表明,0.20%的TFA水溶液作為流動相A進行液相分離的效果最好。
2.2梯度的選擇:
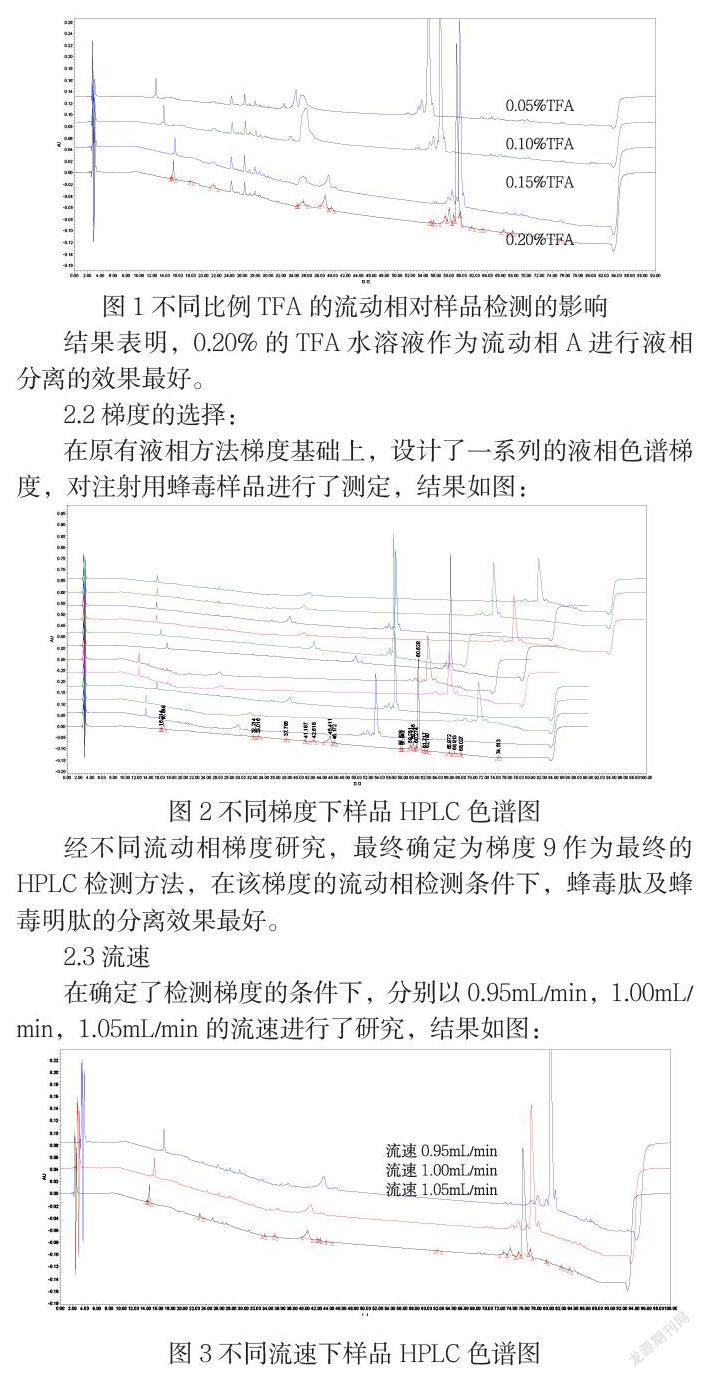
在原有液相方法梯度基礎上,設計了一系列的液相色譜梯度,對注射用蜂毒樣品進行了測定,結果如圖:
經不同流動相梯度研究,最終確定為梯度9作為最終的HPLC檢測方法,在該梯度的流動相檢測條件下,蜂毒肽及蜂毒明肽的分離效果最好。
2.3流速
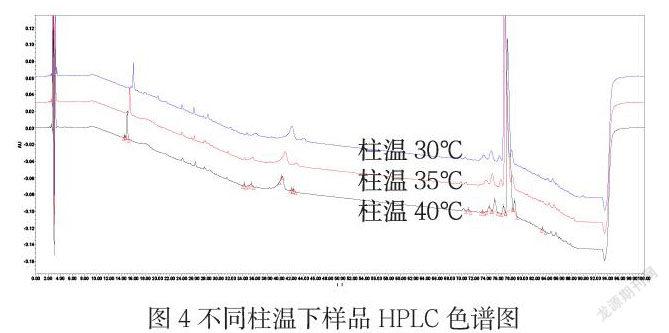
在確定了檢測梯度的條件下,分別以0.95mL/min,1.00mL/min,1.05mL/min的流速進行了研究,結果如圖:
2.4柱溫
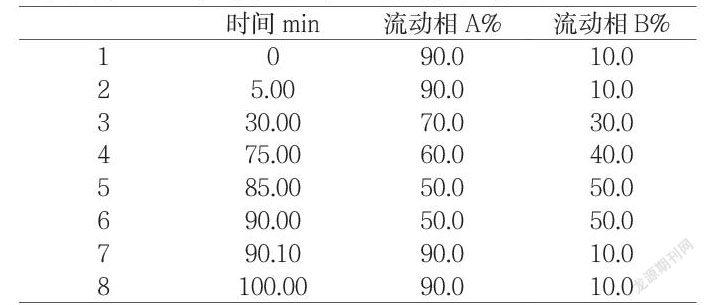
分別將柱溫設置為30℃、35℃、40℃,進行了測定,結果如圖:
2.5樣品濃度選擇
在該檢測方法檢測注射用蜂毒中蜂毒肽及蜂毒明肽的含量時,蜂毒肽計算較為準確,但蜂毒明肽靈敏度較低,故提高了樣品的配置濃度,最終確定了樣品的溶解濃度為5mg/mL,用以測定蜂毒明肽的含量,再稀釋之約為1mg/mL的濃度,用以測定蜂毒肽的含量。其對應的對照品濃度為0.2mg/mL的蜂毒明肽對照品和1.0mg/mL的蜂毒肽對照品。
2.6結果
最終確定了注射用蜂毒中蜂毒肽及蜂毒明肽的HPLC測定含量的方法為:
照高效液相色譜法(中國藥典2015年版四部通則0512)試驗,色譜柱為Zorbax 300 SB C8(250mm×4.6mm,5μm);柱溫35℃;以0.2%三氟乙酸(TFA)水溶液為流動相A,以乙腈為流動相B;流速為每分鐘1mL;按下表進行梯度洗脫;檢測波長為220nm;進樣量20μl。,梯度程序如下:
3、HPLC檢測方法的方法學驗證。
參考《中國藥典》2020版,9101 分析方法驗證指導原則,驗證的指標有:專屬性、準確度、精密度(包括重復性、中間精密度)、檢測限、定量限、線性、范圍和耐用性。
3.1專屬性:
溶劑空白:水。
輔料空白:按照配方,稱取KH2PO4、甘露醇、NaOH配置成濃度分別為13.6mg/mL 、20mg/mL、1.2mg/mL的水溶液。
對照品溶液:稱取蜂毒明肽對照品和取蜂毒肽對照品配置成濃度分為0.04mg/mL和1mg/mL的水溶液。
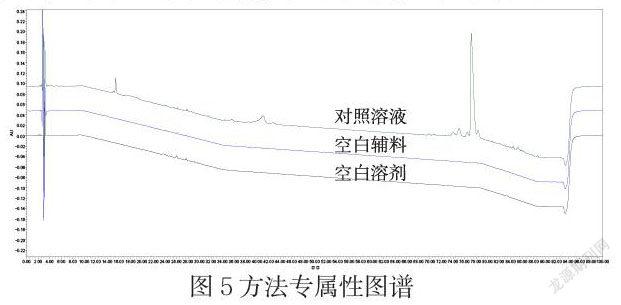
按上述方法進行試驗,分別取溶劑空白、輔料空白、樣品,進樣20μL,注入液相色譜儀,記錄色譜圖,結果如圖:
空白溶液及輔料不干擾注射用蜂毒樣品的測定;3min之前的峰為溶劑峰,80min之后為梯度交換峰,本方法具有較好的專屬性。
3.2準確度
精密稱取蜂毒肽及蜂毒明肽對照品適量,按比例加入空白輔料,用水解并定量稀釋制成80%、100%、120%濃度的溶液各三份,進HPLC檢測,結果在80%到120%濃度范圍內,蜂毒肽回收率在98.85%到 101.3%之間,RSD%為0.87%;蜂毒明肽回收率則在98.39%到 101.3%之間,RSD%為0.98%。表明該液相方法的準確度符合要求。
3.3精密度
用DMG0201批注射用蜂毒平行配制樣品6份,測定該方法的重復性,結果表明,連續測定六次該批次樣品,結果蜂毒肽及蜂毒明肽含量的RSD%分別為0.28%,0.30%。
另更換實驗人員、日期及儀器,重新測定其中間精密度,結果綜合兩次共12次測定數據,蜂毒肽及蜂毒明肽含量的RSD%分別為1.24%,1.25%。
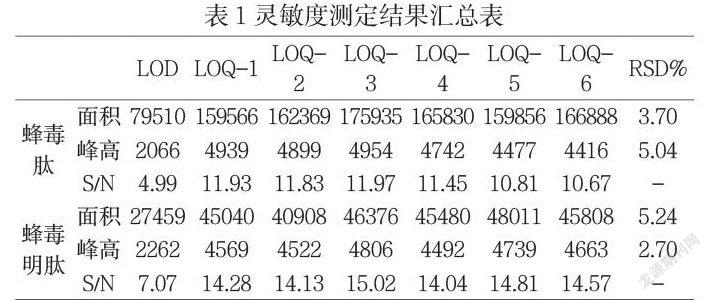
3.4檢測限、定量限
分別精密稱取蜂毒肽和蜂毒明肽對照品適量,用水溶解并定量稀釋制成10μg/mL的溶液作為LOQ溶液,在定量稀釋至5μg/mL作為LOD溶液,進HPLC檢測。另取純水,進HPLC檢測,作為空白噪音,結果見下表:
3.5線性及范圍
精密稱取蜂毒肽對照品適量,用水溶解并定量稀釋制成一系列濃度(100、200、500、800、1000、1200、2000μg/mL)的溶液,進HPLC檢測,以質量濃度(c)為橫坐標,峰面積(A)為縱坐標,進行線性擬合,線性方程為A=12563c-4429,R2=0.9997。
另精密稱取蜂毒明肽對照品適量,用水溶解并定量稀釋制成一系列濃度(50、125、200、250、300、375、500μg/mL)的溶液,進HPLC檢測,以質量濃度(c)為橫坐標,峰面積(A)為縱坐標,進行線性擬合,線性方程為A=6875c-9189,R2=0.9999。
3.6穩定性
精密稱取蜂毒肽及蜂毒明肽對照品適量,用水溶解并定量稀釋制成1mg/mL及25μg/mL的溶液,每隔一段時間,取20μL進HPLC檢測。結果在24h內,蜂毒肽RD%相對0h峰面積不超過0.97%,蜂毒明肽相對0h峰面積RD%不超過1.89%,說明二者在24h內均保持穩定。
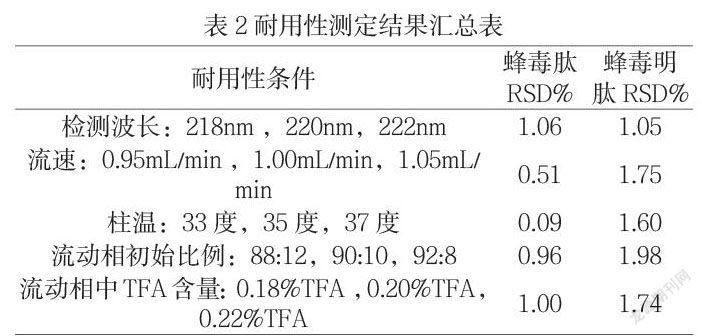
3.7耐用性
耐用性試驗分別測定了HPLC參數(檢測波長、流速、柱溫、流動相初始比例、流動相A中三氟乙酸的量)微小變化時,該方法的耐用性。
調整HPLC參數,于不同條件下對注射用蜂毒樣品進行檢測,結果當波長。
HPLC參數發生改變時,測定同一批次的樣品,其蜂毒肽與蜂毒明肽RSD%均不大于2.0%。
4、注射用蜂毒樣品檢測
取注射用蜂毒三個批號產品DMG0201、EMG0202、FMG0203,用建立的HPLC檢測方法對其進行定量測定,結果三批樣品中蜂毒肽相對標示量分別為81.03%,75.01%,81.77%;蜂毒明肽相對標示量分別為3.77%,3.42%,3.57%。
結論:實驗以原有指紋圖譜檢測方法為基礎,重新優化建立了用以定量檢測注射用蜂毒中蜂毒肽和蜂毒明肽含量的HPLC檢測方法。本方法以注射用蜂毒為研究樣品,從樣品整體性質的角度進行分離分析,方法學驗證表明,本方法專屬性強,重復性、耐用性良好,可以用于控制注射用蜂毒工藝與質量。
參考文獻:
[1] ?F.奧斯伯,R.布倫特,R.E.金斯頓,等精編分子生物學實驗指南[M]. ?科學出版社 1998, 338.
[2] ?汪家政,范明. ?蛋白質技術手冊[M]. ?科學出版社 2000, 257.
[3] ?孟迂 我國產意大利蜂蜂毒多肽的分離純化、結構鑒定、活性測定以及固相合成研究 ?博士學位論文,北京協和醫學院研究生院.

