銀杏酮酯通過抑制鈉、鈣通道和自發性鈣波防治心律失常
劉 備,張光永,劉愛華,張志雄,王星禹
(上海中醫藥大學基礎醫學院生理教研室,上海 201203)
心律失常是許多心血管疾病常見癥狀,易造成循環系統障礙如心輸出量下降,動脈血壓降低,暈厥,甚至導致心源性猝死[1]。心律失常由沖動發生異常和傳導異常引起,沖動發生異常包括異位節律和后除極引起的觸發活動(triggered activity,TA)。后除極一旦除極至閾電位水平就觸發動作電位導致心律失常。延遲后除極(delayed after depolarization,DAD)是在心肌細胞動作電位4期復極結束后發生的短暫性、并呈現振蕩性的除極電活動,又稱晚期后除極。DAD通常發生在肌漿網Ca2+濃度異常升高,亦即所謂鈣超載時[2]。此時細胞內的Ca2+濃度升高,激活非選擇性陽離子通道如鈣通道、鈉通道,促進Ca2+、Na+內流或Na+/Ca2+交換電流,形成內向電流,導致DAD,引發心律失常。
近年來由于激光共聚焦顯微鏡和鈣熒光染料的普及,研究人員發現自發性鈣波(spontaneous Ca2+wave,SCaW)能觸發各種心律失常,鈣波是指心肌細胞內Ca2+濃度增高、胞內Ca2+在局部的自發性釋放增加并發生傳導的現象[3]。SCaW激活Na+/Ca2+交換電流(INa/Ca)內向電流,引起DAD,可能導致心律不齊[4]。
銀杏酮酯(ginkgo biloba extract 50,GBE50)是我國獨立研發的新型銀杏葉提取物制劑,其銀杏內酯含量>0.06,銀杏總黃酮含量>0.44,總黃酮醇苷>0.24,毒性成分銀杏酸含量則控制在5 μg·g-1以下。有研究報道在整體水平GBE50具有抗烏頭堿、哇巴因引起的大鼠心律失常的作用[5];另離體心臟灌流實驗也顯示GBE50能夠降低缺血/再灌注導致的室顫的發生率,部分縮短室顫的持續時間[6]。GBE50抗心律失常作用可能是通過抑制異常的電活動(DAD和TA)實現的[5],但其作用機制尚有待進一步闡明。本研究利用膜片鉗技術研究GBE50對烏頭堿誘發的心室肌細胞異常鈉電流(INa)和L型鈣電流(ICa,L)的影響,通過激光共聚焦鈣離子成像技術觀察GBE50對缺血/再灌注誘導的心室肌細胞自發性鈣波的作用,探討其抗心律失常的作用機制。
1 材料與方法
1.1 材料
1.1.1實驗動物 清潔級SD雄性大鼠,體質量(225±25)g,由上海中科院斯萊克實驗動物有限公司提供,動物合格證號:SCXK(滬)012-0002。經上海中醫藥大學實驗動物福利與倫理委員會審查,實驗符合實驗動物福利及倫理相關規范,倫理編號:PZSHUTCM190614008。
1.1.2藥品與試劑 Taurine、HEPES、Tetraethylammonium Chloride(TEA-Cl)、MgATP、EGTA、Tris-GTP、2,3-丁二酮一肟(BDM)、Na2-ATP、蛋白酶、烏頭堿等試劑購自Sigma公司。Fluo-4-AM購自東仁化學科技有限公司。Ⅱ型膠原酶(Collagenase,Type 2)購自Worthington 公司。Laminin購自賽默飛世爾科技(中國)有限公司。銀杏酮酯(GBE50)由上海杏靈制藥有限公司提供,批號為:111002。其他試劑均為滬試的分析純。
1.1.3儀器 IX-70倒置顯微鏡(日本奧林巴斯光學公司);MultiClamp 700B膜片鉗放大器(美國Molecular Devices公司);LGF-1B Langendorff 心臟灌流裝置(成都儀器廠);TCS SP8激光共聚焦成像系統(德國Leica 公司);P-97微電極拉制儀(美國Sutter公司);SEN-3201電子刺激器(日本NIHON KOHDEN 公司);PB-10 PH計(德國賽多利斯公司)。
1.1.4溶液配制 Krebs-Henseleit(K-H)改良液配方為(mmol·L-1):NaCl 118.0,KCl 4.7,CaCl21.25,KH2PO41.2,MgSO41.2,NaHCO325.0,Glucose 11.0。無鈣緩沖液(mmol·L-1):NaCl 120,KCl 5.4,NaH2PO41.2,NaHCO320,MgSO41.2,Glucose 5.6,BDM 10,Taurine 5,用稀鹽酸將pH調至7.4。在無鈣緩沖液中加入10% FBS和12.5 mmol·L-1CaCl2得到停止酶解液。缺血液(mmol·L-1):NaCl 118.0,KCl 4.7,CaCl21.25,MgSO41.2,KH2PO41.2,NaHCO325,2-Deoxy-D-glucose 10,Na2S2O410[7]。KB液(mmol·L-1):K glutamate 100,KCl 25,MgSO42,KH2PO42,Taurine 20,Creatine base 5,EGTA 0.5,HEPES 5,Glucose 20,加KOH校正pH值至7.4。記錄ICa,L外液(mmol·L-1):NaCl 140,CsCl 10,CaCl21,MgCl21,glucose 10,HEPES 10(加NaOH校正pH值至7.4)。記錄ICa,L電極內液(mmol·L-1):CsCl 130,TEA-Cl 20,MgATP 5,EGTA 5,Tris-GTP 0.1,HEPES 5(用CsOH將pH值調至7.2)。記錄INa外液(mmol·L-1):choline chloride 120,NaCl 25,CsCl 4,CaCl20.1,CoCl22,MgCl21,HEPES 10,Glucose 10(用CsOH將pH值調至7.4)。記錄INa電極內液(mmol·L-1):CsCl 140,NaCl 10,EGTA 5,Na2-ATP 5,HEPES 5(用CsOH將pH值調至7.3)。GBE50母液配制:1.25 g GBE50加入10 mL丙二醇,加熱溶解,然后加超純水至500 mL攪拌溶解,用孔徑為0.22 μm的混合纖維素脂膜過濾置于4 ℃冷藏室待用。
1.2 方法
1.2.1細胞分離 通過酶解法獲得單個大鼠心室肌細胞。腹腔注射20%烏拉坦5 mL·kg-1麻醉大鼠后,迅速開胸取出心臟,在冰冷的K-H緩沖液中洗去余血,迅速將心臟連于Langendorff灌流裝置上,通過主動脈進行逆向灌流。灌流液用 95% O2+5% CO2混合氣飽和,溫度恒定于37 ℃。先用K-H緩沖液灌流15 min,灌流速度為9 mL·min-1;然后以5 mL·min-1的速度改用無鈣緩沖液灌流10 min;再改用含0.05% II型膠原酶、0.01% 蛋白酶、0.1% BSA的無鈣緩沖液灌流2 min,最后無鈣緩沖液加入CaCl2(50 mmol·L-1)對心臟進行循環灌流至全心松軟,取下心臟,剪下心室并剪碎心肌組織,置于搖床中振蕩溫孵5 min進一步酶解,然后加入5 mL的停止酶解液振蕩溫孵5 min,可得到50%-60%桿狀、表面橫紋呈搓衣板狀且邊緣清晰的耐鈣細胞,沉淀后用停止酶解液換去上清兩次,然后用KB液孵育室溫保存待用。
1.2.2膜片鉗技術記錄心肌細胞膜通道電流 所用微電極用玻璃毛細管置于玻璃微電極拉制儀拉制而成,沖灌電極內液后,其尖端電阻值為2.5-5 MΩ。吸取上述分離好的細胞滴放入顯微工作臺上細胞浴槽中,然后用微量恒流泵以1.5 mL·min-1的速度對細胞進行灌流。并選擇形態完整、橫紋清晰、表面干凈規則、無收縮的細胞置于視野下作為實驗對象。打開膜片鉗實驗軟件Clampex 10.3,對細胞進行封接,破膜,將串聯電阻補償到80%以上。選擇設定好的Clampex采樣軟件的Protocol,細胞膜電流信號通過膜片鉗放大器放大后通過軟件進行記錄。并觀察1 μmol·L-1烏頭堿灌流5 min后[8],各組細胞INa、ICa,L電流的變化。其中INa電流記錄方案為:膜電位鉗制于-100 mV,指令電壓以5 mV為步階,脈沖持續時間為100 ms,從-80 mV躍至 +25 mV。ICa,L電流記錄方案為:膜電位鉗制于-40 mV以失活T型鈣通道和鈉通道,以10 mV為步階,脈沖持續時間為200 ms,從-50 mV躍至+25 mV,每個指令電壓之前有個50 ms的-50 mV 的預脈沖。
1.2.3電刺激誘導鈣波 分離好的單個細胞滴加于laminin孵育過的培養皿,棄掉上清液,再用含5 μmol·L-1Fluo-4-AM染料的K-H液孵育15 min。將培養皿固定于激光共聚焦系統的細胞槽中,使用Ar激光在488 nm處激發染料,并檢測到波長大于510 nm的熒光發射。正常組對照組(Control組):K-H液灌流10 min以洗脫染料,開始電刺激10 s(電壓10 mV,頻率1 Hz或3 Hz),同時選擇xt掃描方式[9]進行線掃(掃描分辨率為:512×1像素,每次線掃時長為1.43 ms),待電刺激結束后繼續線掃記錄1 min,以觀察記錄鈣波發生情況。缺血/再灌注組(IR組)或加藥組(IR+GBE50組):先用K-H液或加藥K-H液灌流10 min以洗脫染料,改用缺血液或加藥缺血液灌流4 min,再用K-H液或加藥K-H液再灌流3 min,然后開始電刺激10 s,同時進行線掃,待電刺激結束后繼續線掃記錄1 min,以觀察記錄鈣波發生情況。
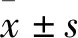
2 結果
2.1 GBE50對烏頭堿灌流的心肌細胞INa電流的作用烏頭堿(1 μmol·L-1)使心肌細胞INa最大電流密度從(-25.94±2.10)pA/pF增至(-37.21±4.23)pA/pF(P<0.05),使INa激活曲線左移,半激活電壓從(-44.07±0.92)mV變為(-49.52±0.81)mV(P<0.01);而25 mg·L-1GBE50使該模型的INa最大電流密度減小至(-27.11±2.18)pA/pF(P<0.05),激活曲線右移,半激活電壓改變為(-46.33±1.19)mV(P<0.05,Fig 1)。
2.2 GBE50對烏頭堿灌流的心肌細胞ICa,L電流的作用使用L型鈣通道特異性阻斷劑Nifedipine(10 μmol·L-1)能明顯阻斷記錄到的電流,證明記錄到的正是ICa,L電流(Fig 2A)。
烏頭堿(1 μmol·L-1)使心肌細胞ICa,L最大電流密度從(-3.79±0.27)pA/pF增至(-5.01±0.26)pA/pF(P<0.01),使ICa,L激活曲線左移,半激活電壓從(-16.22 ± 0.81)mV變為(-23.67±0.85)mV(P<0.01);而25 mg·L-1GBE50使該模型的ICa,L最大電流密度減小至(-3.81± 0.24)pA/pF(P<0.01),激活曲線右移,半激活電壓改變為(-20.84±0.82 mV)(P<0.05,Fig 2B-H)。
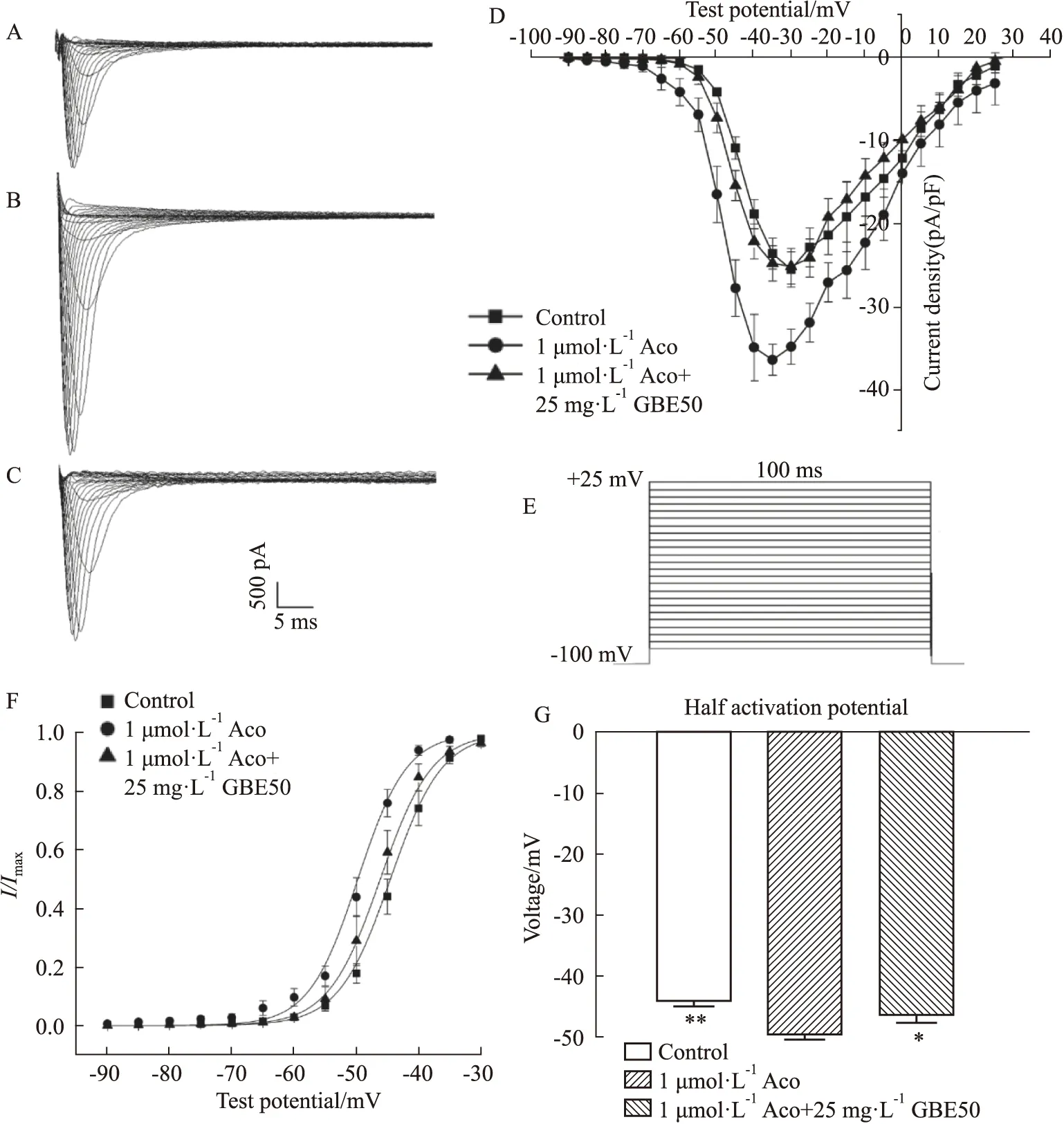
Fig 1 GBE50 inhibited aconitine-induced increase in sodium current in rat ventricular cells n=12-14)A:INa recorded for the control;B:INa recorded in the Aco group;C:INa recorded in Aco+GBE50 group;D:Current density-voltage curves for INa in different groups;E:Recording protocol of INa;F:INa Steady-state activation curves;G:Half activation potential of different groups;.Aco:aconitine;*P<0.05,**P<0.01 vs Aco group
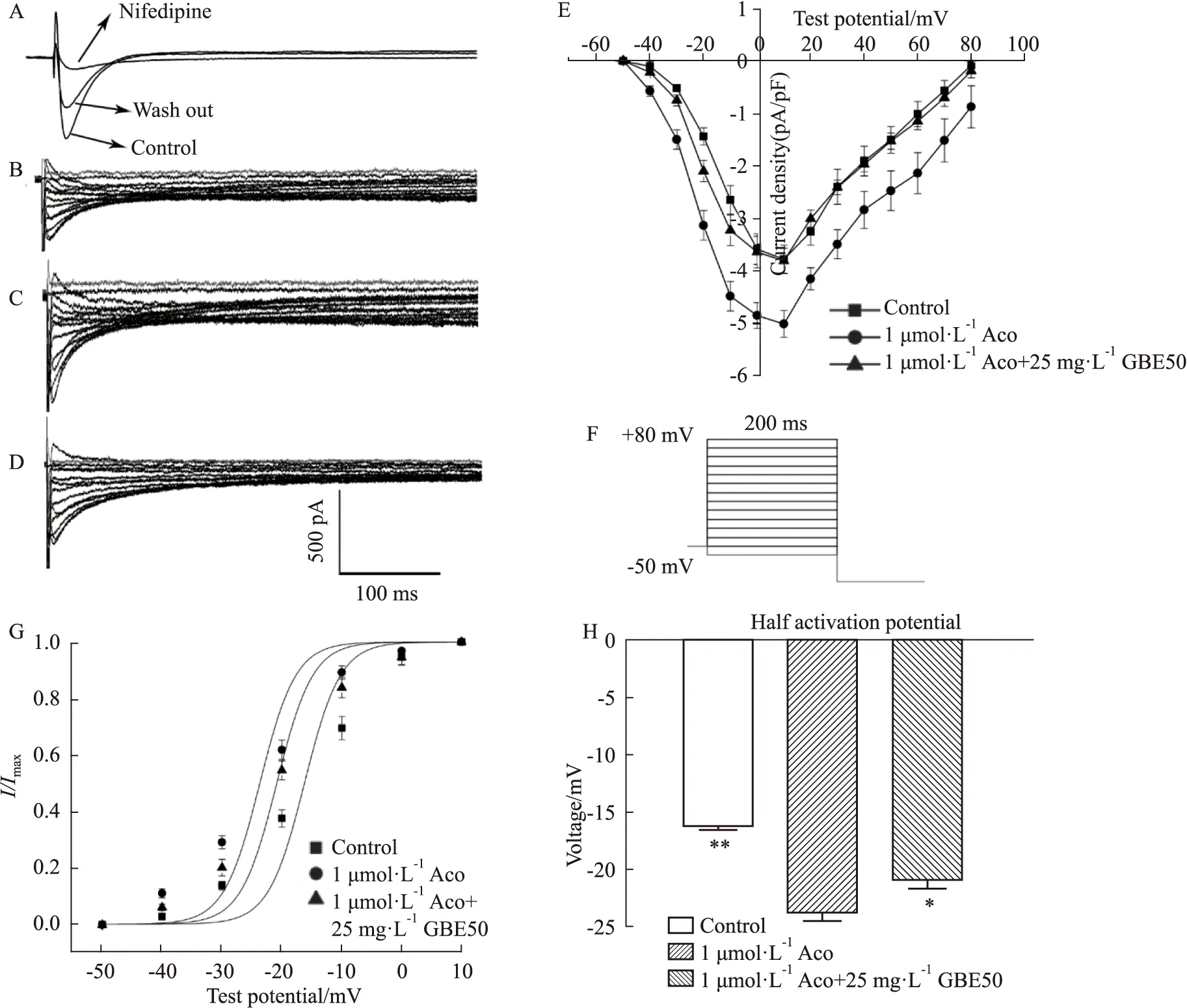
Fig 2 GBE50 inhibited aconitine-induced increase in calcium current in rat ventricular cells n=8)A:Nifedipine block of ICa,L;B:ICa,L recorded for the control;C:ICa,L recorded in the Aco group;D:ICa,L recorded in Aco+GBE50 group;E:Current density-voltage curves for ICa,L in different groups;F:Recording protocol of ICa,L;G:ICa,L Steady-state activation curves;H:Half activation potential of different groups;Aco:aconitine;*P<0.05,**P<0.01 vs Aco group
2.3 GBE50對缺血/再灌注心肌細胞的自發性鈣波的影響使用1 Hz頻率刺激大鼠缺血/再灌注心肌細胞10 s誘導產生自發性鈣波,IR組鈣波的發生率明顯高于Control組,由12.50%上升至81.25%(P<0.01);25 mg·L-1GBE50未引起正常心肌細胞鈣波的發生,可降低IR組的鈣波發生,將鈣波發生率降低至26.67%(P<0.01,Fig 3A,C)。
使用3 Hz頻率刺激大鼠缺血/再灌注心肌細胞10 s誘導產生自發性鈣波,IR組鈣波的發生率明顯高于Control組,由20.00%上升至90.00%(P<0.01);25 mg·L-1GBE50可降低IR組的鈣波發生,將鈣波發生率降低至30.00%(P<0.01,Fig 3B,D)。
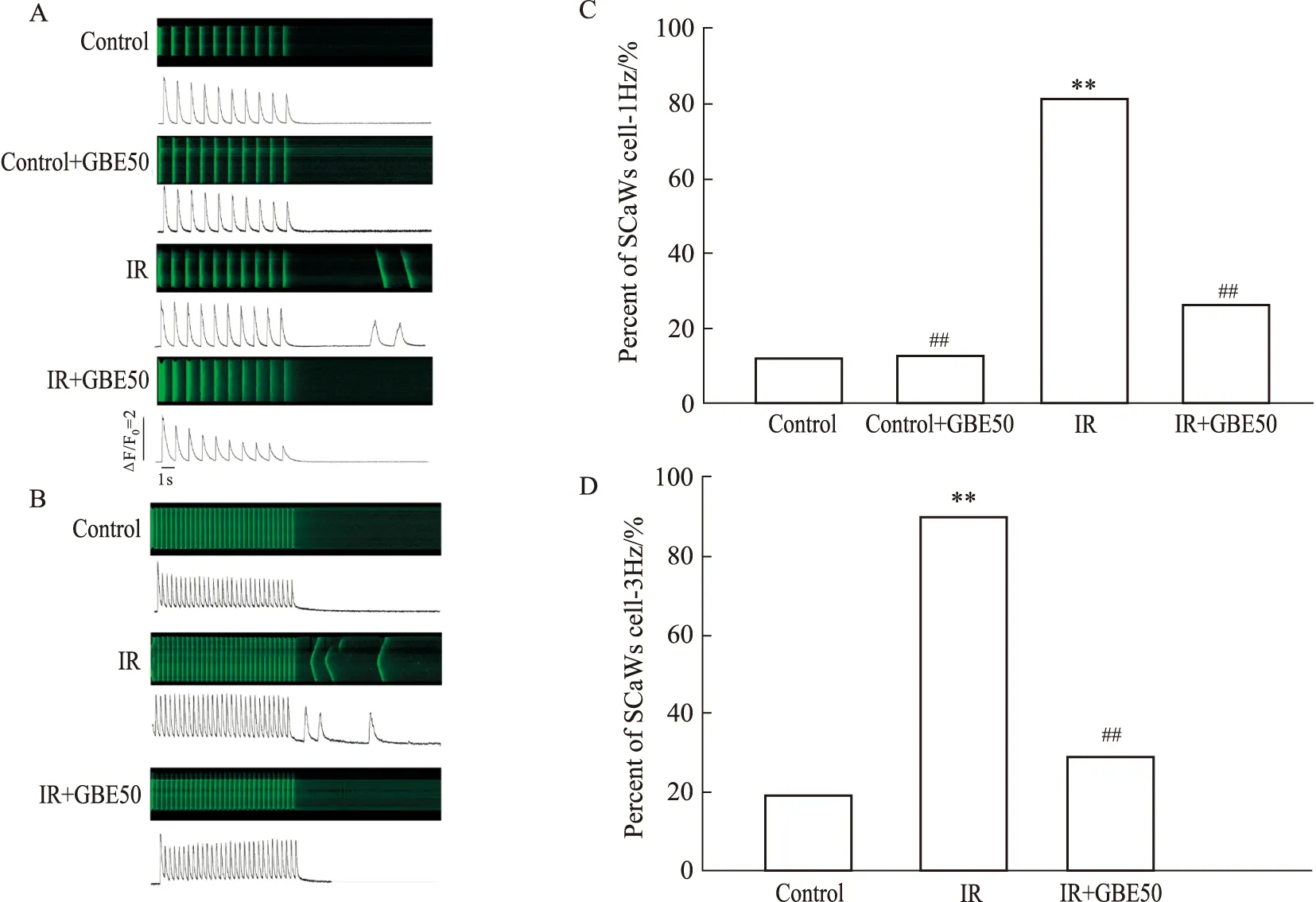
Fig 3 25 mg·L-1 GBE50 inhibited increase of SCaWs during ischemia-reperfusion in rat ventricular myocytes (n=10-15)A:SCaWs was induced by applying depolarizing pulses at 1 Hz;B:SCaWs was induced by applying depolarizing pulses at 3 Hz;C:Percent of cells with SCaWs at 1 Hz (n=15);D:Percent of cells with SCaWs at 3 Hz (n=10);**P<0.05 vs Control group,##P<0.01 vs IR group
3 討論
烏頭堿可導致整體或細胞水平的“心律失常”,已被廣泛用作誘導各種心律失常模型、篩選抗心律失常藥物的工具藥[10]。有文獻報道烏頭堿能夠延長心肌細胞鈉通道的開放,促進Na+向細胞中的滲透[8],并可增加ICa,L離子流[11]。烏頭堿誘導的胞內Na+濃度的增加會促進Na+/Ca2+雙向交換[12],和ICa,L促進Ca2+內流可共同導致細胞內鈣超載,從而引起DAD,同時胞內Na+濃度的增加并導致細胞持續的去極化即觸發活動(TA)。上述過程構成了烏頭堿的致心律失常作用的電生理基礎。本文對INa和ICa,L進行激活動力學分析,發現烏頭堿使INa和ICa,L激活曲線左移,半激活電壓絕對值增加,說明烏頭堿灌流心肌細胞后INa和ICa,L內向電流被激活增強。而25 mg·L-1GBE50使該模型的INa和ICa,L最大電流密度減小,激活曲線右移,半激活電壓減小,提示GBE50明顯抑制烏頭堿激活的INa和ICa,L,可能是GBE50抑制異常的電活動(DAD和TA)抗心律失常的機制。
臨床上大多數的抗心律失常藥物都是通過改變心肌細胞動作電位不同時期的離子通道開放狀態和離子流而發生作用的。近年來發現抗心律失常藥物本身有時也會引起心律失常,如Ιa類藥物中度阻斷鈉通道,使Q-T間期延長,可引起致死性的尖端扭轉性室速的發生。鑒于單通道抗心律失常藥物具有致心律失常的不良反應,有學者提出最佳靶點學說:細胞膜上的鈉、鉀、鈣離子通道與心律失常發生、發展密切相關,一個理想的抗心律失常藥物會對其中的至少兩個通道起作用[13]。理想的抗心律失常藥物應該作用于多通道靶標和非離子通道靶標[14]。1 Hz電刺激下GBE50未能引起正常心肌細胞自發性鈣波的發生,說明GBE50的抗心律失常作用是安全的。GBE50對心肌非選擇性陽離子通道如鈉、鈣離子通道均有作用,抑制鈣超載治療心律失常,致心律失常的風險降低,符合“最佳靶點學說”的要求。
缺血/再灌注后由于鈣釋放和回攝通道的異常作用,導致細胞內鈣循環的紊亂,表現為胞質內鈣超載從而促進肌漿網鈣超載,產生肌漿網的鈣泄漏引起舒張期自發性鈣釋放即鈣波,可誘導DAD的活動,從而引發再灌注性心律失常[15]。我們之前有發現模擬缺血能誘發心室肌細胞內游離鈣濃度增加,GBE50可減輕缺血后鈣超載[16]。本文采用含有2-脫氧-D-葡萄糖和連二亞硫酸鈉的無糖K-H液[7]模擬缺血灌流心室肌細胞4 min,再用K-H液復灌3 min,制備模擬缺血/再灌注模型,觀察自發性鈣波產生。結果發現1 Hz和3 Hz電刺激心室肌細胞尚能發生收縮和鈣瞬變,停止刺激后能觀察到Ca2+在局部的自發性釋放增加并伴傳導即自發性鈣波的發生。GBE50可抑制缺血/再灌注心肌細胞自發性鈣波的發生,提示GBE50可能通過抑制心肌缺血導致的鈣超載,減少肌漿網的鈣泄漏,阻止DAD的發生從而減輕再灌注性心律失常。
自發性鈣波產生的機制尚不清楚,在數學模型中它們的出現與肌漿網的蘭尼堿受體(ryanodine receptors,RyRs)的活性有關[3]。肌漿網鈣釋放有兩條不同的機制:一是通過由L型鈣通道和RyRs共定位形成的所謂鈣釋放單位,也就是經典的鈣誘導的鈣釋放途徑[17]。另一種不依賴于L型鈣通道和RyRs的耦聯,由隨機開放的一個或幾個RyRs引起鈣的釋放。上述兩種情況下局部的鈣釋放都可以通過鈣敏感探針將胞內Ca2+可視化而記錄到鈣火花(Ca2+sparks)。GBE50對鈣火花即肌漿網的鈣泄漏是否有影響及其機制還亟待探索。

