馬鈴薯品種‘并薯6號’遺傳轉化體系的建立
宋倩娜,梅 超,霍利光,王慧杰,馮瑞云
(山西農業大學農學院/作物遺傳與分子改良山西省重點實驗室,山西 太原 030031)
馬鈴薯(Solanum tuberosum L.)為茄科茄屬一年生同源四倍體草本植株,是中國繼小麥、玉米和水稻后的第四大糧食作物[1]。馬鈴薯營養豐富、適應性強、產量高、生育期短、經濟效益高等特點使其成為重要的糧食作物,也是工業加工各種產品的原料[2]。近年來,隨著糧食問題日益地嚴峻,馬鈴薯產業成為了中國糧食安全戰略中不可或缺的一部分。馬鈴薯的產量、品質是影響中國馬鈴薯產業的最根本問題,只有積極的開展種質資源創新和新品種選育才能逐步解決這些問題[3]。目前馬鈴薯品種改良的主要手段包括傳統育種和植物基因工程育種。
馬鈴薯基因型復雜、自交衰退性等特點導致傳統育種周期長和效率低[4]。而植物基因工程育種手段則可以大大的縮短育種周期、提高育種效率[5,6]。農桿菌介導的遺傳轉化是植物基因工程育種中的必要環節。近幾年來,人們利用此方法將外源優良基因轉入到馬鈴薯內進行抗性及品質的改良并取得了一定的進展[7]。但是,根癌農桿菌介導的馬鈴薯遺傳轉化受到各種因素的影響,如基因型[8-10]、外植體類型[11,12]、培養基成分和培養條件[13]、農桿菌類型及濃度、農桿菌與外植體的共培養時間及農桿菌侵染時間[14]等。雖然許多馬鈴薯品種的遺傳轉化體系已經建立,但是這些體系是相對獨立的,不同的體系適合不同的品種。
馬鈴薯‘并薯6 號’是由山西農業大學農學院(山西省農業科學院作物科學研究所)選育而成的品種,其具有生長勢強、抗病性強、抗旱性強、產量高等優點,但是也存在芽眼較深等缺點。因此,‘并薯6 號’的改良對山西省馬鈴薯產業發展具有重要的意義。本研究以‘并薯6 號’為研究材料,通過對遺傳轉化和再生過程中的外植體培養、植物激素的種類及配比、抑菌劑的種類及濃度和篩選劑的濃度進行研究,建立‘并薯6 號’的農桿菌介導的遺傳轉化及再生體系,為馬鈴薯基因功能的驗證和品質改良提供一定的理論基礎。
1 材料與方法
1.1 試驗材料
1.1.1 植物材料
試驗以馬鈴薯品種‘并薯6 號’的無菌試管苗為材料。無菌試管苗由本研究單位提供,由本課題組植物組織培養間培養并保存。
1.1.2 農桿菌菌株及植物表達載體
農桿菌類型為根癌農桿菌(Agrobacterium tumefaciens),菌株為GV3101。農桿菌中含有的植物表達載體為基因過表達載體pMDC85,此載體上攜帶有潮霉素抗性基因Hyg(圖1),并由本課題組保存。

圖1 pMDC85載體圖Figure 1 pMDC85 vector
1.1.3 培養基及其成分
目前,關于馬鈴薯愈傷組織誘導及再生所用的激素主要包括生長素類(IAA、NAA 和2,4-D)、細胞分裂素類(6-BA 和 ZT)以及 GA3等[15,16]。以已發表的研究報道為基礎,設計了以下的試驗。本試驗所用的基本培養基為MS(Murashige & Skoog Medium),各種培養基的命名以及包含的成分見表1。

表1 培養基成分Table 1 Medium components
1.2 試驗方法及培養條件
1.2.1 無菌試管苗的擴繁
剪取帶有一個或者兩個腋芽的‘并薯6 號’的莖段作為外植體,將其形態學下端插入到MS 固體培養基(4.43 g/L MS 粉末、30 g/L 蔗糖和 7 g/L 瓊脂,pH 5.8),每個350 mL 培養瓶中插入的莖段數為8 個。將培養瓶置于組織培養間內進行培養,培養條件為光照強度2 000 lx,溫度(25 ± 2)℃,光照周期為16 h/8 h(光照/黑暗)。待苗齡為4 周后,按照上述相同的方法和培養條件繼續進行擴繁培養。
1.2.2 農桿菌菌液的制備
挑取含有pMDC85 質粒的GV3101 農桿菌單菌落,接種于含有50 g/L 卡那霉素和50 g/L 利福平的LB 液體培養基中(10 g/L 胰蛋白胨、5 g/L 酵母提取物和5 g/L 氯化鈉,pH 7.4),置于搖床內,28℃,220 r/min,黑暗條件下過夜培養至生長對數期。將培養好的農桿菌菌液于3 000 r/min 離心10 min,棄掉上清液。用MS 液體培養基(4.43 g/L MS 粉末和30 g/L 蔗糖,pH 5.8)重懸農桿菌沉淀物,并稀釋至濃度為OD600=0.6,用于后續外植體的浸染。
1.2.3 外植體的預培養
以生長周期約為4周的無菌苗為對象,剪取不帶有腋芽的、長度約為1 cm的莖段為外植體,置于預培養培養基上進行預培養(表1)。培養條件與上述相同,預培養時間設置為0,1,2,3和4 d。每組預培養試驗的莖段數為20個/培養皿,3次重復。
1.2.4 外植體的浸染及共培養
收集預培養處理后的莖段外植體,將其置于提前準備好的農桿菌菌液中浸泡10 min,在此期間輕柔的搖晃混勻幾次,使外植體與農桿菌菌液充分接觸。浸染結束后,將外植體轉移至多層無菌濾紙上,吸干多余農桿菌菌液。將外植體以平鋪方式接種到共培養培養基上進行共培養(表1),黑暗條件下,28℃共培養2 d。
1.2.5 外植體愈傷組織誘導培養基的篩選
將共培養后的外植體莖段轉移到不同的愈傷組織誘導培養基上。以MS 培養基為基礎培養基,激素組合有6-BA、NAA、2,4-D、KT 和GA3。將不同的激素種類及配比進行組合,共設計了4 種培養基,分別為CIM1、CIM2、CIM3 和CIM4(表2)。每組試驗的莖段數為20 個/培養皿,3 次重復。培養條件同上述的試管苗擴繁,4 周之后統計愈傷組織形成率。愈傷組織形成率(%)=(愈傷組織形成數/外植體總數)×100。確定愈傷組織誘導的最佳培養基配方以CIM 命名。

表2 5種激素配比對愈傷組織誘導影響的試驗(mg/L)Table 2 Tests on ratios of five phytohormones for callus induction
1.2.6 愈傷組織分化培養基的篩選
將上述不同愈傷組織誘導培養基中的莖段再次分別轉移到愈傷組織分化培養基上。以MS 培養基為基礎培養基,激素組合有6-BA、ZT 和GA3。將不同的激素種類及配比進行組合,共設計了2 種培養基,分別為SIM1 和SIM2(表3)。每組試驗的莖段數為20 個/培養皿,3 次重復。培養條件同上述的試管苗擴繁,6 周之后統計出芽率。出芽率(%)=(再生芽數/愈傷組織總數)×100。確定愈傷組織分化的最佳培養基配方以SIM命名。

表3 3種激素配比對愈傷組織分化出芽影響的試驗(mg/L)Table 3 Tests on ratios of three phytohormones for shoot induction
1.2.7 愈傷組織誘導和芽分化抗生素的篩選
將共培養2 d 后的外植體莖段置于愈傷組織誘導培養基上,待愈傷組織形成后轉移至含有不同濃度潮霉素(0,5,10,15,30 和40 mg/L)的SIM1 培養基上誘導愈傷組織,每兩周更換一次培養基直至出芽,每組試驗的莖段數為20 個/培養皿,3 次重復。培養條件同上述的試管苗擴繁,統計出苗率。出苗率(%)=(再生植株數/愈傷組織總數)×100。
1.2.8 生根培養時抗生素濃度的篩選
將未轉化的含有腋芽的馬鈴薯外植體扦插到含有不同濃度潮霉素(0,5,10,15,30 和40 mg/L)的RIM 培養基中進行生根處理,每個培養瓶中放入10 株,3 次重復。培養條件同上述的試管苗擴繁,大約3 周之后統計生根率。生根率(%)=(生根外植體數/外植體總數)×100。
1.2.9 最佳抑菌抗生素種類及濃度的篩選
將共培養2 d 后的外植體莖段置于含有不同抗生素種類及濃度的CIM3 培養基上進行愈傷組織的誘導。抗生素的種類包括頭孢霉素(Cefotaxime,Cef)和特美汀(Timentin, TMT),濃度分別為0,100,200和300 mg/L。每組試驗的莖段數為20個/培養皿,3 次重復。培養條件同上述的試管苗擴繁,15 d后統計觀察抑菌情況及愈傷組織生長狀態。
1.2.10 轉化再生植株的PCR檢測
采用CTAB 法提取再生馬鈴薯植株葉片的基因組DNA。以載體上的序列及基因組上的序列為基 礎 設 計 引 物 序 列 F: 5′-AGGTGGCTCCTACAAATGCCACT-3′;R:5′-GTGTCACTGATGAGAAGCCAAAATGACCTTTC-3′,PCR 擴 增 產 物 的 大小為1 000 bp。PCR 擴增的反應程序為:95℃預變性3 min;95℃變性30 s,60℃退火30 s;72℃延伸30 s,35 個循環;72℃延伸 10 min。PCR 產物用1.2%瓊脂糖凝膠電泳進行檢測。
2 結果與分析
2.1 最佳預培養時間的確定
為了探究‘并薯6 號’的最佳預培養時間,共設置了5 個預培養的時間梯度,分別為0,1,2,3 和 4 d。用 OD 值為 0.6 的農桿菌菌液浸染 10 min,共培養2 d 后置于愈傷組織誘導培養基上,培養5周后觀察愈傷組織的生長狀態,并統計愈傷組織形成率。然后將上述的愈傷組織轉移到愈傷組織分化培養基上,大約7 周后統計出苗率及轉化頻率。結果表明,不同預培養時間對外植體形成愈傷組織存在一定的差異。未經過預培養的外植體易發生白化或褐化最后死亡的現象,很難形成愈傷組織。經過預培養后的外植體都可以形成愈傷組織。其中預培養2 d 外植體的愈傷組織形成率、出苗率及轉化頻率均最高,預培養3 和2 d 外植體的愈傷組織形成率和出苗率差異不大,轉化頻率次之。而預培養1 和4 d 外植體的愈傷組織形成率、出苗率及轉化頻率較低(表4)。因此,最佳的預培養時間為2 d。
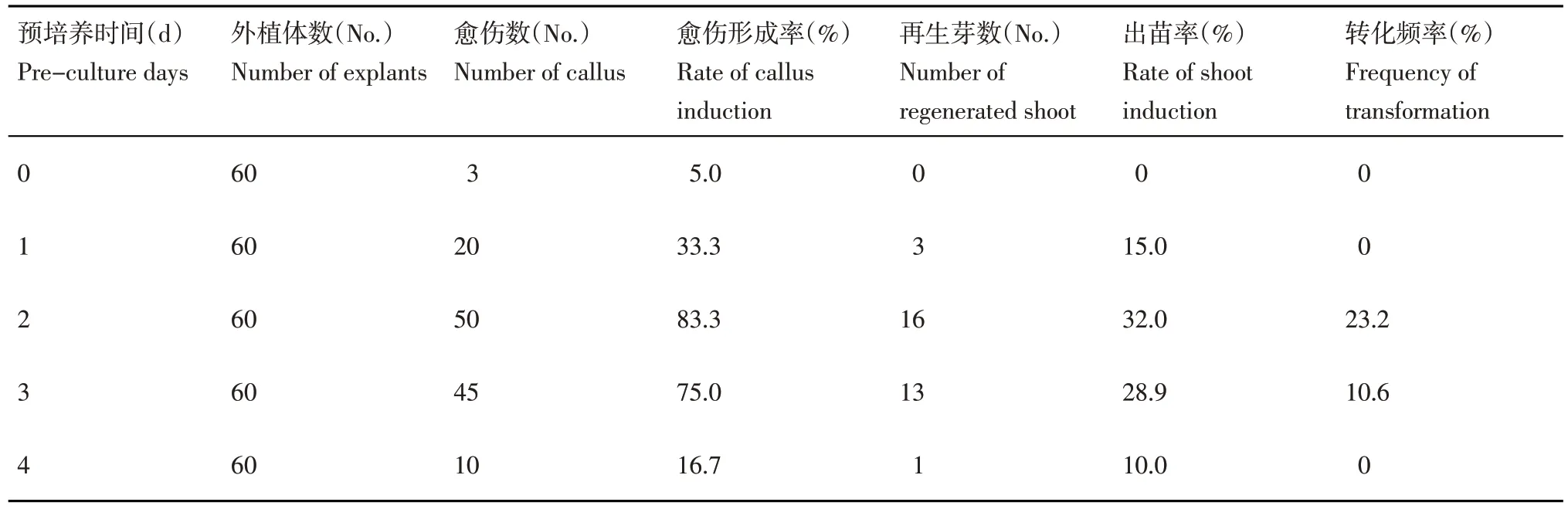
表4 預培養時間對愈傷組織形成和分化的影響Table 4 Effects of pre-culture time on callus induction and differentiation
2.2 不同激素種類及配比對外植體愈傷組織形成的影響
將外植體預培養2 d 后,用OD 值為0.6 的農桿菌菌液浸染10 min,共培養2 d 后置于愈傷組織誘導培養基CIM1、CIM2、CIM3 和CIM4 上,培養5 周后,觀察愈傷組織的狀態并統計愈傷組織形成率(表5)。結果表明,CIM3 的愈傷組織形成率最高,外植體傷口處膨大形成白色的愈傷組織,且形態較緊密;外植體表面幾乎沒有白色須狀物和毛狀根。CIM4 的愈傷組織形成率次之,多數外植體傷口處膨大形成白色的愈傷組織,外植體表面幾乎沒有白色須狀物和毛狀根。CIM1 和CIM2的愈傷組織形成率較低。CIM1 的一些外植體傷口處膨大形成愈傷組織,且表面白色須狀物和毛狀根較多。CIM2 的外植體傷口處膨大,且表面的白色須狀物較多(圖2)。

表5 不同激素種類及配比對莖段愈傷組織誘導的影響Table 5 Effects of different hormones and ratios on callus induction

圖2 在不同類型培養基上外植體愈傷組織誘導及分化的過程Figure 2 Callus induction and differentiation processes of explants on different media
2.3 不同激素種類及配比對愈傷組織分化的影響
將上述處于 CIM1、CIM2、CIM3 和 CIM4 培養基上的愈傷組織分別平移于愈傷組織分化培養基SIM1 和SMI2 上,愈傷組織的體積逐漸的增大。培養3 周后,愈傷組織的底部可見綠色芽點的分化。待培養時間達到7 周后,在愈傷組織的芽點處分化出帶有葉子的芽并從底部延伸出來。不同激素種類及配比對愈傷組織的分化具有一定的影響(表6)。與SIM2培養基相比較,SIM1培養基誘導愈傷組織分化的效果最佳,分化出的苗較粗壯,長勢良好,且有些外植體上有多個芽的分化。其中CIM3+SIM1的愈傷組織分化的效率最高(圖2)。

表6 不同激素種類及配比對莖段愈傷組織分化出苗的影響Table 6 Effects of different hormones and ratios on callus differentiation and shoot induction
2.4 不同潮霉素濃度對植株再生的影響
利用上述篩選出來的最佳愈傷組織誘導及分化的最佳培養基組合CIM3 + SIM1,對芽分化階段的最佳抗生素濃度進行篩選。將預培養2 d 的外植體經過農桿菌浸染及共培養后置于愈傷組織誘導培養基CIM3 上,生長約5 周后,誘導形成愈傷組織。將形成的愈傷組織轉移到含有不同潮霉素濃度的SIM1 培養基上,誘導芽的分化,每兩周換一次培養基。大約培養7 周后,統計再生芽的數目并計算出苗率及轉化頻率(表7)。當潮霉素的濃度為0 和5 mg/L 時,愈傷組織生長正常,對芽的分化也沒有太大的影響,無法起到篩選的作用。當潮霉素的濃度為10 mg/L 時,部分愈傷組織的生長受到抑制,出芽也明顯受到抑制(圖3),潮霉素起到了一定的篩選作用,因此轉化頻率較高。當潮霉素的濃度達到15 和30 mg/L 時,經過一段時間的培養后,大部分的愈傷組織生長受到抑制并逐漸褐化,出苗率很低且再生苗長勢較弱甚至畸形,高濃度的潮霉素對外植體起到了毒害作用。當潮霉素的濃度達到40 mg/L 時,愈傷組織幾乎全部趨于死亡,無法得到再生芽。由此可知,當潮霉素的濃度為10 mg/L 時,即能保證產生抗性芽,又能保證出苗率及轉化頻率,是最佳的植株再生篩選的抗生素濃度。

圖3 不同潮霉素濃度下再生植株的生長狀態Figure 3 Growth status of regenerated shoots under different hygromycin B concentrations

表7 不同潮霉素濃度對再生的影響Table 7 Effects of different hygromycin B concentrations on regeneration
2.5 不同潮霉素濃度對再生苗生根的影響
為了確定最適的再生苗生根的潮霉素濃度,將野生型的含有腋芽的馬鈴薯莖段扦插到含有不同潮霉素濃度的RIM培養基中進行培養,大約8周后統計生根率(表8)。當潮霉素的濃度為0和5 mg/L時,馬鈴薯植株都可以生根。當潮霉素的濃度高于或等于10 mg/L 時,馬鈴薯植株都無法生根,并最后趨于死亡(圖4)。因此,當潮霉素的濃度為10 mg/L 時,未轉化的再生苗無法生根而死亡,轉化的再生苗具有一定的抗性可以正常的生根而生長。所以,10 mg/L 的潮霉素為再生苗生根的最佳篩選濃度。

圖4 不同潮霉素濃度下再生植株的生根狀態Figure 4 Growth status of rooting of regenerated shoots under different hygromycin B concentrations

表8 不同潮霉素濃度對再生苗生根的影響Table 8 Effects of different hygromycin B concentrations on rooting of regenerated shoots
2.6 不同抑菌劑的種類及濃度對轉化的影響
當農桿菌菌液浸染外植體后,后續的試驗需要進行抑菌處理。適宜的抑菌劑濃度不僅可以抑制農桿菌的生長,同時也不會毒害植株。將共培養2 d 后的莖段置于愈傷組織誘導培養基上,培養2周后觀察抑菌情況和愈傷組織生長情況(表9)。當選用的抑菌劑為頭孢霉素時,不論其濃度為100、200 或300 mg/L 都無法抑制農桿菌的生長,外植體也無法正常的進行愈傷組織的誘導。當選用的抑菌劑為100 mg/L特美汀時,無法有效的抑制農桿菌的生長;當特美汀的濃度達到200 mg/L 時,可以有效的抑制農桿菌的生長,并且可以正常的進行愈傷組織誘導及芽的分化;當特美汀的濃度為300 mg/L 時,可以有效的抑制農桿菌的生長,但是抑菌劑濃度過高對愈傷組織誘導及芽的分化有一定的影響(圖5)。因此,選用200 mg/L 的特美汀為最佳的遺傳轉化的抑菌劑濃度。
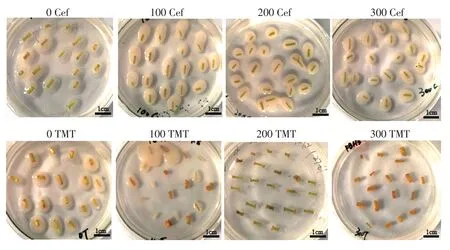
圖5 不同抑菌抗生素種類和濃度下愈傷組織的生長狀態Figure 5 Growth status of callus under different antibiotics and concentrations
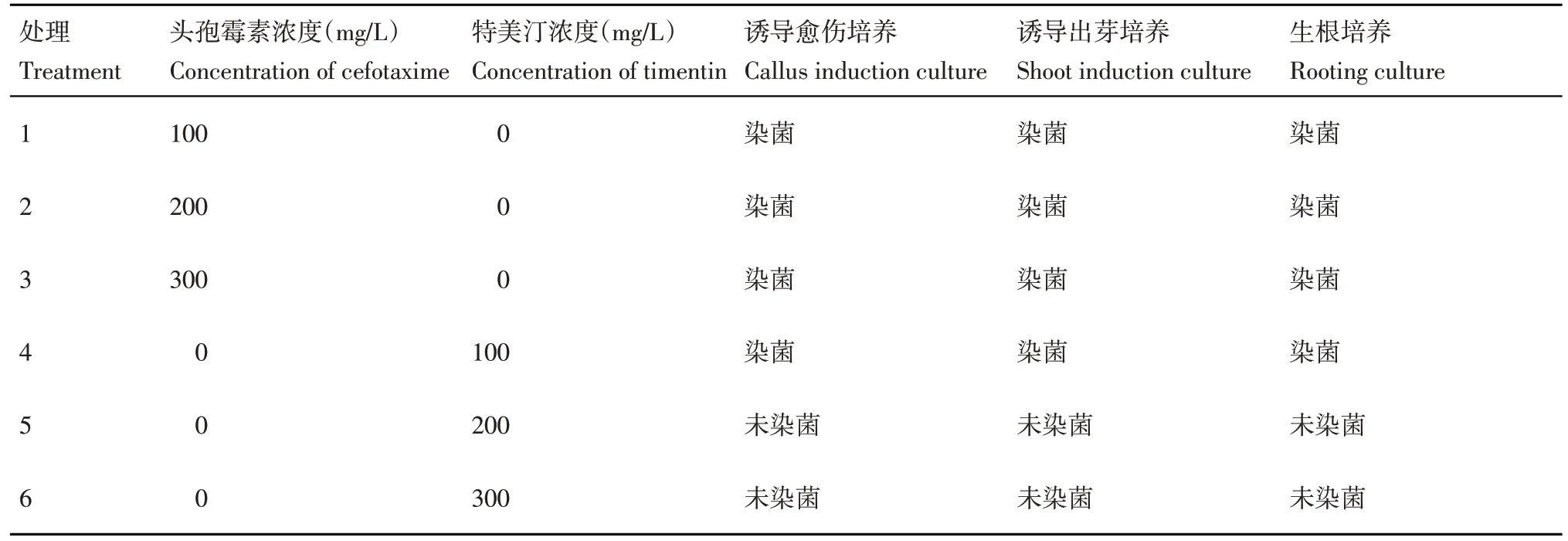
表9 不同抑菌抗生素種類及濃度的抑菌試驗Table 9 Results of antimicrobial tests for different antibiotics and concentrations
2.7 再生植株的陽性檢測
通過上述對預培養時間、愈傷組織誘導及分化階段不同激素組合的篩選,確定了再生率較高的培養基類型。根據上述試驗得到的最適條件進行新的遺傳轉化,最終共得到了58 株再生馬鈴薯植株。將獲得的再生植株轉移到生根培養基上進行篩選后得到了22 株抗性植株。提取再生抗性植株的葉片基因組DNA,經過PCR 擴增后,共有6株植株的基因組DNA 可以擴增出1 000 bp 的條帶,與陽性對照擴增條帶大小一致。因此,馬鈴薯‘并薯6號’的遺傳轉化效率約為27.3%(圖6)。

圖6 再生植株的PCR陽性檢測Figure 6 Positive detection of regenerated plants by PCR
3 討 論
外植體經過預培養后通過調整其生理狀態,減輕脅迫傷害,促進細胞分裂,使細胞處于易轉化狀態,有利于整合外源基因組,從而可以提高遺傳轉化的效率[16]。熊偉等[17]和葉明旺等[18]以馬鈴薯品種‘PB04’和二倍體馬鈴薯為材料,預培養2 d 后的外植體抗性愈傷組織誘導率最高。張西英等[19]研究表明,預培養2 d 的馬鈴薯外植體分化率和轉化率最高。因此,預培養對外植體的再生及遺傳轉化具有一定的影響。本研究結果表明,未經過預培養的外植體易發生白化或褐化最后死亡的現象,很難形成愈傷組織。預培養2 d 外植體的愈傷組織形成率和出苗率最高,預培養3 和2 d 外植體的愈傷組織形成率和出苗率差異不大,而預培養1 和4 d 外植體的愈傷組織形成率和出苗率較低。因此,本試驗中,馬鈴薯外植體的最佳預培養時間為2 d。未經過預培養的外植體浸染農桿菌后容易死亡,預培養時間過長導致外植體傷口處的愈傷組織已經形成,影響農桿菌的浸染,進而影響遺傳轉化的效率[19]。
馬鈴薯的組織再生受到外植體類型及基因型的影響,不同的外植體類型及基因型所需的最適再生體系是不同的。羅源[20]研究結果表明,以‘克新13號’‘克新12號’‘東農303’和‘早大白’的莖段作為外植體,最適的愈傷組織誘導培養基為MS+30 g/L 蔗糖+8 g/L 瓊脂+2 mg/L 6-BA+1 mg/L 2,4-D 和 MS + 30 g/L 蔗 糖 + 8 g/L 瓊 脂 + 2 mg/L 6-BA+0.5 mg/L 2,4-D;最適愈傷組織分化培養基為MS+6-BA 4.0 mg/L+NAA 0.1 mg/L+GA31.0 mg/L,MS+6-BA 2.0 mg/L+NAA 0.5 mg/L+GA31.0 mg/L,MS+6-BA 2.0 mg/L+NAA 0.1 mg/L+GA31.5 mg/L和MS+6-BA 2.0 mg/L+NAA 0.5 mg/L+GA31.0 mg/L。邱礽等[21]研究結果表明,以‘夏坡蒂’和‘費烏瑞它’的莖段作為外植體,最適的愈傷組織誘導培養基分別為MS + 6-BA 2.0 mg/L + NAA 0.5 mg/L + GA30.5 mg/L 和MS+ZT 2.0 mg/L+0.1 mg/L NAA+GA30.5 mg/L;不定芽誘導最佳培養基分別為MS+ZT 2.0 mg/L + 0.1 mg/L NAA + GA35 mg/L 和MS +6-BA 2.0 mg/L+ZT 2.0 mg/L+GA35 mg/L。張之為等[22]研究結果表明,以‘底西瑞’‘費烏瑞它’‘紫花白‘’夏坡蒂‘’大西洋’和‘虎頭’6 個品種的葉片為外植體,6-BA 和GA3對馬鈴薯葉片愈傷組織生長量和不定芽分化率有影響。李晶[23]研究結果表明,以馬鈴薯‘東農303’的莖段和薯塊為外植體,莖段最佳愈傷組織誘導培養基為MS+0.1 mg/L 2,4-D+1 mg/L BA,薯塊最佳愈傷組織誘導及分化培養基均為MS+2 mg/L ZT+1 mg/L IAA。以莖段作為外植體時,相同濃度下,2,4-D 誘導愈傷組織的能力優于NAA[24]。在愈傷組織分化過程中,6-BA 起到主要作用,但其濃度過高則會影響芽的分化[25]。GA3對馬鈴薯幼苗的分化和伸長具有明顯的促進作用[26]。另外,在培養基中加入ZT 對‘東農303’莖段的芽誘導具有很好的效果[27]。在本研究中,利用植物激素6-BA、NAA、2,4-D、KT 和GA3對‘并薯6號’愈傷組織誘導研究發現,利用2,4-D 有利于愈傷組織的誘導,利用ZT 有利于叢生芽的分化。當生長素與細胞分裂素的濃度及比例適合時,愈傷組織的誘導率和分化率較高。
在農桿菌介導的植物遺傳轉化的各個階段中,需要向培養基中添加各類抗生素,但是添加的抗生素往往會影響外植體愈傷組織的誘導和分化,因此抗生素的種類及濃度是植物遺傳轉化過程中的重要環節。抑制農桿菌生長的抗生素一般都是頭孢霉素(Cef)和羧芐青霉素(Carb)。但是由于馬鈴薯對Carb 毒害的忍受力較弱,所以在馬鈴薯遺傳轉化過程中最常使用的是Cef[28]。在本研究中使用的抑菌劑為Cef 和特美汀(TMT),通過研究發現,同樣濃度下,TMT 的抑菌效果優于Cef,并且較低濃度的TMT 就可以達到較好的抑菌效果。抑菌劑不僅可以抑制農桿菌的生長,同樣也會影響植物的正常生長和分化。選擇合適種類的抑菌劑及其濃度在達到抑菌效果的同時又對植物再生影響較小,從而也可以提高植物的遺傳轉化效率。
農桿菌介導的植物遺傳轉化是一個復雜的過程。由于不同植物的基因型存在顯著差異,因此不同植物對遺傳轉化過程中的各種因素的敏感度也不同,遺傳轉化的效率存在很大的差異[29]。雖然農桿菌介導的馬鈴薯愈傷再生轉化體系已經比較成熟,并且在馬鈴薯分子育種中也得到了一定應用。但是對于不同基因型馬鈴薯遺傳轉化效率問題仍存在很大差異。在馬鈴薯育種過程中,馬鈴薯基因型復雜性及自交不親和性等問題限制了雜交育種的進程。因此通過將優異外源基因導入到馬鈴薯中來實現品種改良是一種很好的選擇,而不同基因型馬鈴薯遺傳轉化再生體系的建立是非常必要的[30]。本研究通過對馬鈴薯品種‘并薯6號’愈傷再生轉化體系建立各個階段的影響因素進行研究,初步建立該馬鈴薯品種的農桿菌介導的遺傳轉化體系,為馬鈴薯基因功能驗證、分子育種和品質改良奠定了基礎。

