miR-132基于PGC-1α/SIRT3信號通路對肺炎鏈球菌誘慢性阻塞性肺疾病急性加重期大鼠的干預作用
張松松 劉曼莉 王金龍 潘渝 施賢清
貴州省人民醫院1重癥醫學科,2重癥監護室(貴陽550002)
慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)屬持續氣流受限和不完全可逆的肺部疾病,發生率逐年升高,細菌感染是導致此病的主要因素[1-2]。微小RNA(miR)屬于一類內源性非編碼RNA,隨著臨床上對其的不斷研究發現,多數miR 參與COPD 的進展,如miR-146a、miR-155、miR-145 等,已經證實多數miR 參與COPD 發展過程中炎癥反應的調控[3]。基于上述背景在本文研究中首次分析miR-132 是否經PGC-1α/SIRT3信號通路對肺炎鏈球菌誘慢性阻塞性肺疾病加重期(acute exacerbation of chronic obstructive pulmonary disease,AECOPD)大鼠的干預作用,明確其作用,為臨床上此病的研究提供新方向。
1 材料與方法
1.1 材料研究動物:選取60 只SPF 級SD 雄性大鼠,8~12 周齡,購自冠科生物技術(中山)有限公司,動物許可證號:SYXK(粵)2020-0240,體質量160~210 g,均預喂養7 d,光照12 h。獲我院倫理委員會批準。
1.2 方法
1.2.1 分組及建模選取15只大鼠作為A組,其余構建肺炎鏈球菌所誘導的AECOPD 模型[4],置于煙熏箱,放置香煙,3 個月后自氣道注入0.2 mL 肺炎鏈球菌混懸液。成功標準:初期可見有呼吸短促、精神不振、食欲減退、納呆等表現,繼而出現氣喘、毛色暗淡、反應遲鈍。最終45 只均建模成功。將所制備的模型隨機分為B 組(單純模型)、C 組(模型+沉默)、D 組(模型+過表達)各15 只。
1.2.2 miR-132轉染將miR-132模擬物(過表達)、miR-132 抑制物(沉默)利用Lippofectamine 2000 試劑盒稀釋為5 mmol/L,分別注射于D組、C組大鼠肺部,A、B組注射生理鹽水,注射1 d后觀察大鼠變化。
1.2.3 miR-132 轉染效率驗證取各組中5 只鑒定miR-132 轉染效率,麻醉后處死,取肺組織,采用RT-PCR 法檢測miR-132 轉染效率。
1.2.4 指標檢測(1)全自動動物肺功能測試儀測定肺功能,包括0.3 s 用力呼氣容積與用力肺活量比值(FEV0.3/FVC)、吸氣峰流量(PIF)、呼氣峰流量(PEF)。(2)貝克曼血液分析儀測定白細胞、中性粒細胞百分比計數。(3)酶聯免疫吸附試驗法測定血清IL-1β、IL-6、TNF-α 水平。(4)Western blot法檢測肺組織PGC-1α/SIRT3 信號通路蛋白表達量,將所制備的肺組織做10 000 ×g離心處理10 min,BCA 蛋白定量,DAB 顯色,分析PGC-1α、SIRT3 表達。
1.3 統計學方法采用SPSS 20.0 統計軟件進行分析處理。計量資料采用均數±標準差描述,多組間采用方差分析,兩組間采用獨立樣本t檢驗,P<0.05 為差異有統計學意義。
2 結果
2.1 miR-132 表達對比與A 組相比,B、C 組miR-132 降低,D 組miR-132 升高(P<0.05)。見表1。
表1 miR-132 表達對比Tab.1 miR-132 expression contrast ±s

表1 miR-132 表達對比Tab.1 miR-132 expression contrast ±s
注:與A 組相比,aP<0.05;與B 組相比,bP<0.05;與C 組相比,cP<0.05
組別例數miR-132 A 組B 組C 組D 組5 5 5 5 1.00±0.01 0.63±0.15a 0.19±0.07ab 1.69±0.32abc
2.2 肺功能對比B、C、D組FEV0.3/FVC、PIF、PEF低于A 組(P<0.05);C 組FEV0.3/FVC、PIF、PEF 低于B 組,D 組FEV0.3/FVC、PIF、PEF 高于B、C 組(P<0.05)。見表2。
表2 肺功能對比Tab.2 Pulmonary function comparison ±s
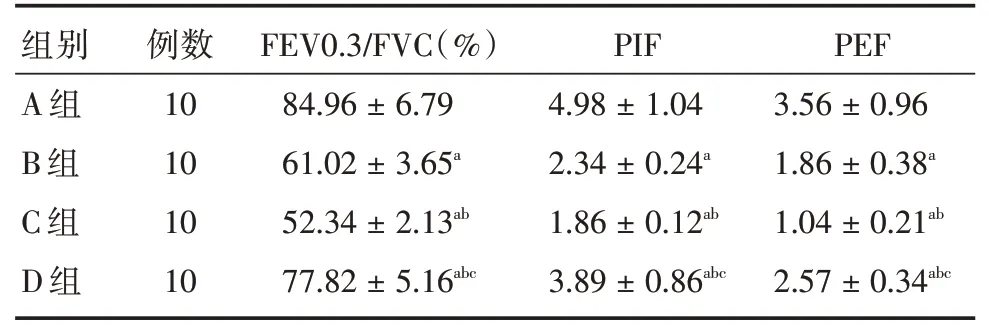
表2 肺功能對比Tab.2 Pulmonary function comparison ±s
注:與A 組相比,aP<0.05;與B 組相比,bP<0.05;與C 組相比,cP<0.05
組別A 組B 組C 組D 組例數10 10 10 10 FEV0.3/FVC(%)84.96±6.79 61.02±3.65a 52.34±2.13ab 77.82±5.16abc PIF 4.98±1.04 2.34±0.24a 1.86±0.12ab 3.89±0.86abc PEF 3.56±0.96 1.86±0.38a 1.04±0.21ab 2.57±0.34abc
2.3 白細胞總數、中性粒細胞百分比計數、氣道炎癥反應對比B、C、D 組白細胞總數、中性粒細胞百分比計數、IL-1β、IL-6、TNF-α 高于A 組(P<0.05);C 組白細胞總數、中性粒細胞百分比計數、IL-1β、IL-6、TNF-α 高于B 組,D 組白細胞總數、中性粒細胞百分比計數、IL-1β、IL-6、TNF-α 低于B、C 組(P<0.05)。見表3。
表3 白細胞總數、中性粒細胞百分比計數、氣道炎癥反應對比Tab.3 Comparison of total leukocyte counts,neutrophils,airway inflammatory responses ±s

表3 白細胞總數、中性粒細胞百分比計數、氣道炎癥反應對比Tab.3 Comparison of total leukocyte counts,neutrophils,airway inflammatory responses ±s
注:與A 組相比,aP<0.05;與B 組相比,bP<0.05;與C 組相比,cP<0.05
組別A 組B 組C 組D 組例數10 10 10 10白細胞總數(×109)1.82±0.49 10.25±2.19a 14.52±2.63ab 5.13±1.01abc中性粒細胞百分比(%)23.36±2.46 67.52±6.49a 76.68±7.26ab 35.15±3.19abc IL-1β 2.00±0.38 6.24±1.02a 8.49±2.24ab 3.59±0.54abc IL-6 2.32±0.55 5.42±0.32a 6.98±1.05ab 3.02±0.21abc TNF-α 1.52±0.24 7.68±1.04a 9.52±2.69ab 2.89±0.52abc
2.4 PGC-1α/SIRT3 蛋白表達對比B、C、D 組PGC-1α、SIRT3 表達低于A 組(P<0.05);C 組PGC-1α、SIRT3 表達低于B 組,D 組PGC-1α、SIRT3 表達高于B、C 組(P<0.05)。見表4。

表4 PGC-1α/SIRT3 蛋白表達對比Tab.4 PGC-1α/SIRT3 protein expression contrast x±s
3 討論
COPD 的發生多因接觸有害氣體、細菌感染所致,急性期更為嚴重,患者病死率較高,目前對于此病的治療手段雖較多,但整體療效不理想,多數患者預后仍不佳[5-6]。因此尋找新的治療COPD 的靶點對改善患者預后、促進患者疾病恢復具有重要的意義。
miR 屬于一類非編碼的內源性微小RNA,其可經介導mRNA 降解、抑制轉錄發揮調控多種基因表達的作用,多種miR 參與機體局部炎癥反應[7-8]。miR-132 屬于miR 家族成員之一,其具有進化保守性,參與機體多種生理病理過程[9-11]。臨床多項研究顯示[12-13],miR-132 參與COPD 肺損傷的修復。基于上述研究基礎,在本文研究中為了進一步驗證miR-132 是否可作為COPD 治療的新靶點,結果顯示,經miR-132 過表達處理的大鼠氣道炎癥反應被抑制,肺功能改善,而miR-132沉默處理的大鼠上述表現更為嚴重。此結果提示,miR-132 可能參與COPD 的進展。
COPD 發生后肺泡上皮細胞出現大量凋亡現象,而肺泡上皮細胞的凋亡可進一步破壞肺泡-上皮屏障,最終形成肺水腫[14-15]。PGC-1α/SIRT3通路與細胞凋亡相關,PGC-1α 屬于轉錄調節因子成員之一,具調控機體氧化應激反應、線粒體代謝、局部炎癥反應作用[16-18]。SIRT3 屬PGC-1α 的下游靶基因,其在線粒體基質中所表達,PGC-1α 被激活后可經誘導SIRT3 表達增加SIRT3 活性,最終參與細胞凋亡、線粒體氧化代謝等過程[19-22]。謝圓媛等[23]研究認為PGC-1α/SIRT3 通路與COPD 相關,經激活此信號通路可抑制氣道炎癥發揮作用。本研究結果發現,經miR-132 過表達處理的大鼠肺組織PGC-1α/SIRT3信號通路蛋白表達明顯升高,因此本文進一步推測miR-132 可能經激活PGC-1α/SIRT3信號通路可抑制氣道炎癥,修復損傷的肺功能。
綜上所述,經轉染miR-132 模擬物可抑制肺炎鏈球菌誘AECOPD 氣道炎癥,修復肺損傷,機制可能與激活PGC-1α/SIRT3 信號通路PGC-1α 上調SIRT3 相關。

