超聲引導聯合腔內心電圖技術在PICC置管尖端定位中的應用
張秀娟 江西省貴溪市人民醫院 335400
化療為惡性腫瘤主要治療方式,具降低腫瘤分期、抑制腫瘤擴散之效。但化療治療周期較長、化療藥物刺激性較大,可增加患者血管刺激,增加化療相關不良反應。外周靜脈置入中心靜脈導管(PICC)為降低患者化療藥物刺激、減少患者反復穿刺痛苦的重要干預措施,為目前惡性腫瘤化療治療重要干預環節,而化療效果與PICC置管尖端定位效果密切相關。超聲定位為PICC置管尖端定位常用技術,通過超聲探頭測定置管深度后進行置管操作,但仍存在一定局限性。腔內心電圖技術近年來在臨床應用頻率逐漸提升。相關研究表示[1],在PICC置管尖端定位中,利用超聲引導+腔內心電圖技術,可提升PICC置管尖端定位效果。但此種技術是否會增加置管期間心律失常發生率仍有待研究。為此,本文選取86例需PICC置管的惡性腫瘤化療患者,探究超聲引導+腔內心電圖技術對PICC置管尖端定位影響,具體報道如下。
1 資料與方法
1.1 一般資料 選取我院2019年1月—2020年10月86例需接受長期化療PICC置管患者,將其隨機分為A、B組,每組43例。兩組資料比較無統計差異(P>0.05),見表1。研究符合醫學倫理,見表1。
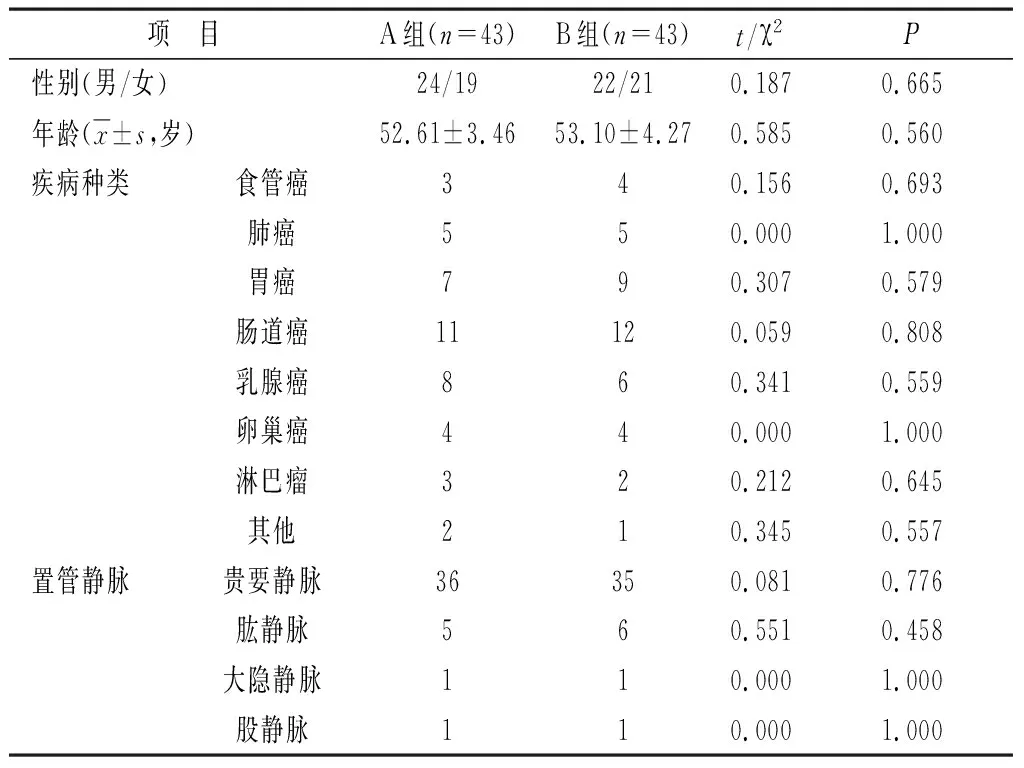
表1 兩組一般資料對比(n)
1.2 選擇標準 納入標準:(1)均經手術病理檢查確診為惡性腫瘤;(2)均符合化療治療標準;(3)均具備PICC條件;(4)體表心電圖為竇性心律;(5)患者、家屬對研究知情同意。排除標準:(1)精神異常,難以配合完成研究者;(2)血管畸形使導管無法達到上腔靜脈者;(3)合并心律失常疾病,或置入起搏器等可能影響P波監測患者;(4)置管不成功,或置管后未拍攝胸X線片者。
1.3 方法 A組(超聲引導置管):(1)以體外超聲方式評估患者血管狀態;患者置管上肢向外伸展至與身體保持垂直,由軟尺測量穿刺部位至右胸鎖關節距離,并向下方測量至第三肋間隙長度,兩次測量總數值為PICC置管長度;(2)創建最大程度無菌范圍,提前準備術中所需物品,預沖導管后穿刺置管;在導管達到預先設定長度后,利用超聲檢查同側頸外、頸內靜脈,腋靜脈及鎖骨下靜脈,確定是否發生導管異位情況,若無異常,固定導管;(3)以胸X線片確認導管尖端部位。B組(超聲引導+腔內心電圖技術置管):(1)患者平臥,體外導長度測量方式與A組相同;(2)心電導聯相互關聯,選Ⅱ導聯基準心電圖,若為竇性心律且可觀測到P波,則利用超聲探頭探查患者血管情況;(3)創建最大程度無菌范圍,準備術中物品,預沖導管后穿刺送管;待PICC導管與預估距離相差5cm時,暫不撤離導絲,將右上導聯按鈕取下接入無菌鱷魚夾,另一端與PICC掃管內導絲尾部暴露在外的導絲相互關聯;(4)觀察患者P波變化,將導管放在預估位置后,PICC導管末端連接抽滿30ml的0.9%氯化鈉溶液,緩慢推注并關注患者P波變化;P波呈現上升狀態時,提示導管成功到達上腔靜脈,在導管靠近上腔靜脈與右心房交匯位置時P波達到峰值,甚至超過QRS波;(5)將導管緩慢推送至預估位置,P波回落;當出現負向P波、雙向P波時,提示導管進入右心房,后將導管緩慢撤出;(6)若P波振幅到達QRS波40%~60%,可判定導管長度;若導管抵達預估長度,但未出現P波變化,提示導管異位,及時調整導管,并觀察P波變化,若多次調整仍未見P波,則將導管置入預估位置,并以超聲探頭檢測同側靜脈情況,無異常后固定導管;(7)以胸X線片確認導管尖端部位。
1.4 觀察指標 (1)比較兩組PICC置管尖端到位率[2]:以置管后胸X線片檢查結果為標準,以導管尖端進入上腔靜脈為到位;(2)比較兩組置管期間心律失常發生率。
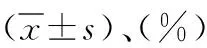
2 結果
2.1 兩組PICC置管尖端到位率比較 B組PICC置管尖端到位率為95.35%,較A組的81.40%高(P<0.05),見表2。
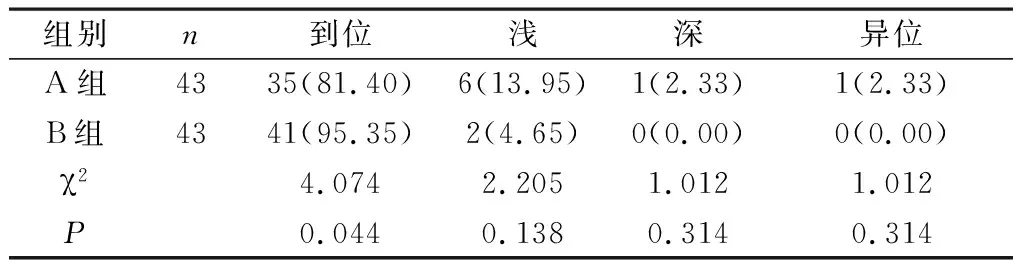
表2 兩組PICC置管尖端到位率比較[n(%)]
2.2 兩組心律失常發生率比較 B組心律失常發生率為2.33%(1/43),較A組的13.95%(6/43)低(χ2=3.888,P=0.049<0.05)。
3 討論
隨臨床靜脈輸液治療頻率增加,PICC置管需求量逐漸增加,但在PICC置管中,受患者靜脈條件、骨性標識、胸鎖關節長度、肥胖、護理人員體表測量主觀因素影響,無法有效保證置管準確率,不僅會影響治療效果,甚至可增加導管相關并發癥發生率,影響治療安全性[3]。在對化療患者PICC置管中,導管尖端最佳位置為右心房上壁與上腔靜脈交接點,該部位置管優勢為:血流量大,能夠保證藥物快速稀釋而不造成血管損傷;可最大限度降低導管相關并發癥發生率,保證置管及治療安全性[4]。
超聲引導為保證PICC置管準確性基礎干預方案,通過體外血管測量方式判斷置管長度,但在置管期間無法確定置管準確性,置管不確定因素較多[5]。腔內心電圖技術原理為:以竇房結為心臟基本竇性節律起搏點,竇房結起搏細胞完成除極后,心電圖上出現P波,P波形態、振幅與電極及心房綜合向量軸之間距離相關,因此在PICC期間,P波會隨導管運動出現相應變化,有利于及時調整導管位置,避免發生置管淺、深或異位情況,保證置管準確性,如P波峰值后回落提示導管尖端達到靠近上腔靜脈與右心房交匯位置,若出現負向P波、雙向P波時,提示導管進入右心房,但若置管期間未出現P波變化,提示置管異位,與單純應用超聲引導技術相比,準確性更強,可準確評估導管尖端位置,避免受置管不確定性增加置管淺、深或異位發生率,保證治療精準性及安全性。
本文中對B組患者實施超聲引導+腔內心電圖技術置管,結果發現,B組PICC置管尖端到位率較A組高。考慮原因為:單純應用超聲引導,置管期間不確定性較大,而利用腔內心電圖+超聲引導,可通過P波峰值變化客觀評估置管深度,提升置管精準性。陳萍等[6]研究發現,在常規監測技術基礎上聯合腔內心電圖,可提升導管尖端一次性到位率(100.00%VS 86.70%),與本文結果相近,提示利用腔內心電圖輔助定位,可提升PICC置管精準性。本文結果發現,B組心律失常發生率較A組低。考慮原因為:應用超聲引導+腔內心電圖技術,可監測PICC過程,降低管路對患者靜脈血管刺激,保證患者血流動力學穩定,減少患者心肌刺激,可保證患者心臟功能穩定,降低心律失常發生率。陳仙等[7]研究發現,在直腸癌患者化療PICC置管中,結合心電導聯,可顯著降低患者PICC置管相關心律失常發生率,與本文結果一致,證實在PICC置管期間應用超聲引導+腔內心電圖定位,可降低心律失常發生率,提升置管安全性。
綜上所述,在PICC置管中,利用超聲引導+腔內心電圖監測,可提升患者PICC置管尖端定位到位率,降低心律失常發生率,與單純使用超聲引導相比,效果理想。

