不同惡性概率預測模型在亞實性肺結節患者中的驗證性研究
劉浩雷,尹 格,向 毅,曹偉云
(湖南中醫藥高等專科學校附屬第一醫院呼吸與危重癥醫學科,湖南 株洲 412000)
肺結節的良惡性鑒別常常困擾著臨床醫生,特別是亞實性肺結節在臨床-影像-病理方面與實性肺結節存在明顯差異,研究報道,混合性磨玻璃結節、純磨玻璃結節和實性結節的惡性概率分別為63%、18%和7%[1]。為了幫助臨床醫生決策,常使用肺結節惡性概率預測模型來判斷肺結節惡性的風險,其中比較認可的模型有梅奧模型[2]、美國退伍軍人醫院(VA)模型[3]、美國Brock大學模型[4](Brock模型)和北大人民醫院模型[5](北大模型)。然而,這4種模型專門對亞實性肺結節的預測效能尚未有驗證。為此,本研究擬利用本院的亞實性肺結節患者的病例資料驗證上述4種預測模型的診斷效能和臨床價值。
1 資料與方法
1.1研究對象 選擇2018年1月至2020年12月在本院經手術切除且病理證實的亞實性肺結節患者作為研究對象。納入標準:(1)符合亞實性肺結節定義即直徑≤3 cm的局灶性、類圓形、密度增高的亞實性肺部陰影,不伴肺不張、肺門淋巴結腫大和胸腔積液[6];(2)有明確的病理診斷結果。排除標準:(1)>3 cm的肺部腫塊;(2)資料不完整者。
1.2方法
1.2.1一般資料采集 記錄患者的性別、年齡、病理結果、既往史、吸煙史和家族史等資料。
1.2.2影像學檢查 所有患者均常規行胸部三維CT檢查,由2位放射科副主任醫師分析患者影像學資料,記錄結節部位、最大直徑和結節類型,對結節是否具有毛刺征、邊界是否清楚、是否有鈣化、是否合并肺氣腫進行判斷,如遇分歧則經討論后決定。
1.2.3惡性概率預測模型 選擇4個國內外公認的肺結節惡性概率預測模型進行惡性概率的計算,計算公式均為Y=ex/(1+ex),其中x取值各不相同,梅奧模型的x=-6.827 2+0.039 1×年齡+0.791 7×吸煙史+1.338 8×腫瘤家族史+0.127 4×直徑+1.040 7×毛刺+0.783 8×上葉結節[2];Brock模型的x=0.028 7×(年齡-62)+性別+腫瘤家族史+肺氣腫-5.385 4×(直徑/10)-0.5-1.581 1+結節類型+上葉結節-0.082 4×(結節數量-4)+毛刺-6.789 2[4];VA模型的x=-8.404+2.061×吸煙史+0.779×年齡/10+0.112×直徑-0.567×戒煙年數/10[3];北大模型的x=-4.496+0.07×年齡+0.676×直徑+0.736×毛刺+1.267×腫瘤家族史-1.615×鈣化-1.408×邊界清楚[5]。
1.3數據處理及統計 收集的數據錄入Excel2012表,建立數據庫。采用MedCalc (20.009版)統計學軟件進行分析,將梅奧、Brock、VA模型和北大模型對亞實性肺結節預測結果與病理診斷結果進行比較,計算各個模型的敏感度、特異度、陽性預測值、陰性預測值、陽性似然比和陰性似然比,繪制ROC曲線,計算AUC,并對4種模型的AUC進行兩兩比較,P<0.05為差異有統計學意義。
2 結 果
2.1一般資料 共有79例亞實性肺結節患者納入本研究,其中男18例(22.8%),女61例(77.2%);年齡(50.8±12.1)歲;結節類型中有純磨玻璃結節27例(34.2%),混合性磨玻璃結節52例(65.8%);肺結節大小(12.8±5.9)mm,良性結節大小(9.2±3.6)mm,惡性結節大小(14.5±5.9)mm。上葉結節50例(63.3%),病理結果顯示良性26例(32.9%),惡性53例(67.1%)。良性結節包括炎性病變2例(2.5%)、非典型腺瘤樣增生2例(2.5%)、原位癌22例(27.8%);惡性結節包括微浸潤性腺癌42例(53.2%)、腺癌11例(13.9%)。有吸煙史者9例(11.4%),既往有腫瘤病史或家族腫瘤病史者14例(17.7%)。
2.24種模型診斷價值比較 4種預測模型的ROC曲線見圖1,AUC均≥0.7,其中Brock模型的AUC最大(0.83),北大模型的AUC最小(0.70);敏感度最高的是北大模型(71.70%),特異度最高的是Brock模型(96.15%),見表1。陽性預測值最高的是Brock模型(0.96),陰性預測值最高的是梅奧模型(0.56);陽性似然比最高的是Brock模型(15.21),陰性似然比最低的是梅奧模型(0.38),見表2。4種模型的AUC相互比較,差異均無統計學意義(P>0.05)。
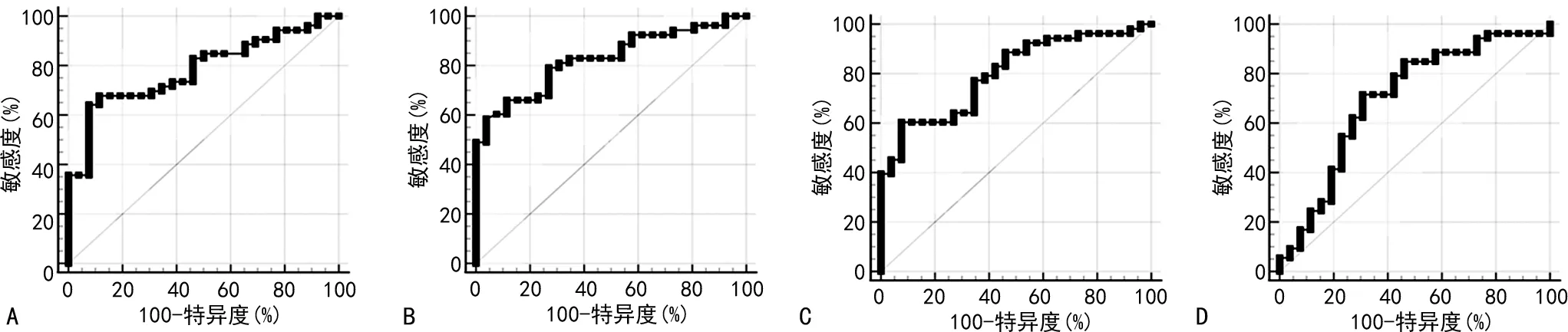
A.梅奧模型;B.Brock模型;C.VA模型;D.北大模型。

表1 4種模型驗證亞實性肺結節惡性概率的比較
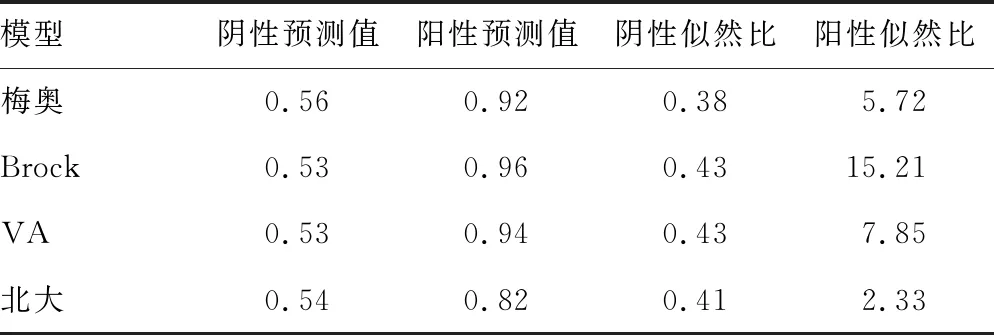
表2 4種模型診斷價值比較
3 討 論
肺結節惡性概率預測模型是一種疾病風險預測模型,其是以惡性肺結節的多種風險因素為基礎,根據影響程度大小劃分分值,利用數學公式計算發生惡性結節概率的一種統計學評估方式。有研究表明,一個有效的肺結節惡性概率預測模型,可使肺癌的診斷提前4~12個月[7]。指南也推薦在進行影像學隨訪和活檢之前,應該用經過驗證的預測模型來評估惡性腫瘤的概率[8]。目前,國內外經過驗證的預測模型有梅奧模型、Brock模型、VA模型、北大模型等。梅奧模型于1997年建立,其建模數據來源于419例X線發現的孤立性實性肺結節患者的臨床資料,該模型參數組成包括年齡、吸煙史、腫瘤家族史、結節直徑、毛刺征和上葉結節。雖然,梅奧模型是通過實性肺結節的數據建立而來的,但在本研究中顯示梅奧模型同樣適合于亞實性肺結節的惡性概率評估,其AUC為0.78,而且其陰性似然比最低,說明梅奧模型判斷為良性結節的效能較高(即判斷真陰性的可能性大)。Brock模型的建模數據也主要來源于實性肺結節(79.0%)患者,其參數組成包括年齡、性別、腫瘤家族史、毛刺征、結節直徑、結節類型(實性結節、純磨玻璃結節和混合性磨玻璃結節)、上葉結節、結節數量和是否合并肺氣腫等。Brock模型是首個納入結節類型的預測模型,模型分別對實性結節、純磨玻璃結節和混合性磨玻璃結節賦予不同分值,其中實性結節賦分最高,其次是混合性磨玻璃結節和純磨玻璃結節,近年來發現混合性磨玻璃結節惡性風險高于實性結節,之所以該模型賦予實性結節的分值最高,可能與建模數據中實性結節的數據占比大有關。在本研究中Brock模型的AUC最高(0.83),而且其陽性預測值和陽性似然比高于其他3種預測模型,說明Brock模型判斷為惡性結節的效能較高(即判斷真陽性的可能性大)。AL-AMERI 等[9]應用244例肺結節患者的臨床資料分別驗證梅奧模型、VA模型、Brock模型和Herder模型的診斷效能,其中Brock模型的AUC為0.902,僅次于Herder模型(AUC 0.924)。由于Herder模型包含PET/CT的攝取值,亞實性結節特別是純磨玻璃結節患者不適合進行PET/CT檢查,故本研究未納入Herder模型的驗證。VA模型建模數據庫中肺結節患者的影像學特征較少,僅有結節直徑和結節部位,所以該模型的參數組成是4個模型中最少的,僅有年齡、吸煙史、戒煙時間和結節直徑,而且納入研究對象主要是老年白人和退伍軍人,因此其應用受到限制,在本研究中其AUC為0.80。北大模型是以中國肺結節患者的臨床及影像數據建立的預測模型,共納入了371例肺結節患者,其參數組成包括年齡、腫瘤家族史、結節直徑、毛刺征、鈣化和邊界是否清楚,國內多個預測模型的驗證性研究均顯示北大模型的診斷價值高于其他模型[10-11],但本研究中北大模型的AUC僅為0.70,這可能與亞實性結節較少出現鈣化、邊界多模糊有關,該模型可能更適合實性結節的惡性風險評估。上述4種預測模型的AUC均≥0.7,說明這4種預測模型診斷價值較高,均可應用于亞實性肺結節惡性概率評估,雖然4種模型的AUC相互比較差異無統計學意義(P>0.05),但從陽性預測值、陽性似然比等指標來看,Brock模型更適合亞實性肺結節的診斷。
本研究也存在一些不足,如樣本量較小,納入對象是進行手術切除的亞實性肺結節患者,存在選擇偏倚、單中心回顧性研究等。因此,本研究結論需用更大樣本量、多中心前瞻性研究和納入更多隨訪觀察的亞實性肺結節患者的研究進一步驗證。

