直接多肽結合試驗的實驗室驗證
黎硯書 熊友文 徐麗瑛 肖小華
摘要:目的:本文旨在實驗室轉化和建立直接多肽結合試驗(DPRA)方法, 并在實驗室內進行驗證,實現對化學物可能引起皮膚致敏性的預測。方法:選擇五種已知皮膚致敏性化合物分別與半胱氨酸多肽和賴氨酸多肽在25℃暗處條件下共孵育24h,使用HPLC測定兩種特征多肽消耗百分率并依據DPRA預測模型判定受試物致敏性程度,再進一步比較試驗數據與OECD TG 442C指南參考結果。結果:DPRA準確的劃分了五種受試物的致敏性。2,4-硝基氯苯和甲醛判定為極強致敏物,肉桂醛判定為中致敏物,正丁醇和6-甲基香豆素為非致敏物。結論:本實驗室建立的DPRA 可準確預測單一化合物的皮膚致敏性及其程度,完成本實驗室直接多肽結合試驗的驗證。
關鍵詞:直接多肽結合試驗;皮膚致敏;替代方法
【中圖分類號】R-1 【文獻標識碼】A 【文章編號】1673-9026(2022)01--01
近年來,隨著致敏免疫分子研究體系的逐漸清晰和動物福利原則的推行,建立體外評價化學物致敏性的方法就顯得尤為重要。基于有害結局通路(AOP)概念的提出,多種體外替代方法被嘗試并通過驗證[1~2]。如DPRA[3]、人細胞系活化試驗[4] 、角質細胞ARE-Nrf2熒光素酶檢測方法[5]等。在皮膚致敏的發生過程中,化學物質與皮膚蛋白質的結合是一個關鍵步驟。大多數化學致敏原都具有親電性,能與氨基酸(半胱氨酸和賴氨酸)的親核中心共價結合[6]。DPRA就是基于該原理開發的一種體外化學分析方法。
1試驗材料
1.1主要儀器
高相液相色譜儀(美國waters儀器公司);色譜柱、保護柱(含柱芯)(安捷倫科技有限公司);超微量電子分析天平(賽多利斯科學儀器有限公司);電熱恒溫培養箱(天津市泰斯特儀器有限公司)。
1.2主要試劑
半胱氨酸多肽(Ac-RFAACAA-COOH,分子量751.9)、賴氨酸多肽(Ac-RFAAKAA-COOH,分子量776.2),購于南京萊昂生物科技有限公司;肉桂醛(上海麥克林生化科技有限公司);2,4-二硝基氯苯(成都艾科達化學試劑有限公司);甲醛(西隴化工股份有限公司);正丁醇(西隴化工股份有限公司);6-甲基香豆素(上海源葉生物科技有限公司)。
HPLC流動相A:往500mL水中加入500uL三氟乙酸。HPLC流動相B:往1L乙腈中加入850uL三氟乙酸。
2試驗方法
2.1 樣品處理
分別將肉桂醛,2,4-二硝基氯苯,甲醛,正丁醇,6-甲基香豆素用乙腈配制成3mL 100mM的溶液作為儲備液。
2.2標準曲線制作
將半胱氨酸多肽和賴氨酸多肽分別配制標準品1(0.667mmol/L)、標準品2(0.267 mM)、標準品3(0.1335 mM)、標準品4(0.0667 mM)、標準品5(0.0334 mM)、標準品6(0.0167 mM),依次進行高效液相色譜進樣分析,用濃度與峰面積繪制標準曲線,此次試驗我們半胱氨酸多肽和賴氨酸多肽的R 2均大于0.990。
2.3共孵育及HPLC進樣
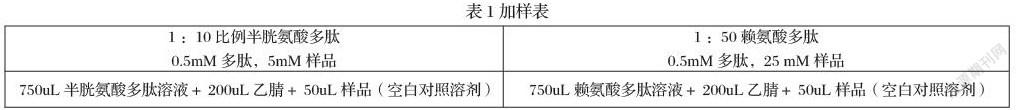
按下列表格(見表1)配制樣品,加樣于2mL進樣瓶中,待充分混勻后再置于電熱恒溫培養箱中,25℃暗處條件下孵育24h。每個樣品組和對照組均配制三個平行樣。24h后將樣品組和對照組置于HPLC中進行檢測分析。
2.4 HPLC條件
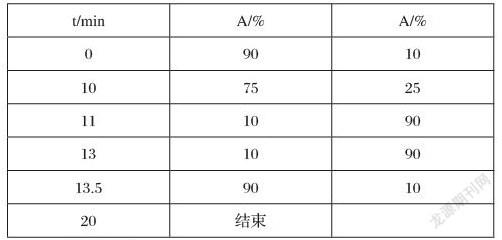
用50%流動相A+50 %流動相B在柱溫為30℃下平衡色譜柱2h,流量0.35mL/min。進樣量為7uL,樣品溫度為25攝氏度。洗脫條件如下。
2.5數據處理
計算樣品和對照品的峰面積,根據峰面積計算多肽消耗率。
多肽消耗率=[1-(平行樣多肽峰面積均值/空白對照C多肽峰面積均值) ] ×100%
2.6預測模型
根據DPRA預測模型對受試物進行判定[5]。當受試物均不與兩種多肽共洗脫時,則計算兩種多肽消除率的均值,均值≤6.38%,反應程度為無或較弱,為非致敏物;6.38%<均值≤22.62%,22.62%<均值≤42.47%,均值>42.47%,此3種情況均為致敏物,反應程度分別為低、中、高。當受試物與賴氨酸多肽發生共洗脫時,僅用半胱氨酸多肽消除率進行判斷,非致敏物為消除率≤13.89%;13.89%<消除率≤23.09%,23.09%<消除率≤98.24%,消除率>98.24%,致敏物反應程度分別為低、中、高。當受試物與兩種多肽均發生共洗脫時,則無法判斷。
5、試驗結果
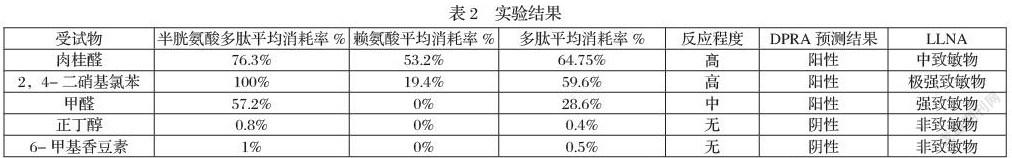
根據實驗數據顯示(見表2),此5種物質均不與兩種多肽發生共洗脫。肉桂醛、2,4-二硝基氯苯、甲醛的多肽消耗率均值分別為64.75%、59.6%、33.6%,根據DPRA預測模型均為致敏物,反應程度分別為高、高、中。正丁醇、6-甲基香豆素多肽消耗率均值分別為0.4%、0.5%,根據DPRA預測模型均為非致敏物。五種受試物測試結果均與OECD TG 442C指南參考結果趨于一致。與體內致敏潛能(LLNA數據)相比程度判定有2個不一樣,但判定致敏物和非致敏物分類一致。
6討論
傳統的化學物致敏性評價主要以動物實驗為主,而近年來出于對動物保護的需求,使得建立可靠有效的皮膚致敏體外評價體系成當下研究的熱點。皮膚致敏的有害結局通路是從分子起始事件、關鍵事件到產生系統效應的連續發生過程[7]。其分子起始事件是致敏原與皮膚蛋白發生結合反應形成半抗原化合物。DPRA使用化學方法模擬致敏原與人工合成多肽(半胱氨酸肽和賴氨酸肽)結合,采用HPLC分析反應液中多肽的損耗,以評估受試物的肽反應性,從而評估化學物質是否可能為皮膚致敏原。
本實驗完成了在實驗室內建立和驗證DPRA方法,其驗證結果與LLNA結果趨于一致。但在實驗過程中仍出現過許多問題,如HPLC體系的干擾,樣品配制誤差,多肽降解,加樣量過少等。本實驗由于實驗室條件限制只驗證了五種受試物的致敏性,在產品檢測應用中還需要積累大量實驗數據和優化實驗條件。
參考文獻:
[1]瞿小婷,程樹軍,秦瑤,等.有害結局通路指南及毒性測試應用分析[J].日用化學品工業,2016,46(8):473-478.
[2]陳彧,喻歡,程樹軍,等.基于有害結局通路原理的皮膚致敏測試替代方法進展[J].日用化學品科學,2016,39(4):4-9.
[3]OECD.Test No.442C:In Chemico Skin Sensitisation:Direct Peptide Reactivity Assay (DPRA) [S].Organization for Economic cooperation and Development,Paris,2015.
[4]OECD.Test No.442D:In Vitro Skin Sensitisation:ARE-Nrf2 Luciferase Test Method[S].Organization for Economic cooperation and Development,Paris,2015.
[5]OECD.Test No.442E:In Vitro Skin Sensitisation:ARE-Nrf2 Luciferase Test Method[S].Organization for Economic cooperation and Development,Paris,2015.
[6]Gerberick G,Vassallo J,Foertsch L,et al.Quantification of chemical peptide reactivity for screening contact allergens:a classification tree model approach[J].Toxicology.2007,97(2):417-427.
[7]OECD.The adverse outcome pathway for skin sensitisation initiated by covalent binding to proteins.part 2:use of the AOP to develop chemical categories and integrated assessment and testing approach.Series on Testing and Assessment No.168[R].Paris, 2012.

