電針對VD大鼠學習記憶能力及海馬CA1區SIRT1/PGC1-α表達的影響*
葉 偉 李文強 汪 玥 胡 馨 王 林 丁 見
皖南醫學院 1 臨床醫學院 2 基礎醫學院,安徽省蕪湖市 241002
血管性癡呆(Vascular dementia,VD)是由于腦中血管發生病變,引起腦血液供應不足,進而表現出認知功能障礙[1]。隨著社會的發展和人口老齡化進程的加速,腦血管病發病率逐年增加,因此VD 的發病率也在不斷上升,據研究發現VD的發生與炎癥反應、缺氧和低灌注引起的氧化應激以及發生的神經元凋亡有著密切的關系[2]。慢性腦缺血狀態下大鼠的線粒體功能發生紊亂,引起氧化應激,損傷海馬CA1區神經元,最終發生神經退行性改變,認知功能下降[3]。
VD的主要疾病特點為學習、記憶等認知功能的減退,大腦海馬CA1區是學習、記憶、情緒等相關的重要腦區。沉默信息調節因子1(Silent information regulator 1,STRT1)在海馬體CA1中有豐富的神經元表達,參與重要的生理學過程,如細胞的氧化應激和細胞凋亡,其機制是去乙酰化調控下游分子[4]。過氧化物酶體增殖物激活受體γ輔激活因子1α(Peroxisome proliferator-activated receptor γ coactivator 1α,PGC1-α)在許多認知功能發生障礙的中樞神經系統疾病的發生發展中起到重要的作用,激活的PGC1-α能夠消除自由基,誘導細胞抗氧化酶的表達,提髙組織的抗氧化能力[5]。研究證實針灸對于改善血管性癡呆患者的癥狀,延緩VD進程方面有確切的效果。趙建新等[6]使用電針干預百會穴后,明顯改善了血管性癡呆在認知功能方面的障礙。本實驗通過電針干預,探究電針治療改善VD大鼠學習記憶能力的機制。
1 材料與方法
1.1 材料 (1)動物:成年健康雄性SD大鼠24只,體重(250±20)g,購自浙江省實驗動物中心,動物生產許可證號:SCXK(魯)20190003。(2)主要試劑:SIRT1(bs-2257R)抗體(北京博奧森生物技術有限公司);PGC1-α(bs-7535R)抗體(北京博奧森生物技術有限公司);兔IgG-免疫組化試劑盒(SA2002 1/4KIT,博士德生物工程有限公司);Nissl staining溶液(北京索萊寶科技有限公司)。(3)主要儀器:輪轉式石蠟切片機(德國Leica公司),華佗牌電子針療儀(蘇州醫療用品有限公司),BX51顯微鏡(日本OLYMPUS公司)。
1.2 方法
1.2.1 動物分組。置于室溫(23±2)℃,相對濕度(60±5)%的環境中適應性喂養1周后,將大鼠隨機分為對照組、模型組和電針組,每組8只。
1.2.2 模型制備。VD模型通過2VO的方法進行復制:大鼠造模前禁食不禁水12h后稱重,麻醉使用1%戊巴比妥鈉(0.3ml/100g)腹腔注射,將大鼠以仰臥位固定在手術臺上,消毒、備皮沿頸正中切口切開,逐層剝離至充分暴露雙側頸總動脈后將其用手術縫線結扎,將分離的組織復位后縫合傷口。術后3d內,每天注射0.5ml青霉素預防后續感染,放回籠中,保溫飼養,控制大鼠的直腸溫度在37℃左右。對照組進行同樣手術操作,但雙側頸總動脈不做結扎處理。
1.2.3 治療方法。對電針組的大鼠用1%戊巴比妥鈉腹腔注射(0.3ml/100g)麻醉后將大鼠側臥位放置,用頻率2Hz、強度3V、波寬1ms的疏密波電針治療“百會”穴和“足三里”穴,百會穴位于頂骨與頂間骨之間正中凹陷處 (即兩耳郭前緣根部連線中點);足三里在后肢前外側, 犢鼻下約6mm, 脛骨前緣旁開約2mm。連續4周,1次/d,30min/次,對照組和模型組用同樣方法麻醉但不電針。
1.2.4 Morris水迷宮實驗。定位航行實驗:在第2~4天,將每組大鼠沿壁從固定象限排列放置在水中。如果大鼠在90s內找到平臺,則將大鼠找到平臺所耗費的時間記錄下來,并使其停留在平臺上20s;如果大鼠在90s內未找到平臺,則將大鼠引到平臺,并同樣在平臺上停留20s的時間,并記錄90s作為此大鼠逃避潛伏期的時間。每天除了平臺所位于水中的象限外,其他三個象限所測定出來的結果依次記錄下來,將平均值作為每天的逃避潛伏期的時間。
空間探索試驗:在第5天,將平臺移開,將進水點選為平臺象限的對立象限,將大鼠沿壁放進水中,并記錄了其在平臺所在象限內所活動的時間。
1.2.5 樣品收集。腹腔注射1%戊巴比妥(0.3ml/100g),暴露心臟,并通過左心室升主動脈灌注4℃4%多聚甲醛緩沖液固定。根據George Baxinos的《大鼠大腦定位立體圖》取出所需要的腦組織,置于4%多聚甲醛溶液中固定24h,最后將其包埋在石蠟中。
1.2.6 尼氏染色。取上述處理好的組織切片放入焦油紫染色液中,避光,然后在56℃恒溫箱中1h后用去離子水洗滌,接著將其放入尼氏液中分化至在顯微鏡下背景接近無色,然后脫水,透明,封片。
1.2.7 免疫組化檢測。取各組大鼠腦組織石蠟切塊進行切片,厚5μm。經脫蠟至水,3%過氧化氫去離子水消除內源性過氧化物酶活性、抗原熱修復,山羊血清封閉,用多克隆抗體在 4℃以 1∶150 稀釋,一抗孵育18h。用山羊抗兔IgG抗體后滴加SABC檢測的表達。用DAB顯色液顯色后,封片。通過顯微鏡觀察、結合大鼠腦立體定位圖譜確定所在位置、最后使用圖像分析系統對檢測大鼠海馬CA1區的SIRT1和PGC1-α的免疫陽性細胞進行拍照,用來計數和測灰度值,統計出陽性細胞數量和平均灰度值。
1.3 統計學方法 統計分析使用SPSS18.0統計軟件,其中組間比較使用單因素方差分析,結果以均數±標準差表示,P<0.05表示差異有統計學意義。
2 結果
2.1 行為學實驗結果 由實驗數據可得,模型組大鼠在第5天時平均逃避潛伏期時間較對照組大鼠高(P<0.05),且其平臺象限活動時間比例低于對照組大鼠(P<0.05);電針組大鼠在第5天時平均逃避潛伏期時間低于模型組(P<0.05),且其原平臺象限活動時間比例相對于模型組要高(P<0.05)。見圖1。
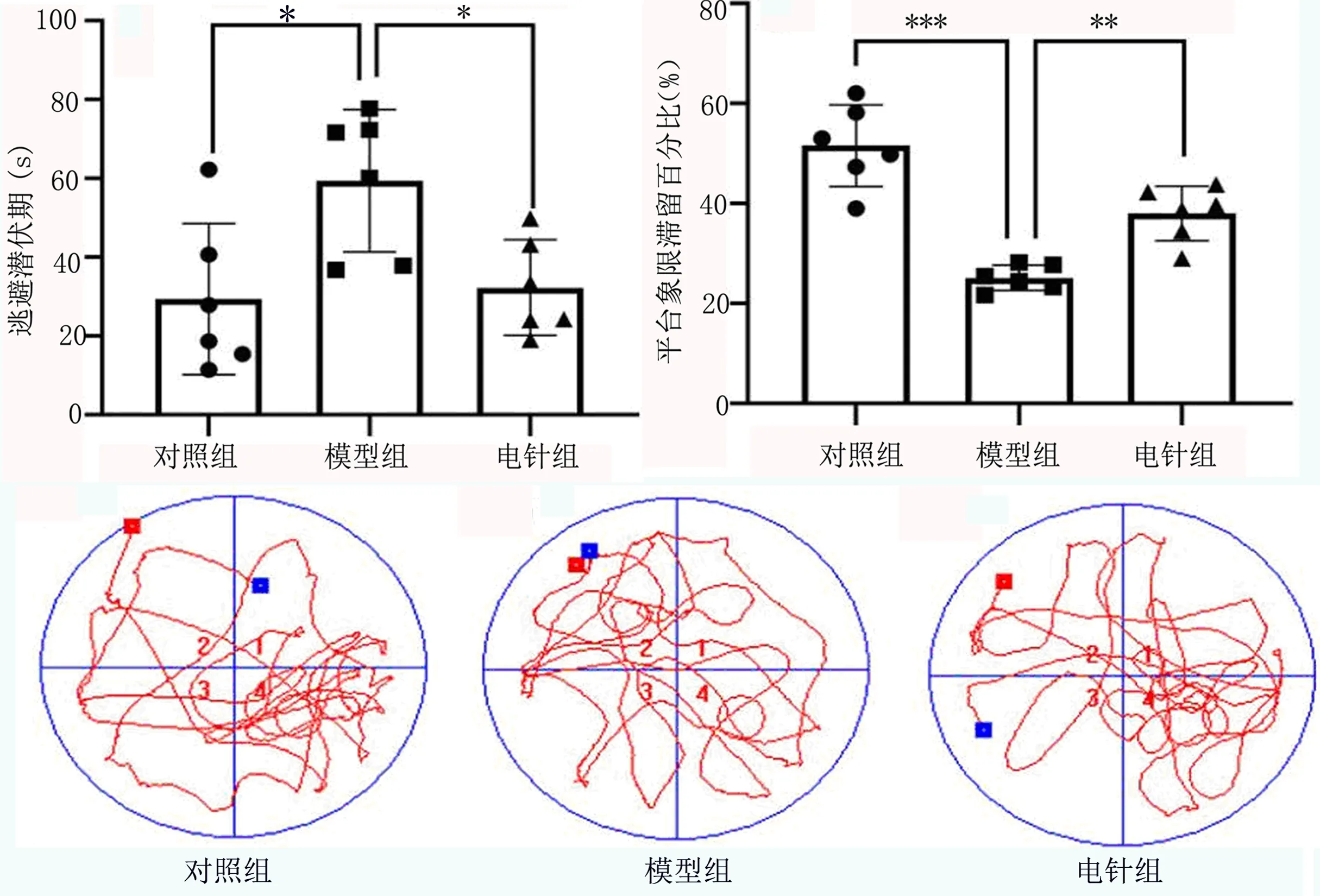
圖1 各組大鼠Morris水迷宮逃避潛伏期(s)和平臺象限滯留百分比(%)*P<0.05,**P<0.01,***P<0.001
2.2 尼氏染色觀察各組大鼠神經元的形態 對照組大鼠海馬CA1區神經細胞形態結構完整,細胞核多為圓形或橢圓形且呈淡紫色,核仁清晰可見,尼氏顆粒豐富散布在細胞質中。對于模型組大鼠來說,其細胞形態多呈空泡狀,神經元核仁固縮或消失,尼氏顆粒不明顯。與模型組相比,電針組海馬CA1區的異常形態學變化明顯減輕,數目減少明顯較少。見圖2。
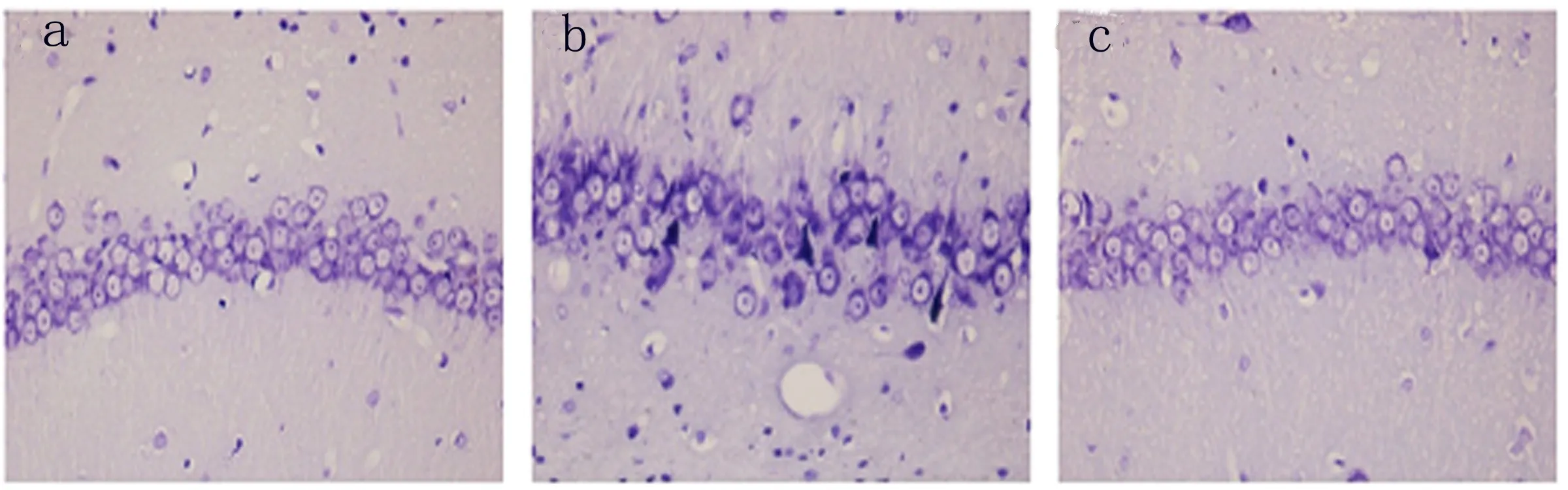
圖2 各組大鼠海馬CA1區尼氏染色結果 a.對照組 b.模型組 c.電針組
2.3 SIRT1和PGC1-α在各組大鼠海馬CA1區表達量的比較 由光學顯微鏡觀察正常大鼠海馬的CA1區可發現,其中含有大量的以胞膜呈棕黃色為特征的SIRT1陽性神經元與PGC1-α陽性神經元。對于SIRT1陽性神經元,觀察模型組,其SIRT1陽性神經元的數量明顯少于對照組(P<0.05),表現為細胞染色變淺,計算其灰度值均數與對照組相比也
有明顯的提高(P<0.05);而觀察治療后的電針組,其SIRT1陽性神經元的數量明顯多于模型組(P<0.05),免疫組化的染色效果也有一定程度的加深,其平均灰度值較模型組顯著降低(P<0.05),對于PGC1-α陽性神經元也有相同的數量、染色效果及平均灰度值的改變。見圖3。
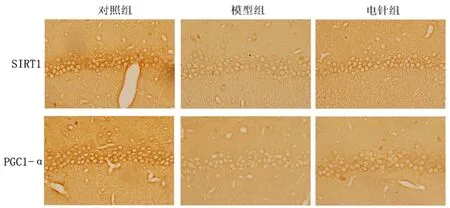

圖3 各組大鼠海馬CA1區SIRT1和PGC1-α的表達(免疫組織化學染色法,×400)與對照組相比,*P<0.05;與模型組相比,#P<0.05
3 討論
血管性癡呆(VD)的發生比例在逐年上升,慢性腦低灌注被認為是VD的重要危險因素[7]。腦卒中后慢性低灌注會導致腦血流量的下降,導致缺氧后的氧化應激使血管內皮細胞神經細胞等受損,使腦血流量下降進一步加重,這些腦血管病理變化將會導致VD[8]。海馬CA1區是人類學習和記憶的重要功能區,慢性腦低灌注時活性氧在腦中積累,導致神經元遭受破壞和中樞膽堿能功能的障礙,從而減少神經元的數量,海馬CA1區的功能發生障礙,導致VD患者的學習記憶等認知功能發生障礙[9]。在造模完成后,通過Morris水迷宮行為學測試并統計結果后發現,模型組大鼠的平均逃避潛伏期顯著高于對照組,且在撤去平臺后,模型組的原平臺象限滯留時間百分比遠低于對照組。
目前VD的主要治療方法是西醫治療,通過降低血糖、血壓、血脂,保護腦細胞和腦循環等藥物進行治療,并同時戒酒、戒煙,但上述治療的方法效果均不明顯[10]。針療法是指以毫針刺入腧穴部,使針刺部位產生一定的經氣感應后,將強度近似于人體生物電的微量脈沖電流接通在針上,通過針刺與電感雙重刺激穴位,使機體的脈絡氣息得以激發并調整,達到治療或預防疾病目的的一種方法。百會位于巔頂,是百脈聚會之處,具有醒腦開竅、補腦益智之效;足三里屬多氣多血之胃經,即可行氣血,又可補氣血;二穴合用,可行其氣,活其血,通督脈,調神志[11]。通過尼氏染色檢測海馬CA1區神經元的損傷情況顯示,與對照組相較,模型組大鼠海馬CA1區神經元陽性細胞數量減少,細胞多呈空泡狀,神經元核仁明顯固縮甚至消失,尼氏顆粒不明顯。而與模型組相較,電針組大鼠海馬神經元陽性細胞顯著提高,細胞空泡狀況有所改善,固縮的核仁減少,尼氏顆粒較明顯。該結果進一步證實了上述預測的結果。
膽堿能傳導通路的受損、炎性因子的過量表達、脂類代謝紊亂、遺傳基因表達異常、氧化應激損害等多種機制都可以導致海馬CA1區組織的損傷,進而引發VD[12],Sirt1在海馬CA1區神經元內的表達是其參與認知功能調節的物質基礎,同時也參與調節神經元的分化功能, PGC1-α是在對抗氧化應激中起到關鍵作用的轉錄調節因子,能夠起到消除自由基,提髙組織抗氧化能力的作用。SIRT1起到類似于一種屏障作用,它將PGC1-α去乙酰化后,有效阻止了蛋白酶體降解PGC1-α,并使靶基因持續產生激活。由此可推斷PGC1-α和Sirt1組成一調節系統,用于調節氧化應激導致的損傷反應,在VD恢復的生物學效應中起積極作用。本實驗中,通過免疫組化的結果可以發現,與對照組相比,模型組SIRT1和PGC1-α陽性神經元的數量明顯下降(P<0.05),通過分析發現,細胞的染色變淺,其平均灰度值與對照組相比也有明顯的提高(P<0.05),這與SIRT1通過去乙酰化促進PGC1-α水平這個觀點相一致。
VD大鼠海馬CA1區SIRT1的表達在電針的作用下可以上調,進而上調其下游的PGC1-α的表達,充分提高腦組織對氧化應激的抵抗反應,阻止血管性癡呆大鼠腦組織被破壞。根據電針組大鼠的免疫組化實驗結果,與模型組相比,PGC1-α陽性神經元的數量有所增加(P<0.05),同時可以分析出細胞染色變深,其平均灰度值也有明顯的降低(P<0.05),而其SIRT1陽性神經元的數量也多于模型組(P<0.05),細胞染色深,其平均灰度值與模型組相比有明顯的降低(P<0.05)這些結果顯示通過電針干預療法可以增加大鼠海馬CA1區中SIRT1的表達水平,進而促進了PGC1-α的表達水平,通過以上結果可以推測,通過電針法刺激穴位等一系列效果,使腦組織的抗氧化應激能力得到一定程度的增強,且可以修復由缺血而損傷的神經元。且由實驗數據可以表明,電針法的修復作用是由于促進SIRT1的表達效果,進一步增強PGC1-α的表達效應,改善了VD大鼠的學習認知能力及記憶功能,但就其具體通路機制而言,還需進一步研究。

