保元湯活性成分4’,7,8-三羥基二氫黃酮抑制過氧化氫誘導人臍靜脈內皮細胞損傷的作用機制研究
孟英心 張子歆 王凌瀟 馬家樂 靳鳳玉 王鑫玉 趙一慕 鄭姣 屠鵬飛
氧化應激損傷是多種心血管疾病的重要誘因,包括動脈粥樣硬化、心肌缺血再灌注損傷、心力衰竭等[1]。心血管疾病發(fā)病過程中,血液中的氧自由基和氧化低密度脂蛋白通過激活血管內皮表面的細胞信號通路刺激活性氧(reactive oxygen species,ROS)的產生誘發(fā)血管內皮細胞的過氧化損傷,從而導致動脈粥樣硬化,因此尋找安全有效的抗氧化先導化合物是目前藥物研發(fā)的熱點。保元湯最早記載于《博愛明鑒》,是根據(jù)李東垣的黃芪湯所更改得來,包含人參、黃芪、肉桂、甘草四味藥材,在中醫(yī)理論上具有大補元氣、治一切元氣虛弱之癥的功效[2]。
近幾年來保元湯在心血管疾病的臨床應用上有著確切療效[3]。本課題組前期對保元湯的化學成分做了系統(tǒng)的分離鑒定,共鑒定出皂苷類、黃酮類等236個化合物[4],其中甘草與黃芪中的大量黃酮類成分可能是保元湯抗氧化的藥效物質。通過前期篩選發(fā)現(xiàn)4',7,8-三羥基二氫黃酮(4',7,8-trihydroxydihydroflavonoid,TF)具有較強的抗氧化作用,因此本研究對TF改善人臍靜脈內皮細胞(human umbilical vein endothelial cells,HUVEC)的過氧化損傷進行了系統(tǒng)的研究,以期闡明保元湯抗氧化的藥效物質和作用機制,為其治療心血管疾病的臨床應用提供理論基礎。
1 材料與方法
1.1 保元湯處方與飲片
保元湯由黃芪(Astragalusmembranaceus(Fisch.)Bge.),人參(PanaxginsengC. A. Mey.),甘草(GlycyrrhizauralensisFisch.)和肉桂(CinnamomumcassiaPresl)以6∶2∶2∶1的比例混合而成。原料藥材于河北省安國藥材市場購買,由屠鵬飛教授鑒定。TF從保元湯總提物中分離得到(圖1),純度大于98%。
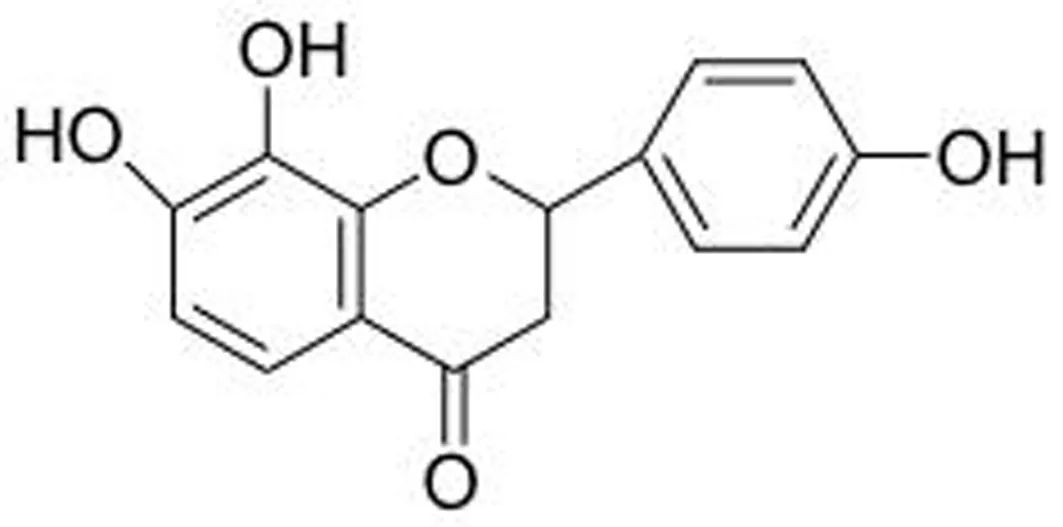
圖1 4’,7,8-三羥基二氫黃酮的化學結構式
1.2 TF的提取與分離
取黃芪飲片30 kg,人參藥材10 kg,炙甘草飲片10 kg,肉桂藥材5 kg,混合,以10倍量去離子水煎煮三次,每次2小時,過濾,合并濾液,減壓濃縮保元湯至密度約為1.10 kg/L,離心得保元湯提取液。保元湯提取液經AB-8型大孔吸附樹脂純化,依次用3倍柱體積的水和不同濃度的乙醇(15%、30%、50%和95%乙醇)洗脫,收集50%乙醇洗脫液,減壓濃縮,干燥,即得50%乙醇洗脫部位(623.4 g)。50%乙醇洗脫部位經硅膠(100~200目)柱色譜分離,氯仿-甲醇-水(95∶5∶0.5,90∶10∶1,85∶15∶1.5,80∶20∶2,70∶30∶3)梯度洗脫,TLC檢測,合并得10個流分(A-J)。G(2.5 g)再經硅膠柱色譜分離,氯仿-甲醇-水(85∶15∶1.5)洗脫,TLC檢測,合并得3個流分(G1-G3)。G3(729 mg)經反相柱色譜分離,甲醇-水(5∶95→70∶30)梯度洗脫,得到化合物TF(10 mg)。保元湯活性化合物的分離,以及4’,7,8 -三羥基二氫黃酮的結構鑒定由北京大學藥學院研究生馬曉麗完成。
1.3 主要試劑與儀器
DMEM培養(yǎng)基(批號:11965092)、青霉素-鏈霉素(批號:15140163)、胎牛血清(批號:12483020)、磷酸鹽緩沖液(phosphate buffer saline,PBS)(批號:20012050)、胰酶(批號:25200072)均購自美國Gibco公司;維生素C(批號:B21293)購自上海源葉生物科技有限公司;CCK-8試劑盒(批號:BN15201)購自北京拜爾迪生物技術有限公司;活性氧檢測試劑盒(批號:S0033S)、總抗氧化能力檢測試劑盒(ABTS法)(批號:S0119)、RIPA裂解液(批號:P0013B)均購自上海碧云天生物技術有限公司;PARP(批號:60004-1-Ig)、β-actin(批號:60004-1-Ig)、GAPDH(批號:60004-1-Ig)、P-Akt(批號:66444-1-Ig)、Bcl-2(批號:60178-1-Ig)均購自美國Proteintech公司。
多功能酶標儀(美國PerkinElmer公司);冷凍離心機(美國Eppendorf公司);CriterionTM型電泳槽(美國Bio-Rad公司);DYY-6D型電泳儀(北京六一儀器廠);細胞培養(yǎng)箱(日本SANYO公司);倒置熒光顯微鏡(德國Leica公司)
1.4 細胞培養(yǎng)
人臍靜脈內皮細胞(human umbilical vein endothelial cells,HUVEC)由北京大學曾克武教授贈予。HUVEC采用含10%滅活胎牛血清,1%的青霉素-鏈霉素雙抗的DMEM培養(yǎng)基,置于37℃,5% CO2細胞培養(yǎng)箱中培養(yǎng),隔天更換1次培養(yǎng)基,取對數(shù)生長期的細胞后,取1 mL胰酶于培養(yǎng)箱中消化細胞1分鐘左右;終止消化后收集細胞,800 r/min離心5分鐘,棄上清,加入完全培養(yǎng)液,適當比例傳于培養(yǎng)瓶中繼續(xù)培養(yǎng)。
1.5 H2O2誘導的HUVEC氧化損傷模型建立
實驗分為對照組和H2O2處理組(給予不同濃度的H2O2),每組每濃度設置六個復孔。HUVEC細胞以5×103個/孔均勻接種于96孔板,生長24小時后,對照組用完全培養(yǎng)基正常培養(yǎng)HUVEC細胞;H2O2處理組每孔加入DMEM培養(yǎng)基和終濃度分別為10 μmol/L、20 μmol/L、30 μmol/L、40 μmol/L、50 μmol/L、60 μmol/L的H2O2,孵育1小時。取出以CCK-8試劑稀釋10倍,每孔加入100 μL,置于37℃含5% CO2的培養(yǎng)箱中培養(yǎng)2小時后,利用酶標儀在490 nm波長處測定各孔OD值。
1.6 TF對H2O2損傷HUVEC存活率的影響
取對數(shù)生長期HUVEC細胞以5×103個/孔均勻接種于96孔板,生長24小時后,設置對照組、模型組、TF低、中、高劑量組(終濃度分別為5 μmol/L、10 μmol/L、20 μmol/L),每組設置六個復孔。對照組加入完全培養(yǎng)基,不做任何處理。TF低、中、高劑量組處理細胞6小時后,再分別用終濃度為15 μmol/L、30 μmol/L的H2O2刺激細胞1小時。細胞加入CCK-8試劑并置于37℃含5% CO2的培養(yǎng)箱中培養(yǎng)2小時后,利用酶標儀在490 nm波長處測定各孔OD值。
按照以上分組方法,TF預處理細胞6小時后,對模型組與TF低、中、高劑量組以終濃度為20 μmol/L的H2O2處理細胞1小時,置于顯微鏡下觀察HUVEC細胞的數(shù)量及形態(tài)學變化。
1.7 檢測指標
1.7.1 檢測細胞內ROS 按照1.6項下方法接種細胞、分組、造模及給藥。根據(jù)DCF-DA試劑盒操作方法測定ROS。
1.7.2 TF對DPPH自由基體外清除的測定 根據(jù)文獻報道的方法[5]測定TF對DPPH自由基的清除活性。取2 mL 0.16 mmol/L DPPH自由基溶液分別加入到2 mL不同濃度的TF溶液中(10 μmol/L、20 μmol/L、50 μmol/L、100 μmol/L),每組設置六個復孔。在室溫下避光30分鐘后。在517 nm下測量反應混合物的OD值,溶液褪色程度與藥物清除自由基活性呈正相關,并以天然抗氧化劑維生素C用作陽性對照。
1.7.3 蛋白免疫印跡法(Western Blot)檢測細胞凋亡相關蛋白表達情況 HUVEC細胞按常規(guī)方法培養(yǎng),取對數(shù)生長期細胞以5×103個/孔均勻接種于12孔板,設置對照組、模型組、TF低、中、高劑量組(終濃度分別為5 μmol/L、10 μmol/L、20 μmol/L)。對照組加入完全培養(yǎng)基,不做任何處理。TF低、中、高劑量組處理細胞6小時后,再以終濃度為20 μmol/L的H2O2處理1小時。收集細胞,加入4℃預冷的SDS細胞裂解液100 μL充分裂解后離心制備蛋白樣品。在10% SDS-聚丙烯酰胺凝膠上電泳分離蛋白質樣品并轉移到PVDF膜上。用TBST配制的5%脫脂乳封閉2小時后,將膜與一抗在4℃下孵育過夜,洗滌印跡并與二抗在室溫下孵育2小時,將膜再次用TBST洗滌3次,使用ECL試劑對蛋白質條帶進行可視化,并用Image J軟件進行定量。
1.8 數(shù)據(jù)處理
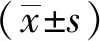
2 結果
2.1 H2O2對HUVEC細胞存活率的影響
通過CCK-8實驗來檢測H2O2濃度對HUVEC細胞損傷的影響,結果顯示與對照組比較,H2O2處理組細胞的存活率明顯降低(P<0.05),IC50=(19.86±0.98)μmol/L,因此本研究后續(xù)實驗選擇15 μmol/L和30 μmol/L濃度的H2O2損傷HUVEC細胞。見表1。
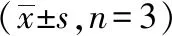
表1 CCK-8法檢測不同濃度的H2O2對HUVEC細胞存活率的影響
2.2 TF對H2O2損傷HUVEC細胞存活率的影響
使用15 μmol/L的H2O2損傷HUVEC細胞后,與對照組相比,模型組HUVEC細胞存活率降低至(76.30±5.31)%(P<0.05),中、高劑量TF給藥后均顯著提高細胞存活率(P<0.01),分別提高(27.42±2.81)%和(42.30±1.41)%。見表2。
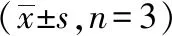
表2 TF對15 μmol/L H2O2誘導的HUVEC細胞存活率的影響
使用30 μmol/L H2O2損傷HUVEC細胞后,與對照組相比,模型組HUVEC細胞存活率降低至(23.90±0.59)%(P<0.05),中、高劑量TF給藥后均顯著提高細胞存活率(P<0.05),分別提高(63.72±12.01)%和(146.43±8.80)%。見表3。
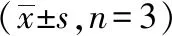
表3 TF對30 μmol/L H2O2誘導的HUVEC細胞存活率的影響
細胞形態(tài)學觀察結果顯示,終濃度為20 μmol/L的H2O2處理細胞后,細胞數(shù)量大量減少,胞體邊緣模糊,折光性減弱,貼壁能力降低。20 μmol/L濃度TF給藥后,HUVEC細胞數(shù)量較模型組顯著上升,細胞折光性及貼壁功能恢復良好。綜上得出,TF預處理能夠抑制H2O2所致的HUVEC的氧化應激損傷。見圖2。

注: A 對照組; B 模型組; C TF低劑量組; D TF中劑量組; E TF高劑量組
2.3 TF對H2O2損傷HUVEC細胞ROS水平的影響
DCFH-DA熒光探針可以在細胞內水解生成DCFH,進而被細胞內的ROS氧化,生成可以產生綠色熒光的DCF。當細胞受到氧化損傷,細胞內的ROS含量增加,熒光強度會增加。模型組用20 μmol/L的H2O2造模,與模型組相比較,TF低、中、高劑量組綠色熒光逐漸減弱,顯示細胞內ROS水平減少,且呈劑量依賴性。綜上,TF預處理能夠降低HUVEC細胞ROS水平。見圖3。
注: A 模型組; B TF低劑量組; C TF中劑量組; D TF高劑量組
2.4 TF對DPPH自由基的清除作用
通過DPPH自由基清除實驗,驗證TF對自由基的體外清除作用。實驗結果發(fā)現(xiàn),終濃度10 μmol/L的TF就可顯著增加自由基的清除(P<0.05),終濃度達到100 μmol/L時自由基清除率可達到(93.69±1.06)%,與相同劑量陽性藥維生素C的自由基清除效果相似,表明TF具有良好的自由基清除活性。見表4。
2.5 TF對HUVEC細胞凋亡相關蛋白表達的影響
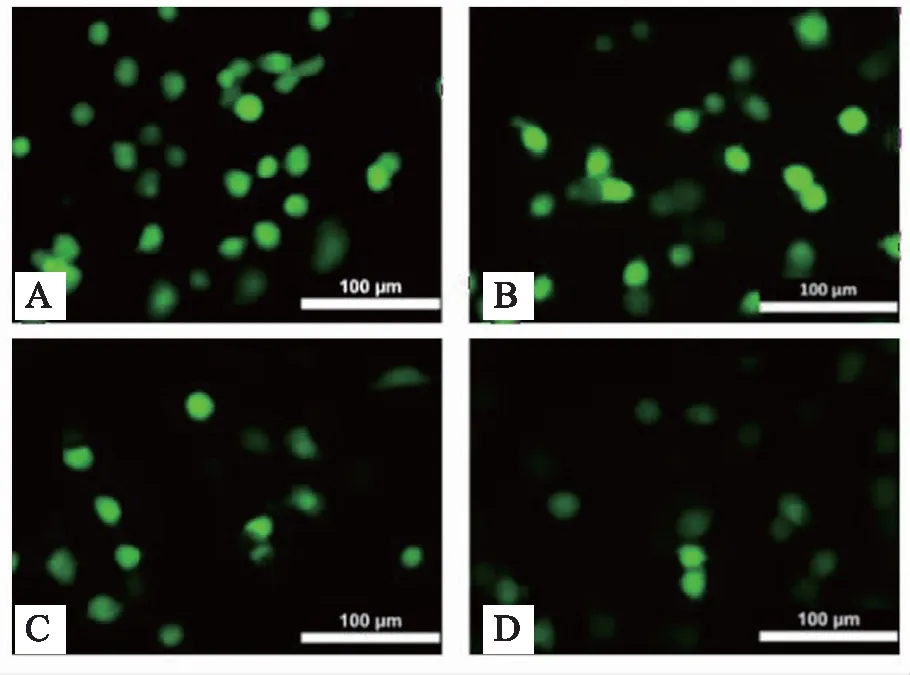
20 μmol/L劑量H2O2損傷細胞后,HUVEC細胞中磷酸化蛋白激酶B(phosphorylated protein kinase B,P-Akt)、B淋巴細胞瘤-2(B-cell lymphoma-2,Bcl-2)以及腺苷二磷酸核糖聚合酶(poly adenosinedip-hosphate-ribose polymerase,PARP)的含量顯著降低(P<0.05) ,而Cleaved PARP的含量顯著增加(P<0.05), 表明細胞凋亡程度增強。 TF給藥后,能劑量依賴地增加P-Akt和Bcl-2的含量,抑制PARP蛋白的裂解,較模型組具有顯著性差異(P<0.05)。結果證實TF通過P-Akt調控PARP的裂解,從而改善HUVEC細胞凋亡。結果見圖4,表5。
表4 TF對H2O2誘導的HUVEC細胞DPPH自由基清除的影響
圖4 TF對H2O2誘導后的HUVEC細胞中凋亡相關蛋白表達的影響
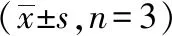
表5 TF對H2O2誘導后的HUVEC細胞中P-Akt、Bcl-2、Cleaved PARP、PARP表達的影響
3 討論
血管內皮細胞功能障礙是心血管疾病最重要的病理改變之一,可導致包括動脈粥樣硬化在內的心血管疾病的形成和發(fā)展[6]。因此,從中草藥中篩選出具有內皮細胞保護作用的活性先導化合物具有重要的臨床意義[7]。根據(jù)記載保元湯可保守真元之氣,提高免疫,延緩衰老,且已被證明有抗氧化作用[8-9],本課題組前期篩選了保元湯中的藥物,實驗結果顯示TF的抗氧化性最佳,因此選擇該藥物進行進一步的實驗。
氧化應激是指活性氮自由基或ROS等高活性酶的過量產生,導致蛋白質變性、生物膜脂質過氧化、DNA損傷、細胞凋亡或壞死。H2O2已被廣泛用于刺激不同細胞類型的氧化應激[10]。這種非自由基氧化劑和可擴散分子已被認為是內皮細胞中促凋亡和促壞死的氧化介質,不同濃度和孵育時間已經用于評估不同研究中的H2O2細胞毒性[11-12],CCK-8法檢測顯示,用15 μmol/L和30 μmol/L的H2O2處理HUVEC細胞1小時,HUVEC細胞存活率明顯降低至45%~55%,并具有一定的劑量依賴性,造模條件穩(wěn)定,因此確定此條件進行后續(xù)實驗研究。本研究通過CCK-8法檢測HUVEC細胞存活率,發(fā)現(xiàn)TF給藥后,細胞存活率呈濃度依賴性提高,提示TF對H2O2誘導的氧化損傷有良好的保護作用。在本研究中,本課題組發(fā)現(xiàn)H2O2顯著誘導HUVEC中ROS的形成,而TF實驗組逆轉了H2O2對ROS形成的促進作用,說明TF可能通過抑制ROS的形成來發(fā)揮其抗氧化作用。
本文進一步研究了TF對DPPH自由基的清除作用,發(fā)現(xiàn)TF可以通過清除自由基DPPH發(fā)揮抗氧化作用。為了繼續(xù)探究TF抑制H2O2誘導HUVEC細胞損傷的作用機制,本課題組評估了TF對HUVEC細胞凋亡相關蛋白表達的影響。Akt是一種絲氨酸/蘇氨酸蛋白激酶,在細胞凋亡的過程中起到著重要的作用,當磷脂酰肌醇-3激酶被激活時,Akt會被細胞外因子激活,發(fā)生構象改變,暴露其磷酸化位點,形成P-Akt[13]。P-Akt被激活后,線粒體途徑的Bcl-2也會被激活。Bcl-2屬于抗凋亡蛋白,過量表達可以改變線粒體膜的通透性,抑制巨孔形成,防止細胞色素c從線粒體中釋放,抑制細胞凋亡[14]。PARP是一種DNA修復酶,對DNA的損傷修復以及細胞凋亡起著重要的作用,受到上游P-Akt與Bcl-2的調控[15]。為了進一步探討TF對H2O2所致的HUVEC損傷細胞的保護作用,本實驗通過Western Blot法觀察了不同處理后P-Akt、Bcl-2以及PARP表達量,結果表明TF預處理可以顯著改善H2O2所致的HUVEC細胞內P-Akt、Bcl-2以及PARP的表達異常。綜上所述保元湯中的單體化合物TF可以通過調控P-Akt/PARP/Bcl-2通路抑制HUVEC細胞的凋亡,從而改善血管內皮細胞的過氧化損傷,因此,TF可能是一種很有前景的抗氧化損傷和氧化應激相關心血管疾病的藥物。
保元湯是治療元氣虛弱的經典名方,臨床上應用于心血管疾病的治療,療效確切,安全性好。在前期的研究中,研究人員更加集中于其臨床療效的探索,而缺乏物質基礎跟藥理學方面的研究。本研究在前期對分離鑒定出的保元湯的化學成分活性篩選的基礎上,發(fā)現(xiàn)保元湯中的化學成分TF具有較強的抗氧化作用,通過血管內皮細胞HUVEC的過氧化損傷模型,明確了TF改善血管內皮細胞過氧化損傷的作用機制,發(fā)現(xiàn)了保元湯保護血管內皮細胞的藥效物質,為其臨床應用提供理論依據(jù)。

