經導管緣對緣技術(MitraClip)治療二尖瓣反流
——亞太心臟病學會(APSC)專家共識
亞太心臟病學會(APSC)專家組
經導管二尖瓣緣對緣修復技術(代表器械:MitraClip)是一項基于導管、經皮介入的緣對緣修復技術,該技術通過夾合反流性二尖瓣的前瓣和后瓣,以糾正二尖瓣反流(MR)。EVEREST Ⅱ高危注冊登記和亞洲注冊登記研究的數據已經證明了MitraClip的可行性與安全性[1-3]。
MITRA-FR 和COAPT 隨機對照試驗已經充分評估了MitraClip 的臨床應用。這兩項研究都納入了合并心力衰竭[盡管接受了指南推薦的最佳藥物治療——即指南指導的管理與(最佳內科)治療(GDMT)后仍有心力衰竭,NYHA 分級≥Ⅱ級]的中-重度或重度繼發MR 患者。這些患者在內科藥物治療基礎上分為——MitraClip 植入組和非手術干預對照組。MITRA-FR 臨床試驗結果顯示,在復合主要終點事件方面(即全因死亡率和12 個月內計劃外心力衰竭住院率),MitraClip 植入組和非手術干預對照組并未顯示顯著的統計學差異(MitraClip 植入組54.6% vs.非手術干預對照組51.3%,P=0.53)[4],而COAPT臨床試驗由于更嚴格的納入標準和更好的二尖瓣介入修復效果等原因,患者治療后24 個月內因心力衰竭再入院的主要終點事件統計結果顯示,MitraClip植入組發生率顯著低于非手術干預對照組(35.8% vs.67.9%,P≤ 0.001)[5]。因此,2020 年美國心臟協會/美國心臟病學會(AHA/ACC)指南推薦MitraClip 可以應用于外科極高風險或外科禁忌的退行性二尖瓣反流(degenerative mitral regurgitation,DMR)患者[6]。
亞太地區專家共識同AHA/ACC 推薦一致,MitraClip 目前適應證為外科手術高危或禁忌的患者。但實際臨床實踐過程中,仍有很多中危或者低危的亞洲患者拒絕接受外科治療[3]。對于這些患者,MitraClip 可能是一個合理的治療選擇;但是對比西方國家,針對亞洲人群的MitraClip 相關研究數據依然有限[7]。MitraClip 亞太注冊登記(MARS)是一項多中心回顧性注冊研究,包含了五個亞太國家在內共計八個臨床中心。該研究報道了MitraClip 在亞洲的早期結果,納入了從2011 年2 月到2013 年10 月進行MitraClip 手術的142 例患者,結果顯示即刻手術成功率為93.7%[2]。
由于亞太地區關于MitraClip 的臨床研究提供的證據有限,亞太心臟病學會(APSC)由此提出本共識,以提供亞太地區MitraClip 治療MR 的專家性指導意見。此共識聲明旨在指導心臟專科醫師治療MR 及評估患者進行MitraClip 修復的可行性。需要注意的是,本共識旨在提供參考而非完全代替臨床決策。
1 方法
APSC組織了包含26 名資深瓣膜介入醫師在內的專家組,回顧了MitraClip 用于MR 治療的現有文獻,并討論現階段管理方法存在的不足,概述今后仍需補充的指導部分,并起草了關于MitraClip 使用的共識。本次邀請的專家都是APSC 的主要成員,由各個國家協會所推薦。參與起草本共識的專家均得到APSC 共識委員會的認可。為了制定共識意見,專家組決定改編美國心臟超聲協會指南中關于彩色多普勒超聲心動圖的相關標準,這些超聲參數將側重識別適合使用MitraClip 進行治療的嚴重MR 患者(圖1),并以此作為共識討論會中的統一定義[8]。
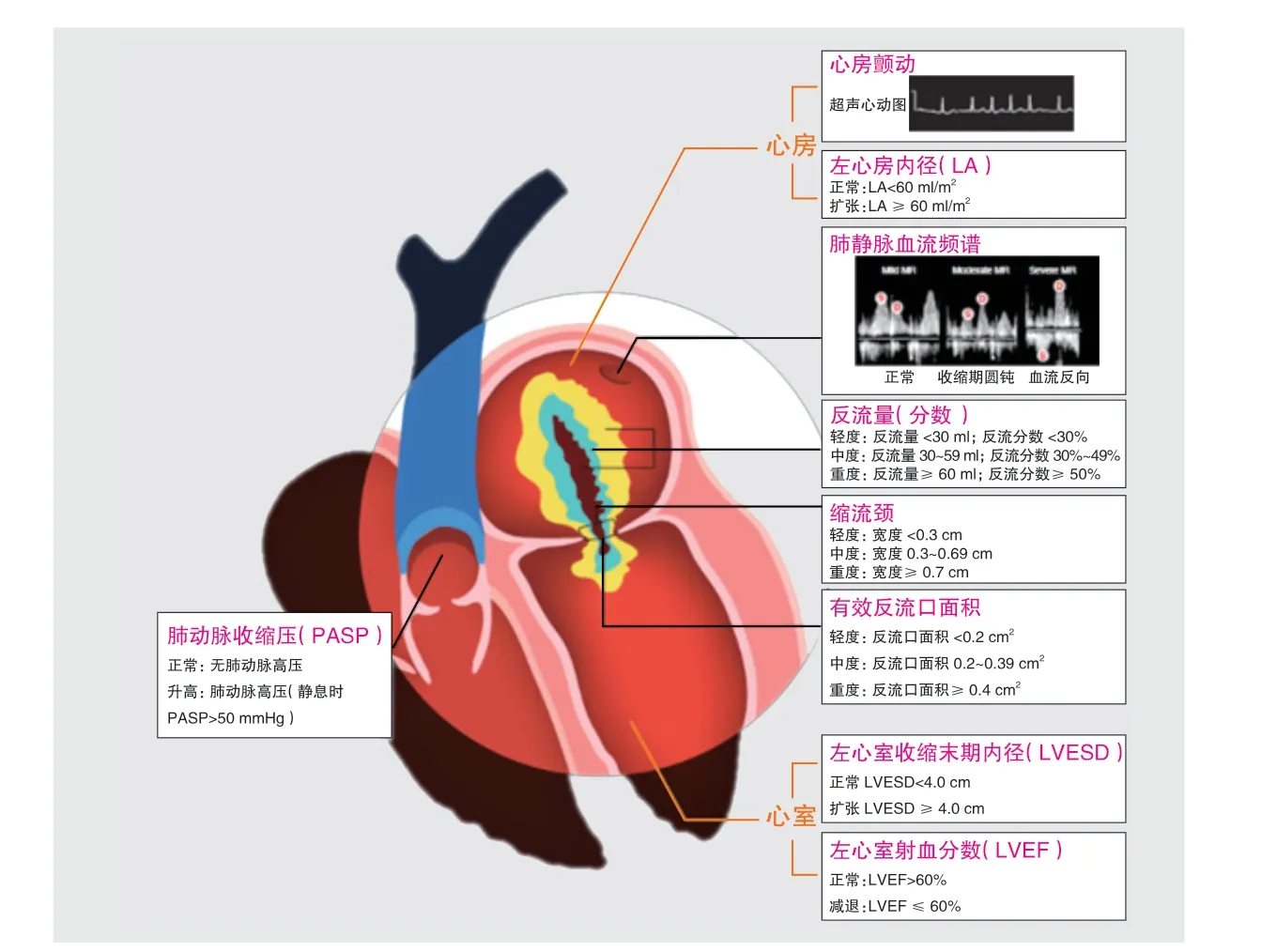
圖1 評估二尖瓣反流的超聲心動圖參數示意圖
專家組進行了全面的文獻檢索,尤其關注以亞洲人群為中心的研究。對共識采納的文章和綜述,采 用Grading of Recommendations Assessment,Development,and Evaluation(GRADE)系統進行證據級別評價,評價后的文獻被分為以下幾類:(1)高質量(文章作者確信真實效應與預估效應相似);(2)中等質量(作者認為真實效應有可能與預估效應相類似);(3)低質量(真實效應有可能與預估效應顯著不同);(4)極低質量(真實效應很有可能與預估效應顯著不同)[9]。專家委員會分別于2020 年1月18 日和2020 年6 月27 日召開的兩次共識會議中討論了目前可用的研究證據。
兩次共識會議中制定了關于MitraClip 在DMR、功能性二尖瓣反流(function mitral regurgitation,FMR)和其他MR 中的適應證,以及在亞太地區應用指征的建議。大會制定的每一項聲明條例都進行了線上投票,并采用三種選項的投票表決模式(同意,中立,不同意)。當一項決議被80%專家投以“同意”或“中立”時,被認為是一致性聲明。專家組通過電子郵件聯系的方式對非一致性聲明進行逐條修改,直至每一項共識建議達成一致意見。
2 共識建議
2.1 MitraClip 在DMR 中的應用
DMR 是指二尖瓣器的某一個部分(瓣葉、腱索、或乳頭肌)受到了影響。退行性二尖瓣疾病是導致DMR 的常見病因,瓣膜結締組織的形態隨疾病發展而發生變化,最終導致了MR[10-11]。纖維彈性組織缺乏或彌漫性黏液樣病變很可能是導致DMR 的重要原因[12-13]。DMR 有可能展現多種解剖病變形式,這些病變形式包括單瓣葉脫垂、雙瓣葉脫垂以及瓣環擴張[10]。
外科二尖瓣修復或置換仍是DMR 治療的金標準,然而,某一亞組患者可能從經導管治療中獲益[7,9,14-15]。MARS 的數據發現,DMR組患者的即刻手術成功率為92%[3];術后30 天主要不良事件發生率為14.7%,與FMR組的患者比較,差異沒有統計學意義(9.2%,P=0.555)。FMR組與DMR組的患者術后30 天MR 程度和NYHA 心功能均得到顯著改善;與DMR組患者相比,FMR組左心室舒張末期內徑(P=0.002)和收縮末期內徑(P=0.017)有更顯著的降低。
除此之外,AVJ-514 試驗也提供了亞洲地區的證據以支持MitraClip 在DMR 患者中的應用。AVJ-514 是一個前瞻性、多中心的單臂研究,納入的患者為有癥狀、慢性、中重度(3+)或重度(4+)DMR(n=16)或FMR(n=14)。在DMR 患者中,即刻手術成功率為87.5%,有81.3%的患者在術后30 天MR 分級≤2+[16]。NYHA 心功能分級為Ⅲ/Ⅳ患者比例從37.5%降低到6.3%,沒有死亡病例。
共識聲明 1
具備手術指征但被心臟團隊判定為外科高危且DMR ≥3+的患者,無論是否存在臨床癥狀,都應該考慮進行MitraClip 治療。
證據等級:中
一致性:同意80%;中立16%;不同意4%
共識聲明2
有癥狀、高危、≥3+DMR、伴或不伴左心室射血分數(LVEF)降低的患者應考慮MitraClip治療。
證據等級:中
一致性:同意84%;中立12%;不同意4%
共識聲明3
無癥狀、高危、≥3+DMR,同時伴有以下情況的患者應考慮MitraClip 治療:
·LVEF 降低和(或)左心室擴張;或
·新發心房顫動或肺動脈高壓
證據等級:低
一致性:同意84%;中立16%;不同意0%
本專家組同意向以下患者推薦MitraClip 手術:高風險、有癥狀的嚴重DMR,伴或不伴有LVEF降低;高風險、無癥狀的嚴重DMR 且有LVEF 降低和左心室擴張;或者有新發心房顫動或肺動脈高壓,滿足外科手術指征但被心臟團隊定義為外科手術高危。但是,部分專家強調無癥狀患者的臨床數據存在缺失,因此降低了這個亞組證據等級。針對聲明1 的反對意見指出,只有無癥狀、有禁忌的高風險患者才應該考慮進行MitraClip 治療。針對聲明2 的反對意見表示,這樣的患者應該首先考慮手術治療,MitraClip 治療應該被限定于外科高危的患者。
盡管部分專家陳述了患者應在疾病早期進行治療,而不是等到心功能惡化或嚴重心肌重構之后,專家小組的整體意見認為沒有理由干預重度DMR、無癥狀、無左心室擴張、LVEF 依舊正常的患者(除非有新發心房顫動或者肺動脈高壓)。這些患者應該持續密切隨訪。
2.2 MitraClip 在FMR 的應用
共識聲明4
對于已經接受GDMT 仍有癥狀的FMR(≥3+)患者可考慮使用MitraClip。FMR 患者在接受進一步干預或應用MitraClip 的評估前,需要接受至少1 個月的最優GDMT,同時合理嘗試負荷劑量藥物治療,有指征的患者可接受心臟再同步化治療和心臟再同步化治療除顫器(CRT-D)。
證據等級:高
一致性:同意88%;中立8%;不同意4%
共識聲明5
對 于 缺 血 性FMR(≥3+),考 慮MitraClip 治療前需進行冠狀動脈解剖、缺血情況評估以及可能的再血管化治療。如果采用經皮冠狀動脈介入治療進行再血管化,應考慮擇期MitraClip治療。如果采用冠狀動脈旁路移植手術(CABG)進行再血管化,可考慮手術同期行二尖瓣成形手術或二尖瓣置換手術。
證據等級:低
一致性:同意100%;中立0%;不同意0%
共識聲明6
FMR 患者需要定期隨訪(如每6 個月),并盡早轉交給心臟團隊(包括MitraClip 專科醫師、心力衰竭專科醫師、彩色多普勒超聲心動圖醫師和外科醫師)進行干預,干預的措施包括MitraClip 植入。患者能否從MitraClip 治療中獲益應交由心臟團隊進行決策。
證據等級:低
一致性:同意100%;中立0%;不同意0%
共識聲明7
有癥狀的FMR ≥3+患者應由心臟團隊評估MitraClip 植入的可行性。
證據等級:高
一致性:同意100%;中立0%;不同意0%
共識聲明8
對于未達到MitraClip 植入適應證的FMR 患者(例如無癥狀患者,MR 嚴重程度≤2+,未進行最優GDMT 的患者),需要密切隨訪。這些患者一旦達到適應證標準,需考慮MitraClip 植入。
證據等級:低
一致性:同意100%;中立0%;不同意0%
在FMR 患者中,二尖瓣器的結構仍是完整的,但通常由于心室或瓣環擴大,導致瓣葉對合不良,最終造成MR[11]。FMR 的患者常有左心室功能不全,其中多數患者因合并癥,如高血壓、高血脂、心房顫動、冠狀動脈疾病和心力衰竭,需要接受藥物治療。指南推薦在治療MR 的同時,對這些原發病變情況應進行充分治療,包括有指征時使用心臟再同步化治療和CRT-D[14]。
在亞洲FMR 患者中,66%的患者屬于缺血性二尖瓣關閉不全[3]。因此,評估心肌缺血程度是評價患者的關鍵步驟。雖然冠狀動脈CT 影像及其它方法在某些特定患者中可獲得滿意結果,冠狀動脈造影仍是評估心肌缺血首選的方法。可糾正的缺血性疾病應得到充分治療(如再血管化及內科保守治療);對于糾正缺血病因后仍殘余嚴重癥狀FMR(≥3+)的患者可考慮MitraClip。
由EVEREST Ⅱ試驗首次提出,MitraClip 是有癥狀FMR 患者可選擇的合適治療方案[1]。COAPT最終的試驗結果也證明,接受MitraClip 治療的中-重度(3+)或重度(4+)繼發MR 患者,相比于對照組,在24 個月內有著更低的因心力衰竭住院率(主要 終 點,35.8% vs.67.9%,P<0.001)[5]。MitraClip組的全因死亡率也明顯更低(29.1% vs.46.1%,P<0.001)。在次要終點方面,如生活質量、功能儲備、MR 程度及左心室重塑,MitraClip組相比于對照組也均有優勢。COAPT 研究以后,由于介入緣對緣技術的優異結果,國際范圍內罕有關于FMR 患者進行二尖瓣緣對緣修復的新隨機對照研究。
在MITRA-FR 試驗中,復合主要終點包括12 個月內全因死亡及計劃外因心力衰竭再次住院。相比對照組,試驗組在復合主要終點方面并未顯現出顯著差異[4]。通過后期數據分析,雖然COAPT 試驗和MITRA-FR 試驗納入了相似的FMR患者群體,但兩項研究在患者選擇上存在一些關鍵差異,這些差異對正確選擇MitraClip 患者有指導意義,也可以解釋兩項研究結果的不同。首先,與MITRA-FR 研究相比,COAPT 研究被認為是一項更有力的研究,研究設置了中心委員會,有更大(幾乎兩倍)的樣本量,詳盡的超聲心動圖和功能檢查(如6 分鐘步行試驗)隨訪,并且在入組前要求患者達到最大劑量的GDMT。其次,COAPT研究比MITRA-FR 研究報道了更高的手術成功率以及更低的并發癥發生率。第三,COAPT 研究及MITRA-FR 研究評估MR 嚴重程度的標準也不相同,COAPT 研究采用了更嚴格的標準評估重度MR。最后,也可能是最重要的,COAPT 研究納入了更多不成比例的嚴重MR 患者,而MITRA-FR研究納入的患者有更多成比例的MR。不成比例的MR 這一概念,首次由Grayburn 等[17]描述,超出了本篇共識的討論范圍。簡而言之,不成比例的MR 指的是MR 程度比左心室容積變化所反映的情況更嚴重。這說明MR 是導致潛在心力衰竭加重的一個重要因素。
根據ACCESS-EU 注冊研究,其中納入了以FMR 為主的患者(77%是FMR),12 個月時MR 嚴重程度較基線有所改善(P<0.0001),78.9%的患者在12 個月時MR ≤2+[18]。6 分鐘步行試驗提高了(59.5 ± 112.4)m,1 年生存率是81.8%。MARS 注冊研究也報道了MitraClip 治療FMR 的即刻手術成功率為95.5%[3]。AVJ-514 試驗納入了14 例FMR患者,即刻手術成功率為 85.7%,30 天后MR 程度≤2+的患者占92.9%。NYHA 心功能Ⅲ/Ⅳ級的患者比例從35.7%減至0.0%[1,16],并且沒有死亡病例報道。
對于FMR 患者,專家組建議,滿足最優劑量的藥物治療至少1 個月,并在符合適應證的情況下已CRT-D,就可以考慮使用MitraClip。雖然部分專家推薦接受GDMT 的患者至少觀察3 個月,但COAPT 的數據指出患有嚴重疾病的患者不應進行不必要的等待。
對于可能接受MitraClip 治療的FMR 患者,應由心內科醫師規律隨訪超聲心動圖,一旦符合適應證(如有癥狀的中-重度MR),立刻轉交給心臟團隊(MitraClip 專科醫師、心力衰竭專科醫師、彩色多普勒超聲心動圖醫師和外科醫師)。同時,對于伴有左心室功能不全的患者需密切監測隨訪。
專家組推薦應用經食道超聲心動圖(trans-esophageal echocardiography,TEE)明確MR 病因,而經胸超聲心動圖(TTE)適合評估病例的嚴重程度。因為鎮靜期間,TEE 可能受血流動力學變化的影響。只有當使用TTE 有困難的情況下(如圖像顯示不清晰),TEE 可以獨立使用以評估病情。
在決定最佳治療策略時,心臟團隊應該考慮外科手術風險,但需要注意的是外科手術風險并不是MitraClip 手術成功或失敗的預測因素。如需行外科CABG,可以考慮同期行外科二尖瓣手術[14]。相反,對于不考慮進行外科手術的伴有左心室功能不全的嚴重FMR 患者,可考慮MitraClip。圖2 展示了≥3+FMR 患者評估及初期管理的流程圖。

圖2 ≥3+FMR 患者評估及初期管理的流程
此外,專家概述了使用MitraClip 治療DMR 和FMR 的注意事項(表1)。

表1 使用MitraClip 治療二尖瓣反流的注意事項
MitraClip 近來推出了第四代“G4”設備,擴增到了4 種不同臂長及臂寬的Clip 規格(NTR,NTW,XTR,XTW),增加了獨立瓣葉捕獲的特性以及實時左心房壓監測的功能[19-20]。G4 系統已在一部分亞洲地區上市,這些新的特性可以治療解剖難度更大的病例。
2.3 MitraClip 在研究亞組與特殊人群中的應用
亞組和特殊患者組也可考慮使用MitraClip,這類患者包括房性FMR、合并三尖瓣反流(TR)、急性MR 和肥厚型梗阻性心肌病(HOCM)。
共識聲明9
如果房性FMR 的患者存在臨床癥狀,則應由心臟團隊(包括電生理學專家和心力衰竭專家)進行評估。如果患者目前已得到最優治療,則可以考慮使用MitraClip。
證據等級:低
一致性:同意96%;中立0%;不同意4%
盡管左心房擴張在沒有心房顫動的情況下也有可能發生,但長期持續性心房顫動是左心房擴張的一個常見原因[21]。在心房顫動引起心房擴張的患者中,擴張的二尖瓣環可導致瓣葉閉合欠佳和MR。而顯著擴張的左心房可使二尖瓣后葉受牽拉和限制,從而導致房性FMR[22]。
在一項研究中,研究人員對比了使用MitraClip分別治療房性FMR 患者(n=38)和室性FMR 患者(n=49)的療效。該研究將房性FMR 定義為左心室射血功能保留(LVEF ≥50%)且左心室壁運動正常的MR,將室性FMR 定義為左心室功能不全(LVEF<50%)或左心室壁運動異常的MR[23]。研究發現,MitraClip 治療與MR 的改善相關,并且房性FMR 患者與室性FMR 患者相比,其瓣葉對合更佳,二尖瓣瓣環前后徑縮小更明顯,二尖瓣環面積減少也更多[23]。
基于這項研究,專家組認為MitraClip 是針對癥狀性房性FMR 患者的一種可行的治療選擇;因此,心臟團隊(包括電生理和心力衰竭專家)應在其他治療方案已充分優化后,評估此類患者植入MitraClip是否可行。然而,部分專家反對這一觀點,指出許多房性FMR 患者屬于低手術風險人群,仍可接受外科二尖瓣修復術治療。盡管如此,對于不適合手術的患者(例如一些老年患者),MitraClip 依然是一個合理的選擇。
最后,值得注意的是,房性FMR 患者往往并發重度TR[24],這可能限制了經導管二尖瓣介入治療的臨床獲益。因此,這類并發癥同樣應該納入臨床評估。
共識聲明10
專家組肯定了MitraClip 成功應用于一些特殊情況(如急性MR、動力性MR、HOCM、手術修復失敗的MR 和TR)的個案報道。盡管如此,共識應優先考慮臨床試驗或注冊研究。這類患有非常見疾病的患者應由心臟團隊進行個體化評估,針對個體情況以確定使用MitraClip 的可行性和獲益。
證據等級:低
一致性:同意100%;中立0%;不同意0%
個案報道顯示了在一些特殊疾病情況下成功使用MitraClip 的臨床實踐,如急性MR、動力性MR、HOCM、和TR[25-32]。
IREMMI 是一項在急性心肌梗死患者中使用MitraClip 治療急性MR 的國際多中心注冊研究。該研究報道了MitraClip 用于治療急性心肌梗死患者(n=93)并發急性MR 的可行性,手術成功率超過90%,30 天死亡率為6.5%[25]。
另一項研究納入了221 例接受了MitraClip 植入的患者,研究發現動力性重度MR 患者與靜息狀態下重度MR 患者在臨床改善方面相似,大多數動力性重度MR 患者的NYHA 心功能分級從Ⅲ/Ⅳ級改善至Ⅰ/Ⅱ級,這一結果與靜止期重度MR 患者相近(59% vs.56%;P=0.566)[26]。
另一項研究納入了64 例不適合外科手術,患有重度TR 并且已接受最佳藥物治療但無效的患者,這些患者同樣接受了MitraClip 治療。研究結果顯示,91%的患者TR 降低了至少1 級以上[31]。患者的有效反流口面積顯著縮小(P<0.001)、腔靜脈收縮寬度(P=0.001)和反流量(P<0.001)也顯著減少。6 分鐘步行試驗的距離也顯著增加(P=0.007)[30]。除了上述成功臨床應用,一項國際前瞻性、單臂、多中心研究正在開展以評估基于經導管途徑的TR治療方法(TriClip)。這項名為TRILUMINATE 的研究發現,在中度或中度以上TR 的患者中,有71%的患者在治療后TR 降至中度或更低(基線時為8%;P<0.0001)[33]。入組患者在NYHA 心功能分級Ⅰ/Ⅱ級(P<0.0001)、6 分鐘步行試驗(P=0.0023)和堪薩斯城心肌病問卷評分(P<0.0001)等方面有顯著的臨床改善。
對于HOCM 和手術修復失敗的MR 患者而言,目前的證據僅限于個別病例報告[28-29,32]。盡管有上述報道,但并沒有設計良好的對照試驗來評估針對這些患者使用MitraClip 的效果;因此,理想情況下,這些患者應該被納入臨床試驗或患者注冊研究。如果考慮使用MitraClip,心臟團隊應該對這些特殊患者進行個體評估以確定使用MitraClip 治療的可行性與潛在獲益,并且在充分告知目前有限研究結果的情況下獲得患者的知情同意。本意見適用于外科手術高風險或不同意外科手術的患者。
3 結論
在所有的MR 患者中,MR 的病因、性質和嚴重程度,以及患者的癥狀和總體外科手術風險都應該得到全面評估。心臟團隊應同期處理瓣膜問題和導致MR 的可糾正病因,并全面評估患者的受益-風險,以確定MitraClip 植入術的可行性。
共識專家組成員(排名不分先后順序):David Sim(新加坡國家心臟中心),Edgar Tay(新加坡國家心臟中心),Jack Wei Chieh Tan(新加坡國家心臟中心),Kenny YK Sin(新加坡國家心臟中心),Khung Keong Yeo(新加坡國家心臟中心),See Hooi Ewe(新加坡國家心臟中心),David Muller(澳大利亞St.Vincent's 私立醫院),Darren Walters(澳大利亞St.Vincent's 私立醫院北區),JoAnn Lindenfeld(美國范德堡大學醫學中心),Michael Lee(中國香港伊麗莎白女王醫院),Angus Chui(中國香港伊麗莎白女王醫院),Sai Satish(印度阿波羅醫院),Teguh Santoso(印度尼西亞Medistra 醫院),Shunsuke Kubo(日本倉敷中心醫院),John Chan Kok Meng(馬來西亞CVSKL 醫院),Meemook Krissada(泰國曼谷瑪希頓大學Ramathibodi 醫院),Shih-Hsien Sung(中國臺灣臺北榮民總醫院),Quang N Nguyen(越南國家心臟中心),Makoto Amaki(日本國家心腦血管病中心),Misaki Izumo(日本圣瑪莉安娜大學醫學院),Kentaro Hayashida(日本慶應大學醫學院),Jung Sun Kim(韓國延世大學),Do-Yoon Kang(韓國峨山醫學中心),Gregg Stone(美國西奈山伊坎醫學院),Takashi Matsumoto(日本仙臺庫西醫院),潘湘斌(中國醫學科學院阜外醫院)
本文英文版已發表在European Cardiology Review,2021,16:e25.

