初診肥胖的2型糖尿病患者采用利拉魯肽配合胰島素對糖脂代謝強化治療的效果觀察
王艷楠
(北部戰區總醫院內分泌科,遼寧 沈陽 110000)
2型糖尿病(T2DM)發病機制復雜,通常認為與β細胞功能障礙、胰島素生物調節減弱、胰島素抵抗等有關[1],尚無特效治愈藥物,臨床治療重點為預防并發癥、控制血糖水平。相關報道指出,T2DM合并肥胖者可因脂肪組織過多而加重胰島素抵抗[2],影響血糖控制效果,甚至提升心腦血管意外事件發生率。因此,針對初診肥胖T2DM 患者,必須規范治療,以便獲得良好的遠期療效。另外,相關研究認為[3],胰島素強化治療雖然能改善患者血糖水平,但難以降低體質量,而利拉魯肽作為胰高血糖素樣肽-1(GLP-1)類似物[4],既能保持胰島素強化療法的成果,又能調節體質量,改善血脂代謝與炎癥反應。基于此,本研究旨在分析初診肥胖的T2DM 患者接受利拉魯肽配合胰島素治療對糖脂代謝強化治療的效果,現報道如下。
1 資料與方法
1.1 臨床資料 選取 2018 年 6 月至 2019 年 6 月于本院接受治療且行胰島素強化治療的40 例初診肥胖T2DM患者作為對照組,將2019年7月至2020年7月于本院接受治療且在對照組基礎上加用利拉魯肽治療的40 例初診肥胖T2DM 患者作為觀察組。對照組男 25 例,女 15 例;年齡 36~67 歲,平均年齡(51.5±12.3)歲;病程6~17 個月,平均病程(11.6±2.3)個月。觀察組男 24 例,女 16 例;年齡 37~68歲,平均年齡(51.9±12.1)歲;病程5~16 個月,平均病程(10.5±2.1)個月。兩組臨床資料比較差異無統計學意義,具有可比性。本研究獲得醫院倫理委員會審核批準。納入標準:均為T2DM,且均未使用降血糖藥物;體重指數(BMI)≥28 kg/m2;知情且同意參與本研究。排除標準:高血糖高滲、感染、酮癥酸中毒等急性并發癥者;胃腸道疾病者;心腦血管疾病、肝腎功能損害者;甲狀腺疾病者;全身感染性疾病者;對本研究藥物過敏者。
1.2 方法 對照組行胰島素強化治療,持續皮下泵入門冬胰島素注射液[丹麥諾和諾德(中國)公司,國藥準字J20150073],初次0.4~0.6 U/kg,之后結合血糖水平予以調整,直至血糖平穩,連續治療3個月。
觀察組在對照組基礎上加用利拉魯肽治療,胰島素強化治療方法同對照組,同時,每天皮下注射利拉魯肽(丹麥諾和諾德公司,國藥準字J20160037),初次每天0.6 mg,治療1周,若無不良反應,且血糖不達標,需增加至每天1.2 mg,仍未達標可增加至每天1.8 mg,連續治療3個月。
1.3 觀察指標 比較兩組血糖及胰島素指標、血脂代謝指標、生物學指標。①血糖及胰島素指標:葡萄糖氧化酶法測定空腹血糖(FPG)、餐后2 h 血糖(2 h PG),化學發光法測定空腹胰島素(F-INS)、餐后2 h胰島素(P-INS)[5];②血脂代謝指標:以全自動血生化分析儀測定載脂蛋白B(ApoB)、三酰甘油(TG)、總膽固醇(TC)[6];③生物學指標:評價內臟脂肪厚度(以超聲測量)、腰圍、BMI[7]。
1.4 統計學方法 采用SPSS 23.0統計學軟件進行數據分析,計量資料以“”表示,行t檢驗,以P<0.05為差異有統計學意義。
2 結果
2.1 兩組血糖及胰島素指標比較 治療前,兩組FPG、2 h PG、F-INS、P-INS比較差異無統計學意義;治療后,兩組血糖及胰島素指標均降低,且觀察組低于對照組(P<0.05),見表1。
表1 兩組血糖及胰島素指標比較()Table 1 Comparison of blood glucose and insulin between the two groups()
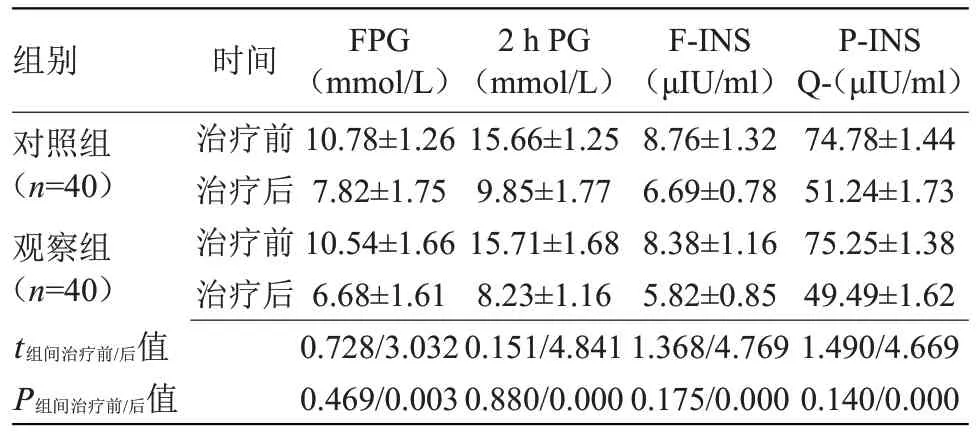
表1 兩組血糖及胰島素指標比較()Table 1 Comparison of blood glucose and insulin between the two groups()
注:FPG,空腹血糖;2 h PG,餐后2 h 血糖,F-INS,空腹胰島素;P-INS,餐后2 h胰島素
組別對照組(n=40)觀察組(n=40)P-INS Q-(μIU/ml)74.78±1.44 51.24±1.73 75.25±1.38 49.49±1.62 1.490/4.669 0.140/0.000時間治療前治療后治療前治療后t 組間治療前/后值P 組間治療前/后值FPG(mmol/L)10.78±1.26 7.82±1.75 10.54±1.66 6.68±1.61 0.728/3.032 0.469/0.003 2 h PG(mmol/L)15.66±1.25 9.85±1.77 15.71±1.68 8.23±1.16 0.151/4.841 0.880/0.000 F-INS(μIU/ml)8.76±1.32 6.69±0.78 8.38±1.16 5.82±0.85 1.368/4.769 0.175/0.000
2.2 兩組血脂代謝指標比較 治療前,兩組ApoB、TG、TC 比較差異無統計學意義;治療后,兩組ApoB、TG、TC 均降低,且觀察組低于對照組(P<0.05),見表2。
表2 兩組血脂代謝指標比較()Table 2 Comparison of blood lipid metabolism indexes between the two groups()
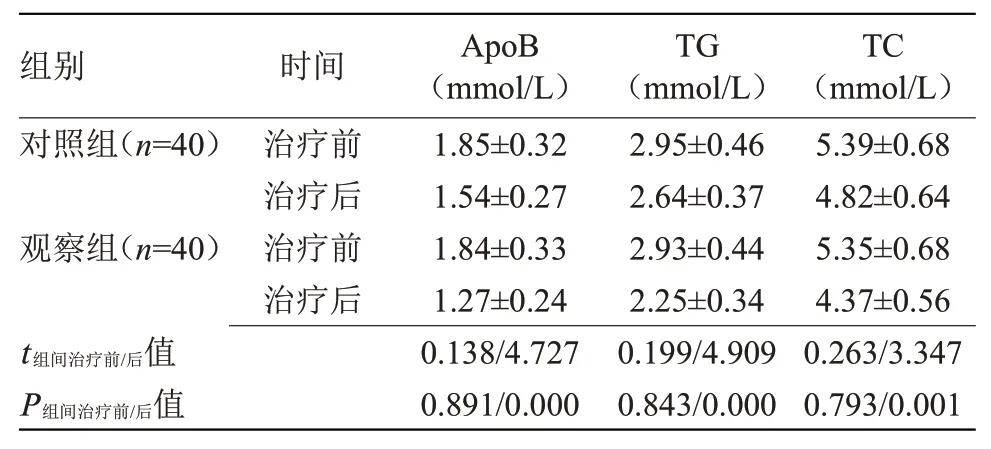
表2 兩組血脂代謝指標比較()Table 2 Comparison of blood lipid metabolism indexes between the two groups()
注:ApoB,載脂蛋白B;TG,三酰甘油;總膽固醇(TC)
組別對照組(n=40)觀察組(n=40)治療前治療后治療前治療后t 組間治療前/后值P 組間治療前/后值5.39±0.68 4.82±0.64 5.35±0.68 4.37±0.56 0.263/3.347 0.793/0.001 1.85±0.32 1.54±0.27 1.84±0.33 1.27±0.24 0.138/4.727 0.891/0.000 2.95±0.46 2.64±0.37 2.93±0.44 2.25±0.34 0.199/4.909 0.843/0.000時間TC(mmol/L)ApoB(mmol/L)TG(mmol/L)
2.3 兩組生物學指標比較 治療前,兩組內臟脂肪厚度、腰圍、BMI 比較差異無統計學意義;治療后,兩組內臟脂肪厚度、腰圍、BMI均降低,且觀察組低于對照組(P<0.05),見表3。
表3 兩組生物學指標比較()Table 3 Comparison of biological indexes between the two groups()
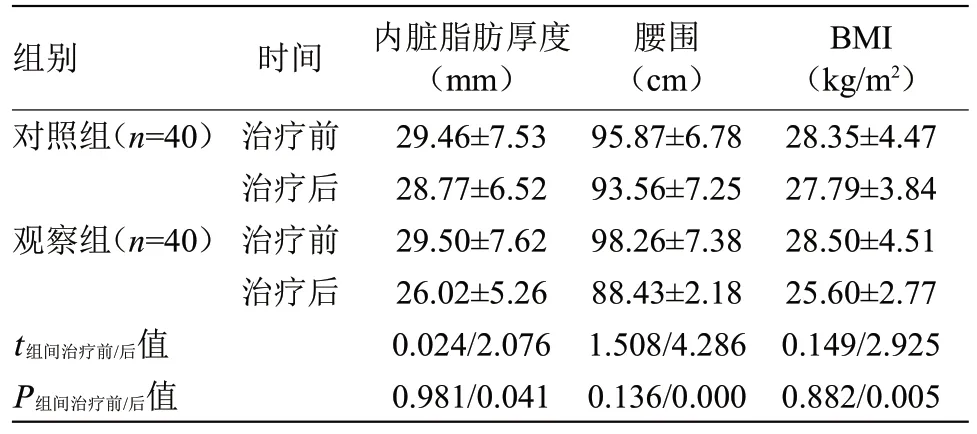
表3 兩組生物學指標比較()Table 3 Comparison of biological indexes between the two groups()
BMI(kg/m2)28.35±4.47 27.79±3.84 28.50±4.51 25.60±2.77 0.149/2.925 0.882/0.005組別對照組(n=40)觀察組(n=40)時間治療前治療后治療前治療后t 組間治療前/后值P 組間治療前/后值內臟脂肪厚度(mm)29.46±7.53 28.77±6.52 29.50±7.62 26.02±5.26 0.024/2.076 0.981/0.041腰圍(cm)95.87±6.78 93.56±7.25 98.26±7.38 88.43±2.18 1.508/4.286 0.136/0.000
3 討論
T2DM是發病率較高的內分泌疾病,不僅會使患者處于高血糖狀態,還會引發多種并發癥,而初診時心腦疾病、嚴重肥胖等高危狀態會增加并發癥發生率[8],加重病情。因此,針對初診T2DM患者需要采取降尿酸、減壓、減脂等措施,以增強T2DM治療效果,尤其是對于初診肥胖T2DM 患者,具有胰島細胞功能受損、高血脂、超重等特點,單藥治療療效欠佳,需聯合用藥。
本研究結果表明,治療后,觀察組血糖及胰島素指標均低于對照組(P<0.05)。胰島素泵強化治療經由模擬機體胰島素分泌,可幫助T2DM 患者穩定、準確地吸收胰島素,盡快達到血糖控制目標,但長期治療易增加體質量,而利拉魯肽屬于GLP-1類似物,半衰期可達12~14 h[9],能活化蛋白激酶,增加胰島β細胞數量,從而逆轉胰島功能,改善血糖水平。T2DM 合并脂質代謝紊亂較為多見,且相關動物實驗報道指出,高脂飼養易導致胰島素抵抗,而胰島素增敏劑具有逆轉脂毒性的作用,且可對胰島細胞進行保護,表明血脂異常與該病患者密切相關。ApoB、TG、TC 水平,其中ApoB 屬于密度脂蛋白脂質,由肝臟合成,若ApoB 呈高表達,易增加T2DM患者心血管并發癥發生風險;TG、TC可從宏觀層面反映血脂代謝狀態[10]。本研究結果顯示,治療后,觀察組ApoB、TG、TC 低于對照組,且內臟脂肪厚度、腰圍、BMI低于對照組(P<0.05),提示利拉魯肽配合胰島素還具有調節脂質代謝的作用。另外,T2DM合并肥胖患者具有嚴重的胰島素抵抗,治療難度較大,且隨著內臟脂肪增多,會提升起始胰島素劑量,從而提高心血管疾病發生率,利拉魯肽作為新型降糖藥物,能在不發生低血糖的情況下,增強血糖控制效果,同時,可激活胃壁GLP-1受體、下丘腦中樞GLP-1 受體,從而延緩胃排空、降低食欲,進而達到降低體質量的效果。
綜上所述,由于初診肥胖T2DM 患者強化治療期間采用利拉魯肽+胰島素,可改善糖脂代謝、胰島功能,減輕體質量,值得臨床推廣。

