腸道沙門氏菌雙相亞利桑那亞種檢驗特征分析及檢驗方法比較研究







摘 要:目的:通過參加中國食品藥品檢定研究院組織的能力驗證,比對不同檢驗方法對巧克力樣品中沙門氏菌的檢出及鑒定效果,找出不同檢驗方法對樣品中不典型沙門氏菌分離及鑒定的特性,有效提升實驗室對不典型沙門氏菌檢驗能力及質量控制水平。方法:實驗中樣品前處理按照考核方案作業指導書進行,沙門氏菌的分離按照《食品安全國家標準 食品微生物學檢驗 沙門氏菌檢驗》(GB 4789.4—2016)要求進行操作,通過BAX? system Q7快速篩查可疑樣品,MALDI-TOF-MS定位可疑菌株,VITEK 2 COMPACT全自動微生物分析系統確認陽性菌株,MLST技術對沙門氏菌陽性菌株進行分子生物學分型。結果:3個樣品中兩個樣品檢出沙門氏菌,樣品CODE-0695檢出鼠傷寒沙門氏菌,樣品CODE-0050未檢出沙門氏菌,樣品CODE-0542檢出腸道沙門菌雙相亞利桑那亞種。結論:實驗發現腸道沙門菌雙相亞利桑那亞種在顯色培養基上菌落形態及生化表征與常見沙門氏菌不一致,易漏檢,實際工作中應加強對不典型沙門氏菌檢驗能力的建設。
關鍵詞:腸道沙門菌雙相亞利桑那亞種;菌株鑒定;血清分型;多位點序列分型;基質輔助激光解析電離飛行時間質譜
Comparative Study on Test Characteristics Analysis and Test Methods of Salmonella Enterica Subspecies Diarizonae
LIU Yang1, MA Bingcun2, LIU Zheng1, WANG Can1, QIN Yuan1, HE Qiaoling3*
(1.Sichuan Center for Medical Product Technical Inspection, Chengdu 610000, China; 2.Sichuan Institute for Drug Control, Chengdu 610000, China; 3.Sichuan Institute of? Food Inspection, Chengdu 610000, China)
Abstract: Objective: By participating in the capability test organized by China food and drug testing and Research Institute, comparison of the detection and identification effects with different testing methods on Salmonella in chocolate samples, find out the characteristics of different testing methods on the isolation and identification of atypical Salmonella in samples, and effectively improve laboratory atypical Salmonella inspection capability and quality control level. Methods: The samples pre-treatment in this experiment were carried out in accordance with the assessment plan instructions. The isolation of Salmonella was carried out according to the requirements of GB 4789.4—2016 National food safety standard-Food microbiological testing-Salmonella testing. And the suspicious samples could be screened quickly through the BAX? system Q7. Suspicious strains were located by MALDI-TOF-MS. Using VITEK 2 COMPACT automatic microbial analysis system to confirm positive strains. Then performed the molecular biology typing for positive Salmonella by MLST. Results: Salmonella was detected in two of the three samples. Salmonella typhimurium was detected in sample CODE-0695, no Salmonella was detected in sample CODE-0050. Salmonella enterica subspecies diarizonae was detected in sample CODE-0542. Conclusions: The experiment found that the colony morphology and biochemical characteristics of Salmonella enterica subspecies diarizonae in the chromogenic medium were inconsistent with common Salmonella, which could be missed detection easily. The ability to test atypical Salmonella should be strengthened in practical work .
Keywords: salmonella enterica subspecies diarizonae; identification of strains; serotyping; multilocus sequence typing; MALDI-TOF-MS
腸道沙門氏菌(Salmonella enterica)是一種常見的人畜共患病病原菌,主要傳播方式是食用被污染的食物、水及接觸帶菌者,該菌造成的食物中毒事件多發于夏季。腸道沙門氏菌造成的危害范圍覆蓋全球,在我國腸道沙門氏菌感染是造成食物中毒的主要原因之一[1]。因此,快速準確地將該菌污染的食物檢出并進行有效的分型,對確定污染源進而采取有效措施切斷污染源頭,維護人們的飲食安全有重要意義。
實際工作中面對沙門氏菌污染的食品,傳統國家標準檢測方法雖然能準確可靠的檢測出被污染樣品,但面對生化表征不典型的沙門氏菌,如腸道沙門菌雙相亞利桑那亞種(Salmonella enterica subspecies diarizonae),對檢驗人員的經驗要求較高,且耗時較長。隨著現代微生物學鑒定技術的發展,分子生物學及基質輔助激光解析電離飛行時間質譜(MALDI-TOF-MS)鑒定技術開始大量應用于實際檢驗工作中,和傳統檢驗方法相結合,能有效提高沙門氏菌的檢出效率,減少因人員經驗不足導致的漏檢[2]。此次實驗在采用傳統國標進行沙門氏菌檢驗的同時引入最新的檢驗技術,比較了不同檢驗方法的優點及缺點,為今后實際工作中進行非典型沙門氏菌檢驗技術的選擇提供了參考。
1 材料與方法
1.1 材料與試劑
食品中沙門氏菌能力驗證樣品,每份考核樣品為裝有巧克力基質的獨立樣品瓶,樣品瓶編號分別為CODE-0695、CODE-0050和CODE-0542。
大腸埃希菌(Escherichia coli)〔CMCC(B)44 102〕、銅綠假單胞菌(Pseudomonas aeruginosa)〔CMCC(B)10 104〕、乙型副傷寒沙門菌(Salmonella paratyphi B)〔CMCC(B)50 094〕、阿貢納沙門氏菌(Salmonella agona)。
緩沖蛋白胨水(BPW):BD;亞硒酸鹽胱氨酸(SC)增菌液、四硫磺酸鈉煌綠(TTB)增菌液、亞硫酸鉍(BS)瓊脂、沙門氏菌生化鑒定試劑盒:廣東環凱微生物科技有限公司;沙門氏菌顯色培養基:科馬嘉;營養瓊脂、胰酪大豆胨瓊脂培養基(TSA)、胰酪大豆胨液體培養基(TSB):北京三藥科技開發公司;沙門氏菌屬診斷血清:寧波天潤生物藥業有限公司。
1.2 儀器與設備
1300型生物安全柜:美國賽默飛公司;KB400培養箱:BINDER;FORMA 311培養箱:Thermo fisher;滅菌器-自動高壓蒸汽:致微(廈門)儀器有限公司;均質器400型:IUL公司;BAX? system Q7全自動病原微生物檢測系統:美國杜邦公司;VITEK 2 COMPACT全自動微生物分析系統:法國生物梅里埃公司;BX51顯微鏡:OLYMPUS;基質輔助激光解析電離飛行時間質譜(MALDI-TOF-MS):美國布魯克道爾頓公司;PCR擴增儀:德國Eppendorf公司等。
1.3 實驗方法
按照NIFDC-PT-135巧克力中沙門氏菌檢驗作業指導書進行沙門氏菌檢驗,依據《食品安全國家標準 食品微生物學檢驗 沙門氏菌檢驗》(GB 4789.4—2016)進行檢驗,同時輔以BAX? system Q7全自動病原微生物檢測系統進行快速篩查,以基質輔助激光解析電離飛行時間質譜進行可疑菌株鑒定,VITEK 2 COMPACT全自動微生物分析系統對可疑菌株進行生化鑒定后,利用多位點序列分型(MLST)方法對沙門氏菌陽性菌株進行分型。以阿貢納沙門氏菌作為陽性對照菌,大腸埃希菌作為陰性對照菌開展試驗。
1.3.1 樣品處理與前增菌
準備90 mL預熱到45 ℃已滅菌的BPW,在生物安全柜內無菌操作打開樣品瓶蓋,加入20 mL滅菌BPW緩沖液,蓋好瓶蓋待巧克力樣品融化后加入無菌均質袋內。取20 mL滅菌BPW清洗樣品瓶2次,將洗液加入無菌均質袋內,最后向均質袋內加入30 mL滅菌BPW充分均質混勻,制成樣品稀釋液。陽性對照:取阿貢納沙門氏菌的TSB液體培養物稀釋液1 mL(含菌量約為50~100 CFU/mL)加入到盛有90 mL滅菌BPW增菌液的無菌均質袋中,混勻。陰性對照同法操作。空白對照:直接將90 mL滅菌BPW增菌液加入無菌均質袋中。將上述各組樣品置36 ℃培養18 h。
1.3.2 BAX? system Q7全自動病原微生物檢測系統檢測
移取0.2 mL上述BPW培養物至10 mL腦心浸液培養基(BHI)中,于37 ℃培養3 h后移取5 μL培養物至盛有200 μL裂解液的裂解管中,于37 ℃金屬浴
20 min,再95 ℃金屬浴10 min,取出裂解管于4 ℃冷卻5 min,再移取50 μL裂解物到PCR反應管中,采用BAX? system Q7全自動病原微生物檢測系統檢測。
1.3.3 增菌與分離
輕輕搖動混勻BPW培養物,移取1 mL培養物轉種于10 mL的TTB培養基內,于42 ℃培養24 h。同時,另取1 mL培養物轉種于10 mL的SC培養基內,于36 ℃培養24 h。分別用接種環取TTB和SC增菌液1環,劃線接種于BS瓊脂平板(36 ℃培養48 h)和沙門氏菌屬顯色培養基瓊脂平板(36 ℃培養24 h),培養結束后觀察平板上的菌落特征[3]。
1.3.4 基質輔助激光解析電離飛行時間質譜(MALDI-TOF-MS)檢測
分別從BS、沙門氏菌顯色平板上挑取不同菌落,劃線接種于同種培養基進行純化培養后轉接于TSA平板。挑取TSA平板上新鮮的純培養物,在MALDI-TOF-MS金屬靶點上涂成一個薄層,在上述靶點上覆蓋1 μL的70%甲酸水溶液并在室溫下自然晾干,然后再覆蓋1 μL的HCCA基質并在室溫下自然晾干,采用MALDI-TOF-MS進行鑒定(鑒定前對儀器進行校準),同時與實驗室保存的大腸埃希氏菌、銅綠假單胞菌、乙型副傷寒沙門圖譜進行比對。
1.3.5 生化鑒定
根據MALDI-TOF-MS鑒定結果,挑取相應可疑菌落,按照《食品安全國家標準 食品微生物學檢驗 沙門氏菌檢驗》(GB 4789.4—2016)進行生化鑒定試驗。
1.3.6 VITEK 2 COMPACT全自動微生物分析系統鑒定
根據MALDI-TOF-MS鑒定結果,挑取相應可疑菌落,接種營養瓊脂平板,取營養瓊脂平板單個菌落,置于3 mL的0.45%生理鹽水的試管中,調整菌懸液濃度達到革蘭氏陰性鑒定卡要求的濁度,菌懸液加入到鑒定卡后,用VITEK 2 COMPACT全自動微生物分析系統進行鑒定。
1.3.7 血清學分型
按照《食品安全國家標準 食品微生物學檢驗 沙門氏菌檢驗》(GB 4789.4—2016)進行血清學分型。從營養瓊脂平板上挑取多個儀器鑒定為沙門氏菌屬的單菌落進行血清反應,根據上述反應結果,查沙門氏菌抗原表,得出分型結果。
1.3.8 MLST分型
實驗中采用MLST數據庫(https://enterobase.warwick.ac.uk/)提供的腸道沙門氏菌多位點序列分型引物和擴增程序,對實驗中分離陽性菌株的7個等位基因(aroC、thrA、purE、dnaN、sucA、hisD 和hemD)進行擴增并測序。將獲得的等位基因序列輸入MLST數據庫分析待測菌株序列型(Sequence Type,ST)[4-6]。
2 結果與分析
2.1 BAX?system Q7全自動病原微生物檢測系統檢測結果
BAX? system Q7檢測結果如表1所示,CODE-0695、CODE-0542和陽性對照檢出沙門氏菌,CODE-0050和陰性對照未檢出沙門氏菌。實驗中發現直接將樣品BPW培養物進行BAX? system Q7檢測,儀器無法給出檢驗結果,這可能是樣品中巧克力基質干擾PCR反應造成的。將樣品BPW培養物轉接到BHI培養基培養后進行BAX? system Q7檢測,儀器可以得出正確結果。因此BAX? system Q7可以快速確定樣品中是否含有沙門氏菌,為后面進一步開展確認實驗提供了參考。
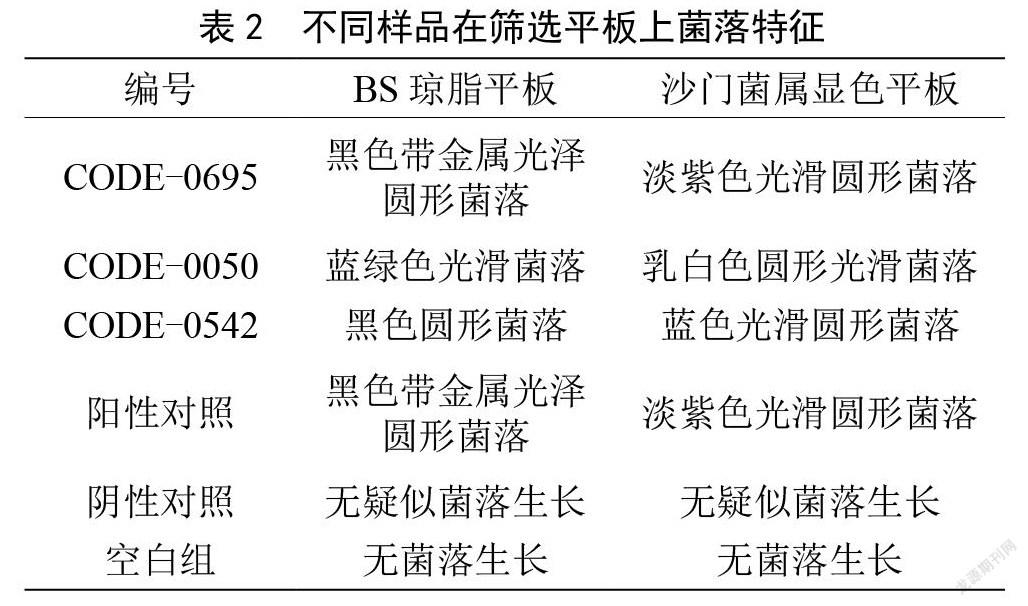
2.2 不同菌株在篩選平板上的菌落特征
將TTB、SC培養物劃線于BS和沙門氏菌顯色培養基進行培養,結果如表2所示。樣品CODE-0695和陽性對照在BS瓊脂平板和沙門氏菌顯色培養基上顯示典型的沙門氏菌菌落形態特征,判斷為可疑沙門氏菌。樣品CODE-0050在BS瓊脂平板分離出藍綠色光滑菌落,在沙門顯色培養基分離出乳白色圓形光滑菌落,樣品CODE 0542在BS瓊脂平板分離出黑色圓形菌落,在沙門顯色培養基分離出藍色光滑圓形菌落,以上兩個樣品在篩選平板菌落特征均不顯著,應進一步開展確認實驗。
2.3 基質輔助激光解析電離飛行時間質譜(MALDI-TOF-MS)對可疑菌株鑒定
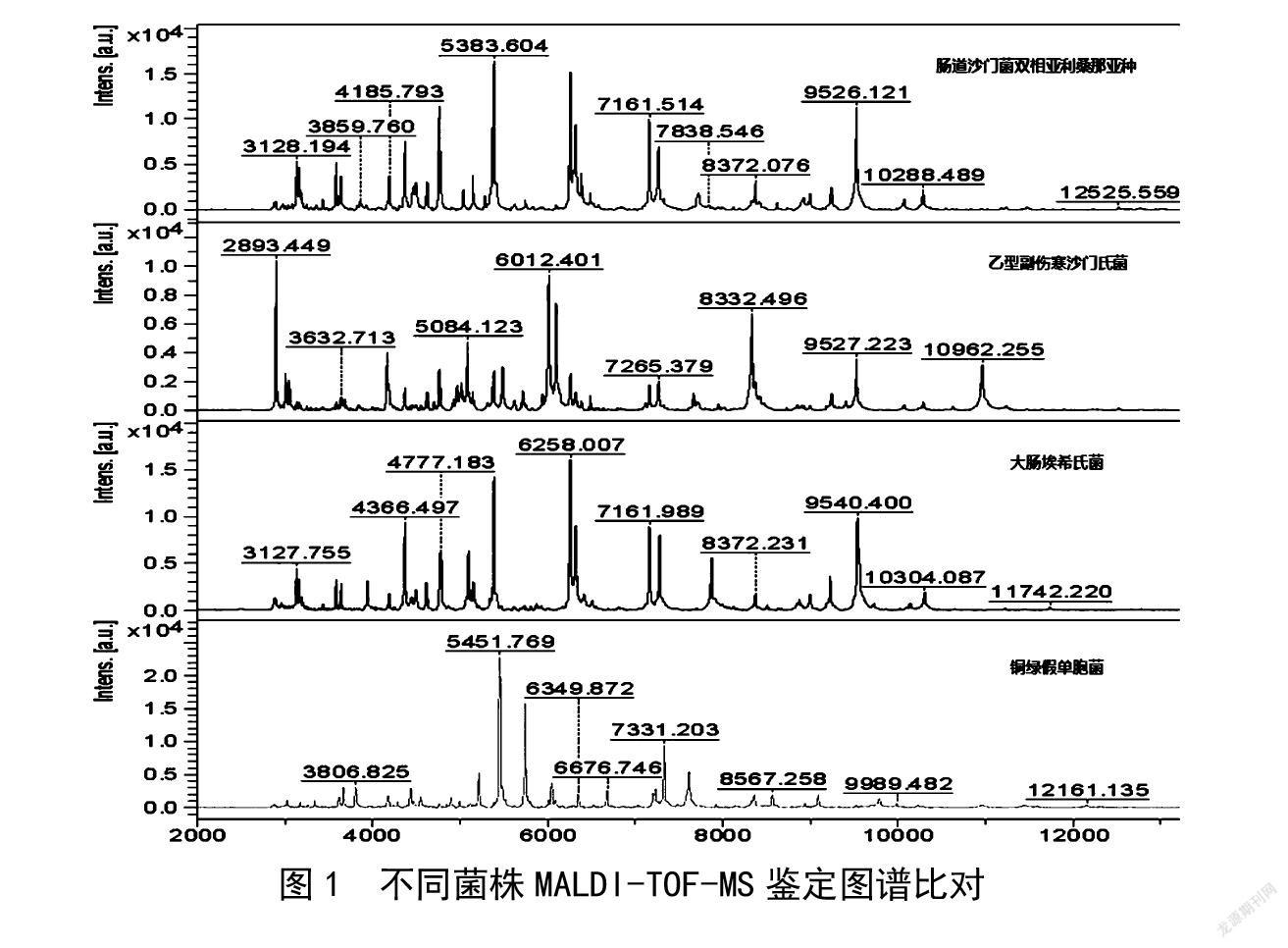
挑取不同樣品TSA培養基上新鮮的純培養物進行MALDI-TOF-MS鑒定,結果如表3所示。3個樣品中CODE-0695、CODE-0542及陽性對照均檢出沙門氏菌,同BAX? system Q7檢測結果一致。比較不同菌株鑒定圖譜,具體見圖1,可以看出銅綠假單胞菌和沙門氏菌圖譜有明顯區別,大腸埃希氏菌和沙門氏菌圖譜比較相似。由表4可知,實驗中儀器能準確將沙門氏菌、大腸埃希氏菌、銅綠假單胞菌鑒定出來,且鑒定評估分數均在2.4分以上。根據鑒定結果顯示MALDI-TOF-MS只能將上述兩種不同血清型的沙門氏菌鑒定到屬,無法鑒定出相應沙門氏菌的血清型。
2.4 生化鑒定結果
將樣品中MALDI-TOF-MS鑒定結果為沙門氏菌陽性的菌落及樣品CODE-0050中生長的菌落進一步純化進行生化鑒定,結果如表5所示。樣品CODE-0695篩選菌株生化鑒定結果與陽性對照結果一致,均符合GB 4789.4—2016中沙門氏菌生化反應特征;樣品CODE-0050生化鑒定結果不符合GB 4789.4—2016中沙門氏菌生化反應特征。因此可以判斷樣品CODE-0695檢出沙門氏菌,樣品CODE 0050未檢出沙門氏菌,檢驗結果和BAX? system Q7、MALDI-TOF-MS一致。樣品CODE-0542需進一步進行生化鑒定。
2.5 VITEK 2 COMPACT全自動微生物分析系統對可疑菌株的鑒定結果
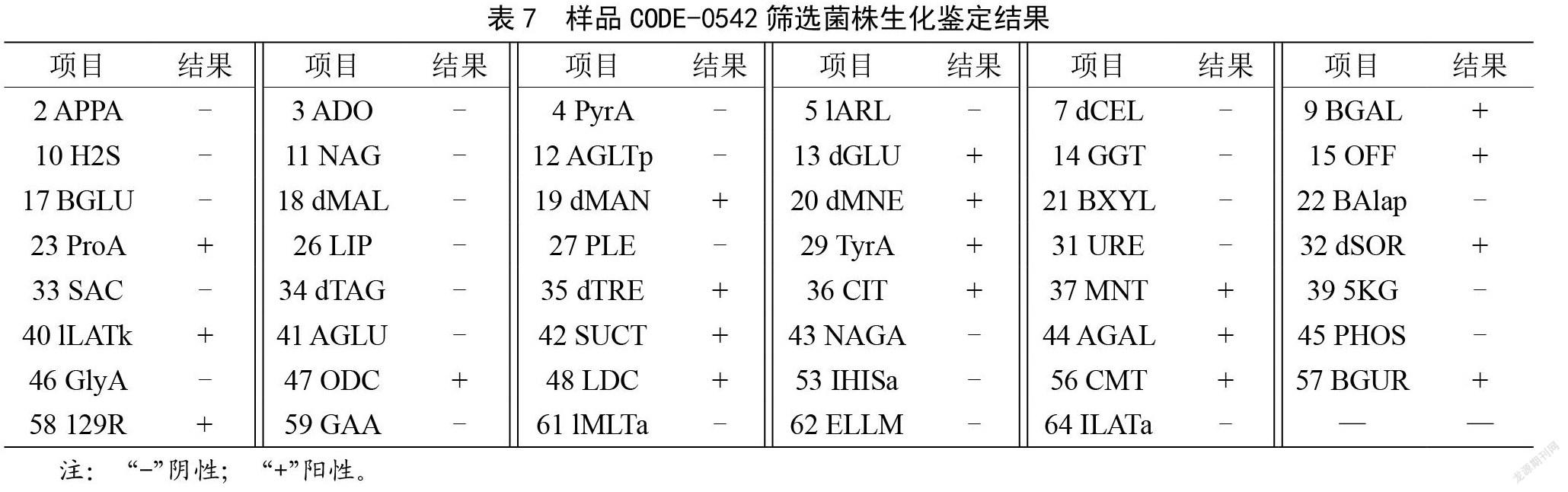
將篩選出的可疑沙門氏菌陽性菌株進行VITEK 2 COMPACT全自動微生物分析系統鑒定,結果如表6所示。樣品CODE 0695、CODE 0542均檢出沙門氏菌,其中CODE 0695鑒定結果為沙門菌屬,需進一步進行補充實驗,才能確定為哪一種血清型沙門氏菌,而樣品CODE 0542可通過該儀器直接鑒定為為腸道沙門氏菌雙相亞利桑那亞種,其生化反應結果如表7所示。
2.6 血清型分型結果
將篩選出的陽性菌株純化后進行血清型實驗,結果如表8所示。樣品CODE-0695培養物自凝實驗:無自凝,A-F O多價為陽性,O抗原:O4為陽性,O12為陽性,H抗原第1相:i為陽性,H抗原第2相:2為陽性;根據上述反應結果,查詢沙門氏菌抗原表鑒定為鼠傷寒沙門氏菌(S.Typhimurium)。CODE 0542培養物自凝實驗:無自凝,A-F O多價為陰性,通過實驗室現有血清無法判定其血清型。
2.7 多位點序列分型(MLST)對沙門氏菌陽性菌株進行分子生物學分型結果
將樣品CODE-0695、CODE0-0542陽性菌株的7個等位基因測序,經MLST數據庫比對分析結果如表9所示,陽性菌株ST型分別為ST19、ST63。其中ST19抗原式為1,4,12︰i︰1,2,血清型為鼠傷寒沙門氏菌,與本實驗血清型鑒定結果一致;ST63抗原式為60︰r︰e,n,x,z15,鑒定結果為腸道沙門菌Ⅲb亞種(腸道沙門菌雙相亞利桑那亞種)[2],與本實驗VITEK 2 COMPACT全自動微生物分析系統鑒定結果一致。
3 結論與討論
本次實驗通過分析腸道沙門菌雙相亞利桑那亞種的生化特征及不同檢驗方法的檢測特性,總結出以下幾點經驗為今后的一線檢驗工作提供參考。
(1)檢驗中通過對樣品BPW培養物轉接BHI培養基能有效避免巧克力基質對PCR反應的干擾,利用BAX? system Q7可以在30 h內準確快速的篩查出可疑陽性樣品,為后續實驗提供了參考。
(2)實驗發現腸道沙門菌雙相亞利桑那亞種在沙門氏菌顯色平板上菌落特征及生化鑒定反應不典型,容易造成漏檢。實驗中使用不同篩選平板,挑選不典型菌落結合BAX? system Q7及MALDI-TOF-MS等檢驗方法能有效降低漏檢風險。
(3)利用MALDI-TOF-MS高通量、快速鑒定的特點,對篩選平板上生長的各類型菌株純化后進行鑒定,可快速、精準定位可疑的沙門氏菌菌落,有效降低沙門氏菌陽性菌落在篩選平板上特征不典型造成漏檢的風險,為后期的生化鑒定提供了參考。比較MALDI-TOF-MS實驗結果,該系統可以將沙門氏菌、大腸桿菌及銅綠假單胞菌有效鑒定區分,但無法指出沙門氏菌具體血清型,但該系統快速、高通量篩選出陽性沙門氏菌菌落的能力是其他鑒定手段暫時無法比擬的。
(4)實驗中由于腸道沙門菌雙相亞利桑那亞種血清凝集試驗A-F O多價為陰性,很多實驗室不一定常備相關的鑒定血清,通過MLST分型技術能有效的彌補實驗室血清缺失造成無法分型的困境。
(5)比較VITEK 2 COMPACT全自動微生物分析系統對不同沙門氏菌的鑒定結果發現,該系統可以鑒定出腸道沙門菌雙相亞利桑那亞種,鑒定結果同MLST結果一致,但無法對鼠傷寒沙門氏菌進行分型鑒定,系統提示需要做補充生化實驗。
此次實驗,在采用傳統國標檢驗方法的基礎上,結合現代檢驗儀器及分子分型,分析了腸道沙門菌雙相亞利桑那亞種的生化特征,比對了不同檢測方法對該菌的檢測特性,不僅有效地提高了檢驗效率,縮短了檢驗時間也提高了檢驗的準確性降低了漏檢的可能,為今后更好地開展食品中非典型沙門氏菌檢驗,防止漏檢提供了參考。
參考文獻
[1]陳國強,陳揚,薛峰,等.多位點序列分型分析華東地區動物源產品中腸道沙門氏菌分離株[J].揚州大學學報(農業與生命科學版),2010,31(3):13-16.
[2]曲梅,黃瑛,呂冰,等.引起腹瀉的腸道沙門菌雙相亞利桑那亞種病原學鑒定[J].中國預防醫學雜志,2016,17(6):405-408.
[3]國家衛生和計劃生育委員會,國家食品藥品監督管理總局.食品安全國家標準 食品微生物學檢驗 沙門氏菌檢驗:GB 4789.4—2016[S].北京:中國標準出版社,2016.
[4]劉雯靜,邱少富,劉雪林,等.沙門氏菌的分子分型方法[J].現代生物醫學進展,2010(20):3948-3950.
[5]劉慧玲,萬志剛,洪小柳,等.進出口食品中不同血清型沙門氏菌PFGE和MLST分型比較研究[J].食品安全質量檢測學報,2014,5(11):3454-3461.
[6]Aanensen D M,Spratt B G. The multilocus sequence typing network: mlst.net [J].Nucleic Acids Research,2005(33):728-733.

