神經內鏡輔助多技術聯合在乙狀竇后鎖孔入路聽神經瘤切除術中的臨床應用
李海紅, 宋國智
(河北省邯鄲市中心醫院 神經外五科, 河北 邯鄲, 056001)
聽神經瘤(AN)是橋小腦角區(CPA)最常見的腫瘤類型,約占CPA腫瘤80%以上[1]。由于CPA解剖特性復雜, AN不及時治療可能會引發面部麻木、無力、聽力喪失、腦積水等癥狀的進展[2]。乙狀竇后入路(RSA)是AN顯微外科手術治療最常見的入路方式,其難點和臨床關注的重點,則轉移至最大程度保護周邊正常組織,保持長期面神經功能,減少術后并發癥的發生[3]。因此針對這一目的的多技術聯合應用在AN手術治療中有重要價值。本研究分析了本院近年來84例AN患者RSA手術治療中應用神經內鏡輔助下多技術聯合的效果,現報告如下。
1 資料和方法
1.1 一般資料
回顧性選取邯鄲市中心醫院2019年5月—2020年12月收治的AN患者84例為研究對象。入選者經術前磁共振成像(MRI)檢查及病理診斷均確診AN, 且由同一術者主刀,排除其他腫瘤及復發性AN患者。根據手術方法的不同將患者分為觀察組(n=44)和對照組(n=40)。觀察組采用神經內鏡輔助下多技術聯合治療,對照組采用傳統顯微外科治療。2組一般資料見表1。
1.2 方法
對照組采用鎖孔RSA顯微鏡手術治療。患者取側俯臥位, RSA常規切口,自乳突的內側1 cm處,以耳屏為上端取5~6 cm切口,視MRI顯示腫瘤大小,以星點為內緣做直徑2~3 cm骨窗,鎖孔理念在顯微鏡直視下弧形切開硬腦膜,以便與乙狀竇后緣弧形切口縫合。沿后腦神經方向,銳性剪切蛛網膜,至橋小腦角池。釋放腦脊液后,小腦半球塌陷到腫瘤可順利切除的程度。顯微鏡下在瘤內將部分腫瘤直接切除,之后沿包膜分離,待瘤壁塌陷后,將瘤壁和小腦、內聽道的粘連處進行分離,待腫瘤切除后,觀察面神經,避免損傷,盡量保留。觀察并直接刮除內聽道中腫瘤,部分難以直接刮除者,應用高速磨鉆處理后壁,并切開小部分硬腦膜,以便切除。術中為保護面神經,應用神經電生理監測(IONM), 對面肌肌電圖(EMG)、腦干聽覺誘發電位(BAEP)及自由肌電進行監測,術中單極刺激,定位面神經,實時監測自由肌電,觀測面神經走向,切除腫瘤后,給予小電流刺激腦干端,確定面神經保留情況。
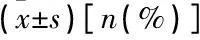
表1 2組一般資料比較
觀察組采用鎖孔RSA入路神經內鏡輔助下顯微鏡手術治療,并聯合IONM及超聲骨刀技術。體位、切口、骨瓣、IONM操作同對照組。骨瓣形成后,先應用內鏡對周邊結構進行觀測,確定腫瘤周邊情況后,顯微鏡下進行蛛網膜間分離,腫瘤切除過程中顯微鏡應用同對照組。當大部分腫瘤瘤內切除后,置入內鏡對面神經附著的腫瘤包膜進行剝離。內聽道需切開者給予外側壁超聲骨刀切開,之后對其內腫瘤進行刮除。
1.3 觀察指標
術后根據MRI結果評估2組患者手術全切率及觀察并發癥發生情況。2組患者術后均接受6個月隨訪。2組術前、出院前及術后6個月給予面神經功能評定,評定采用H-B(House-Brackmann)分級[4]: Ⅰ級為面部功能完全正常(100%), Ⅱ級為輕微面肌功能異常(>75%~<100%), Ⅲ級為中度不嚴重聯帶運動,但無損面容(>50%~75%), Ⅳ級為中重度無力或不對稱(>25%~50%), Ⅴ級為重度面部功能喪失(>1%~25%), Ⅵ級為完全喪失(0~1%)。其中Ⅰ~Ⅲ級為功能良好, Ⅳ~Ⅵ級為功能較差[5]。
1.4 統計學分析
采用SPSS 25.0軟件進行統計學分析,其中計量資料采用t檢驗,計數資料采用卡方檢驗。P<0.05為差異有統計學意義。
2 結 果
2.1 手術情況及面神經功能
觀察組腫物全切41例(93.2%), 對照組腫物全切31例(77.5%), 觀察組腫物全切率高于對照組,差異有統計學意義(P<0.05)。
2組術前、出院前面神經功能比較,差異無統計學意義(P>0.05); 術后6個月,觀察組面神經功能保留率(97.7%)高于對照組(82.5%), 差異有統計學意義(P<0.05)。見表2。
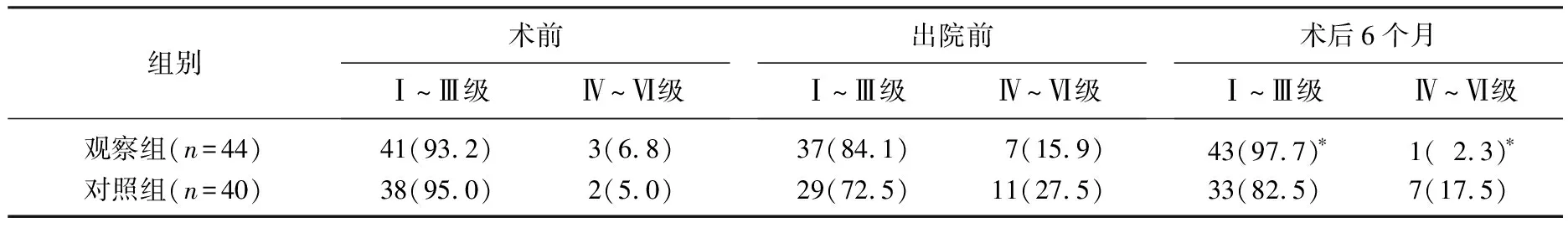
表2 2組患者術前、出院前、術后6個月H-B評級比較[n(%)]
2.2 術后并發癥
觀察組術后并發癥總發生率為6.8%, 低于對照組的22.5%, 差異有統計學意義(P<0.05)。見表3。

表3 2組術后并發癥發生率比較[n(%)]
3 討 論
AN所在解剖位置CPA區域的腫物周圍組織結構非常復雜,隨著占位的加重,患者聽力、面神經功能及顱內壓力逐步受到影響[6]。臨床中對于該類患者的治療以保留面神經功能、減少術后并發癥及改善患者的生存質量為目標[7]。
影響面神經功能損傷的因素較為復雜,與患者腫瘤的大小及類型、手術入路、切除程度及術中操作、既往治療均有一定的關系[8]。目前研究[9]表明,隨著瘤體的增大,面神經將逐漸被牽拉和推擠,從而加重壓迫和粘連的程度,增加術中剝離的難度; 囊性AN的囊壁和面神經之間的分界不清,當其與神經粘連時,過度剝離囊壁將增加面神經損傷的程度[10]; 再者,腫瘤清除越徹底,其面神經的損傷可能性就越大,為保留面神經而清掃不徹底,腫瘤則易復發[11]; 術中過度的機械牽拉和雙極電凝的應用,也可對面神經及毛細血管造成一定不良影響; 既往采用放射治療的患者,也可導致面神經與腫瘤之間的邊界粘連,從而增加剝離難度[12]。
針對以上面神經損傷相關因素,在顯微手術中聯合應用IONM技術已成為確保手術安全及保護面神經功能的優選[13]。IONM技術能夠在術中操作,特別是對神經直接接觸性操作的過程中,觀察不同強度電位的誘導波形改變,及時提醒操作停止,減少對神經組織的直接損傷; IONM技術還能夠通過對神經功能狀態的實時評估提高操作的精準性,或者提醒術者臨時調整手術步驟。本研究觀察組與對照組術中均給予IONM技術的聯合應用,患者手術均順利完成,無1例術中發生惡性不良事件,術后面神經功能的保留程度也較高。
RSA入路是AN切除術最常用的入路方式。相較傳統RSA入路,鎖孔RSA入路的優點是創口更小,術后恢復速度更快,同時皮下積液和顱內感染的發生率都可得到大幅度降低[14],且其更符合解剖學特性,能夠有效減少大腦的暴露,從而降低術后并發癥發生率。但較小的骨窗和視野也極大程度影響了術中的操作范圍、角度,對術者要求極高。神經內鏡輔助有效改善了這一問題,其有助于改善手術視野,對于控制對周圍組織的損傷具有較好的作用。
此外,對于內聽道內的腫瘤需要后壁切開者,傳統操作多應用高速磨鉆對后壁進行操作,并切開硬腦膜,以便去除腫瘤,但也增加了對面神經及腦組織損傷的可能性,因此導致面神經損傷及其他并發癥的發生[15]。聯合超聲骨刀技術,對外側壁切開可以更好地保持硬腦膜的完整性,從而減少顱神經創傷可能性。本研究結果顯示,神經內鏡輔助下顯微鏡手術治療并聯合IONM及超聲骨刀技術,腫瘤全切率更高,術后無1例術區出血、腦脊液漏及顱內感染的發生,并發癥總發生率相對更低,術后面神經功能H-B評級相對更好,其應用效果好,安全性高。
綜上所述,神經內鏡輔助多技術聯合在乙狀竇后鎖孔入路AN切除術中應用能夠有效提高腫瘤全切率,減少術中面神經損傷,在術后面神經功能保留方面效果較理想,同時可減少術后并發癥,但聯合技術較新,具有一定的操作難度。

