血脂、同型半胱氨酸與帕金森病合并認知障礙相關性
郭 暢,沈慧楠,孫藝萌,王東玉
(1.錦州醫科大學 研究生學院,遼寧 錦州 121000;2.東北育才外國語學校,遼寧 沈陽 110000;3.錦州市中心醫院 神經內科,遼寧 錦州 121000)
帕金森病(Parkinson’s disease,PD)是常見的以運動癥狀為主的進行性神經退行性疾病。隨著對疾病研究的深入,其非運動癥狀也得到了廣泛關注。認知障礙是PD最常見及嚴重的非運動癥狀,早期表現為PD輕度認知障礙(PD mild cognitive impairment,PD-MCI),晚期進展為PD癡呆(PD dementia,PDD)[1]。一項流行病學調查顯示有高達42%的新診斷PD患者符合PD-MCI的標準[2]。一項隨訪研究表明初診斷PD認知正常的患者,5年后隨訪PD-MCI的患者達到29%,39%的PD-MCI病例在5年后進展為癡呆,其中59%的PD-MCI病例僅持續1年就轉變為PDD[3]。目前認知功能的減退已成為PD致殘的重要因素,因此早期識別、預防、改善認知功能損害對提高PD患者生活質量具有重要的臨床意義。目前,PD的發病機制尚不明確,近年研究表明,血脂代謝異常、同型半胱氨酸(Hcy)水平升高可能與PD的發生相關[4];在對PD認知障礙的研究中發現患者血脂異常、Hcy升高[5-6],這提示血脂、Hcy水平可能與PD認知障礙有關,但目前的相關研究較少。本研究通過測定PD患者的血脂、血清Hcy水平及認知功能,探討血脂、血清Hcy水平與PD認知障礙程度的相關性。
1 資料與方法
1.1病例選擇 選擇2019年9月至2021年8月在錦州市中心醫院神經內科就診的PD患者100例納入PD組,其中男性54例,女性46例,平均年齡(67.38±6.83)歲,病程1~12年。納入標準:(1)年齡在40~80歲之間;(2)符合中華醫學會神經病學分會PD及運動障礙學組PD診斷標準[7]。排除標準:(1)帕金森綜合征和帕金森疊加綜合征、其他神經系統變性疾病;(2)阿爾茨海默病、血管性癡呆、額顳葉癡呆等其他類型癡呆;(3)嚴重的其他全身性疾病等導致的認知障礙;(4)嚴重焦慮、抑郁和精神分裂癥等精神疾病;(5)糖尿病、甲狀腺疾病等代謝疾病;(6)心、肝、腎功不全,全身重度感染等嚴重疾病;(7)近3個月服用影響血脂及Hcy水平藥物。
選取同時期在本院體檢的健康體檢者50例納入對照組,男26例、女24例,平均年齡(65.44±7.87)歲。納入標準:無PD和PD家族史,體檢史均正常。排除標準:同PD組。兩組性別、年齡相匹配。所有研究對象均為本地區居民,飲食結構及生活習慣相似,且未服用降脂藥物。所有入組者或其家屬均為自愿并簽署知情同意書。
1.2方法
1.2.1神經心理評估及亞組分組 本研究分別采用漢密爾頓抑郁量表(Hamilton depression scale, HAMD)、漢密爾頓焦慮量表(Hamilton anxiety scale, HA-MA)評估PD患者的抑郁和焦慮;采用蒙特利爾認知評價量表(Montreal cognitive assessment scale,MoCA)評估認知功能。評分標準:≥26分為PD認知正常(Parkinson disease normal cognition,PD-NC), 21~25分為PD-MCI,<21分為PDD。受教育年限≤12年者 ,MoCA評分上加1分以校正。根據MoCA評分結果將PD組患者分為PD認知功能正常(PD-NC)亞組38例、PD-MCI亞組32例和PDD亞組30例。上述評分操作是由專業人員實施。
1.2.2生化檢查 所有被檢測者于清晨空腹抽取外周靜脈血5 ml,由錦州市中心醫院檢驗科使用全自動生化分析儀檢測血脂和血清Hcy水平,其中血脂包括總膽固醇(TC)、甘油三酯(TG)、低密度脂蛋白膽固醇(LDL-C)、高密度脂蛋白膽固醇(HDL-C)。
2 結 果
2.1PD組與對照組血脂、血清Hcy水平比較 PD組Hcy水平顯著高于對照組(P<0.05),TC、TG、LDL-C水平顯著低于對照組(P<0.05),HDL-C水平差異無統計學意義(P>0.05),見表1。
表1 PD組與對照組血脂、血清Hcy水平比較
2.2PD組各亞組間血脂、血清Hcy水平比較 PD組3個亞組的TG、LDL-C、Hcy水平差異有統計學意義(P<0.05)。與PD-NC亞組相比,PD-MCI亞組、PDD亞組Hcy水平均顯著增高(P<0.05),而PDD亞組TG、LDL-C水平顯著增高(P<0.05);與PD-MCI亞組相比,PDD亞組Hcy水平顯著增高(P<0.05);3個亞組間TC、HDL-C水平差異無統計學意義(P>0.05), 見表2。
表2 PD組各亞組血脂、血清Hcy水平比較
2.3PD認知障礙影響因素的多因素分析 將是否患有PD認知障礙作為因變量, 以影響PD認知功能的有統計學意義的因素(TG,LDL-C,Hcy)作為自變量進行多因素Logistic回歸分析, 結果顯示Hcy水平是影響PD認知障礙的獨立危險因素, 見表3。
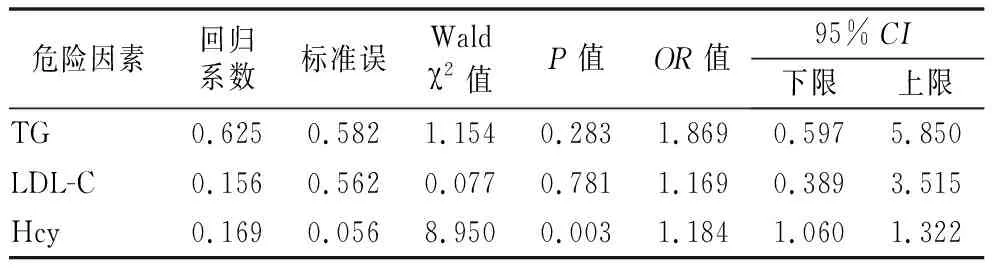
表3 PD認知障礙影響因素Logistic回歸分析
3 討 論
PD是一種以含α-突觸核蛋白的路易小體和黑質多巴胺神經元缺失為特征的神經系統退行性疾病。其發病機制十分復雜,目前主要認為可能是氧化應激、神經毒性作用、中樞神經系統炎癥及免疫反應、線粒體功能障礙等互相交織共同作用的結果[8-11]。
在對PD血清標志物的研究中,主要認為低血脂水平與高Hcy水平可能與PD的發病相關,本研究顯示PD組Hcy水平顯著高于對照組(P<0.05),TC、TG、LDL-C水平顯著低于對照組(P<0.05),推測血脂水平降低、Hcy水平升高可能與PD發病具有相關性,這與國內外大部分研究結果相一致[12-13]。有研究顯示交感神經活性降低在PD運動障礙發生前已經被發現,進而使機體分泌兒茶酚胺和皮質醇減少,從而引起血脂水平的降低,并且血脂水平的降低可能在PD發病前就已經出現[14-15];同時發現血清TC水平的降低與血清輔酶Q10水平降低相關,輔酶Q10水平降低可導致線粒體功能障礙,進而引起多巴胺能神經元變性死亡[16],因此,血脂水平的降低可能在PD發生前就已出現。同時PD的一些非運動癥狀如消化不良、攝入不足、焦慮抑郁等也可引起營養不良導致血脂降低[17],而PD患者營養不良還與左旋多巴制劑的不良反應相關[18],低血脂到底是PD營養不良的伴隨癥狀,還是PD的致病因素,目前尚未明確,還需要進一步的臨床研究來證實。
認知障礙作為PD最常見的非運動癥狀之一,嚴重影響患者的生活質量,增加社會負擔。PD認知能力下降可能涉及多種因素的復雜相互作用,包括運動和非運動癥狀、醫學共病和社會心理問題等。隨著病程的延長,發病風險逐漸增高,但PD認知障礙的發病機制尚無統一定論。目前其病生理基礎主要認為可能是α-突觸核蛋白聚集形成的路易小體與β淀粉樣蛋白(amyloid β,Aβ)沉積共同作用導致認知功能受損[19-20]。
在對血脂的研究中,Fantini 等[21]發現α-突觸核蛋白含有兩個膽固醇結合領域,膽固醇可能調節α-突觸核蛋白聚合, 表明膽固醇可能參與認知障礙發病的過程。有研究表明TG可穿過血腦屏障,作用于下丘腦,并誘導體內瘦素和胰島素抵抗[22];同時有研究證明TG水平升高還可使大腦內Aβ沉積增加[23],從而使認知功能下降。研究顯示PD黑質神經元和路易小體邊緣出現載脂蛋白E(ApoE)過度表達,ApoE是腦內主要的脂質和膽固醇轉運體,其中ApoE2基因被證實與LDL-C水平降低有關,而ApoEε4等位基因表達則會損害PD患者的認知功能[24-25]。Chaudhary 等[26]研究表明ApoE4等位基因與LDL-C水平升高有關。以上研究表明血脂可能與PD認知障礙有關。本研究結果顯示PD不同認知水平的3個亞組間的TG、LDL-C水平差異有統計學意義(P<0.05),且隨著認知障礙程度加重,TG、LDL-C水平逐漸升高,推測TG、LDL-C水平升高可能與PD認知障礙發生有一定的相關性。但本研究樣本小,研究方法等存在局限性,血脂水平是否會增加PD認知障礙的發病風險,以及是否對PD認知障礙產生預測作用,有待于更多臨床與基礎類的研究來證實。
Hcy是人體內一種重要的含硫氨基酸,參與機體的甲基化途徑與氧化應激的發生。有研究表明Hcy水平升高是認知能力下降和癡呆的危險因素,并與MCI、阿爾茨海默癥、血管性癡呆和抑郁癥有關[27]。Song等[28]發現Hcy水平升高可能與PD患者的認知能力下降有關。此外,Sleeman 等[29]研究也發現高Hcy水平與認知能力下降有關,Hcy可能是預測認知能力下降的標志物。本研究結果表明PD組不同認知水平的3亞組間Hcy水平差異有統計學意義(P<0.05), 且隨著認知障礙程度加重而升高。以是否患PD認知障礙作為因變量對Hcy水平的Logistic 回歸分析顯示Hcy是PD認知障礙的獨立危險因素。推測高Hcy水平可能與PD患者認知功能損害嚴重程度具有一定的相關性,Hcy可能是PD認知障礙的獨立危險因素。本研究結果與上述研究結果相一致。近年來,研究發現高Hcy水平導致認知障礙可能與以下因素相關:Hcy通過谷氨酸受體通道介導神經毒性作用,誘導鈣內流,使胞質內鈣累積,激活細胞凋亡途徑,從而誘導多巴胺能神經元細胞凋亡[30];Hcy還可以增加神經元內α-突觸蛋白含量和Aβ沉積, 促進路易小體形成,介導神經元損傷, 從而加重患者認知損害[31-32]。
綜上所述,PD患者中TG、LDL-C、Hcy水平可能與認知功能損害有關,并且TG、LDL-C、Hcy水平增高可在一定程度上反映PD患者認知功能損害的程度。但本研究存在樣本量小、臨床量表評估主觀性強的局限性,還需要進行大規模的研究來探討血脂、Hcy與PD認知障礙程度的相關性,以及血脂與Hcy成為PD認知障礙生物標志物的可行性。

