重癥監護病房耐碳青霉烯類肺炎克雷伯菌分子流行病學研究
楊程茹,王 英,李 瑩,張吉生,曾令怡,胡可望,張曉麗
(1. 佳木斯大學附屬第一醫院檢驗科,黑龍江 佳木斯 154007;2. 重慶醫科大學附屬永川醫院檢驗科,重慶 402160;3. 重慶醫科大學附屬永川醫院核醫學科,重慶 402160)
肺炎克雷伯菌(Klebsiellapneumoniae, KP)是一種臨床常見病原體,可引起傷口、呼吸道、泌尿道和胸腔積液多種感染[1]。由于碳青霉烯類抗生素的使用,導致耐碳青霉烯類肺炎克雷伯菌(carbape-nem-resistantKlebsiellapneumoniae, CRKP)已在全球范圍內流行。據報道,北美、南美、歐洲和亞洲CRKP的病死率分別為33.24%、46.71%、50.06%和44.82%,嚴重威脅著全球公共安全[2]。產碳青霉烯酶是CRKP主要的耐藥機制,因編碼碳青霉烯酶基因可位于基因組(染色體)DNA或質粒上,并可通過質粒進行水平轉移,所以在同一醫院同一病區更易發生CRKP克隆傳播和水平傳播。本研究分析重癥監護病房(ICU)臨床CRKP菌株,明確其耐藥機制及快速傳播途徑,為醫院感染控制提供分子流行病學依據。
1 對象與方法
1.1 研究對象 重慶醫科大學附屬永川醫院2018年7月—2020年7月ICU患者分離的51株CRKP,無重復分離株。
1.2 菌株鑒定及藥敏試驗 采用法國生物梅里埃公司VITEK 2 Compact 全自動微生物分析儀鑒定菌株以及進行藥敏試驗,根據美國臨床和實驗室標準協會(CLSI)2020年版指南的規定,選取對碳青霉烯類(亞胺培南、美羅培南或厄他培南)耐藥的臨床分離株。所有患者信息均從電子病歷中獲得,包括年齡、性別、入住ICU的時間、診斷和轉歸等信息。微量肉湯稀釋法檢測亞胺培南(IMP)、美羅培南(MEM)、左氧氟沙星(LEV)、阿米卡星(AK)、多粘菌素B(PB)、替加環素(TIG)和頭孢他啶/阿維巴坦(CAZ/AVI)的最低抑菌濃度(MIC)。ATCC 25922、ATCC 700603和BAA-1705作為質控菌株,3次平行檢測。TIG藥敏結果根據歐洲抗菌藥物敏感性試驗委員會(EUCAST)的標準判讀,其他抗菌藥物的藥敏結果根據2020年版CLSI標準判讀。接合菌株EC600由浙江邵逸夫醫院俞云松教授團隊惠贈。
1.3 高黏液表型及耐藥表型檢測 采用拉絲試驗方法,用接種環挑取血瓊脂平板上新鮮菌落進行牽拉,黏液絲形成且長度≥5 mm則判斷為高黏液表型陽性,反之判斷為陰性。同時采用mCIM和eCIM方法檢測CRKP中碳青霉烯酶。按2020年版CLSI操作。
1.4 碳青霉烯酶等耐藥基因和毒力基因檢測 采用煮沸法[3]提取菌株DNA。參照文獻[4-7]設計引物,引物由上海生工生物工程公司合成,包括碳青霉烯酶基因(blaKPC、blaNDM、blaIMP-4、blaIMP-8、blaVIM-1、blaVIM-2和blaOXA-48)、ESBLs基因(blaSHV、blaTEM、blaCTX-M-1和blaCTX-M-9)、AmpC β-內酰胺酶基因(blaDHA和blaACC)、喹諾酮類耐藥基因[qnrA、qnrB、qnrS、qepA和aac(6’)lb-cr],以及質粒介導的多粘菌素耐藥基因(mcr-1和mcr-9),染色體介導的多粘菌素耐藥基因(mgrB、pmrA、pmrB、phoP和phoQ)。毒力基因包括:fim-H、magA、aero、allS、iroNB、kpn、mrkD、rmpA、uge和wcaG。陽性擴增產物送上海生工生物工程公司進行測序,并在BLAST中比對測序結果(https://blast.ncbi.nlm.nih.gov/Blast.cgi) 。
1.5 質粒接合試驗 供體菌(CRKP)和受體菌(大腸埃希菌EC600)1∶3混合于LB肉湯中,將混合物置于貼有濾膜的血平板上,在雙抗LB平板(含利福平600 μg/mL,美羅培南1 μg/mL)上篩選接合子。雙抗平板上生長的菌株檢測16S rRNA確認為大腸埃希菌,并檢測耐藥基因。
1.6 同源性分析 采用多位點序列分型(MLST)和脈沖場凝膠電泳(PFGE)進行同源性分析。 擴增肺炎克雷伯菌7個管家基因進行MLST分析(http://bigsdb.pasteur.fr/klebsiella/primers_used.html)。將PCR擴增陽性產物的測序序列上傳至MLST數據庫(https://bigsdb.pasteur.fr/klebsiella/klebsiella.html)。限制性內切酶Xba1在37℃下酶切,用Bio-Rad Chef Mapper系統在1%脈沖場認證的瓊脂糖凝膠上分離,18 h,14℃,電壓6 V/cm,使用BioNumerics軟件分析條帶圖譜。分析采用未加權對組法和算術平均法(UPGMA),用dice系數判斷菌株的親緣關系,聚類定義為相似度≥80%。
2 結果
2.1 菌株來源及藥敏結果 51株CRKP標本來源分別為痰31株(60.8%),肺泡灌洗液13株(25.5%),尿4株(7.8%),血2株(3.9%),分泌物1株(2.0%)。根據ICU分布圖(圖1),標本來源Ⅰ區13株(25.5%),Ⅱ區6株(11.8%),Ⅲ區8株(15.7%),Ⅳ區13株(25.5%),Ⅴ區5株(9.8%),Ⅵ區0株以及Ⅶ區6株 (11.8%)。45例(88.2%)患者有肺部疾病,其中44例(86.3%)接受了侵入性手術治療(氣管插管或有創通氣)。51株CRKP對IMP、MEM、頭孢他啶(CAZ)、LEV、AK、PB和TIG的耐藥率分別為96.1%(49株)、98.0%(50株)、100.0%(51株)、98.0%(50株)、49.0%(25株)、64.7%(33株)和3.9%(2株),對CAZ/AVI敏感率100%,見圖2。
2.2 毒力及耐藥表型檢測 51株CRKP中,僅4株(7.8%)在拉絲試驗中表現為高黏液表型。mCIM試驗陽性率為96.1%(49/51),其中mCIM陽性的CRKP中,1株eCIM陽性。見圖3。
2.3 耐藥基因和毒力基因檢測結果 51株CRKP檢出1種碳青霉烯類耐藥基因blaKPC-2,3種ESBLs基因(blaSHV、blaTEM、blaCTX-M-65),未檢出AmpC β-內酰胺酶基因(blaDHA、blaACC)。質粒介導的喹諾酮類耐藥基因(PMQR)僅檢出qnrS和aac(6’)lb-cr,均為1株。33株PB耐藥菌株未檢出質粒介導的PB耐藥基因mcr-1和mcr-9,而染色體介導的PB耐藥基因pmrA、pmrB、phoP和phoQ均表達,其中pmrA基因中未發現突變;但在pmrB基因發現了N8T、T228A、R256G、L254F、A246T 5種不同類型的突變,在phoP基因中發現了I201F突變,在phoQ基因中發現了D150G的突變;在mgrB基因中,也發現了IS3、IS1341和IS5不同類型的插入序列。檢出毒力基因uge、mrkD、kpn和fim-H,未檢測到wcaG、iroNB、allS和magA。僅1株菌(CRKP59)同時檢出aero和rmpA。見表1。
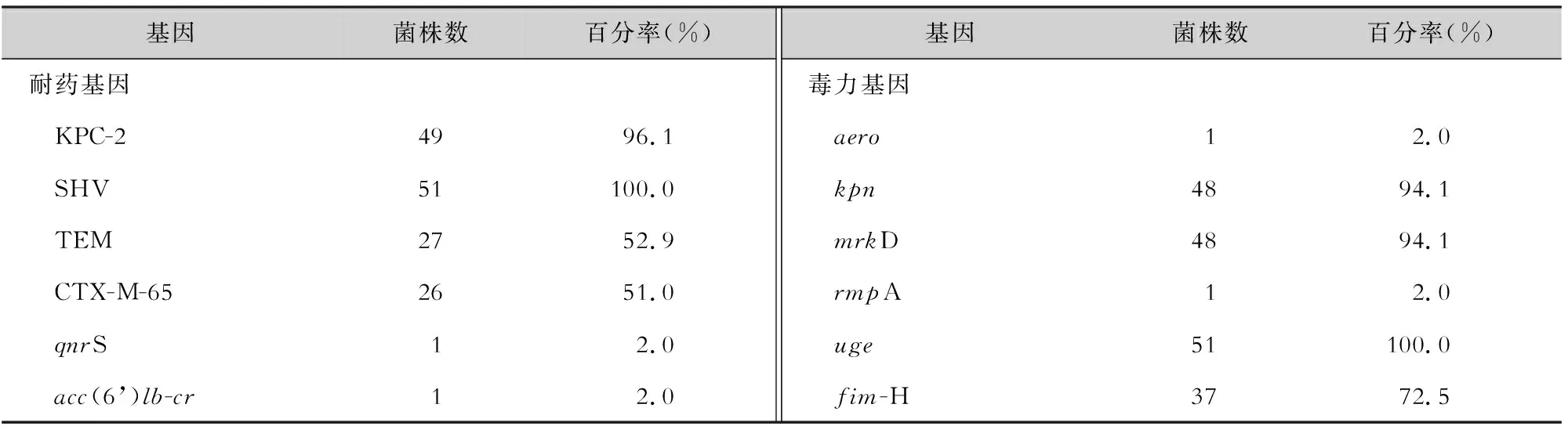
表1 51株CRKP菌株耐藥基因和毒力基因檢出情況
2.4 同源性分析 51株CRKP依據MLST分析共鑒定出2種ST分型,其中ST11型50株(98.0%),ST1373型1株(2.0%)。根據國際標準對PFGE結果進行解釋,將所有分離物分為5個不同的克隆群(A~E),A群32株(62.7%),B群11株(21.6%),C群4株(7.8%),D群3株(5.9%),以上均屬于ST11;E群(2.0%)1株,屬于ST1373。兩種檢測方法均顯示ICU中CRKP具有很高的同源性。見圖2。
2.5 接合試驗結果 49株攜帶blaKPC-2基因的菌株進行接合試驗,6株CRKP接合成功,接合成功率為12.2%。采用PCR檢測接合子耐藥基因攜帶情況,采用藥敏試驗檢測接合子藥敏情況,原始菌株與接合子在接合前后各基因的攜帶情況及MIC值變化見表2。
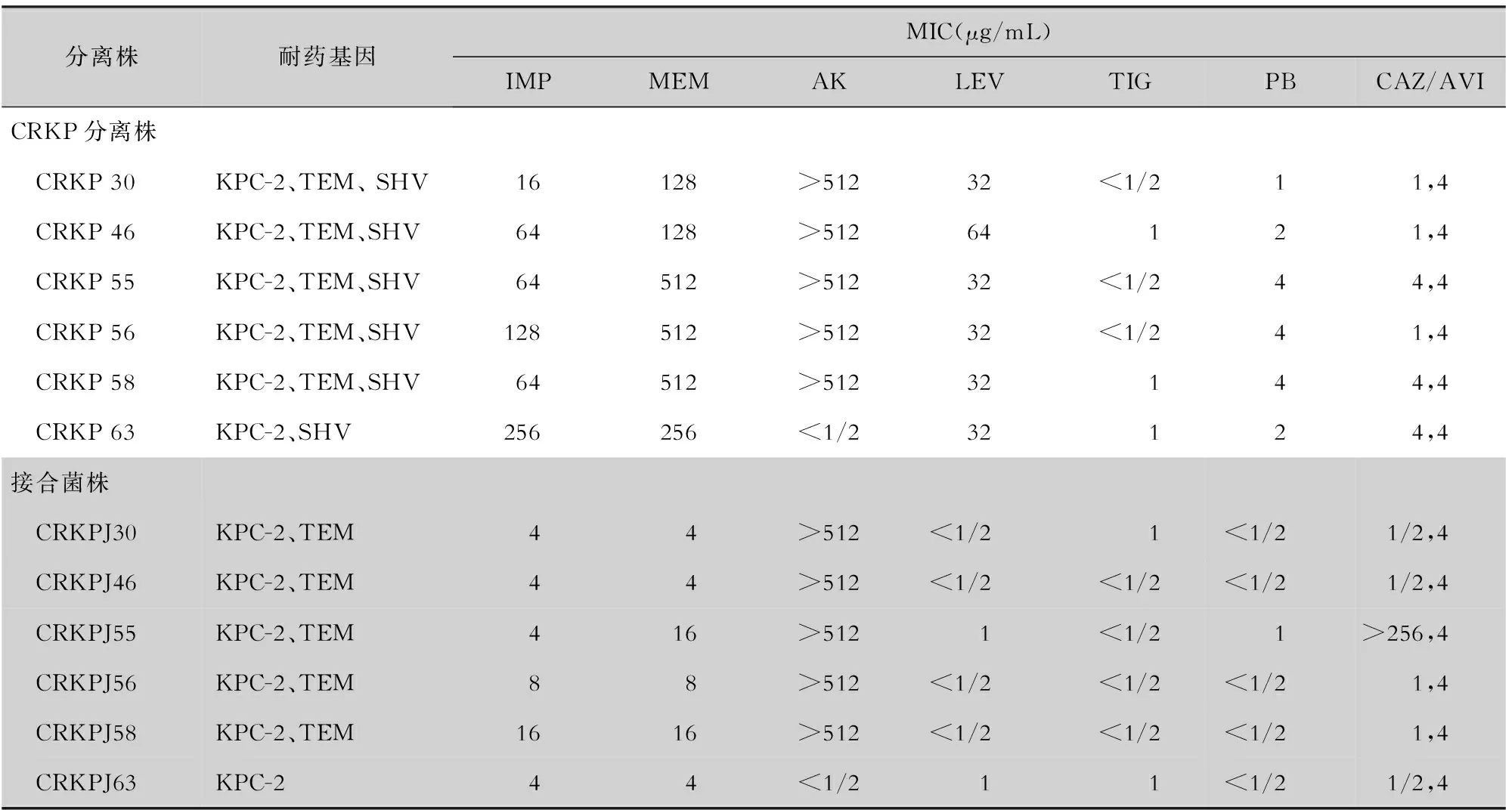
表2 CRKP原始菌株及接合子的耐藥基因攜帶情況及藥敏結果
3 討論
2019年CHINET細菌耐藥檢測網報道,全國、重慶和ICU CRKP檢出率分別由2014年的6.4%、2.5%和14.7%上升至2019年的10.9%、5.5%和23%[8],應加強抗菌藥物合理使用的管理以及醫院感染防控工作,減緩CRKP檢出率的持續上升。本研究針對2018年7月—2020年7月重慶醫科大學附屬永川醫院ICU CRKP暴發進行回顧性分析,為感染控制及其治療提供實驗室數據。
國內流行的CRKP主要以攜帶blaKPC-2基因的ST11為主[9-10],ICU患者CRKP感染率以及病死率均很高[11]。本研究中,49株mCIM陽性的菌株均攜帶KPC-2耐藥基因,且MLST均屬于ST11,與我國流行的基因型及克隆型一致[9]。同時所有菌株通過PFGE分成五簇,其中A、B、C、D四個簇的同源性非常高,均是ST11型。在兩種同源性分析方法中CRKP59均獨立成一型,分別為ST1373和E簇。分析ICU空間位置分布及患者感染時間圖(圖1、3)得出,攜帶blaKPC-2和blaSHV基因的ST11耐藥菌首先出現在Ⅳ區,并逐漸擴散到除Ⅵ區(可能與該區床位較少有關)外的其他相鄰區域,在Ⅰ區停留的時間最長,其中Ⅰ和Ⅳ區檢出數最高(均為13株),以A簇為主(20株)。單獨成一型的CRKP59菌株在Ⅲ區檢出,并且與該區上次耐藥菌檢出時間間隔大約6個月。攜帶blaKPC-2基因的ST11型CRKP暴發時間主要集中在2019年1月—10月,持續10個月之久。醫院受新型冠狀病毒肺炎疫情的影響,從2020年1月開始患者量有所下降,CRKP主要集中在Ⅰ區。針對此次ST11型CRKP在ICU暴發流行可追溯到某一菌株在不同區域間的水平傳播,需重視對耐藥菌的監測及追蹤,及時與病區工作人員溝通,加強醫院感染防控意識,以及病區的衛生與儀器設備的清潔消毒及醫護工作者手衛生的管理,更好地控制CRKP的播散。
此次暴發的菌株中,均對至少一種碳青霉烯類藥物耐藥,表型結果提示ICU內CRKP的耐藥機制以產絲氨酸酶為主,僅有1株(CRKP52)eCIM陽性,但PCR方法未檢測到本研究所用引物覆蓋范圍內的金屬β-內酰胺酶基因(MBLs),因此推測該細菌可能會產生其他超出范圍的MBLs,如blaSPM、blaGIM、blaSIM和blaAIM。KPC-2是本研究中的關鍵酶,其余耐藥基因也有檢出,與之前報道[12]一致,表明攜帶多種滅活酶是多重耐藥的主要機制。攜帶blaKPC-2基因是ICU中大多數CRKP產生耐藥的主要原因,blaKPC-2是一種典型的質粒介導的耐藥基因,廣泛分布于不同大小和類型的質粒中,這些質粒通常包含幾個編碼對氨基糖苷類、喹諾酮類、四環素類等耐藥的其他耐藥基因,并且高風險克隆促進不同的質粒、移動元件和耐藥基因在CRKP中傳播[13],接合試驗的成功證明耐藥質粒的可轉移性。blaTEM基因通常是blaKPC-2基因遺傳環境的一部分[14],結果顯示,這兩個基因都在質粒內轉移。在歐洲和美國,攜帶blaKPC基因的移動元件以Tn4401轉座子為主,而我國ST11 CRKP以Tn1721轉座子為主,說明blaKPC基因周圍環境存在一定的可變性及多樣性,是blaKPC基因在全球有效傳播的主要原因[15]。耐藥質粒的水平傳遞可以加速多重耐藥基因的擴散,介導多重耐藥菌的產生。接合試驗結果還表明,接合子的碳青霉烯類抗生素MIC值降低,說明還有其他耐藥原因,如膜蛋白、外排泵等不隨質粒轉移。
除碳青霉烯類藥物外,ICU患者對頭孢菌素類、AK、LEV表現出不同程度的耐藥。值得注意的是,由于未檢測到很高的PMQR,推測可能與染色體介導的喹諾酮類藥物耐藥決定區(QRDR)有關[16],這些CRKP可能在gyrA、parC基因和其他位點有突變,同時接合子對喹諾酮類藥物敏感性提高也證實了該假設,說明耐藥性基因沒有隨質粒轉移,而是可能存在其他的耐藥原因,如靶位染色體突變或者孔蛋白丟失等等。同時檢出較高的多粘菌素耐藥性(PR),由于多粘菌素被認為是治療CRKP感染的最后手段,盡管多粘菌素具有毒性強等不良反應,但由于效果好,在過去的幾年中還是被廣泛地使用[17]。多粘菌素暴露是PR出現的主要原因[17],但本研究中,僅1例患者接受了PB的治療。所以檢測了多粘菌素相關耐藥基因,未檢測到mcr-1及mcr-9基因,但與染色體介導的雙組份調節基因phoP/phoQ以及pmrB的突變、mgrB基因中插入序列的存在,其他學者的研究[18-19]也發現了類似結果,并且CRKP接合子對多粘菌素的敏感性提高,均表明研究中染色體變化是介導多粘菌素耐藥的重要原因之一。本研究中所有菌株對CAZ/AVI均敏感,該藥可作為該院產KPC酶CRKP的一種有效治療選擇。鑒定出的接合子CRKPJ55對CAZ/AVI產生耐藥,而供體菌并未表現耐藥,KPC-2沒有發生氨基酸變異,后續研究將進一步分析其與抗生素壓力下轉錄組表達的差異是否有關。
由于拉絲試驗對CRKP的毒力檢測敏感率低,有學者[20]將拉絲試驗和rmpA基因均陽性的菌株定義為高毒力肺炎克雷伯菌(hvKP)。本組研究發現,ICU中僅檢出1株(2.0%)hvKP(拉絲試驗陽性的基礎上同時攜帶rmpA和aero),低于其他報道[21]。研究鑒定的ST1373 hvKP對IMP、LEV、AK和TIG保持敏感性,可能是由于攜帶的耐藥基因數量較少所致。然而,除了ST1373 hvKP以外的其他菌株,與細菌定殖、菌毛黏附相關的fimH、mrkD和kpn,與細菌脂多糖相關的uge毒力基因檢出率高,表明毒力風險依然存在。88.2%的患者患有肺部疾病,60.8%的標本來自痰,由于患者呼吸受阻,44例(86.2%)患者接受了氣管插管和氣管切開等侵入性手術。研究[22]指出,有創機械通氣和腸外營養≥48 h是感染的危險因素。因此,應盡早拆除ICU中不必要的侵入性操作,預防醫院獲得性感染,并盡快建立腸內營養,以減少危險因素。
總之,針對此次 ST11 CRKP在該院ICU的暴發流行,耐藥機制主要為攜帶blaKPC-2基因,并可以通過接合水平傳播,雖然未對ICU污染區域進行長期、系統的抽樣,但有必要了解CRKP的動態分布和傳播,這是臨床治療中不容忽視的問題。及時、有效地采取感染控制措施對于減輕和控制醫院感染傳播和暴發的風險至關重要。根據歐洲臨床微生物學和傳染病學會(ESCMID)的指南,應實施手衛生教育計劃,采取接觸預防措施,并使用警告碼及時識別CRKP感染患者,并應隔離感染患者。此外,應實施積極篩查培養和抗菌藥物使用管理計劃,以減少多重耐藥革蘭陰性菌在醫院患者中的傳播,特別是在ICU中[23]。
利益沖突:所有作者均聲明不存在利益沖突。

