磁微粒化學發光法與電化學發光法檢測促甲狀腺激素受體抗體的一致性評價
隋 鑫 解 朋 黃建敏 高建青 景建敏 魏玲格▲ 吳煒杰 于宏偉
1.河北醫科大學第三醫院超聲醫學科,河北石家莊 050051;2.河北醫科大學第三醫院核醫學科,河北石家莊 050051
促甲狀腺激素受體抗體(thyrotropin receptor an-tibody,TRAb)陽性率高達80%~100%,不僅對于毒性彌漫性甲狀腺腫(Graves 病)的輔助診斷具有重要的價值,而且對于判斷Graves 病的活動期及制訂停藥計劃等均具有一定意義[1-3]。TRAb 是一組多克隆抗體,主要包括甲狀腺刺激性抗體和甲狀腺刺激阻斷性抗體,其中甲狀腺刺激性抗體是誘發Graves 病的主要致病抗體,通過激活促甲狀腺激素(thyroid stimulating hormone,TSH)受體引起甲狀腺功能亢進癥,而甲狀腺刺激阻斷性抗體可阻斷TSH 與受體結合,與甲狀腺功能減退癥發生有關[4]。隨著醫學檢驗技術的發展,TRAb 檢測方法逐漸增多,如放射免疫分析法、電化學發光法(electrochemical luminescence assay,ECLIA)等。由于放射免疫分析法耗時、具有放射性等缺點,目前已經較少使用[5-7]。電化學發光法測定TRAb 已經在科研中廣泛應用,但該方法在臨床上存在成本較高的缺點,一定程度上限制了其應用。磁微粒化學發光法(chemical luminescence assay,CLIA)具有操作簡便、耗時短、成本低等優點,已經在中國廣泛使用,但其在測定TRAb 的準確性上,目前缺少相關的研究[8-9]。本實驗室將磁微粒化學發光法與電化學發光測定TRAb進行對比分析,探討磁微粒化學發光法測定血清TRAb的可行性。
1 資料與方法
1.1 一般資料
收集2020 年11 月至12 月河北醫科大學第三醫院(以下簡稱“我院”)內分泌科門診及住院部送檢患者血清樣本。納入標準:①樣本容量>3 ml;②最終診斷明確;③年齡>18 歲。排除標準:①樣本存在溶血、脂血、乳糜血等情況;②高于或低于任意一種方法的檢測范圍;③補充生物素的患者除外。共納入118 例,其中女82 例,男36 例;年齡18~80 歲,平均(42.3±17.6)歲。臨床診斷原發性甲狀腺功能亢進癥43 例,其中36 例經甲狀腺血清學指標、超聲及體征確診為Graves 病患者,原發性甲狀腺功能減退癥8 例,橋本氏甲狀腺炎9 例,亞急性甲狀腺炎4 例,甲狀腺結節5 例,甲狀腺癌1 例,健康查體20 例及臨床診斷非甲狀腺疾病者28 例。
1.2 儀器和試劑
將血清樣本同時分別采用直接CLIA 和ECLIA兩種方法檢測TRAb。CLIA:使用深圳新產業Snibe MAGLUMI 4000Plus 磁微粒化學發光免疫分析儀及配套試劑、校準品、質控品。ECLIA:使用德國Roche Cobas e602 電化學發光免疫分析儀及配套試劑、校準品、質控品。實驗所需樣本容量為50 μl,總體實驗時間30 min,CLIA 和ECLIA 定量檢測TRAb 的線性范圍分別為0.25~40.00 IU/L 和0.3~40.0 IU/L,參考區間分別為<1.5 IU/L 和<1.75 IU/L。
1.3 研究方法
1.3.1 一致性評價 依據CLSI EP09-A3[10]文件,對118 例血清樣本進行兩種方法學一致性評價。
1.3.2 精密度驗證 參考CLSI-A3 文件,取低濃度和高濃度血清樣本,以CLIA 法,每個水平每天重復測定4 次,連續測定5 d,計算各自測量的均值、標準差及變異系數。判斷標準:以室間質評評價界限作為允許總誤差(TEa),批內變異系數(CV)<1/4 TEa,批間CV<1/3 TEa。
1.3.3 線性范圍驗證 參考EP6-A 文件,選擇一份濃度值在線性范圍上限的高值血清樣本(H)和一份濃度接近于零值的血清樣本(L),將2 份樣本按比例5H、4H+1L、3H+2L、2H+3L、1H+4L、5L 混合,以CLIA法檢測其濃度,每個樣本測定3 次,計算平均值,按照平均斜率法得出回歸方程Y=aX+b(Y 為均值,X 為理論值)。判斷標準:斜率a 為0.97~1.03 且R2≥0.95 則通過驗證。
1.3.4 參考區間驗證 參考CLSI C28-A3c 文件,選取健康查體人群20 名,入選標準為促甲狀腺激素、三碘甲狀腺原氨酸、甲狀腺素、游離三碘甲狀腺原氨酸、游離甲狀腺素、抗甲狀腺過氧化物酶抗體、甲狀腺球蛋白抗體均正常,以CLIA 法檢測TRAb,驗證試劑盒給定參考區間的適用性。判斷標準:若檢測結果≤2 例在參考區間之外,則該參考區間適用;若>2 例則需要自行建立參考區間。
1.4 統計學方法
采用SPSS 21.0 軟件對所得數據進行統計分析。利用散點圖及相關系數評價二者之間的相關性,差異性比較采用McNemar 檢驗。采用MedCalc 15.2 軟件進行Bland-Altman 偏差分析。
2 結果
2.1 ECLIA 和CLIA 檢測TRAb 的一致性評價
2.1.1 兩種方法檢測結果相關性 采用CLIA 和ECLIA兩種檢測系統檢測分別測定118 例血清樣本的TRAb濃度,ECLIA 為參比方法(X),CLIA 為待評價方法(Y),將檢測結果進行直線相關分析,散點圖顯示兩種方法檢測的TRAb 數值間存在直線相關性(圖1),決定系數R2=0.939,相關系數r=0.969,提示兩種檢測方法之間呈現較好的相關性。
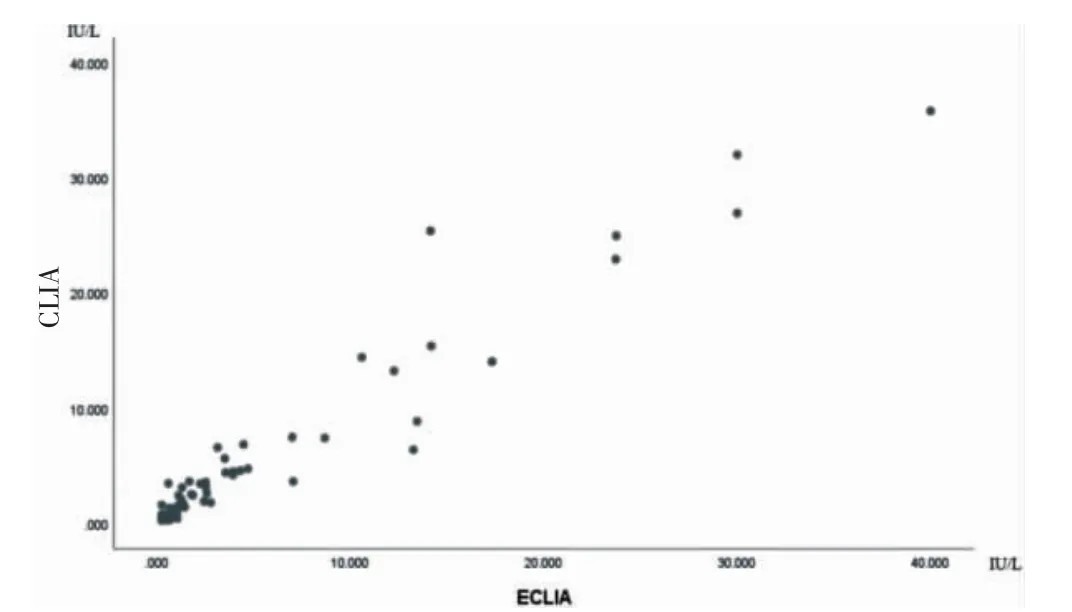
圖1 ECLIA 法與CLIA 法檢測TRAb 的散點圖
2.1.2 Bland-Altman 偏差分析 ECLIA 與CLIA 檢測TRAb 結果在低值區域(0~5 IU/L)一致性良好,95%界值范圍為-2.846~3.334 IU/L。隨著TRAb 濃度升高,偏差逐漸增大,其中有5.9%(7/118)的點在95%界限范圍之外,差值絕對值最高可達11.24 IU/L,即使在一致性界限范圍內,差值絕對值最高達3.5 IU/L。見圖2。

圖2 ECLIA 法和CLIA 法檢測TRAb 的Bland-Altman 偏差分析
2.1.3 診斷符合率 本實驗室共檢測我院門診及住院送檢患者血清樣本118 例。兩種方法檢測結果的陽性符合率為86.84%,陰性符合率為100%,總符合率為95.76%;一致性檢驗Kappa 值為0.8995(P <0.01),陰陽性符合率良好。見表1。

表1 兩種方法檢測TRAb 陰陽性差異性分析(例)
2.2 CLIA 法性能驗證
2.2.1 精密度 隨機選取低值和高值血清樣本采用CLIA 方法檢測其批內和批間精密度CV。見表2。兩個水平TRAb 的批內精密度CV 分別為2.68%和0.92%,批間精密度CV 分別為5.70%和1.48%。
表2 CLIA 法檢測TRAb 精密度結果(±s)
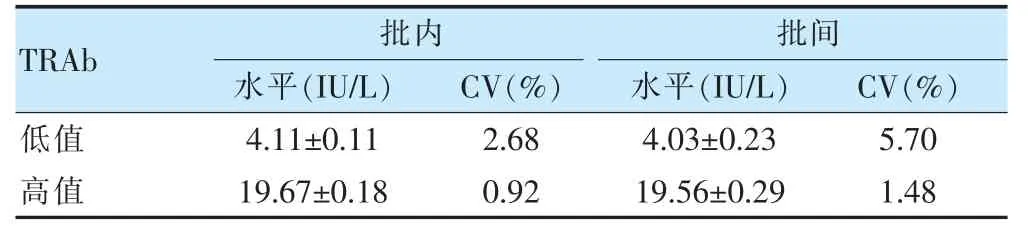
表2 CLIA 法檢測TRAb 精密度結果(±s)
注 CLIA:光化學發光法;TRAb:促甲狀腺激素受體抗體
2.2.2 線性范圍 選取的低濃度(L)血清樣本,濃度值為0.25 IU/L,高濃度(H)血清樣本,濃度值為40.0 IU/L。兩份血清樣本以不同比例混合后用CLIA 法檢測。對檢測結果與理論結果進行線性分析,擬合后線性方程為Y=1.0134X+0.0439,決定系數R2=0.9987,提示CLIA 檢測TRAb 值在0.25~40.00 IU/L 范圍內線性良好。
2.3 CLIA 法參考區間驗證
20 名健康體檢人群樣本,TRAb 檢測結果均在試劑盒給定的參考區間內,參考區間通過驗證。
3 討論
Graves 病是一種甲狀腺激素分泌增多的自身免疫性疾病[11-13]。現已證實TRAb 與Graves 病的病情發生和演變密切相關[14-15],TRAb 陽性的Graves 病患者停用抗甲狀腺藥物后復發風險顯著高于TRAb 陰性患者,而且TRAb 陽性率與甲狀腺激素水平呈正相關[16]。
ECLIA 是臨床及科研上目前測定TRAb 的常用方法[17-19],是基于“生物素-鏈霉親和素”系統的方法學可特異并高效地放大檢測信號,提高免疫檢測的靈敏度。但隨著越來越多人群補充生物素而造成外周循環中濃度的上升,一旦使用“生物素-鏈霉親和素”系統的免疫檢測試劑對這些人群的外周血樣本進行檢測,樣本中高濃度的游離生物素就會干擾鏈霉親和素捕獲目標分析物的能力,從而造成檢測結果的假性升高或者降低[20-22]。而且,ECLIA 的成本偏高,不利于在臨床上廣泛應用[8-9]。
CLIA 是基于人工合成的有機化合物異魯米諾為基礎的檢測方法,異魯米諾在人血清中不存在,因此不會對試驗結果產生干擾。其在測定TRAb 的準確性方面,目前沒有相關的研究[23-25]。
本研究共收集血清標本118 例,通過兩種方法檢測TRAb,相關系數r=0.969,兩種方法具有良好的一致性和相關性;而Bland-Altman 偏差分析顯示兩種方法在低值濃度部分(0~5 IU/L)一致性良好,但隨著TRAb 濃度的升高,偏差也逐漸增大;在陰陽性差異性分析中,陽性符合率為86.84%,陰性符合率為100%,總符合率為95.76%,提示兩種檢測方法總體檢驗一致性較好。此外,本研究中對CLIA 檢測TRAb 的批間、批內精密度、線性范圍進行驗證,其均符合檢測要求。
因此,本研究認為CLIA 和ECLIA 相關性良好,CLIA 可以作為臨床上檢測血清TRAb 含量的可靠方法。

