大豆長片段插入/缺失標記的開發與應用
李 曼,史曉蕾,邸 銳,劉志芳,孟慶民,付 才,楊春燕,王冬梅,張孟臣,張 潔,閆 龍
(1.華北作物改良與調控國家重點實驗室,河北省植物生理與分子病理學重點實驗室,河北農業大學 生命科學學院,河北 保定 071001;2.河北省農林科學院 糧油作物研究所,國家大豆改良中心石家莊分中心,農業農村部黃淮海大豆生物學與遺傳育種重點實驗室,河北省作物遺傳育種實驗室,河北 石家莊 050035;3.河北省種子總站,河北 石家莊 050031;4.河北省農林科學院 遺傳生理研究所,河北 石家莊 050051)
大豆(Glycinemax(L.)Merrill)為人類提供了1/3的植物蛋白和食用油,在農產品貿易中地位重要。近年來,我國大豆種業市場日趨活躍,大豆種子企業初具規模,育成品種(如黑河43、齊黃34、中豆63等)也已經實現品種權高價轉讓。但種子純度低、套名裝袋等不規范行為在市場上屢有發生。大豆種質資源保存過程中,同名異種、同種異名等現象也時有發生[1]。
我國各級區域試驗要求利用分子標記鑒定種子純度、并建立品種指紋圖譜[2-3]。簡單重復序列(Simple Sequencing Repeat,SSR)標記[4]、單核苷酸多態性(Single Nucleotide Polymorphic,SNP)標記[5]和插入/缺失片段長度多態性(Insertion/Deletion,InDel)標記[6-8]等,可用于大豆品種純度檢測和指紋圖譜構建[9]。SSR標記是目前各級區試品種純度檢測中普遍使用的分子標記,但利用SSR標記進行基因型分析時,多數位點產生的等位變異數目多,導致不同批次試驗結果間可比性差。插入/缺失標記是由于在不同個體間,等位基因位點的DNA序列發生核苷酸片段的插入/缺失產生的多態性變異[10-11],具有分布廣、全基因組密度高、等位變異數量少等優點。當某個標記的插入/缺失片段長度達到一定閾值后,其等位變異差異即可以通過PCR反應和瓊脂糖凝膠電泳分辨,從而開發成穩定可靠、操作簡便的分子標記。
為鑒定黃淮海地區各育種單位育成品系的農藝性狀、增產潛力以及適應區域[12],自2010年以來,黃淮海大豆育種協作網對有關育種單位選育出的新品系在西北春大豆區、黃淮夏大豆區覆蓋的10個省市開展了聯合多點鑒定,共有1 380份品種(含對照)參加聯合試驗。多點鑒定試驗報告已經成為推薦參加黃淮海地區各省級區試和國家區試主要的試驗依據。
本研究旨在開發在基因組中均勻分布、擴增效果好、插入/缺失片段大、可用于大豆品種指紋圖譜構建、操作簡便的插入/缺失標記,并利用所開發的標記,構建2018年黃淮海聯合鑒定的96份大豆參試材料的指紋圖譜,進行遺傳多樣性分析,為大豆種質資源評價利用和品種純度鑒定等提供參考。
1 材料和方法
1.1 試驗材料
1.1.1 用于開發InDel標記的試驗材料 用于開發InDel標記的材料包括:一年生野生大豆ZYD02738,美國引進品種Hobbit,我國東北地區育成品種綏農14、吉育101,黃淮海地區育成品種(系)冀豆17、冀豆12、冀HJ117、中黃13、中黃42、齊黃34、鄭196、徐豆16。
1.1.2 用于遺傳多樣性分析的鑒評材料 從2018年大豆黃淮海多點聯合鑒定試驗材料中,按照選育單位來源,選取96份材料,構建指紋圖譜并進行遺傳多樣性分析。
1.2 試驗方法
1.2.1 基因組DNA提取 按照康為世紀Nuclear Plant Genomic DNA Kit 新型植物基因組DNA提取試劑盒提取參試大豆材料的DNA。收集提取的DNA溶液后,用Nanodrop分光光度計檢測樣品DNA濃度和質量(OD260/OD280≈1.8),將檢測合格的DNA樣品濃度調至20 ng/μL,-20 ℃保存備用。
1.2.2 大豆基因組重測序 提取植物材料DNA利用超聲波將質檢合格的植物材料DNA片段化,然后將片段化的DNA進行片段純化、末端修復、3′端加A、鏈接測序接頭,用瓊脂糖凝膠電泳選擇片段長度大小,PCR擴增建立測序文庫,用Illumina HiSeqTM2500對質檢合格的文庫進行10倍深度重測序。對測序得到的原始reads進行質量評估,過濾得到Clean reads,用于后續的基因組序列拼裝[13-14]。重測序由北京諾禾致源科技有限公司完成。
1.2.3 InDel位點挑選與引物設計 將12份材料重測序結果與參考基因組序列(Glyma.Wm82.a2v1)進行對比,使用GATK軟件[15],挖掘大豆基因組中的InDel標記。在此基礎上,挑選長片段插入/缺失位點設計引物,選擇標準為:在大豆每條染色體選擇均勻分布的位點;插入/缺失片段長度≥20 bp;每個位點有且只有2個等位變異;多態性信息含量大于0.25。利用BioXM 2.6[16]設計引物,由金唯智公司合成。
1.2.4 PCR反應體系與引物篩選 PCR擴增采用康為世紀公司的2×EsTaqMasterMix(Dye),20 μL PCR反應體系為:DNA(20 ng/μL)1 μL,2×EsTaqMasterMix 10 μL,上游、下游引物(10 μmol/L)各1 μL,ddH2O 7 μL,將各組分充分混勻后,置于PCR儀中,反應程序為:94 ℃預變性3 min;94 ℃變性15 s,55 ℃退火15 s,72 ℃延伸 30 s,34個循環;72 ℃終延伸10 min。取5 μL PCR產物在1.0%瓊脂糖凝膠進行電泳檢測。120 V電泳35 min,凝膠成像儀下觀察。能夠擴增出條帶穩定、多態性高、且可用肉眼觀察插入/缺失類型條帶的引物可作為分子標記加以應用。
1.3 數據分析
1.3.1 InDel位點檢測注釋與分析 使用SnpEff軟件[17]對InDel進行注釋,統計分析基因間隔區、外顯子、內含子等區域內分布的InDel標記的數量。
1.3.2 遺傳多樣性指數計算 利用Popgene 32[18]軟件對引物在供試材料的擴增結果進行分析,計算每對引物的遺傳多樣性指數。
期望雜合度(Expected heterozygous number)[19]:即基因多樣性He=1-∑Pi2,其中,Pi為第i個等位基因的頻率,計算每個位點的期望雜合度,取平均值代表該群體的期望雜合度;
Nei指數(Nei diversity index)[19]:Nei=nHe/(n-1),其中,n為樣品數,He為期望雜合度;
香農指數(Shnnon wiener index)[19]:SHI=-∑(Pi×lnPi),其中Pi為第i個等位基因的頻率,分別計算獲得各位點的SHI,取平均值代表該群體的SHI;
多態性信息含量(Polymorphysm information content,PIC)[19]:
其中Pi和Pj分別為第i個和第j個等位基因頻率,n為等位基因數。
1.3.3 Structure群體遺傳結構分析 利用基于貝葉斯法的Structure 2.3.4軟件[20]對96份材料進行遺傳結構分析。步驟如下:①利用Excel整理電泳結果,變異類型為插入的位點記為1,變異類型為缺失的位點記為0,未檢測到變異類型的位點記為9,將Excel轉換為Structure支持的格式。②確定最佳群體組群K值。軟件K值范圍設置在2~7,重復次數設置為2,每個參數運行10次,每次運行的Burnin time和重復次數都設置為80 000。依據后驗概率值LnP(D)確定分組K值,當LnP(D)值最小時的K值即確定為最佳K值。
1.3.4 指紋圖譜構建 根據每個InDel標記對試驗材料檢測出等位變異的類型及有無構建指紋圖譜,變異類型為插入的位點記為1,變異類型為缺失的位點記為0,未檢測到變異類型的位點記為9,品種(系)純度計算公式:P=(S1-S2)/S1×100%,其中,S1為檢測InDel位點數,S2為雜合位點數[2,21]。
2 結果與分析
2.1 插入/缺失片段分布特征
參試材料全基因組重測序結果顯示,正確識別率大于Q20(99.9%)的堿基占比平均值為97.50%,正確識別率大于Q30(99.9%)的堿基占比平均值為93.48%,基因組GC含量平均值為36.23%,樣品平均重測序覆蓋率為98.70%,平均測序深度18.73X。
檢測到SNP、InDel共2種主要變異類型。其中,檢測到插入/缺失片段長度大于20 bp(包括20 bp)的InDel標記的數量為66 561,平均每條染色體的InDel標記的數量為3 262,其中第18號染色體分布的InDel標記最多,數量為4 521,第12號染色體分布的InDel最少,數量為2 019。各品種InDell數量不同(圖1),野生大豆基因組內分布的InDel多,大豆品種Hobbit染色體內分布的InDel較少。
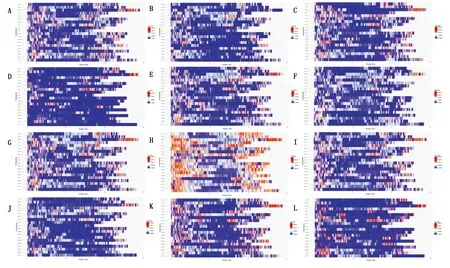
A—L.冀豆17、冀豆12、綏農14、中黃13、冀HJ117、Hobbit、吉育101、齊黃34、徐豆16、ZYD2738、鄭196、中黃42。A—L.Jidou 17,Jidou 12,Suinong 14,Zhonghuang 13,JiHJ117,Hobbit,Jiyu 101,Qihuang 34,Xudou 16,ZYD2738,Zheng 196,Zhonghuang 42.
如表1所示,檢測到的66 561個InDel標記主要位于基因間隔區、內含子區、外顯子區、5′-UTR、3′-UTR、基因上游序列和下游序列。位于基因上游序列和下游序列的InDel數量分別為17 190個(25.83%)和13 602個(20.44%),位于基因間隔區的InDel數量為22 893個(34.39%),位于外顯子的InDel數量為125個(0.19%),位于內含子的InDel數量為8 222個(12.35%),位于3′-UTR和5′-UTR的InDel數量分別為1 004(1.51%),617個(0.93%)。

表1 插入/缺失在基因組的分布Tab.1 Distribution of InDel in the genome
檢測到的66 561個InDel標記中,可鑒定長度的InDel有65 229個。片段長度大小介于20~40 bp的InDel數量為42 453個,介于41~60 bp的InDel數量為13 044個,介于61~80 bp的InDel數量為5 034個,介于81~100 bp的InDel數量為2 285個,大于100 bp的InDel數量為2 413個(圖2)。
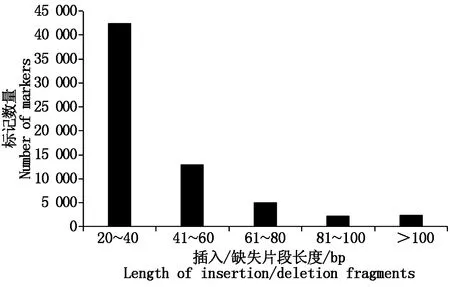
圖2 插入/缺失片段的長度分布特征Fig.2 Length distribution characteristics ofinsertion/deletion fragments
分析66 561個InDel標記在12份重測序材料中的PIC指數、Nei多樣性指數、香農指數可得,PIC指數為0.067~0.375,Nei多樣性指數標記數量為0.710~0.667,香農指數在0.154~0.693(圖3)。其中,PIC指數集中分布在0.100~0.200,0.300~0.400,所占比例分別為35.58%,33.01%;Nei多樣性指數集中分布在0.100~0.200,所占比例為33.56%;香農指數集中分布在0.200~0.300,0.600~0.700,所占比例分別為29.30%,24.09%。
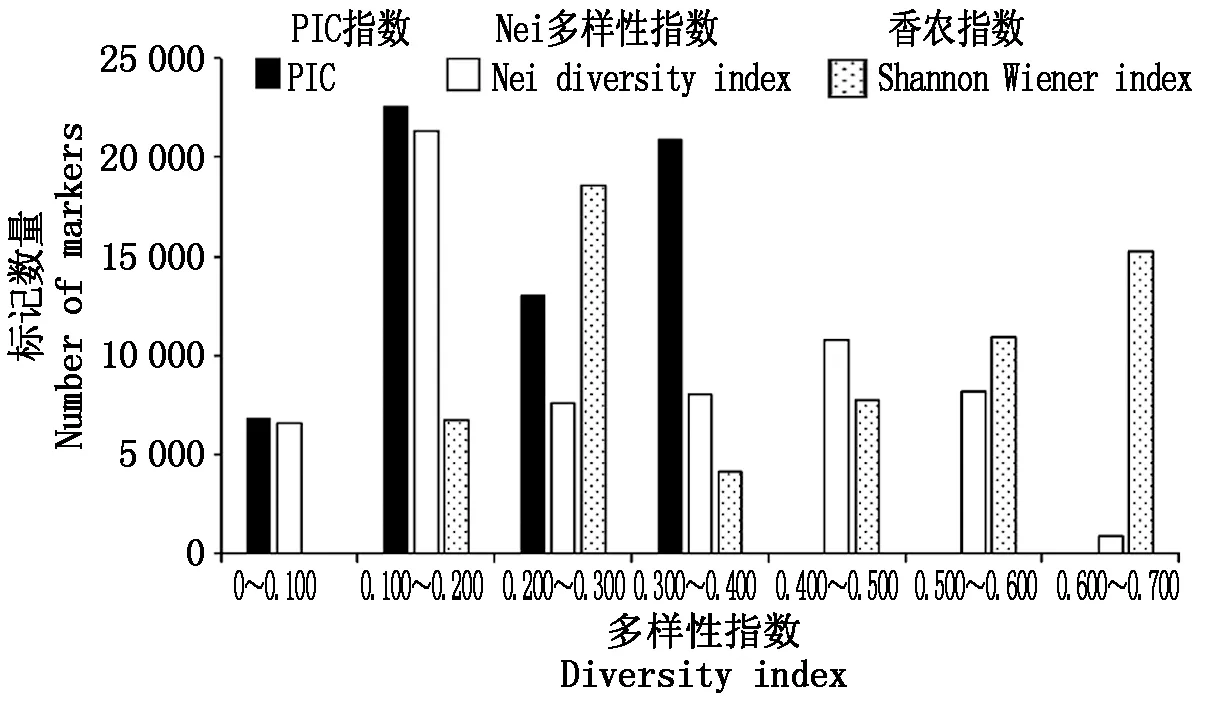
圖3 InDel標記的PIC指數、Nei多樣性指數、香農指數分布特征Fig.3 PIC,Nei diversity index,Shannon Wiener index′s distribution characteristics of InDel marker
2.2 長片段InDel標記開發
共設計160對InDel標記引物,在55 ℃的退火溫度下,109對引物擴增效果穩定、條帶清晰。其中,32對引物的擴增條帶經1%瓊脂糖凝膠電泳后,肉眼可分辨片段插入/缺失類型(表2、圖4)。
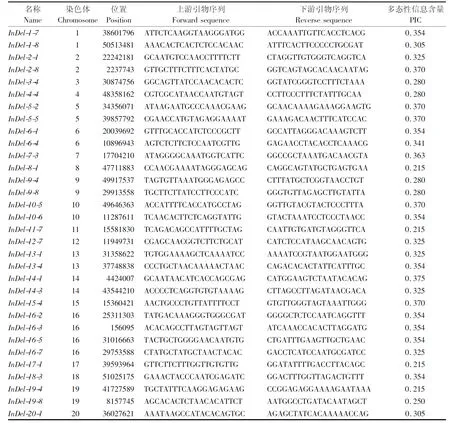
表2 32對插入/缺失標記引物信息Tab.2 Primer information of 32 insertion/deletion markers
2.3 InDel標記應用
利用 Popgene 32 軟件對32對引物在96份大豆材料中的擴增結果進行分析,每對引物的Nei指數分布在0.148 6~0.499 9,均值為0.393 5;香農指數分布在0.280 7~0.693 1,均值為0.577 9;PIC指數分布在0.152 8~0.595 3,均值為0.396 3,表明InDel標記在96份大豆材料中能較好地反映出其豐富的遺傳多樣性信息。
用InDel標記對參試材料構建指紋圖譜時,將檢測出變異類型為插入的位點記為1,變異類型為缺失的記為0,未檢測到變異類型的位點記為9(表3)。結果發現,用32對引物可將96份材料區分開,參試的大豆材料純度為96.84%,每份材料有唯一的指紋代碼,且沒有同物異名現象發生,因此,證明基于InDel標記構建的遺傳圖譜可以用于品種的鑒定。
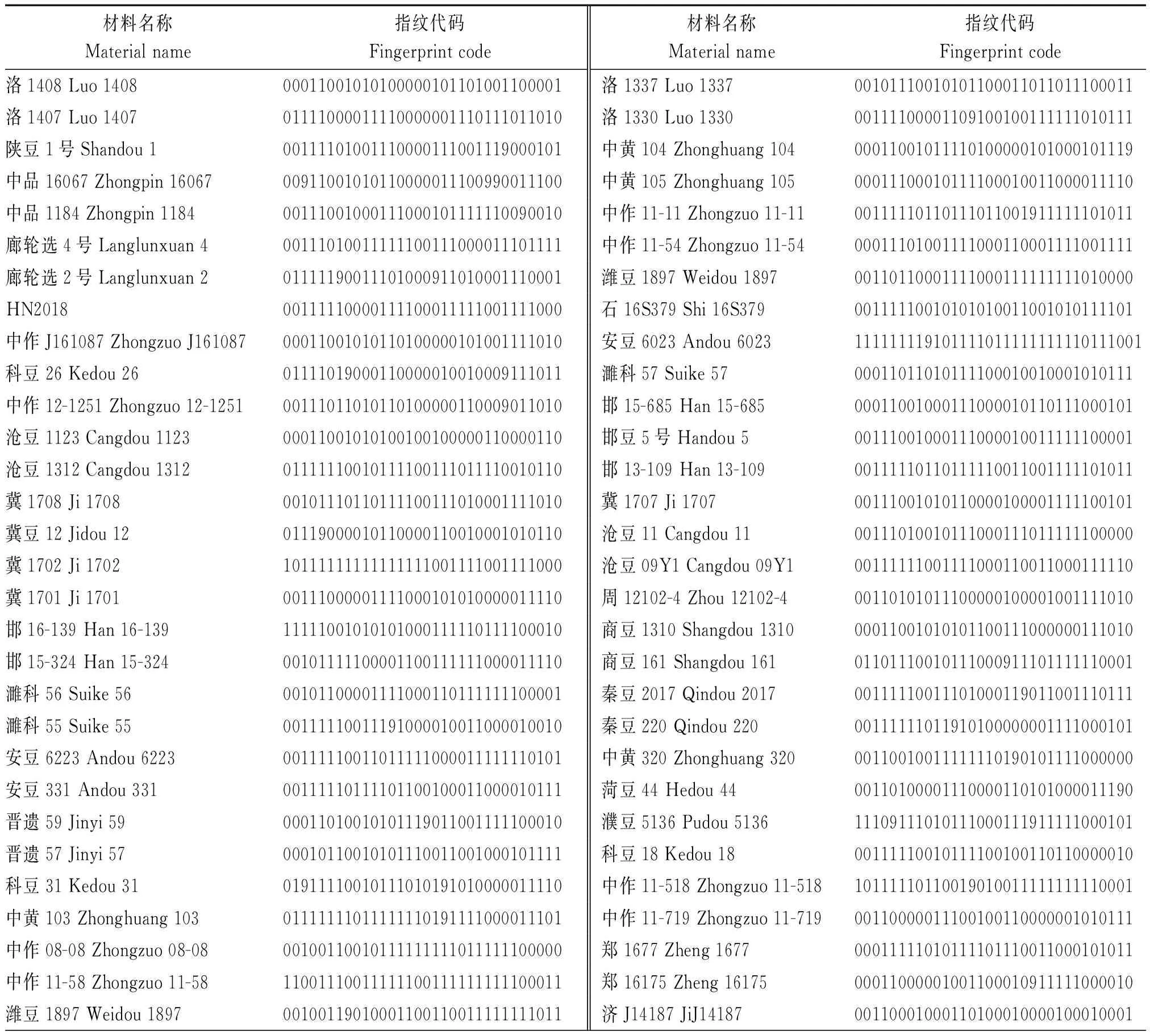
表3 96份黃淮海多點鑒定試驗材料指紋圖譜Tab.3 Fingerprint of 96 Huanghuaihai test materials
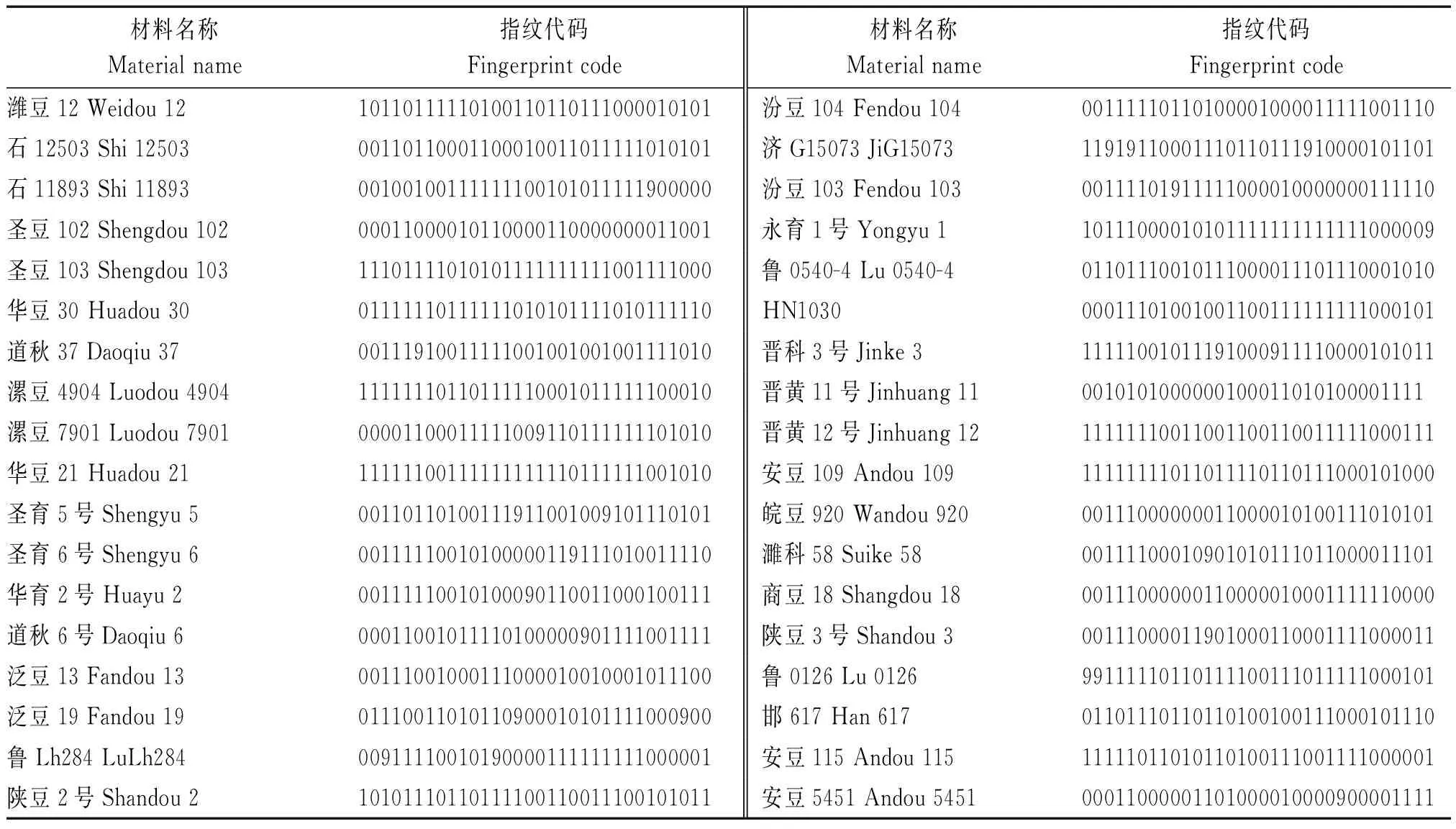
表3(續)
群體遺傳結構分析顯示,當K=5時,ΔK達到最大值。當K=5時擬合結果中的bar plot繪制大豆各品種所占比例。從圖5可以看出,Structure軟件將96份大豆材料分成了五大類群,分別用5種顏色表示,柱狀圖的高度描述的是不同品種被分到五類群所占比例。
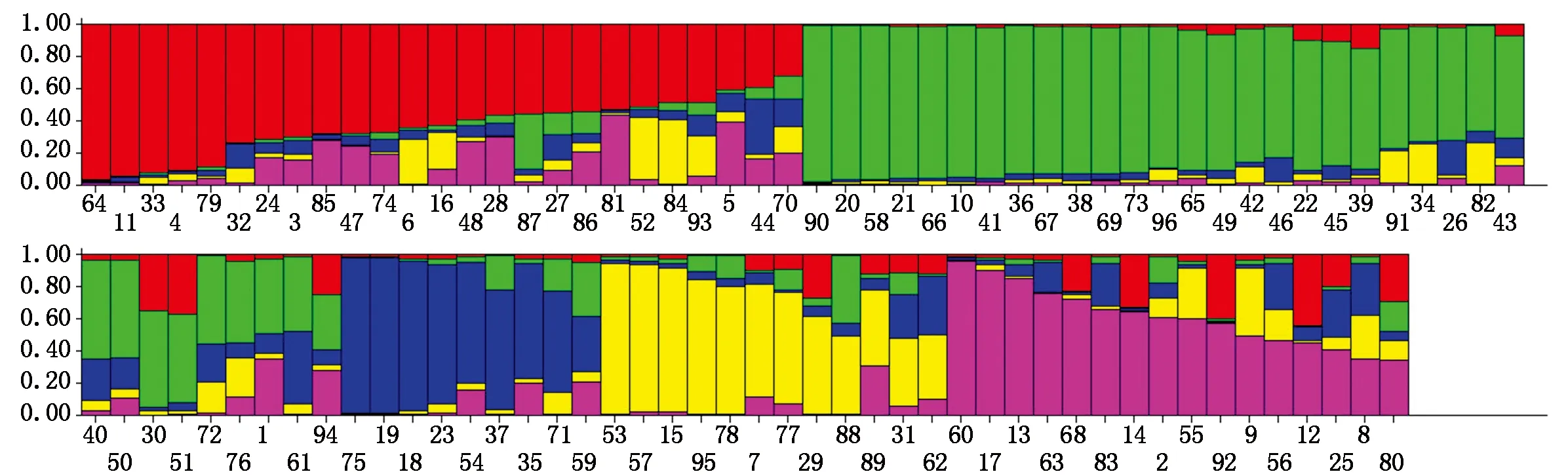
圖5 96份大豆種質的遺傳結構Fig.5 The genetic structure of 96 soybean germplasms
3 結論與討論
本研究中,InDel標記在基因組中的分布,呈現出兩端分布密度高,靠近著絲粒區域分布密度低的趨勢。并且,基因內無轉錄信息區域分布的InDel標記最多(34.39%),基因上、下游序列分布的InDel次之(分別為25.83%,20.44%),基因片段內分布的InDel最少(0.19%)。究其原因,如果InDel分布在基因CDS區內,核苷酸片段的插入/缺失可能會導致基因功能的喪失,進而影響生物體正常生命活動,導致該InDel標記不能在物種內穩定存在;反之,如果InDel發生在無轉錄信息的區域,則該InDel標記在物種中保留下來的機會將大大提高。
InDel標記具有特異性高、穩定性好、多態性高、經濟實用等特點,因此,InDel標記對種質資源的遺傳多樣性及種質資源鑒定具有廣闊的研究前景[22],在大豆[23]、水稻[24]、玉米[25]等作物中應用較多。本研究所開發的長片段插入/缺失標記具有2個突出特點:一是在種質資源里,每個位點有且僅有2個等位變異,因此,檢測結果易于讀取,不同批次試驗結果也易于比較。而目前國家區域試驗品種純度分析采用30對SSR標記進行檢測[2],大豆中平均每個SSR位點等位變異在6個左右,增加了數據讀取的難度。二是插入/缺失片段長(大于40 bp),可通過瓊脂糖凝膠電泳檢測。前人[26]開發的插入/缺失標記,沒有專門關注片段長度問題,大多數是介于1~5 bp,需要通過聚丙烯酰胺凝膠電泳檢測,操作繁瑣、不便于檢測。本研究開發的標記,可用瓊脂糖凝膠電泳對標記的有效性進行檢測,檢測手段方便快捷,結果便于觀察分析,可靠性高。利用本研究開發的InDel標記,構建了2018年黃淮海大豆多點鑒定參試品系DNA指紋圖譜,參試的大豆材料純度為96.84%,沒有同物異名現象發生,進一步證實了所開發標記的可靠性和簡便性。
本研究以全基因組重測序技術為基礎,對12份大豆種質資源進行重測序,建立了數據豐富、準確性高的測序文庫。比對大豆參考基因組序列,設計開發基于電泳檢測技術可清晰分辨的長片段插入/缺失InDel標記,可以對大豆種質進行遺傳多樣性分析,具有良好的應用前景。

