轉錄因子SlMYB-related 2對番茄耐冷性的影響
吳紅紅,段學粉,郭仰東,張喜春
(1.北京農學院 植物科學技術學院,北京市蔬菜遺傳育種與生物技術實驗室,北京 102206;2.中國農業大學 園藝學院,北京 100094)
番茄(SolanumlycopersicumL.)是茄科(Solanaceae)番茄屬(Lycopersicon)一年或多年生植物,在北方日光溫室冬春茬番茄生產中,夜間低溫是影響番茄植株生長最敏感的因素之一[1-2]。番茄生產經常遭受低溫冷害而降低經濟效益,影響產業發展[3]。
在植物生長發育過程中,MYB轉錄因子可以廣泛調控植物的生物和非生物脅迫,其可以與其他相關轉錄因子協同作用,特異激活防御相關基因的表達,在基因調控網絡中是其他調控因子的中間靶標。因而,通過調節轉錄因子活性來改良植物的綜合抗逆性是一種很有潛力的方法。CRISPR/Cas9(Clustered regularly interspaced short palindromic repeats/CRISPR associated systems)是來源于原核生物的適應性病毒技術。在自然界中,當病毒入侵時,CRISPR系統表達Cas蛋白和與病毒基因組互補的guide RNA,guide RNA引導Cas蛋白結合到對應病毒基因組切割DNA,進而抑制病毒,起到防御作用[4],近幾年在植物基因編輯研究中應用得越來越廣泛。2019年,Yuan等[5]率先通過CRISPR/Cas9技術對花生的脂肪酸去飽和酶基因ahFAD2進行突變,實現了對花生的基因編輯。2020年,Dong等[6]通過CRISPR/Cas9技術實現在水稻基因組中的安全位置插入了5.2 kb類胡蘿卜素生物合成元件,結果表明,該水稻種子中的類胡蘿卜素含量高,并且形態及產量特性與野生型相似,為在作物中精確的基因敲入提供了思路。Zhou等[7]針對J809、L237和CNXJ這3個優質水稻品種進行產量相關性狀基因的QTL定位,發現了影響籽粒大小相關的基因GS3、長度和質量相關的基因GW2(Grain width and weight gene 2)和數量相關的基因Gn1a,利用CRISPR/Cas9技術對3個基因進行靶向編輯,使得水稻品種J809和L237的三重突變體的單穗產量分別增加了68%和30%。Zaman等[8]利用CRISPR/Cas9技術定向敲除影響油菜莢果形狀和大小的JAG(Jagged gene)同源基因JAG.A08,所得突變體與野生型比較,莢果開裂區發生顯著變化,莢果細胞變大,果實凹凸不平,體積變小,抗碎莢性提高了2倍。
病毒誘導的基因沉默(Virus-induced gene silencing,VIGS)是一種快速鑒定基因功能的方法,近年來在植物基因功能研究中應用廣泛。宋恬等[9]首次在扁桃花器官上建立了以TRV為載體的VIGS沉默體系,成功用攜帶pTRV2-AcCBF1的農桿菌侵染扁桃花器官且出現沉默效果。邱潤霜等[10]以番茄斑萎病毒(Tomatospottedwiltorthotospovirus,TSWV)N構建到pTRV-PTV00載體上,完成了TSWV介導NVIGS載體的構建,開闊了構建病毒內源基因沉默體系的新思路。CRISPR/Cas9技術實現基因編輯有賴于PAM序列,在附近無PAM序列的區域時無法進行編輯[11]。VIGS具備將cDNA文庫整合到病毒載體上進行高通量基因篩選分析的優勢[12]。VIGS技術可用于不同蔬菜物種間比較基因組學的研究[13]。
本研究根據低溫處理前后輻照誘變的番茄抗寒突變體和對照番茄(CK)的轉錄組測序結果,篩選響應低溫脅迫的差異表達基因SlMYB-related2作為研究對象,通過構建CRISPR/Cas9基因敲除載體獲得沉默陽性植株,選取SlMYB-related2基因片段,構建VIGS瞬時干擾沉默體載體,獲得轉基因再生植株,通過對番茄轉基因植株抗寒性的測定,進一步研究SlMYB-related2基因的功能,以期為進一步揭示番茄植株抗寒的分子機制以及為選育番茄抗寒品種提供理論依據。
1 材料和方法
1.1 試驗材料
1.1.1 植物材料 以俄羅斯栽培番茄品種Bolgogragsky(本實驗室種質編號25)為供試材料。該品種具有產量高、番茄紅素含量高等優點,但不耐低溫,易受冷害危害。
1.1.2 菌株、載體、酶和試劑 大腸桿菌菌株DH5α、農桿菌感受態細胞GV3101購自博邁德生物技術有限公司;CRISPR/Cas載體購自杭州百格生物技術有限公司;TRV載體由本實驗室保存;CRISPR/Cas載體構建試劑盒購自杭州百格生物技術有限公司;DNA Marker、pLB克隆試劑盒、質粒提取試劑盒均購自天根生化科技有限公司;DNA膠回收和純化試劑盒購自美國Omega Bio-Tek公司;XbaⅠ、SmaⅠ、rTaqDNA聚合酶、T4DNA連接酶及各種限制性內切酶、PrimeSTAR Max Premix等均購自寶生物(TaKaRa)工程(大連)有限公司。植物激素為Sigma產品;其他生化試劑由本實驗室保存。
1.2 試驗方法
1.2.1 CRISPR/Cas9基因敲除載體 通過百格網站(www.biogle.cn)在線生成基因的gRNA序列。CRISPR載體帶有U6啟動子及CaMV35S啟動子,后者表達潮霉素抗性基因,靶點序列一般選擇19 bp,然后加上AGG,AGG為PAM序列。CRISPR/Cas9載體示意及sgRNA靶位點信息如圖1。通過在線軟件查詢基因的CRISPR靶點引物,引物序列設計如表1所示。制備引物二聚體,將合成的引物加水溶解至10 μmol/L,按照表2體系混合后,95 ℃加熱3 min,然后以約0.2 ℃/s的速度緩慢降至20 ℃(可使用PCR儀)。將Target二聚體構建至CRISPR/Cas9載體,按表3體系在冰上混合各個組分,混勻后室溫反應1 h。參考標準步驟轉化大腸桿菌及農桿菌,大腸桿菌DH5α的轉化方法按照說明書進行操作,將單克隆菌液送至公司測序,測序正確的菌液提取質粒轉化農桿菌GV3101。
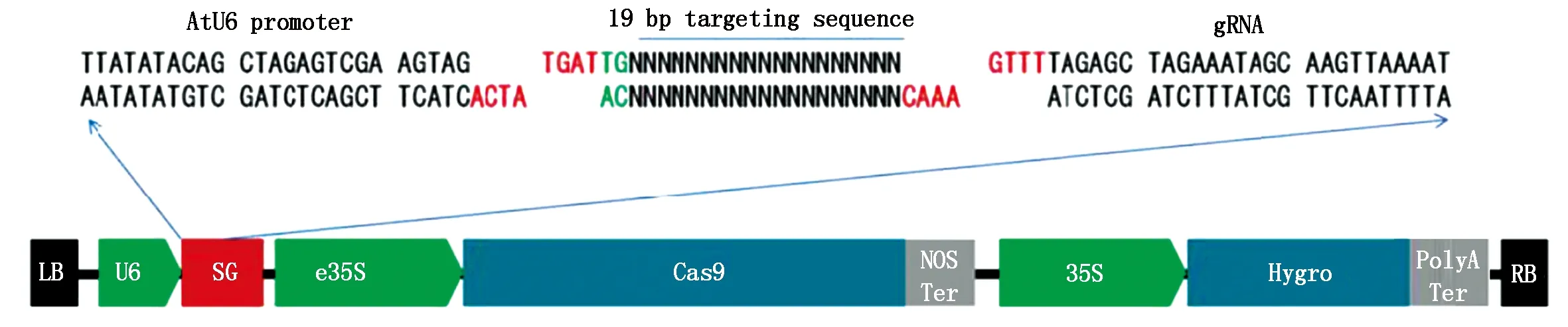
LB.T-DNA左邊界;Cas9.優化Cas9;RB.T-DNA右邊界;NOS Ter.NOS終止子;U6.擬南芥U6啟動子;35S.CaMV 35S啟動子;SG.向導RNA;Hygro.潮霉素選擇標記;e35S.增強子35S啟動子;Poly Ter.PolyA終止子。LB.Left border of T-DNA;Cas9.Optimized Cas9;RB.Right border of T-DNA;NOS Ter.NOS terminator;U6.Arabidopsis U6 promoter;35S.CaMV 35S promoter;SG.sgRNA;Hygro.Hygromycin selection marker;e35S.Enhanced 35S promoter;PolyA Ter.PolyA terminator.

表1 引物序列Tab.1 Primer sequence

表2 引物二聚體反應體系Tab.2 Primer dimer reaction system
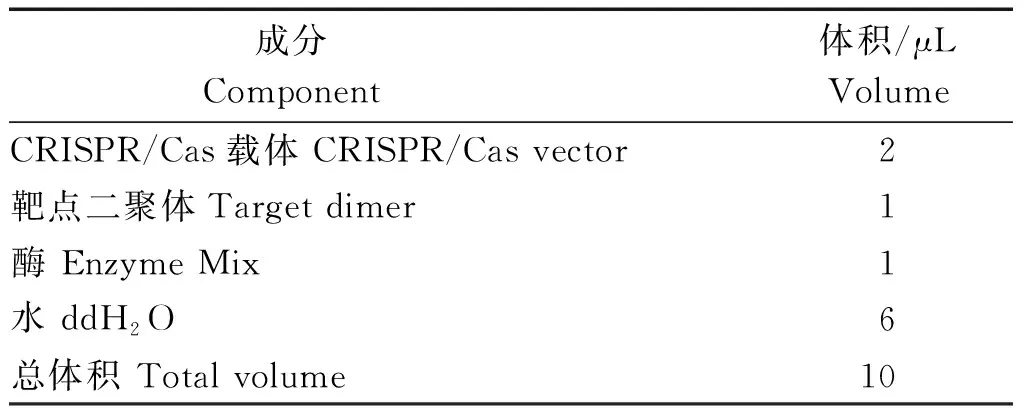
表3 CRISPR雙元載體構建Tab.3 Binary vector construction of CRISPR
1.2.2 農桿菌介導法遺傳轉化番茄 將番茄種子消毒后,播于MS培養基中,于溫度25 ℃、光照強度1 600 lx、光照時間16 h/d條件下進行培養,即得無菌苗;于溫度25 ℃、光照強度1 600 lx、光照時間16 h/d條件下進行預培養,用MS液體培養基懸浮農桿菌菌體(OD值0.3~0.5)制備成重組菌液;菌液侵染15 min,然后濾紙吸干菌液,放到A2培養基暗培養2 d;然后進行生根培養基的篩選與馴化移栽;最后鑒定并篩選陽性轉化苗,進行后續試驗。
1.2.3 轉基因植株的陽性鑒定 提取再生植株的DNA,以其為模板,根據載體上的潮霉素基因序列設計陽性鑒定引物,進行PCR驗證,1%瓊脂糖凝膠電泳。
1.2.4 VIGS瞬時沉默表達載體的構建 根據NCBI上提供的番茄SlMYB-related2基因CDS序列,利用Sol Genomics Network在線軟件設計SlMYB-related2VIGS特異性表達引物。目的片段用PCR擴增,瓊脂糖凝膠電泳回收,回收方法按照試劑盒進行,將純化回收的目的基因片段轉化大腸桿菌DH5α,將菌液送去測序。對測序結果正確的菌液以及含TRV質粒的菌液提取質粒,并用XbaⅠ和SmaⅠ酶切,純化后用T4連接酶連接,構建TRV-MYB-related2沉默表達載體。質粒提取和純化方法、酶切和連接體系,轉化方法按照試劑盒進行。取3~4葉期番茄幼苗用于VIGS試驗,將活化后的菌液用1 mL無針注射器侵染3~4葉期的番茄幼嫩葉片。侵染后,將番茄苗置于人工氣候箱中(16 ℃,65%相對濕度)暗培養24 h;后轉移至20 ℃、16 h 光照/8 h黑暗、65%相對濕度下培養。侵染植株分組為野生型(WT),野生型攜帶TRV空載(CK)和SlMYB-related2基因轉化組。侵染10 d后,分別提取3組植株嫩葉的總RNA,選取質量較高的RNA進行反轉錄合成第一鏈cDNA。以cDNA為模板,以載體上的TRV2F和TRV2R為引物,PCR擴增,驗證陽性植株。
1.2.5 低溫處理植株的理化指標測定 將番茄植株侵染14 d后,置于4 ℃培養8 h,之后按4 ℃、黑暗8 h/光照16 h、60%相對濕度培養,在低溫處理的第0,1,2,3,5,7,9 天分別采集野生型(WT)及其野生型攜帶TRV空載(CK)、SlMYB-related2基因轉化組番茄葉片液氮凍存,用于理化指標丙二醛(MDA)、可溶性糖、游離脯氨酸的測定。丙二醛和可溶性糖含量的測定參照《植物生理學實驗教程》[14]和Kong等[15]的方法,略有改動;游離脯氨酸含量的測定參照《植物生理學實驗教程》[14]和Ahmad等[16]的方法,略有改動。所有試驗均包含至少3個生物學重復,3次數據的平均值即為所得結果。對平均值進行方差分析(ANOVA,F-檢驗),并且在P<0.05(IBM SPSS?19)水平下使用Duncan多范圍測驗(DMRT)比較數據的平均值。
2 結果與分析
2.1 CRISPR/Cas9基因敲除載體的構建
將構建好的CRISPR/Cas9基因敲除載體轉化大腸桿菌感受態,單菌落進行PCR驗證。測序結果準確無誤的,提取質粒轉化農桿菌。圖2為載體測序比對結果,其中未匹配部分為載體序列,選取的基因靶點引物序列為gRNA:5′-CATTGGCATTCCCACCTTGTAGG-3′。

圖2 CRISPR/Cas9基因敲除載體序列比對Fig.2 CRISPR/Cas9 gene knockout vector sequence alignment
2.2 CRISPR沉默陽性植株的獲得
農桿菌轉化結果共獲得組培再生植株5株,經PCR驗證獲得2株陽性植株,結果見圖3。引物序列為,F:5′-CGAGAGCCTGACCTATTGCAT-3′和R:5′-CTGCTCCATACAAGCCAACCAC-3′,目標產物長度為481 bp。
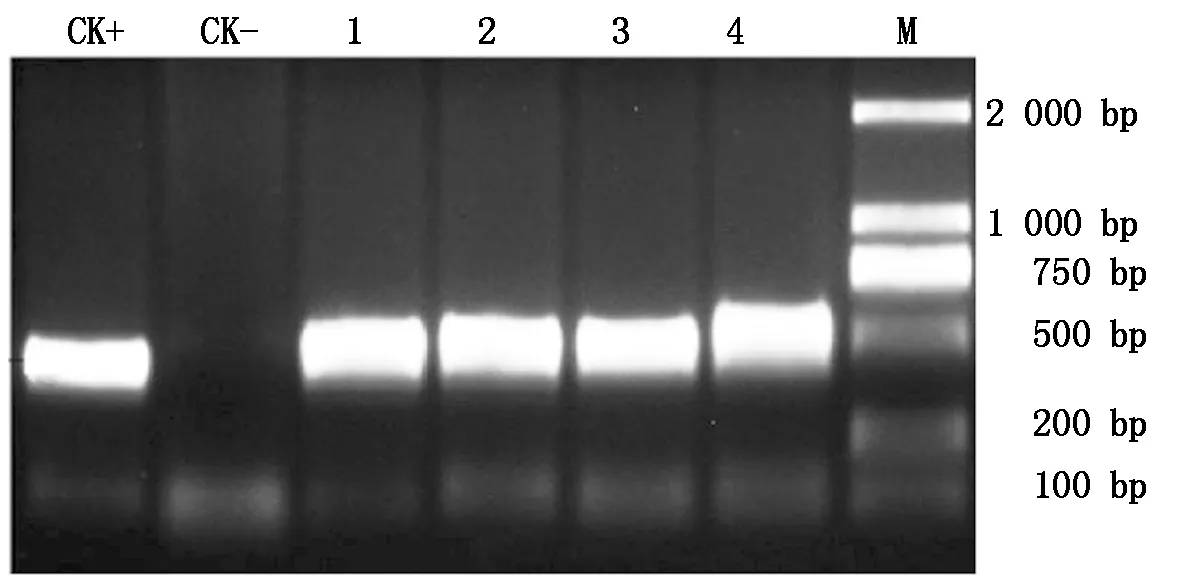
M.Marker;1—2.1號轉基因植株;3—4.2號轉基因植株。M.Marker;1—2.Transgenic plant 1;3—4.Transgenic plant 2.
2.3 VIGS瞬時沉默表達載體的構建
用XbaⅠ和SmaⅠ酶切野生型攜帶TRV空載(CK),插入目的基因片段,構建重組表達載體;將載體轉化大腸桿菌后,菌液測序結果與基因序列比對無點突變(圖4)。

圖4 VIGS瞬時沉默表達載體序列比對Fig.4 VIGS transient silence expression vector sequence alignment
2.4 陽性番茄植株鑒定
植株被侵染10 d后,分別提取3組植株上部嫩葉的總RNA,反轉錄合成cDNA。以cDNA為模板,通過克隆幼苗中的TRV病毒片段來驗證陽性植株,用RT-PCR法檢測番茄幼苗新生葉中的TRV病毒以驗證陽性植株(圖5)。經驗證,各組陽性植株數量為:攜帶TRV空載植株(CK)22株;攜帶TRV-SlMYB-related2質粒植株25株。目的基因長度為520 bp。

M.Marker;1.WT;2、3、4、6、7.TRV陽性;5.TRV陰性。M.Marker;1.WT;2,3,4,6,7.TRV positive;5.TRV negative.
2.5 低溫處理沉默轉基因植株的理化指標分析
2.5.1 游離脯氨酸含量比較 當植物受到外界低溫脅迫時,會加速合成脯氨酸,從而提高植物的抗寒性,脯氨酸含量可作為抗寒育種的生理指標。不同低溫處理時間的3組番茄植株的脯氨酸含量的變化水平如圖6所示,WT和CK組隨處理時間的延長脯氨酸含量逐漸升高,7 d達到最大值且差異顯著,然后略有下降,而轉基因組的脯氨酸含量1 d達到最大值,之后逐漸下降且均低于WT和CK組。說明轉基因組番茄植株遭遇低溫脅迫時未能較多地合成脯氨酸,推測SlMYB-related2基因可能與脯氨酸合成有關,通過對SlMYB-related2基因的沉默作用,抑制了脯氨酸的合成。
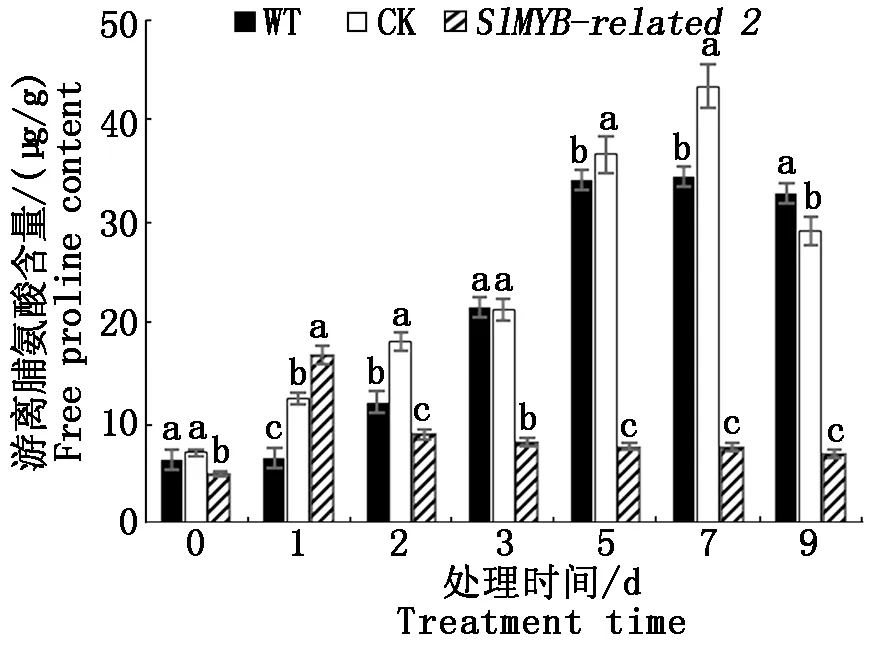
不同小寫字母表示0.05水平差異顯著性。圖7—8同。Different lowercase letters indicate significant differences in0.05 levels. The same as Fig.7—8.
2.5.2 丙二醛含量比較 不同番茄植株在不同低溫處理時間下丙二醛含量的變化如圖7所示,WT和CK以及轉基因組的丙二醛含量均有顯著性變化,其中在5~9 d轉基因組顯著高于WT和CK(P<0.05)。說明轉基因組的細胞膜損傷大于野生型和CK,低溫脅迫可能在一定程度上誘發了野生型和對照組植株對細胞膜損傷的修復。
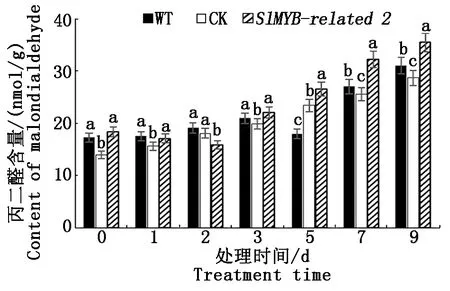
圖7 不同植株材料丙二醛含量比較Fig.7 Comparison of malondialdehyde content in different plant materials
2.5.3 可溶性糖含量比較 不同番茄植株在不同低溫處理時間下可溶性糖含量的變化如圖8所示,WT和CK以及轉基因組的可溶性糖含量均有顯著性變化,其中在處理5,7,9 d,WT和CK均顯著高于轉基因組(P<0.05)。說明隨低溫處理時間的延長,轉基因組的可溶性糖含量增長趨勢慢于WT和CK,即轉基因植株的耐寒性低于WT和CK。
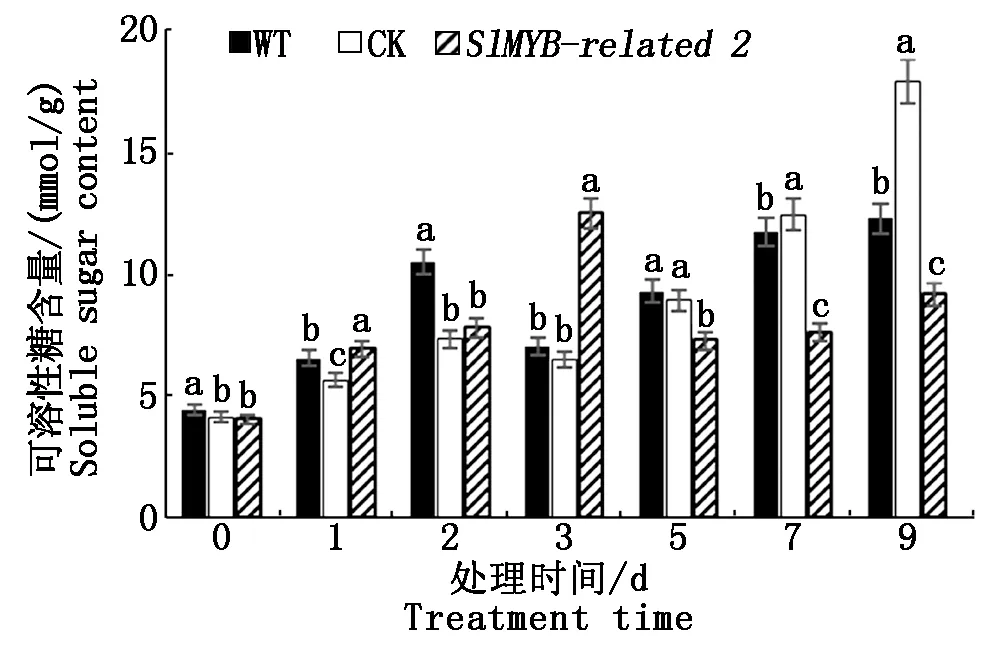
圖8 不同植株材料可溶性糖含量比較Fig.8 Comparison of soluble sugar content of different plant materials
3 結論與討論
CRISPR/Cas9技術已被廣泛應用在植物基因工程領域,其通過對作物抗逆基因進行定向修飾,增強植株對環境的抗性,成為作物抗逆育種的一種有效方式。Zhang等[17]利用CRISPR/Cas9技術構建OsRR22基因敲除載體轉入水稻中,所得T2突變株與野生型相比,苗期耐鹽性顯著提高。Liu等[18]從番茄中鑒定出1個LBDⅡ(Lateral organ boundaries domain Ⅱ)型基因家族LBD40(Lateral organ boundaries domain gene 40)基因,該基因能在植物根和果實中高表達,在PEG和鹽的誘導下顯著表達,利用CRISPR/Cas9技術靶向敲除番茄LBD40基因,獲得突變體,干旱脅迫處理后,與野生型相比較,突變體的保水能力提高。在本試驗中,也成功利用CRISPR/Cas9系統構建出番茄SlMYB-related2基因的敲除載體,并轉化番茄外植體獲得陽性植株。
植物受到低溫脅迫時會發生膜脂過氧化反應,MDA的積累是植物受活性氧(ROS)毒害作用的表現[19]。MDA被用作判定植物逆境條件下膜脂過氧化強度的指標,而且是衰老的標記[20]。脯氨酸作為一種有機滲透調節物,在植物遭受非生物脅迫時合成[21],其積累能夠降低細胞質的水勢,保持水分平衡,維持細胞膜的穩定性,同時脯氨酸可以清除羥自由基[22-24],保護蛋白質結構的穩定性。MDA、可溶性糖和游離脯氨酸的含量大小,均可用于鑒定植株耐冷性的強弱。本試驗構建VIGS介導的基因瞬時沉默載體并成功轉化得到陽性植株,經低溫處理后,通過測定VIGS試驗植株丙二醛、可溶性糖和游離脯氨酸等指標的變化情況,沉默株系在遭遇低溫后較WT和CK丙二醛含量升高,游離脯氨酸含量基本保持不變,可溶性糖含量變化不大,分析結果表明,VIGS試驗中SlMYB-related2基因沉默株系確實耐低溫性降低,說明SlMYB-related2基因在番茄抗寒過程中起調控的作用。SlMYB-related2基因的沉默使番茄幼苗細胞膜受到了損傷,打破了原有的代謝平衡,影響了對低溫的耐受性,可見SlMYB-related2基因在低溫脅迫中起到了正調控作用。
本試驗只選取了一個野生番茄品種進行該基因的沉默來驗證該基因的功能,后續試驗可以選用不同的栽培番茄品種,甚至在其他作物中進行該基因在耐低溫性性能驗證。試驗通過VIGS技術和CRISPR/Cas9對SlMYB-related2基因進行了基礎研究和初步的探索,可為發掘更多的MYB轉錄因子功能提供理論基礎和參考指導。

