氮素營養和根瘤菌接種對大豆結瘤固氮和生長的影響
王曉麗,王 敏,岳愛琴,郭數進,王 鵬,王利祥,楊婷婷,張海生,張永坡,高春艷,張武霞,牛景萍,杜維俊,趙晉忠
(1.山西農業大學 農學院,山西 太谷 030801;2.山西農業大學 基礎部,山西 太谷 030801;3.山西農業大學 生命科學學院,山西 太谷 030801)
氮素是植物生長發育所必需的大量元素之一,在植物的生長發育、產量和品質形成過程中起著至關重要的作用[1]。因此,提高氮素吸收效率、適當增施氮肥是大豆高產穩產的重要保障。當氮素供應不足時,植物新陳代謝發生紊亂,體內物質合成和轉化受到影響,氮素利用下降,生長發育會受到影響。Chun等[2]研究表明,在低氮誘導下,水稻中葉片的生長素含量上升,另外,根長、根的密度和根冠比增加。低氮脅迫導致植物葉片的光合作用受到抑制,從而導致產量下降。李強等[3]研究表明,耐低氮玉米能夠緩解低氮脅迫對光合作用的影響,從而使得較高的氮素含量在植物體內積累。孫年喜等[4]研究表明,不同氮素水平對玉米光合特性具有不同的影響,隨著供氮水平的增加,其光合速率和葉綠素值(SPAD值)均呈現逐漸下降趨勢。當植物受到低氮環境脅迫時,可將氮素從衰老的葉片中運輸到較年輕的葉片中,從老葉中輸出的氨基酸用于正在發育中的幼葉中酶、核苷酶、葉綠素和調節蛋白等物質的合成,以維持植物正常生長發育[5]。
豆科植物不僅可以從大氣土壤中吸收氮素營養,還能夠與根瘤菌共生固氮,為其自身提供氮素。大豆作為重要的共生固氮糧食作物,其生長所需氮素營養的50%~90%是由根瘤菌-大豆共生體系固定的,接種根瘤菌后其種子周圍和土壤中的根瘤菌數量增加,其根部能夠獲得更多根瘤,進而提高作物產量[6]。梁福琴等[7]研究表明,在大豆中,當氮素與根瘤菌共同作用時,其生理指標能夠達到最佳值,使得大豆獲得豐產。研究表明,大豆播種前施用適量氮肥,能夠促進根瘤原基形成和根瘤生長,提高土壤中根瘤菌性能,促進植株生長,為共生固氮提供有效的碳匯和能量匯[8]。因此,在氮素循環中,豆科作物與根瘤菌共生固氮互作體系充當著非常重要的角色。研究發現,輕度缺失硝態氮的情況下能促進根系生長,重度缺失硝態氮或硝態氮濃度較高時會抑制根系生長[9]。而豆科植物共生固氮的特點使其有別于其他植物,Gan等[10]研究不同氮濃度對大豆結瘤性狀的影響發現,氮濃度高于10 mmol/L時,無論供氮形式是硝態氮、銨態氮還是硝酸銨,均顯著降低了大豆根瘤數、根瘤質量以及總固氮量,硝態氮對根瘤生長發育及固氮酶活性抑制作用較銨態氮更強。
大豆既可通過主動運輸的方式吸收利用外界氮素營養,也可通過其根部特化組織根瘤進行共生固氮(Symbiotic nitrogen fixation,SNF),獲取氮素營養[11]。目前,豆科植物氮素營養的吸收和根瘤菌接種對大豆結瘤固氮和生長的影響鮮有研究。
本研究通過對大豆不同濃度氮處理及接種根瘤菌劑同時處理,以探究大豆結瘤固氮情況和不同組織器官中氮素積累情況以及對葉表型性狀的影響,旨在為大豆氮素高效利用提供科學依據。
1 材料和方法
1.1 試驗材料
供試大豆品種為Williams 82;大豆根瘤菌株(Bradyrhizobiumjaponicum)采用中國農業大學CCBAU提供的USDA110。
1.2 試驗方法
試驗在山西農業大學大豆溫室進行。
1.2.1 根瘤菌株的活化 在超凈工作臺中,用接種環挑取1環甘油菌在YMA培養基上劃線,倒置于28 ℃培養箱培養;后挑取1環活化后的菌株接種至裝有200 mL YMA培養液的500 mL錐形瓶中,并于28 ℃、160 r/min的恒溫振蕩培養箱中進行培養,每隔1 d觀察根瘤菌株USDA110培養液渾濁情況,需要培養5 d左右。
1.2.2 不同氮濃度處理 根據大豆生長發育所需氮素營養,以KNO3為氮源,分別設置無氮(0 mmol/L,NN)、低氮(0.25 mmol/L,LN)和高氮(10 mmol/L,HN)3個不同濃度的硝酸鹽營養液,將Williams 82分別種植在含有不同濃度硝酸鹽營養液浸濕的蛭石基質中,均以不接菌為對照,3次重復。
1.2.3 接種根瘤菌處理 蛭石滅菌裝入10 cm×10 cm的營養缽中。將大豆Williams 82于92%的酒精中滅菌5 min,再用5%的NaClO進行表面消毒5 min,之后用無菌水清洗10次,于營養液浸濕的蛭石中發芽(基礎營養液配制參照文獻[12])。7 d之后進行間苗,每個營養缽留有2株長勢一致的大豆,放置于光照培養箱中進行培養,16 h光/8 h暗,光照溫度25 ℃,黑暗溫度16 ℃,光照強度10 000 lx,相對濕度70%;待第1片真葉完全展開后,將大豆慢生根瘤菌USDA110(OD600=0.08)輕輕接在大豆幼苗根系周圍,每株大豆接30 mL菌液,分別在接菌后0.5 h(根毛識別根瘤菌)、1 d(根毛卷曲)、4 d(結瘤原基形成)、16 d、28 d(2個結瘤早期發育時期)[13]觀察其結瘤情況,取葉片、根、根瘤樣品,測定每個植株的根干質量、根瘤數、根瘤干質量,以不接菌為對照,接種USDA110作參照菌株,3次生物學重復。
1.3 測定項目及方法
1.3.1 葉形態特征的測定 植物樣品葉片形態特征采用智能葉面積測量系統(YMJ-C/CH)進行測定。
1.3.2 氮含量的測定 試驗樣品氮含量測定采用國家標準方法凱氏定氮法進行。將樣品放置在烘箱中105 ℃殺青30 min,80 ℃烘干,稱取等質量樣品,用球磨儀將樣品粉碎,過200 mm篩備用。取樣品0.1 g置于消化管底部,以硫酸銅和硝酸鉀作為催化劑,向消化管中加入3 g的混合催化劑,然后加入5 mL濃硫酸搖勻,消解植物樣品;待消煮管中液體呈現綠色透明顏色時,將消煮管取下進行凱氏定氮法測定氮含量,在高溫下將植物葉片中的含氮化合物轉變為硫酸銨,然后用氫氧化鈉堿化,加熱蒸餾出氨,此時消化管中液體顏色為褐色表明反應完全,經硼酸吸收后,用硫酸標準溶液滴定,計算含氮量。
1.4 數據分析
采用SPSS 19.0和Excel 2016對數據進行統計分析;采用R語言進行作圖;使用CS 6.0對試驗圖片進行編輯。
2 結果與分析
2.1 不同施氮水平接種根瘤菌對大豆根瘤數目、根瘤干質量和根干質量的影響
待第1片真葉完全展開后,對不同氮濃度處理的大豆實生苗接種根瘤菌,28 d后觀察其表型,結果顯示(圖1),接種根瘤菌后的結瘤情況表現為NN>LN>HN,無氮接菌下結瘤數最多,隨著氮濃度的增加,根瘤數逐漸減少。此外,不同氮濃度下根瘤數目和根瘤干質量均呈現相同的變化趨勢,無氮處理顯著高于低氮處理(P<0.05),低氮處理顯著高于高氮處理(P<0.05)(表1);而根干質量呈現相反的變化趨勢,無論接菌與不接菌,高氮處理下根干質量均顯著高于低氮和無氮處理(P<0.05),而在低氮和無氮處理間則不存在顯著差異。由不同氮濃度接種根瘤菌對大豆根系的影響數據表明,不同施氮水平對根瘤數目、根瘤干質量和根干質量都有不同程度的影響。

圖1 不同氮濃度處理下接種根瘤菌的結瘤情況Fig.1 Nodular situation of rhizobia inoculated under different nitrogen concentrations
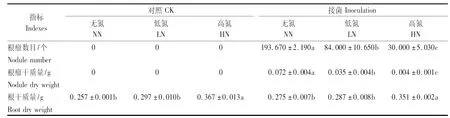
表1 不同氮濃度下接種根瘤菌對大豆根部的影響Tab.1 Effect of inoculation of rhizobia with different nitrogen concentration on soybean root
2.2 不同氮水平下接種根瘤菌大豆植株氮素積累變化
在不同施氮水平下,大豆不同器官氮素含量在接種和不接種間表現出不同的變化趨勢,且不同器官氮素含量整體呈現葉>根>莖的現象(圖2)。對于葉組織中氮素含量而言,無論接菌與不接菌,高氮處理下葉組織的氮素含量均顯著高于低氮處理(P<0.05),而在不接菌的情況下,低氮處理下的氮素含量顯著高于無氮處理(P<0.05),接菌后二者之間差異不顯著;對于莖組織的氮素含量,無論接菌與不接菌,其氮素含量在不同氮濃度處理下表現為相同的變化趨勢,即高氮>低氮>無氮,且差異均達顯著水平(P<0.05)。根組織中的氮素含量變化趨勢與葉組織一致。
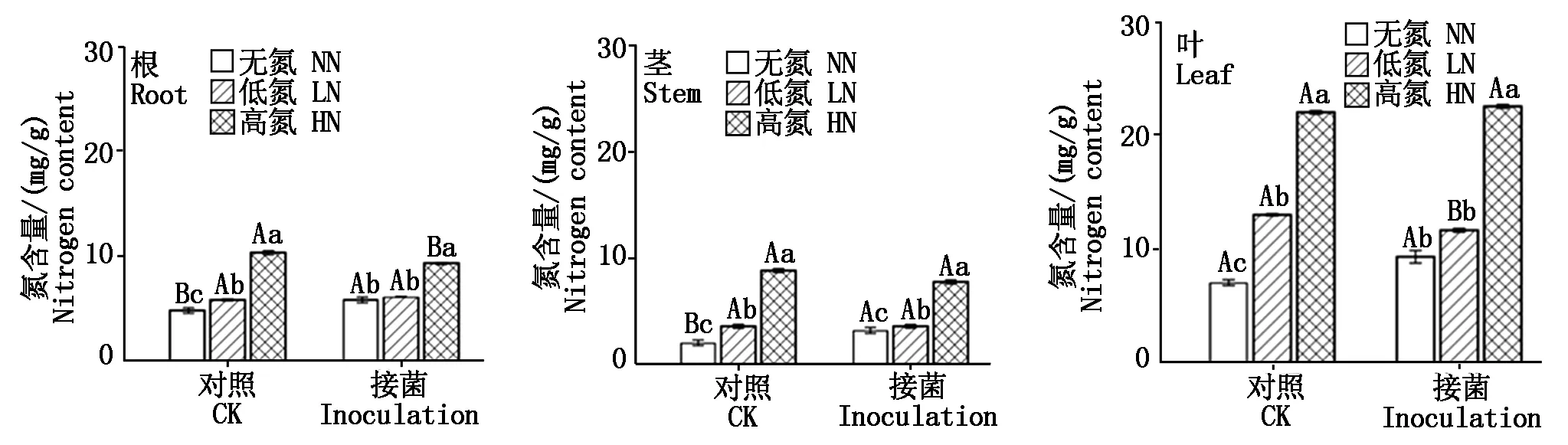
不同小寫字母表示接菌或不接菌下不同氮水平上存在顯著差異(P<0.05);不同大寫字母表示同一氮水平上接菌和不接菌間存在顯著差異(P<0.05)。Different lowercase letters indicated significant differences between inoculated and non-inoculated nitrogen levels(P<0.05);Different capital letters indicated significant differences between inoculated and non-inoculated at the same nitrogen level(P<0.05).
2.3 不同氮素水平條件下接種根瘤菌不同葉位葉綠素值(SPAD)的變化
由圖3可知,不同處理條件下,不同葉位SPAD值均呈現不同的變化趨勢。除了在接菌下,第1葉的SPAD值表現為HN>LN>NN,且存在顯著差異(P<0.05)外,其他葉位的SPAD值在不同氮水平處理下均為高氮處理顯著高于低氮和無氮處理(P<0.05),而在低氮和無氮處理之間不存在顯著差異。此外,不同葉位之間SPAD值在不同氮素水平下也呈現出不同的變化趨勢,其中,在無氮水平下,SPAD值依次為第1對真葉>第1葉>第2葉,且彼此之間存在顯著差異(P<0.05);無論在接菌還是不接菌在低氮水平下,第1對真葉和第1葉時SPAD值顯著高于第2葉(P<0.05),而在第1對真葉和第1葉之間差異不顯著;在接菌情況下,高氮處理的SPAD值在第1葉中含量顯著高于第1對真葉和第2葉(P<0.05),說明高氮處理可以促進地上部氮素向第1葉轉運。無論是在不同氮素水平上,還是不同葉位之間,接菌與不接菌都呈現相同的變化趨勢,說明接菌不影響葉片之間氮素的轉運。
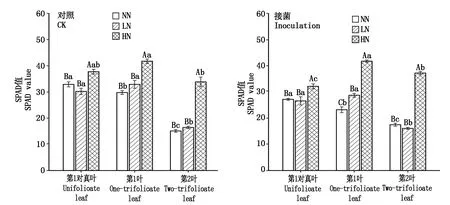
不同小寫字母表示同一氮水平上不同葉位間存在顯著差異(P<0.05);不同大寫字母表示同一葉位上不同氮水平間存在顯著差異(P<0.05)。Different lowercase letters indicated significant differences between different leaf positions at the same nitrogen level(P<0.05);Different capital letters indicated significant differences between different nitrogen levels at the same leaf position(P<0.05).
從圖4植株的生長狀況也可以看出,高氮處理下植株的長勢明顯優于無氮和低氮處理,且從葉片的顏色也可以看出,無氮和低氮處理葉片整體發黃,而在高氮處理下,葉片呈現青綠色,尤其是第1葉更為明顯,這也與圖3結果相吻合。

圖4 不同氮水平條件下接菌后的植株生長Fig.4 Plant growth after inoculation under different nitrogen levels
2.4 不同氮素水平下接種根瘤菌葉形態指標的變化
由表2可知,在不接菌情況下,不同葉位在不同氮素水平上葉形態指標均呈現相同的變化趨勢,葉面積、葉周長、葉長和葉寬在低氮和高氮處理均顯著高于無氮處理(P<0.05);在接菌情況下,第1對真葉形態指標在不同氮素水平上呈現HN>NN>LN,而第1葉葉面積、葉周長和葉寬在不同氮素水平上沒有顯著差異,第1葉葉長在無氮水平下顯著高于低氮(P<0.05)。在不接菌情況下,葉長在低氮和高氮水平下顯著高于無氮處理(P<0.05);第2葉的葉面積、葉周長、葉長、葉寬在低氮和高氮水平下均顯著高于無氮(P<0.05)。此外,在同一氮素水平上,不同葉位的葉形態也表現出不同的變化趨勢,在不接菌情況下,無氮處理條件下除了葉長呈現第1葉>第1對真葉>第2葉外,其他葉形態指標(葉面積、葉周長、葉寬)均表現為第1對真葉和第1葉顯著高于第2葉(P<0.05),且第1對真葉和第1葉之間差異不顯著;而在低氮和高氮處理下,不同葉位之間的葉形態指標(葉面積、葉周長、葉長、葉寬)均差異不顯著;在接菌情況下,在無氮處理下,第1葉的葉面積、葉周長均顯著高于第1對真葉和第2葉(P<0.05),第1葉的葉長顯著高于第1對真葉,第1葉的葉寬顯著高于第2葉(P<0.05),而在高氮處理下,不同葉位之間差異不顯著。
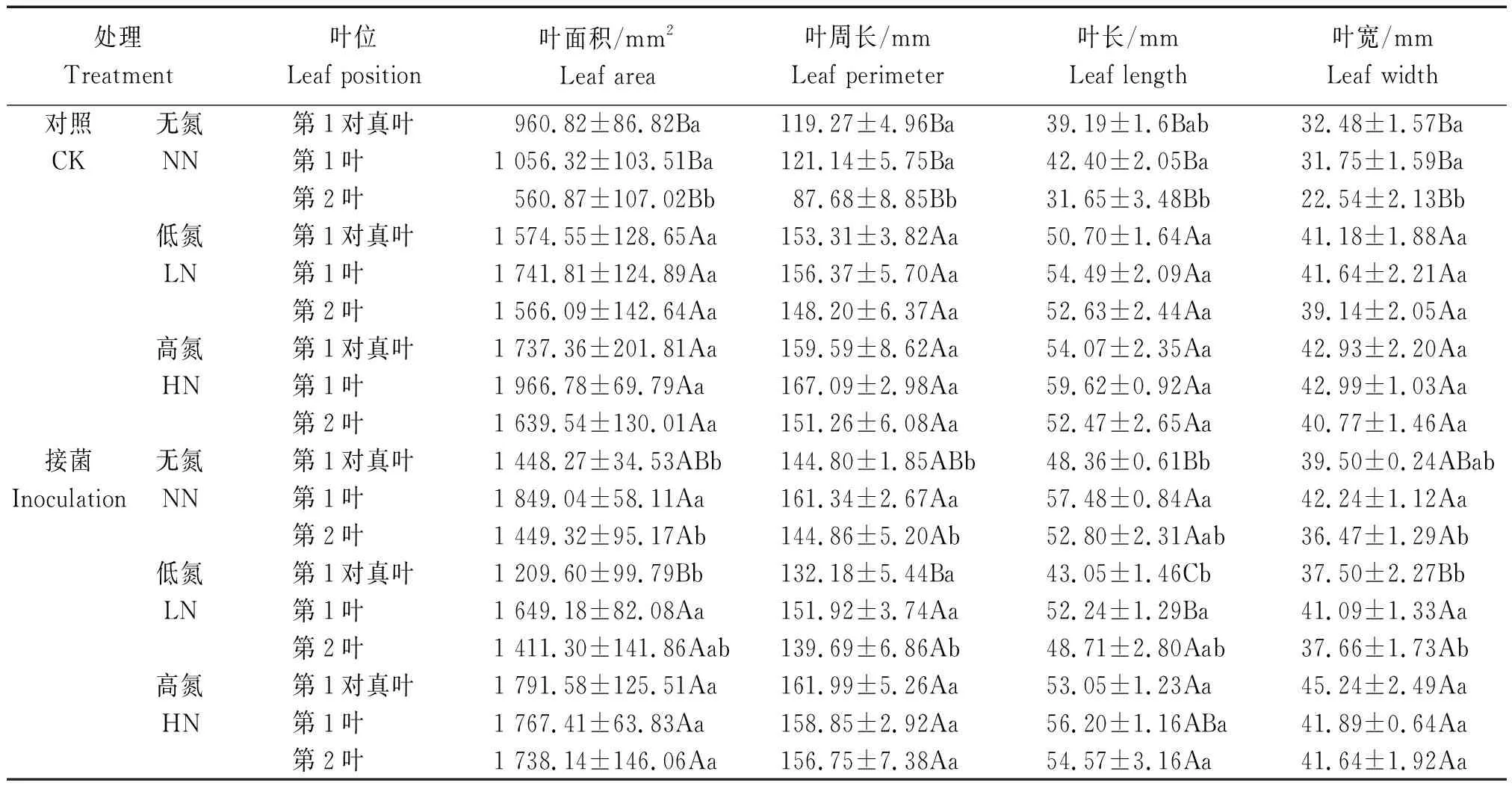
表2 不同處理下不同葉位的葉形態指標的變化Tab.2 Leaf morphological indexes changes of different leaf positions under different treatments
3 結論與討論
有研究表明,根瘤數目和質量與施氮量的增加呈負相關[14];但當外源氮素水平較高時,會對結瘤起到抑制作用[15]。本研究為了研究不同氮素水平下接種根瘤菌對大豆根部及其結瘤的影響,在幼苗期接種根瘤菌28 d后,對根干質量、根瘤性狀與植物各組織氮含量進行測定表明,隨著施氮量的增加根瘤數逐漸減少,無氮處理下根瘤最多,高氮處理下根瘤最少;在高氮處理下,大豆根瘤出現氮阻遏現象,可能是由于氮素濃度過高,破壞了根瘤菌菌體結構,降低了固氮酶的活性,抑制了根瘤的生長,這與鄭永美等[16]的研究結果相一致。此外,過度結瘤會導致中午光合作用降低,從而降低總根向蒸發組織提供水的能力。能夠結瘤的豆科植物通過蒸騰作用彌補水分損失的能力有限,導致氣孔關閉,從而降低光合速率[17];在這種情況下,寄主植物和根瘤之間爭奪碳水化合物的競爭會加劇,導致植物生長和種子產量進一步下降[18]。事實上,大豆結瘤固氮和氨同化需要大量的光合作用產物,以提供根系結瘤所增加的呼吸負擔和氮有機合成所需的碳骨架[19]。無氮處理的根干質量最小,根瘤數最多,而高氮處理的根干質量最大,根瘤數最少。隨著氮濃度的增加,根干質量與根瘤數呈負相關,這可能與大豆植株結瘤減少了根系生物量有關。有報道表明,根瘤是較強的碳水化合物匯,因此,根瘤可以減少糖向根細胞的轉運,減少根系的生長[20]。
大豆在生育前期,子葉所含的氮素不足以支持大豆生長發育,而根瘤的固氮作用尚未完全建成,在短時間內會出現氮素的缺乏,因此,要通過氮素的添加來滿足大豆生長發育[21]。本研究表明,無論在根、莖還是葉中,氮含量在高氮處理時均大于低氮處理,低氮處理大于無氮處理。在大豆苗期時,施氮能夠明顯增加大豆植株前期的氮素積累,氮濃度越高促進效果越明顯[22]。不管是接菌還是不接菌處理,葉中氮含量均大于根中氮含量,根中氮含量均大于莖中氮含量。葉綠體是進行光合作用的場所,氮素是葉綠素的重要組成成分,適當增施氮肥有利于葉綠素的合成,研究表明,葉綠素含量越高,氮含量越高[23]。不接菌時,低氮處理的葉和莖的氮含量顯著高于無氮處理,接菌后,低氮處理莖的氮含量顯著高于無氮處理,此時根瘤開始固氮,并向地上部運輸。Sun等[24]研究表明,低氮脅迫會抑制植物葉片的光合作用,葉片所吸收的光能產生了過量的活性氧和丙二醛等物質,使植物體內活性氧代謝失調,生物膜結構系統遭到破壞,植物最終失去光合能力。
有研究表明,較高的葉片氮含量,能夠提高葉綠素含量并參與光合電子傳遞的蛋白質水平,提高初級光化學反應的效率和光合能力[25]。本研究中,在不同葉位,不同接菌處理條件下,高氮處理的SPAD值最大,葉片墨綠,植株高大;低氮與無氮處理,植株矮小,葉片發黃,分枝變少,這是由于當氮素供給不足時,植株體內核酸、葉綠素、蛋白質合成受到阻礙,導致植物出現缺綠癥;降低其光合速率及光合產量。研究表明,氮含量越大,葉綠素含量越大,SPAD值越大[9]。在氮誘導下,氮的積累根據植株葉片生長程度的不同而存在差別,具體表現為成長中葉片(第1葉)>新生葉片(第2葉)>成熟葉片(第1對真葉),植株氮素構成的變化直接影響著新生莖、葉氮素構成變化,老葉通過葉肉降解,提供給幼葉營養物質,維持幼葉正常生長發育[26]。無氮處理下,不同葉位的SPAD值自下而上依次遞減,此時,由共生固氮合成的氮素逐漸向缺氮部位轉運。另外,葉片性狀是決定植物品質的重要因素,主要包括葉面積、葉周長、葉長、葉寬等[27]。有研究表明,良好的群體葉面積指數、葉面積持續時間(光合面積持續期)、光合勢是大豆獲得高產的基礎[28]。本研究中,第1葉的葉片性狀最好,與其SPAD值相吻合。在無氮處理條件下,接菌之后,不同葉位葉面積均顯著增加,高于低氮接菌處理;在低氮和高氮處理條件下,接菌之后,葉面積均減少。研究表明,更多的結瘤提供的更高的氮利用率(氮含量)可以促進植物的生長,因為生物量的產生依賴于氮來合成多種分子,如葉綠素和Rubisco,以及蛋白質、核酸和各種酶輔助因子[29]。
綜上所述,大豆共生固氮不需要外界施加過量氮素營養,施氮量越多,根瘤數越少,共生固氮效果越差。根瘤可以減少糖向根細胞的轉運,減少根系的生長;施氮量越多,根瘤數越少,根干質量越大。在大豆苗期,施氮能夠明顯增加大豆植株前期的氮素積累,促進葉表型性狀,氮濃度越高促進效果越明顯,適當增加氮素營養可以提高大豆各器官中氮素的積累量。

