太陽燃料甲醇合成
王集杰,韓哲,陳思宇,2,湯馳洲,2,沙峰,3,唐珊,2,姚婷婷,李燦
(1 中國科學院大連化學物理研究所,催化基礎國家重點實驗室,遼寧 大連 116023;2 中國科學院大學,北京 100049;3 南開大學材料科學與工程學院,天津 300350)
全球氣候變化給人類社會可持續發展造成了嚴重危機。二氧化碳等溫室氣體的大量排放是造成全球氣候變化的主要原因之一,因此控制二氧化碳排放成為應對全球氣候變化中非常重要的一部分。2020年9月我國政府在聯合國大會上承諾,中國要力爭于2030 年實現二氧化碳排放達到峰值,努力爭取2060 年前實現碳中和。考慮到我國當下以化石能源為主的能源結構,要實現這一目標,必須要發展切實可行的可再生能源技術。液態陽光,其科學表述為液態太陽燃料,是指以太陽能、風能等可再生能源制取綠氫,耦合二氧化碳加氫技術制備以甲醇為代表的液體燃料和化學品,其本質是利用可再生能源將二氧化碳和水轉化為液體燃料,是銜接化石資源與以太陽能為代表的可再生能源的重要樞紐。相比于碳捕集與封存(CCS),將二氧化碳轉化為液態陽光甲醇是碳捕獲并資源化利用(CCU)的技術,可得到高附加值燃料及化學品,具有技術可行性和一定的經濟效益,可兼顧二氧化碳減排與經濟發展,是積極應對二氧化碳問題切實可行的策略。
1 液態陽光技術路線
多年前,諾貝爾化學獎得主Olah曾提出“甲醇經濟”概念,其本質是基于可再生能源制氫,進而轉化二氧化碳制備甲醇、二甲醚等。他認為通過二氧化碳循環再加氫生產甲醇,將使人類不再依賴化石燃料來提供運輸燃料和烴類產品,從而使人類擺脫對化石燃料的依賴。2018 年,施春風、張濤等提出液態陽光的理念,其字面意思是把陽光(太陽能)變為液體燃料,即利用太陽能等可再生能源轉化水和二氧化碳制取液體燃料,甲醇是液態陽光首選目標產物。
本文作者研究團隊長期致力于人工光合成研究,即利用二氧化碳和水在太陽能的作用下生成有機物,所開展的工作主要包括太陽能光催化、光電催化和電催化分解水制氫及二氧化碳資源化利用合成有機物,若合成的有機物用作燃料則叫作太陽燃料。甲醇可直接作為清潔燃料來替代汽油、柴油等傳統化石燃料,又是大宗基礎化學品,可用來制備烯烴、芳烴、甲醛、二甲醚等一系列重要化工產品。同時,甲醇是良好的儲氫分子,可實現常溫常壓儲存和運輸,通過甲醇水蒸氣重整反應,可將甲醇變回氫氣(甲醇儲氫量可達18.75 %,質量分數),用于氫燃料電池等供能領域,因此甲醇是太陽燃料合成的首選。太陽燃料強調,二氧化碳加氫制甲醇是暗合光合作用暗反應的過程,是二氧化碳資源化利用的典型代表。“太陽燃料”“甲醇經濟”“液態陽光”本質上相同,下文中統一用液態陽光進行表述。
液態陽光甲醇合成有以下技術路線:①光催化二氧化碳和水制甲醇;②光催化制氫+二氧化碳加氫制甲醇;③光伏發電+電催化二氧化碳和水制甲醇;④光伏發電+電解水制氫+二氧化碳加氫制甲醇。目前來看,光伏發電+電解水制氫+二氧化碳加氫制甲醇技術路線是最有希望規模化應用的技術路線,本文主要介紹這條技術路線中的兩個關鍵技術,即電解水制氫和二氧化碳加氫制甲醇。
2 液態陽光甲醇合成中的關鍵技術
2.1 規模化、低能耗和高穩定性電解水制氫技術
電解水制氫的技術主要有三種,分別是堿水電解制氫(ALK)、質子交換膜電解水制氫(PEM)以及固體氧化物電解水制氫(SOEC),如圖1所示。
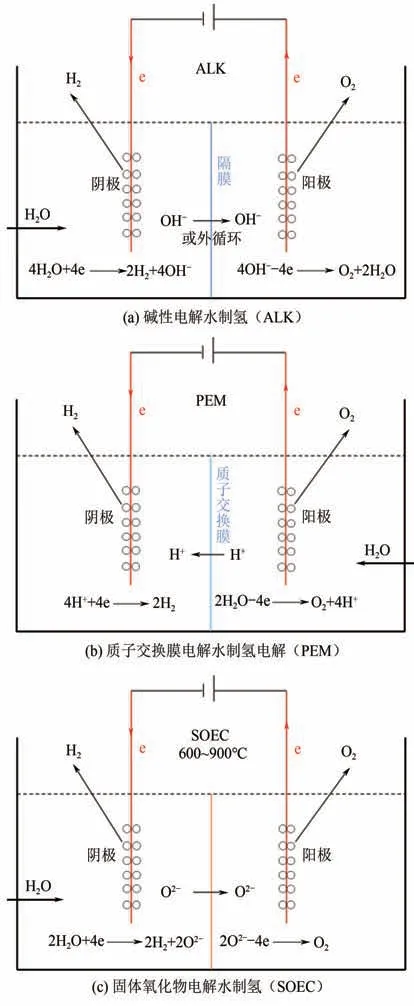
圖1 電解水制氫原理圖
水分解制氫是一個Δ>0 的反應,在光、電等外場注入能量時才能發生。電解水制氫有兩個半反應——產氫反應(HER)和產氧反應(OER),這兩個半反應熱力學勢壘高、動力學速率緩慢,需要開發高效催化劑來加速反應過程。
對于ALK 電解水制氫,通常采用KOH 溶液作為電解液,水分子在陰極發生解離產生氫氣,OH在陽極上發生反應放出氧氣。在HER中,MoNi、Ni-MoS、PtNi等催化體系被開發出來用于代替傳統的Ni 催化劑;在OER 中,催化劑為以過渡金屬如Fe、Co、Ni、Mn等為主的非貴金屬。ALK電解水制氫陰陽兩極均可使用非貴金屬催化劑,難點在于需要同時進一步提升陰陽兩極的催化劑效率。
對于PEM 電解水制氫,水分子的解離發生在陽極,質子通過交換膜遷移到陰極直接生成氫氣,HER 常用的催化劑是Pt 催化劑,而OER 常用催化劑為IrO和RuO等,PEM 電解水制氫的難點在于解決催化劑的效率問題。貴金屬催化劑限制了PEM 電解水制氫的大規模使用,目前發展重點為低載量貴金屬催化劑和非貴金屬催化劑的研發,如HER 反應中開發的MoS、CoP催化劑以及OER反應中開發的CoMnO催化劑等。
SOEC 電解水制氫可以直接將電能和熱能轉化為化學能,通常在600~900℃,水分子在陰極上解離成H和O,O穿過致密的固體氧化物電解質層到達陽極,失去電子得到O。根據熱力學規律,當反應溫度上升時,水分解制氫的Δ減小,則水的理論分解電壓降低。動力學上,溫度升高有利于陰陽兩極上的過電位降低,從而減少電解過程的能量損失。SOEC 由于其所需溫度過高,對反應器材料、催化劑及體系密封等均是挑戰,目前仍處于基礎研究階段。
堿性電解水制氫盡管已經實現工業化,但依然存在較多待解決的關鍵科學和技術問題。如:①實驗條件多為室溫下的1mol/L KOH 溶液,但實際工業條件為85~90℃下的7mol/L KOH溶液,且在電流密度、評價裝置等方面也與實際工業條件有一定偏差;②高電流密度下過電位高,能效較低。
本文作者研究團隊開發了原子級分散的非貴金屬摻雜鎳基底催化劑,在規模化堿性電解水制氫中試示范工程設備上實現了穩定運行。電解水制氫電流密度穩定在400mA/cm時,平均單位制氫能耗低于4.3kW·h/m氫氣(標準狀況,下同),能效值大于82%;電流密度穩定在300mA/cm時,單位制氫能耗低于4.1kW·h/m氫氣,能效值約87%。這是目前已知的規模化堿性電解水制氫的最高效率,并實現了單槽大于1000m/h產能。
2.2 高選擇性、高穩定性二氧化碳加氫制甲醇技術
液態陽光中的另一關鍵技術是二氧化碳加氫制甲醇,其反應方程式如式(1);其主要的副反應為逆水煤氣反應(RWGS),方程式為式(2)。
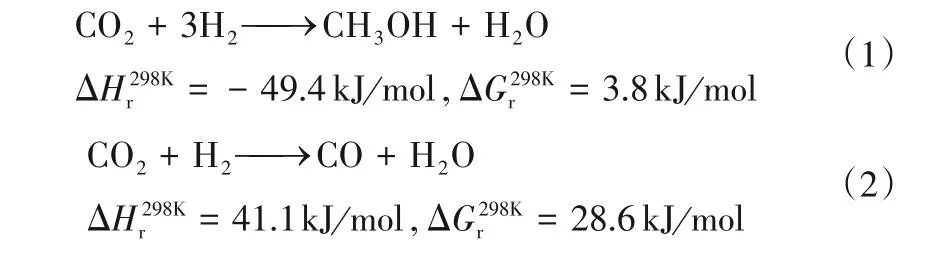
從熱力學角度分析,甲醇合成是放熱反應,分子數減少;副反應逆水煤氣反應為吸熱反應,分子數不變。因此溫度降低,提高反應物的分壓,有利于主反應正向進行。二氧化碳是一種熱力學穩定的化合物,因此提高溫度有利于二氧化碳的活化,提高反應的轉化率。
此外,二氧化碳甲烷化反應也是副反應之一,其反應方程式為式(3)。
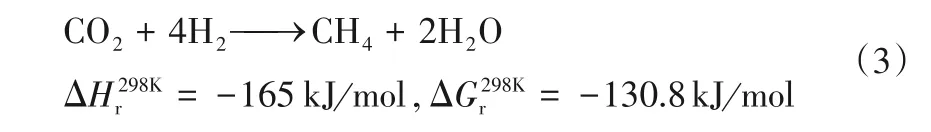
二氧化碳甲烷化反應是必須要抑制的副反應,因該反應放熱劇烈,造成能量浪費。而且甲烷在系統中為惰性組分,在循環工藝中,甲烷不斷循環會造成累積,不得已地弛放使得氫和二氧化碳原料利用率大大降低。因此在二氧化碳加氫制甲醇中必須降低甲烷選擇性。
雖然工業上合成氣制甲醇過程中使用的Cu/ZnO/AlO催化劑也可以催化CO加氫到甲醇,但是該催化劑在應用于CO加氫時,更易于生成CO。不同于CO加氫,CO加氫到甲醇過程中會產生大量水,水會加速催化劑的燒結與失活。近年來,基于金屬氧化物的催化劑在CO加氫制甲醇中的應用得到了廣泛關注。具有代表性的催化劑有ZnO-ZrO、GaZrO、CdZrO、InO等。
2.2.1 Cu基催化劑
目前,Cu 基催化劑的研究主要集中在催化結構-活性關系建立、反應機理研究等方面。此外,許多工作還探索了反應器的設計和優化,以緩解HO 引起的催化劑燒結,從而提高甲醇的選擇性,降低能耗。目前,針對Cu/ZnO 催化劑的活性位點有兩種觀點:①Cu 與ZnO 在界面的協同作用,促進了CO的加氫反應,其協同作用應發生在Cu與ZnO 的界面,或ZnO 覆蓋在Cu 表面,通過X 射線光電子能譜(XPS)和Auger 譜進一步確認了ZnO的存在;②另一種觀點認為Cu-Zn表面合金位點是活性中心,這種合金位點的形成將促進ZnO部分還原為Zn,或構成了Zn 原子對Cu 表面的修飾。Behrens等認為Zn原子修飾的、位于臺階位的Cu是活性位點,這些位于臺階位的Cu只有在體相缺陷和表面活性物種共同存在時才可發揮催化作用。此外,由于金屬載體之間強相互作用(SMSI)和吸附質誘導的氧化作用,導致氧化態的Zn 發生部分還原,使其向Zn方向轉變。Lunkenbein等通過透射電鏡(TEM)發現,在Cu納米顆粒上形成SMSI 誘導的亞穩態石墨狀ZnO覆蓋層。Nakamura 等則認為Zn 并沒有被氧化成ZnO,所觀察到的O 物種來自于甲酸鹽。
Cu 基催化劑上二氧化碳加氫制甲醇的催化活性不僅與金屬的分散度或金屬比表面積有關,還與Cu-ZnO 界面的尺寸、組成和電子狀態等有關。研究者通常添加助催化劑,如K、Ba 等堿土金屬,La、Ce 等稀土金屬,TiO、ZrO等過渡金屬氧化物,以及SiO等主族元素,載體則通常選用金屬氧化物如AlO、ZrO、CeO[等,也包括諸如SBA-15、MCF、KIT-6 的介孔SiO分子篩,碳納米管(CNTs)。在催化劑制備方法方面,研究者發展了利用碳酸鹽的記憶效應制備的核殼結構催化劑以及可同時作為催化劑前驅體和載體的含有Cu和Zn層狀雙金屬氫氧化物(LDHs)等,但目前最廣泛的還是共沉淀法。
2.2.2 InO基催化劑
除了Cu基催化劑以外,InO基催化劑也逐步進入人們的視野。Ge 等通過密度泛函理論(DFT)計算發現InO可以同時對CO和H進行活化。CO可以吸附在InO(110)晶面上,與表面O 反應生成吸附態碳酸鹽物種。而H可以在InO(110)晶面上發生異裂活化,一個H轉移到表面O上,形成OH,另一個H轉移到表面In上。吸附態的CO和H可以繼續反應生成HCOO 物種。在后續工作中,Ge 等通過DFT 計算發現在InO(110)晶面的氧空位缺陷上CO可以逐步加氫,經過HCOO、HCO、HCO 中間物種最后生成甲醇,隨后,Liu 等通過實驗證實InO可以催化CO加氫到甲醇。
Pérez-Ramírez 等用氨水沉淀法制備了InO,實現了二氧化碳加氫高選擇性制備甲醇,其中甲醇選擇性最高達到了99.8%,但二氧化碳轉化率只有5.2%。該作者還認為在反應氣體中引入少量CO可以幫助催化劑表面形成更多氧空位缺陷,從而提高催化劑的活性。在隨后的工作中,該作者對CO在InO上加氫到甲醇的動力學和機理進行了研究并發現,InO上包含氧空位缺陷的InO結構是CO加氫的活性位點。Sun 等通過DFT 計算發現,InO的晶體結構和暴露晶面對其催化活性有影響。Müller 等發現,在InO催化CO加氫到甲醇過程中表現出活化、穩定反應和失活三個階段。在InO表面發生部分還原,形成氧空位缺陷而引起活化,以及被過度還原成金屬態的In 導致了催化劑的失活。
研究者對InO的載體進行研究,結果表明ZrO作載體時表現出較高的甲醇生成速率。此外,向InO中引入Pd、Pt、Rh、Au、Ni、Co等元素作為助劑也可以提高InO催化劑的性能。
2.2.3 固溶體催化劑
本文作者研究團隊研發了一種用于催化CO加氫制甲醇的ZnO-ZrO固溶體催化劑。實驗結果表明(如圖2所示),單獨的ZrO和ZnO催化CO加氫制甲醇的活性均很低,而ZnO-ZrO催化劑卻表現出較高的催化活性。當Zn 質量分數為13%時,催化劑的活性最高,在5.0MPa、24000mL/(g·h)、H/CO= (3/1)~(4/1)、320~315℃的反應條件下,該催化劑可以實現單程超過10%的CO轉化率和高達86%~91%的甲醇選擇性。同時,該催化劑有非常高的熱穩定性以及抗SO和HS 毒化的能力。這些優點使ZnO-ZrO催化劑適合于大規模工業應用。
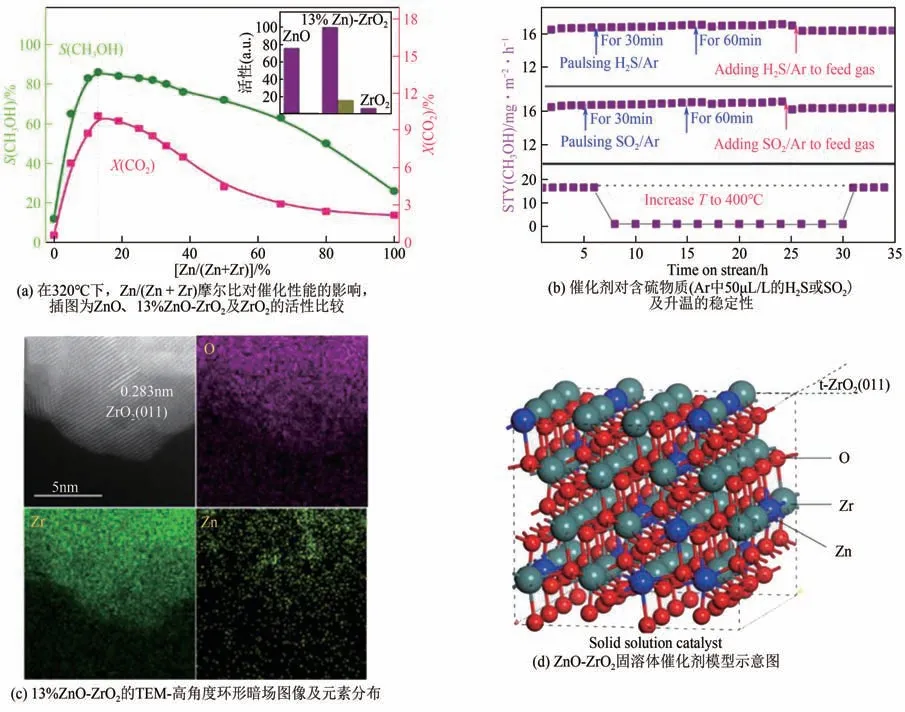
圖2 ZnO-ZrO2固溶體催化劑的性能與結構[16]
結構表征表明,當Zn 含量較低時,Zn 摻入ZrO晶格中形成固溶體結構。對于13%ZnO-ZrO,其體相為立方結構,次表層為四方結構,最表層可能處在四方結構向單斜結構過渡的狀態。原位紅外研究捕捉到了催化劑表面存在的甲酸鹽(HCOO*)和甲氧基(HCO)兩種中間物種。DFT 計算表明H優先在Zn 位點處發生吸附活化,而CO更傾向在配位不飽和的Zr 位點吸附,吸附的CO*可以被加氫生成HCOO或者OCOH,這兩種物種都可以進一步轉變成甲醇。其中,HCOO被加氫生成HCOO,接著進一步加氫并分解生成HCO和OH。隨后HCO繼續加氫到HCO,最后變成甲醇。而OCOH被加氫并分解,生成CO和HO,CO被加氫,經過HCO、HCO和HCO,最后變成甲醇。兩條路徑的能量變化表明HCOO路徑更容易發生,是CO加氫到甲醇的主要路徑。
本文作者研究團隊對固溶體催化劑的體系進行了拓展。通過篩選大量的兩組分復合氧化物,發現CdZrO和GaZrO催化劑也可以實現二氧化碳高選擇性加氫到甲醇(如圖3所示)。Cd和Ga含量優化實驗結果表明,Cd和Ga在金屬原子中所占的原子比為11.5%時催化劑的性能最好。在5.0MPa、24000mL/(g·h)、H/CO=3/1的反應條件下,這兩種催化劑可以實現高達80%的甲醇選擇性和4.3%~12.4%的CO轉化率。這兩種催化劑的X射線衍射(XRD)圖中都只有四方相ZrO的衍射峰,表明Cd和Ga也可以摻雜到ZrO晶格中,形成固溶體結構。化學吸附表明CO主要在Zr 位點活化,而Cd/Ga 與Zr 位點之間對H的活化存在協同效應。DFT計算結果表明這兩種催化劑中Cd/Ga和Zr分別負責活化H和CO,在CO加氫過程中起到協同作用。
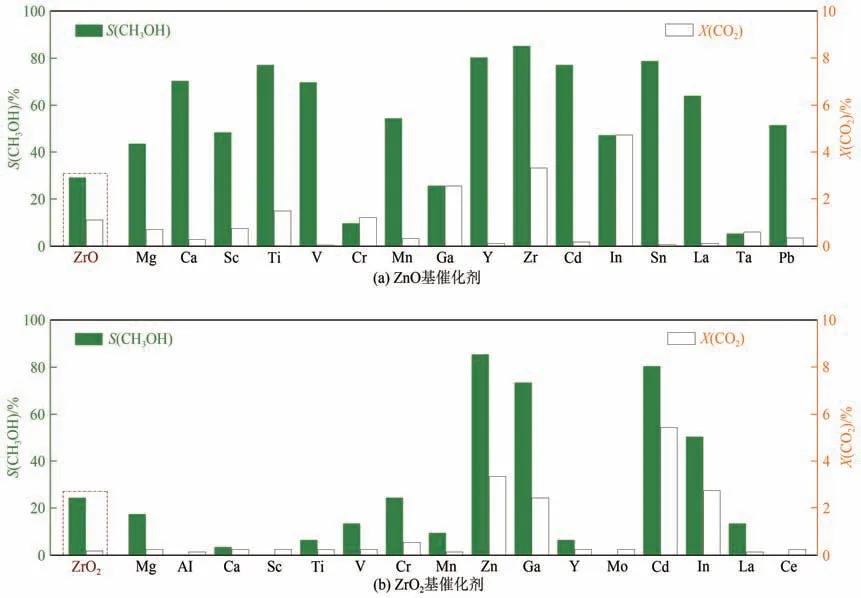
圖3 催化劑的CO2加氫反應性能[17]
近期,本文作者研究團隊對ZnO-ZrO催化劑進行了進一步改進,采用蒸發誘導自組裝法制備了具有有序介孔結構的ZnO-ZrO固溶體催化劑,與之前報道的共沉淀法制備的催化劑相比,該催化劑具有更大的比表面積,表現出更高的催化性能。
3 二氧化碳加氫制甲醇應用進展
國際上,冰島碳循環國際公司(CRI)開發ETL技術,完成了由地熱能驅動的二氧化碳加氫制甲醇中試。該公司從熱電廠排放氣體中捕集二氧化碳,由地熱能產生的電力電解水得到氫氣,在此基礎上合成甲醇(如圖4 所示)。據悉,該甲醇面向美國和歐洲市場,注冊名稱為Vulcanol,可同汽油混合用于生物燃油制品。

圖4 冰島二氧化碳合成甲醇工廠
中國科學院上海高等研究院、中海油富島公司和中國成達工程有限公司合作,采用了限域結構的銅基催化劑,建成5000t/a工業試驗裝置。
2018 年,本文作者團隊聯合蘭州新區石化產業投資集團有限公司、華陸工程科技有限責任公司在甘肅省蘭州新區開始建設全球首個液態陽光甲醇合成工業示范項目。該項目利用大規模太陽能發電,進而電解水產氫,用可再生能源產生的氫氣與二氧化碳反應生成甲醇,從而把可再生能源的能量存儲在液體燃料甲醇中,是真正意義上的液態陽光,即直接利用太陽能實現液體燃料合成。
該項目主要由三個單元構成,即光伏發電、電解水制氫、二氧化碳加氫制甲醇(如圖5所示)。第一部分光伏發電按照下游電解水制氫裝置消耗的電能計算規模,發電裝機容量為10.4MW,占地面積約250畝(1畝=666.67m);第二部分電解水制氫單元和第三部分二氧化碳加氫制甲醇單元占地共約30畝。第二部分使用兩臺電解槽為下游流程提供綠氫,其中一臺配備了本文作者團隊的新一代電解水制氫催化劑。第三部分二氧化碳加氫制甲醇則采用本文作者團隊自主研發的ZnO-ZrO固溶體催化劑。
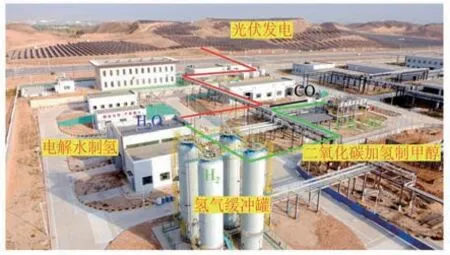
圖5 液態陽光示范項目全景圖
該項目通過了中國石化聯合會組織的現場驗收和科技成果鑒定,專家委員會鑒定結論為:該項目集成創新了液態太陽燃料合成全流程工藝,具有完全自主知識產權,整體技術處于國際領先。其中電解水技術單元采用了在鎳基體上原子級分散的過渡金屬電解水制氫催化劑,并裝配于工業電解槽中,實現單槽千立方米/小時以上規模制氫生產,超過GB 32311—2015規定的一級能效標準值(<4.3kW·h/mH@400mA/cm),能量轉化效率超過82%。對比商業催化劑,在相同制氫負荷下平均單槽過電位降低了18mV,直流單位制氫能耗降低了10%以上,顯著提高了電解水制氫效率。針對二氧化碳加氫制甲醇,本文作者團隊發明了新型鋅鋯氧化物固溶體催化劑,甲醇時空收率達到194 kg/(m·h)、選擇性達到98.5%,甲醇在有機相中含量達到99.7%,表現出優異的催化活性、選擇性和穩定性,顯著提高了二氧化碳加氫制甲醇收率。
4 液態陽光甲醇經濟性分析
目前,我國甲醇主要以煤、天然氣、焦爐氣等為原料進行合成,其中煤制甲醇占比最高。以60萬噸/年規模,折舊周期10年為例,對煤制甲醇和液態陽光甲醇生產成本進行了如下分析。
在固定資產投入中,煤制甲醇的基本單元包括造氣、空分、變換、凈化和其他公用工程。而液態陽光基本單元為電解水裝置和其他公用工程。運行成本投入中,煤制甲醇基本單元包括煤消耗、空分和其他三項,而液態陽光基本單元包括制氫電耗、二氧化碳捕獲和其他三部分。
二氧化碳捕集場景主要包括化工尾氣二氧化碳捕集和火力發電煙氣捕集。化工過程如合成氨/甲醇尾氣,經低溫甲醇洗后,二氧化碳體積分數在85%以上,其捕集成本在150CNY/t左右。火力發電煙氣體積分數約13%,其捕集成本約300CNY/t。隨著2021年7月16日碳排放權交易市場的正式啟動,全國碳市場碳排放配額(CEA)的價格也應該被考慮在內。生態環境部2021 年8 月18 日新聞發布會表示,2021年7月16日開市以來,全國碳市場排放配額累計成交量達到702×10t,累計成交額是3.55×10CNY,其平均成交價格約為50CNY/t。煤制甲醇二氧化碳排放系數約為3.0t二氧化碳/t甲醇,因此煤制甲醇成本與液態陽光成本估算如表1所示。
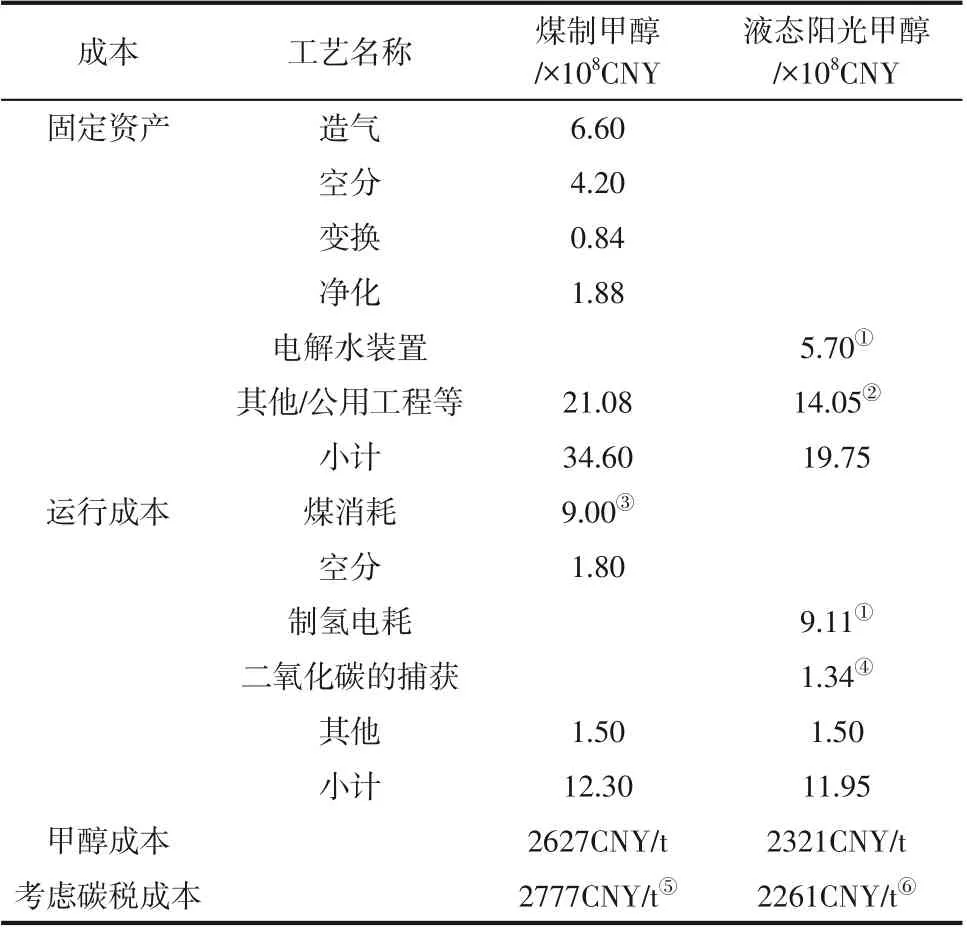
表1 煤制甲醇基本單元與液態太陽燃料基本單元甲醇生產成本對比
目前市場上甲醇售價持續走高,主要是煤炭價格升高,煤制甲醇成本與煤炭價格相關。而液態陽光甲醇成本與可再生能源發電成本緊密相關。二者成本與其最敏感因素變化關系見表2。可以預期,煤制甲醇的成本隨著煤炭價格的變化而處于高位,而液態陽光甲醇的成本隨著可再生能源發電成本的降低而不斷降低。
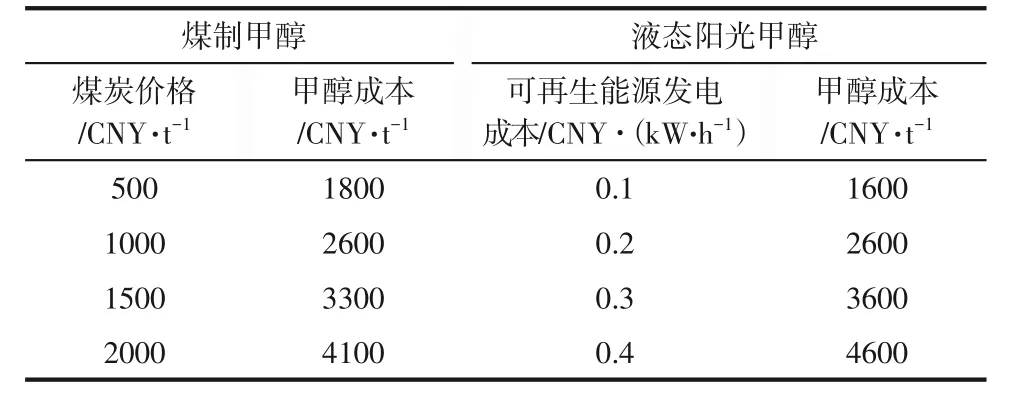
表2 煤制甲醇與液態陽光甲醇成本變化表
5 結語
我國可再生能源資源豐富,具有廣闊的發展前景,但主要分布在西部及北部地區,而我國能源消費主要集中在東部沿海地區。液態陽光技術提供了特高壓輸電外的可再生能源利用新模式,實現了可再生能源的長周期、大規模存儲及運輸。液態陽光技術也為水泥、鋼鐵、化工等二氧化碳剛性排放行業提供了切實可行的減排技術路徑。光伏-電解水制氫-二氧化碳加氫制甲醇是當下工業上最可行的液態陽光技術路線。其中堿性電解水制氫在規模和穩定性上具備更大的應用前景,目前已實現了單槽1000m/h 產氫量,單位制氫能耗已降至4.3~4.5kW·h/m。為適應大規模可再生能源制氫需求,未來發展的趨勢是單槽產氫量進一步提升(如1500~2000m/h),單位制氫能耗繼續降低(如4.0~4.2kW·h/m)。二氧化碳加氫制甲醇單元中,ZnO-ZrO固溶體催化劑在保證轉化率的基礎上,極大地提升了甲醇的選擇性和穩定性,但目前反應溫度需要300℃左右,熱力學上不利于甲醇合成,未來需要開發反應溫度較低的新型催化劑。此外,還需盡可能控制低的甲烷選擇性。未來,隨著工藝技術的不斷優化改進,可再生能源發電成本的進一步降低,將有望實現每年十萬至百萬噸液態陽光甲醇合成技術大規模推廣,為可再生能源消納和二氧化碳減排作出重要貢獻。

