經典名方枳實薤白桂枝湯物質基準的量值傳遞研究
徐瑞杰,薛 蓉,梅 茜,宮靜雯,張 倩,婁 悅,趙曉莉,許金國,嚴國俊,陸兔林,毛春芹
經典名方枳實薤白桂枝湯物質基準的量值傳遞研究
徐瑞杰,薛 蓉,梅 茜,宮靜雯,張 倩,婁 悅,趙曉莉,許金國,嚴國俊,陸兔林*,毛春芹*
南京中醫藥大學藥學院,江蘇 南京 210023
建立經典名方枳實薤白桂枝湯(Zhishi Xiebai Guizhi Decoction,ZXGD)基準樣品的HPLC特征圖譜并對其進行多成分含量測定,研究ZXGD物質基準量值傳遞規律,為復方制劑研究奠定基礎。制備20批ZXGD基準樣品,建立其特征圖譜,明確其特征峰并對其進行特征峰的歸屬;對ZXGD基準樣品進行多成分含量測定,分析主要成分從飲片-物質基準的傳遞規律。20批ZXGD基準樣品的特征圖譜相似度均大于0.93,共匹配得到11個特征峰,分別來自于方中枳實(峰1、3~5、9)、厚樸(峰2、10、11)、桂枝(峰6~8);各指標性成分的含量范圍及飲片-基準樣品的平均轉移率分別為辛弗林0.46%~0.85%和103.80%,橙皮苷0.58%~1.07%和42.36%,肉桂酸0.025%~0.047%和105.53%,桂皮醛0.09%~0.17%和5.40%,厚樸酚與和厚樸酚0.005 6%~0.010 3%和0.23%。采用HPLC特征圖譜和多成分含量測定對ZXGD物質基準的量值傳遞規律進行研究,該方法科學合理,且明確了飲片-物質基準的傳遞規律,實現了對經典名方ZXGD開發研究的全過程質量控制。
經典名方;枳實薤白桂枝湯;基準樣品;物質基準;特征圖譜;量值傳遞;枳實;厚樸;桂枝;辛弗林;橙皮苷;肉桂酸;桂皮醛;厚樸酚;和厚樸酚
枳實薤白桂枝湯(Zhishi Xiebai Guizhi Decotion,ZXGD)來源于東漢張仲景的《金匱要略》[1],全方共由枳實、薤白、桂枝、瓜蔞、厚樸5味藥組成,主要治療胸痹等疾病。現代臨床上主要應用于心腦血管系統、消化系統以及呼吸系統等方面疾病,其對冠心病、心絞痛、高脂血癥、功能性消化不良、肺栓塞等都有一定的治療作用[2-7]。近年來,國家大力支持古代經典名方中藥復方制劑的開發,對于經典名方的申報可免臨床研究資料,雖然與其他復方制劑的開發過程相比減少了臨床研究,但對其質量控制方面卻有著嚴格的要求。而特征圖譜和多成分含量測定是對經典名方質量控制研究的2個重要手段,特征圖譜結合多成分含量測定可較為全面地對經典名方物質基準的量值傳遞過程進行分析,從而對經典名方的質量控制提供參考價值[8-10]。
目前,針對ZXGD的報道主要集中于其藥理作用和臨床相關應用,對于其質量控制研究較少[11-14],通過建立ZXGD特征圖譜且結合多成分含量測定的研究還未見報道。為了進一步推進經典名方ZXGD中藥復方制劑的研究應用,根據國家藥品監督管理局發布的《古代經典名方中藥復方制劑物質基準的申報資料要求》[15],開展有關ZXGD的特征圖譜、多成分含量測定及物質基準的量值傳遞研究[16-18]。通過對國家發布的古代經典名方關鍵信息的考證[19],并結合具體情況研制ZXGD基準樣品,通過特征圖譜及指標成分的含量測定對ZXGD飲片-基準樣品研究全過程進行質量控制。為下一步進行ZXGD中藥復方制劑的研究奠定基礎,也為古代經典名方的開發與利用提供參考。
1 儀器與材料
1.1 儀器
島津LC-20AD型高效液相色譜儀,日本Shimadzu公司,包括LC-20AD溶劑輸送泵,SIL-20A自動進樣器,CTO-20AC柱溫箱,SPD-M20A紫外-可見檢測器,CBM-20A色譜數據工作站;FA1104N型電子分析天平,上海菁海儀器有限公司;MS-105DU型電子分析天平,瑞士梅特勒-托利多公司;KQ-500B型超聲波清洗器,昆山市超聲儀器有限公司;AE-1106A型多功能紅外爐,中山市愛米生活電器有限公司;FD-1A-50型冷凍干燥機,上海利聞科學儀器有限公司。
1.2 材料
枳實、厚樸、薤白、桂枝、瓜蔞5味藥材購于雷允上藥業有限公司,均來源于道地產區或主產區,經南京中醫藥大學藥學院陳建偉教授鑒定,5味藥材的基原分別為蕓香科柑橘屬植物酸橙L.的干燥幼果、木蘭科木蘭屬植物厚樸Rehd.et Wils.的干燥干皮、百合科蔥屬植物小根蒜Bge.的干燥鱗莖、樟科樟屬植物肉桂Presl的干燥嫩枝、葫蘆科栝樓屬植物栝樓Maxim.的干燥成熟果實。每味藥材共采購5批,參照《中國藥典》2020年版進行炮制,每批藥材炮制得3批飲片,因此得枳實、厚樸、薤白、桂枝、瓜蔞各15批飲片。
對照品辛弗林(批號110727-201809,質量分數99.5%)、和厚樸酚(批號110730-201614,質量分數99.3%)、厚樸酚(批號110729-201714,質量分數100.0%)、桂皮醛(批號110710-201821,質量分數99.6%)、橙皮苷(批號110721-201818,質量分數96.2%)、肉桂酸(批號110786-201604,質量分數98.8%),均購自中國食品藥品檢定研究院。
甲醇,分析純,山東禹王實業有限公司化工分公司;甲醇,色譜純,江蘇漢邦科技有限公司;娃哈哈純凈水,杭州娃哈哈集團有限公司;乙腈,色譜純,德國Merck公司;磷酸,色譜純,上海阿拉丁生化科技股份有限公司。
2 方法與結果
2.1 20批ZXGD基準樣品的制備
根據對《金匱要略》中記載的ZXGD的處方原文和國家發布的關鍵信息進行考證,并通過對浸泡時間、加蓋與否、濾過方式等因素進行考察,最終確定ZXGD基準樣品的制備工藝。
取枳實9 g、厚樸12 g,置陶瓷鍋中,加水1000 mL,浸泡60 min,以武火煮沸后,轉文火繼續煎煮至400 mL,2層紗布趁熱濾過。取薤白24 g、桂枝3 g、瓜蔞15 g,置于上述濾液中,浸泡60 min,武火沸騰后,轉文火繼續煎煮至100 mL,2層紗布濾過,濾液放冷至室溫。取濾液至?80 ℃冰箱預凍12 h后,放入冷凍干燥機,于?54 ℃、0.74 Pa真空度冷凍干燥為凍干粉,即得。
同法制備單味飲片及缺單味藥陰性樣品。
將枳實、厚樸、薤白、桂枝、瓜蔞各15批次飲片隨機組合形成20批次基準樣品,編號為ZXGD1~ZXGD20,具體批次組合信息見表1。
2.2 ZXGD基準樣品特征圖譜的建立
2.2.1 色譜條件 Kromasil C18色譜柱(250 mm× 4.6 mm,5 μm),流動相為乙腈-0.05%磷酸水溶液,梯度洗脫:0~7 min,1%乙腈;7~8 min,1%~5%乙腈;8~12 min,5%~15%乙腈;12~30 min,15%~20%乙腈;30~40 min,20%乙腈;40~50 min,20%~25%乙腈;50~51 min,25%~26%乙腈;51~65 min,26%~27%乙腈;65~68 min,27%~30%乙腈;68~70 min,30%~45%乙腈;70~75 min,45%乙腈;75~79 min,45%~65%乙腈;79~96 min,65%~95%乙腈;體積流量為1 mL/min;柱溫30 ℃;檢測波長為290 nm;進樣量10 μL。
表1 20批ZXGD基準樣品隨機組合信息
Table 1 Information table of random combination of 20 batches of ZXGD reference samples
編號枳實厚樸薤白桂枝瓜蔞 ZXGD1ZS-M1811004-3HP180612-2XB180321-3GZ-181014-2GL181016-3 ZXGD2ZS-M1811004-1HP180609-2XB180322-3GZ-181012-3GL181015-3 ZXGD3ZS-M1811004-1HP180610-1XB180322-3GZ-181014-3GL181016-3 ZXGD4ZS-M1811004-3HP180611-1XB180322-3GZ-181011-1GL181019-1 ZXGD5ZS-M1811002-3HP180612-3XB180323-2GZ-181015-1GL181018-2 ZXGD6ZS-M1811005-2HP180609-2XB180324-1GZ-181013-3GL181015-1 ZXGD7ZS-M1811001-3HP180609-2XB180323-2GZ-181011-2GL181018-1 ZXGD8ZS-M1811003-2HP180611-3XB180320-2GZ-181011-3GL181019-3 ZXGD9ZS-M1811005-1HP180610-1XB180323-3GZ-181014-1GL181016-1 ZXGD10ZS-M1811004-1HP180612-2XB180320-2GZ-181015-1GL181018-3 ZXGD11ZS-M1811001-3HP180612-3XB180320-3GZ-181013-1GL181016-2 ZXGD12ZS-M1811003-2HP180608-1XB180323-3GZ-181014-2GL181019-1 ZXGD13ZS-M1811004-3HP180610-1XB180322-2GZ-181013-3GL181017-3 ZXGD14ZS-M1811002-3HP180608-2XB180321-2GZ-181015-1GL181019-3 ZXGD15ZS-M1811002-2HP180608-3XB180321-1GZ-181013-2GL181019-3 ZXGD16ZS-M1811004-3HP180608-3XB180322-2GZ-181015-3GL181015-3 ZXGD17ZS-M1811004-3HP180608-3XB180322-2GZ-181015-3GL181015-3 ZXGD18ZS-M1811004-3HP180608-3XB180322-2GZ-181015-3GL181015-3 ZXGD19ZS-M1811004-3HP180608-3XB180322-2GZ-181015-3GL181015-3 ZXGD20ZS-M1811004-3HP180608-3XB180322-2GZ-181015-3GL181015-3
2.2.2 供試品溶液的制備 取10 mL煎煮液對應的凍干粉,置50 mL量瓶中,加甲醇40 mL,加蒸餾水至刻度,稱定質量,超聲處理(功率500 W、頻率40 kHz)20 min,放冷,再稱定質量,用80%甲醇補足減失的質量,搖勻,濾過,取續濾液,即得供試品溶液。
2.2.3 精密度試驗 取編號為ZXGD1的基準樣品1份,按照“2.2.2”項下方法制備供試品溶液,按照“2.2.1”項下色譜條件連續進樣6次,記錄色譜圖。以橙皮苷為參照峰,計算各特征峰相對保留時間和相對峰面積,結果各特征峰的相對保留時間RSD均小于0.28%,相對峰面積RSD均小于4.88%,表明儀器精密度良好。
2.2.4 穩定性試驗 取編號為ZXGD1的基準樣品一份,按照“2.2.2”項下方法制備供試品溶液,按照“2.2.1”項下色譜條件分別在0、2、4、8、12、24 h進樣,記錄色譜圖。以橙皮苷為參照峰,計算各特征峰相對保留時間和相對峰面積,結果各特征峰的相對保留時間RSD均小于0.31%,相對峰面積RSD均小于3.56%,表明供試品溶液在24 h內穩定性良好。
2.2.5 重復性試驗 取編號為ZXGD1的基準樣品一份,按照“2.2.2”項下方法平行制備6份供試品溶液,按照“2.2.1”項下色譜條件進樣,記錄色譜圖。以橙皮苷為參照峰,計算各特征峰相對保留時間和相對峰面積,結果各特征峰的相對保留時間RSD均小于0.29%,相對峰面積RSD均小于3.62%,表明該方法重復性良好。
2.2.6 特征峰的指認 按照“2.2.2”項下方法制備20批供試品溶液,按照“2.2.1”項下色譜條件進樣,記錄20批色譜圖。將20批ZXGD基準樣品特征圖譜以AIA格式導入《中藥色譜指紋圖譜相似度評價系統(2012版)》,以S1為參照圖譜,采用平均數法,時間窗設為0.5,并計算相似度。20批ZXGD(ZXGD1~ZXGD20)基準樣品特征圖譜的相似度分別為0.961、0.959、0.960、0.966、0.941、0.969、0.955、0.972、0.936、0.942、0.957、0.955、0.950、0.959、0.976、0.935、0.941、0.962、0.961、0.968,特征圖譜相似度均大于0.93,表明ZXGD的質量穩定均一,各批次間物質群較為穩定,特征圖譜疊加圖見圖1。
ZXGD基準樣品特征圖譜共標定了11個特征峰,通過與對照品色譜峰進行比對,指認到6個特征峰,其中1號峰為辛弗林、4號峰為橙皮苷、6號峰為肉桂酸、7號峰為桂皮醛、10號峰為和厚樸酚、11號峰為厚樸酚,混合對照品及ZXGD基準樣品特征圖譜見圖2。ZXGD基準樣品特征圖譜中有11個特征峰,其中6個峰(峰1、4、6、7、10、11)分別與相應的參照物保留時間相同,以橙皮苷參照物峰相應的峰為S峰,計算其余特征峰的相對保留時間,其相對保留時間應在規定值的±5%之內。規定值為0.52(峰2)、0.91(峰3)、1.51(峰5)、1.94(峰8)、2.08(峰9)。
2.2.7 飲片-基準樣品特征峰的傳遞 對ZXGD基準樣品中特征峰從飲片到基準樣品的傳遞規律進行分析。枳實、厚樸、桂枝單味飲片及缺單味飲片陰性樣品的特征圖譜分別見圖3。對ZXGD基準樣品中特征峰進行歸屬,其中1(辛弗林)、3、4(橙皮苷)、5、9號峰歸屬于枳實;2、10(和厚樸酚)、11(厚樸酚)號峰歸屬于厚樸;6(肉桂酸)、7(桂皮醛)、8號峰歸屬于桂枝。大部分色譜峰具有良好的傳遞性,且歸屬關系清晰,飲片中的物質群能夠較為穩定的向基準樣品中傳遞。
2.3 ZXGD基準樣品多成分含量測定
2.3.1 色譜條件 Kromasil C18色譜柱(250 mm×4.6 mm,5 μm),以乙腈-0.05%磷酸水溶液為流動相,梯度洗脫:0~7 min,1%乙腈;7~8 min,1%~5%乙腈;8~12 min,5%~15%乙腈;12~30 min,15%~20%乙腈;30~40 min,20%乙腈;40~50 min,20%~25%乙腈;50~51 min,25%~26%乙腈;51~65 min,26%~27%乙腈;65~68 min,27%~30%乙腈;68~70 min,30%~45%乙腈;70~75 min,45%乙腈;75~79 min,45%~65%乙腈;79~96 min,65%~95%乙腈;體積流量為1 mL/min;柱溫30 ℃;檢測波長為214 nm(辛弗林)、290 nm,進樣量10 μL。
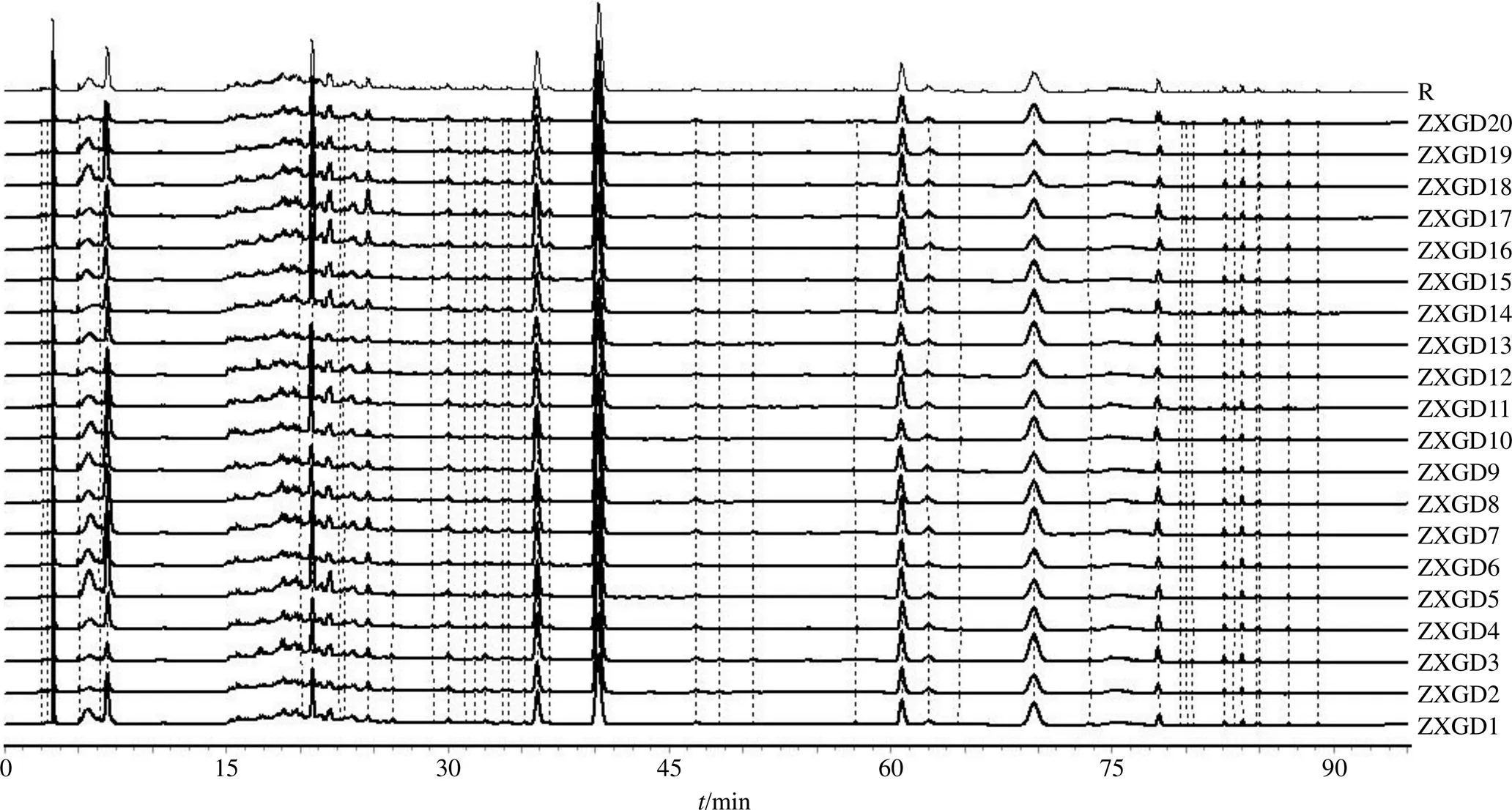
圖1 20批ZXGD基準樣品HPLC特征圖譜疊加圖
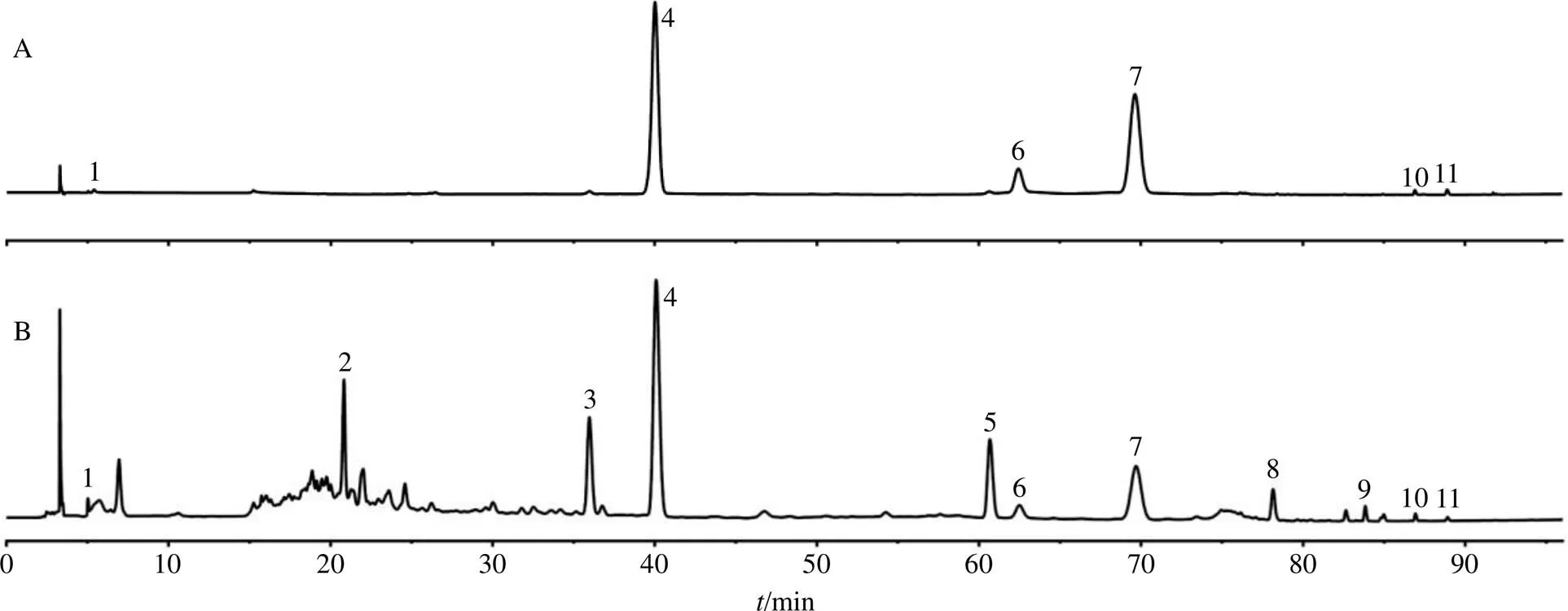
1-辛弗林 4-橙皮苷 6-肉桂酸 7-桂皮醛 10-和厚樸酚 11-厚樸酚
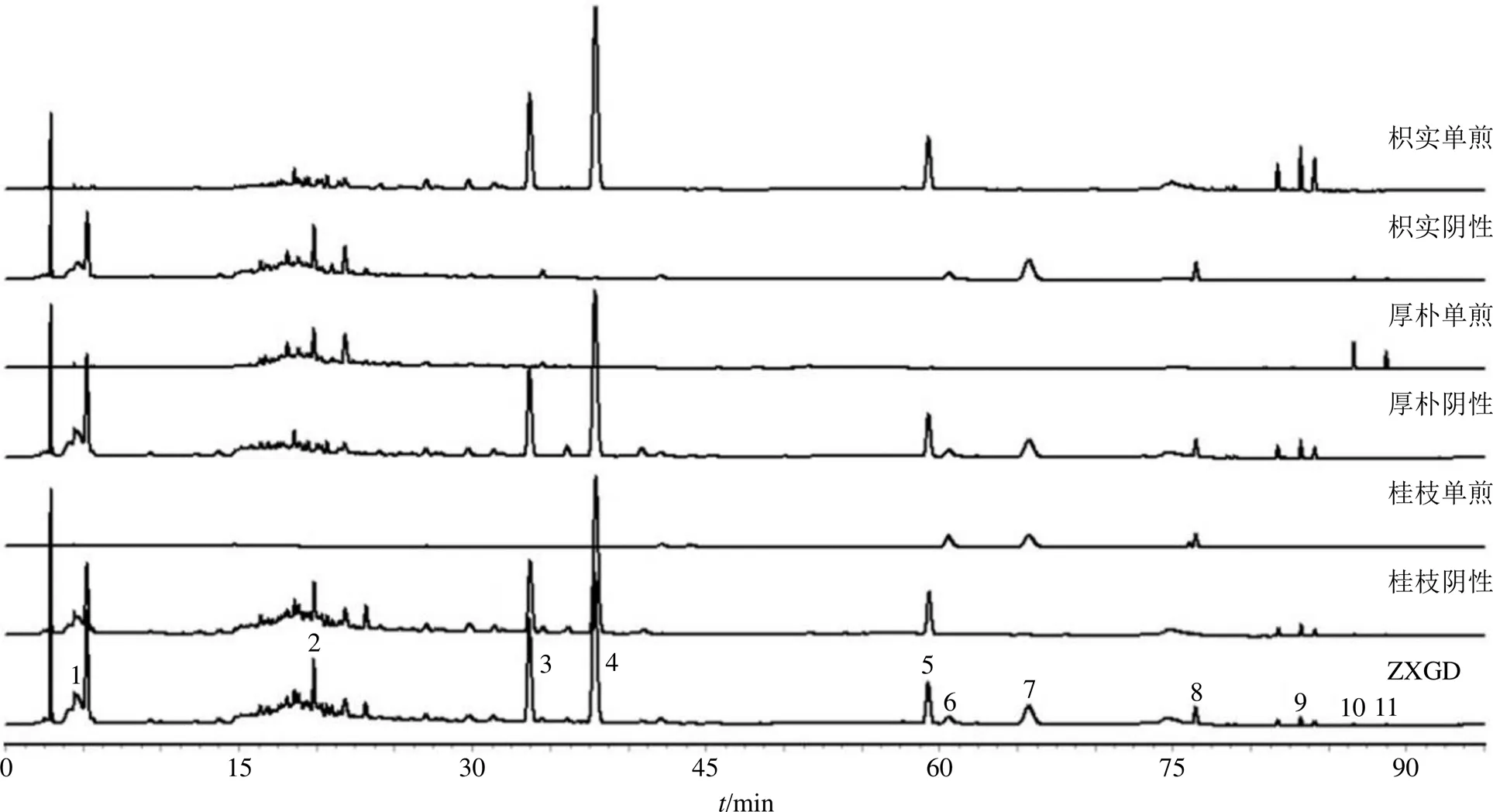
圖3 ZXGD特征峰傳遞圖譜
2.3.2 供試品溶液的制備 與“2.2.2”項下供試品溶液的制備方法一致。
2.3.3 對照品溶液的制備 取辛弗林、橙皮苷、肉桂酸、桂皮醛、和厚樸酚、厚樸酚對照品適量,精密稱定,加甲醇制成質量濃度為600.96、506.00、10.10、24.78、2.14、4.00 μg/mL的混合對照品溶液。
2.3.4 線性關系考察 精密量取“2.3.3”項下混合對照品溶液,按照2、4、6、8、16的倍數進行倍比稀釋,以甲醇為溶劑制成系列混合對照品溶液。按照“2.3.1”項下色譜條件進樣,記錄各指標成分峰面積,以進樣質量濃度為橫坐標(),峰面積為縱坐標(),進行線性回歸分析。得到回歸方程及線性范圍分別為辛弗林=2 493.47-46 034.63,=0.999 7,線性范圍37.56~600.96 μg/mL;橙皮苷=15 493.88-42 649.10,=0.999 8,線性范圍31.63~506.00 μg/mL;肉桂酸=66 637.13- 10 059.70,=0.999 8,線性范圍0.63~10.10 μg/mL;桂皮醛=105 449.40+49 387.90,=0.999 1,線性范圍1.55~24.78 μg/mL;和厚樸酚=17 489.30-154.06,=0.999 8,線性范圍0.13~2.14 μg/mL;厚樸酚=14 415.17-366.31,=0.999 9,線性范圍0.25~4.00 μg/mL;結果表明,6種指標成分在各自線性范圍內線性關系較好。
2.3.5 精密度試驗 取編號為ZXGD1的基準樣品一份,按照“2.2.2”項下方法制備供試品溶液,按照“2.3.1”項下色譜條件連續進樣6次,記錄各成分峰面積。計算辛弗林、橙皮苷、肉桂酸、桂皮醛、和厚樸酚、厚樸酚含量的RSD值,分別為0.41%、0.54%、1.23%、0.26%、1.95%、3.72%,表明儀器精密度良好。
2.3.6 穩定性試驗 取編號為ZXGD1的基準樣品一份,按照“2.2.2”項下方法制備供試品溶液,按照“2.3.1”項下色譜條件分別在0、2、4、8、12、24 h進樣,記錄各成分峰面積。計算辛弗林、橙皮苷、肉桂酸、桂皮醛、和厚樸酚、厚樸酚含量的RSD值,分別為0.58%、1.19%、2.48%、0.60%、1.60%、2.94%,表明供試品溶液24 h穩定性良好。
2.3.7 重復性試驗 取編號為ZXGD1的基準樣品一份,按照“2.2.2”項下方法平行制備6份供試品溶液,按照“2.3.1”項下色譜條件進樣,記錄各成分峰面積。計算辛弗林、橙皮苷、肉桂酸、桂皮醛、和厚樸酚、厚樸酚含量的RSD值,分別為2.35%、1.80%、1.74%、2.86%、3.57%、3.00%,表明方法重復性良好。
2.3.8 準確度試驗 取5 mL已知含量的ZXGD基準樣品對應的凍干粉,共取6份,分別加入與其各成分含量相等的對照品(辛弗林對照品3.08 mg、橙皮苷對照品3.8 mg、肉桂酸對照品0.05 mg、桂皮醛對照品0.25 mg、和厚樸酚對照品0.017 mg、厚樸酚對照品0.085 mg),按照“2.2.2”項下方法制備成供試品溶液,按照“2.3.1”項下色譜條件進樣,記錄各指標成分峰面積,并計算加樣回收率。辛弗林、橙皮苷、肉桂酸、桂皮醛、和厚樸酚、厚樸酚含量的RSD值分別為1.60%、0.39%、1.22%、1.68%、1.34%、2.52%,各成分的平均加樣回收率分別為102.60%、101.70%、103.29%、98.63%、100.53%、101.46%,表明方法準確度良好。
2.3.9 多成分含量測定 按照“2.2.2”項下方法制備20批ZXGD供試品溶液,并按照“2.3.1”項下色譜條件進樣,對20批ZXGD基準樣品進行含量測定,混合對照品和基準樣品的色譜圖見圖4,多成分含量測定結果見表2。20批ZXGD基準樣品中各成分質量分數為辛弗林0.35%~0.87%;橙皮苷0.62%~1.00%;肉桂酸0.029%~0.043%;桂皮醛0.10%~0.17%;厚樸酚與和厚樸酚0.003 3%~0.016 1%。根據《古代經典名方中藥復方制劑及其物質基準的申報資料要求》中含量測定的波動范圍一般不超過均值的70%~130%,因此,暫定ZXGD基準樣品中各成分的含量范圍為辛弗林0.46%~0.85%,橙皮苷0.58%~1.07%,肉桂酸0.025%~0.047%,桂皮醛0.09%~0.17%,厚樸酚與和厚樸酚0.005 6%~0.010 3%。
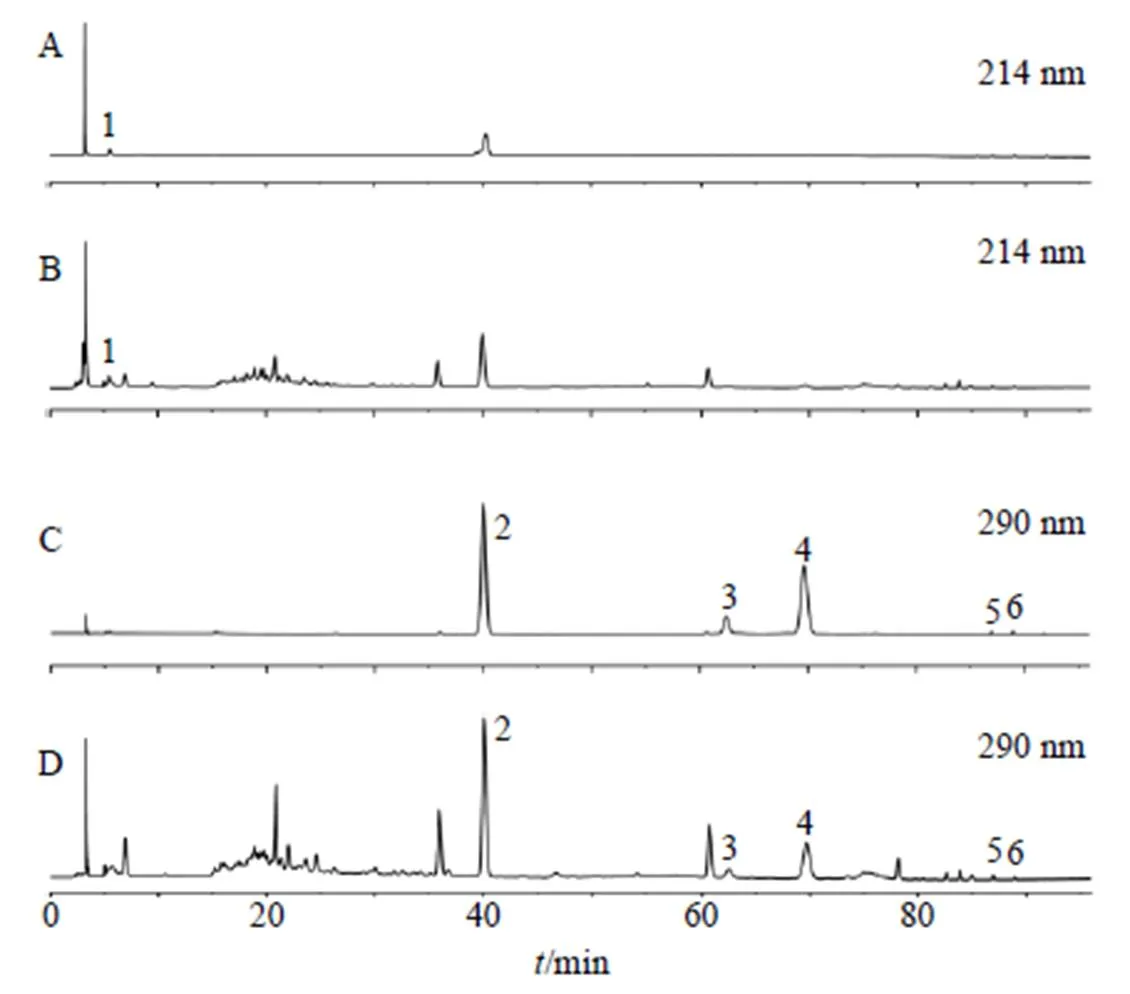
1-辛弗林 2-橙皮苷 3-肉桂酸 4-桂皮醛 5-和厚樸酚 6-厚樸酚
2.4 量值傳遞關系研究
20批ZXGD基準樣品和對應飲片中指標成分含量測定結果及轉移率見表3。20批ZXGD基準樣品中辛弗林質量分數為0.46%~0.85%,平均轉移率為103.80%;橙皮苷質量分數為0.58%~1.07%,平均轉移率為42.36%;肉桂酸質量分數為0.025%~0.047%,平均轉移率為105.53%;桂皮醛質量分數為0.09%~0.17%,平均轉移率為5.40%;厚樸酚與和厚樸酚質量分數總量為0.005 6%~0.010 3%,平均轉移率為0.23%。
根據相關規定,不同批次基準樣品的轉移率也應在其均值的70%~130%,在本研究中辛弗林、橙皮苷、肉桂酸和桂皮醛4個成分的轉移率基本都在其均值的70%~130%,說明前期枳實和桂枝的飲片及基準樣品的制備工藝相對穩定可行。但是部分批次中厚樸酚與和厚樸酚的轉移率超出了其均值的70%~130%,考慮到由于厚樸酚與和厚樸酚為木脂素類成分,難溶于水,而ZXGD基準樣品的制備工藝是加水煎煮,因此在基準樣品中該類成分含量較小,取其均值的70%~130%,存在的誤差相對較大,且厚樸各批次間含量差異也較大[20]。因此,在制備ZXGD基準樣品時,要嚴格把控所用原料飲片的質量,確定飲片中各成分的標準范圍,保證飲片質量的均一和穩定。
表2 20批ZXGD基準樣品含量測定
Table 2 Content determination of 20 batches of ZXGD reference samples
編號質量分數/%編號質量分數/% 辛弗林橙皮苷肉桂酸桂皮醛厚樸酚與和厚樸酚總量辛弗林橙皮苷肉桂酸桂皮醛厚樸酚與和厚樸酚總量 ZXGD10.800.650.0300.140.005 2ZXGD130.610.620.0340.150.005 0 ZXGD20.580.760.0330.130.004 2ZXGD140.860.890.0390.140.010 4 ZXGD30.680.920.0370.170.003 8ZXGD150.700.820.0290.130.010 4 ZXGD40.730.880.0350.140.011 2ZXGD160.710.850.0390.100.013 0 ZXGD50.680.930.0380.130.012 8ZXGD170.530.840.0420.120.007 8 ZXGD60.530.820.0300.120.005 4ZXGD180.590.990.0340.100.016 1 ZXGD70.691.000.0430.160.005 1ZXGD190.550.780.0400.100.009 8 ZXGD80.690.850.0400.140.003 3ZXGD200.650.770.0360.120.009 0 ZXGD90.540.820.0360.120.006 2均值0.650.820.0360.130.008 0 ZXGD100.350.660.0330.140.004 7均值70%~0.46~0.58~0.025~0.09~0.005 6~ ZXGD110.870.870.0380.120.008 5130%0.851.070.0470.170.010 3 ZXGD120.700.770.0390.120.007 2
表3 ZXGD基準樣品指標成分含量測定及轉移率
Table 3 Content and transfer rate of indicator components in ZXGD
編號辛弗林/%橙皮苷/%肉桂酸/%桂皮醛/%厚樸酚與和厚樸酚/% 飲片基準樣品轉移率飲片基準樣品轉移率飲片基準樣品轉移率飲片基準樣品轉移率飲片基準樣品轉移率 ZXGD10.700.80114.292.010.6532.340.0310.03096.772.430.145.764.070.005 20.13 ZXGD20.720.5880.561.940.7639.180.0280.033117.862.380.135.463.080.004 20.14 ZXGD30.720.6894.441.940.9247.420.0290.037127.592.210.177.692.080.003 80.18 ZXGD40.700.73104.292.010.8843.780.0310.035112.902.430.145.763.170.011 20.35 ZXGD50.540.68125.931.860.9350.000.0420.03890.482.610.134.984.010.012 80.32 ZXGD60.550.5396.361.730.8247.400.0290.030103.452.410.124.983.080.005 40.18 ZXGD70.620.69111.291.981.0050.510.0300.043143.332.510.166.373.080.005 10.17 ZXGD80.540.69127.782.050.8541.460.0380.040105.262.300.146.093.130.003 30.11 ZXGD90.550.5498.181.770.8246.330.0390.03692.312.470.124.862.080.006 20.30 ZXGD100.720.3548.611.940.6634.020.0420.03378.572.610.145.364.070.004 70.12 ZXGD110.620.87140.321.980.8743.940.0330.038115.152.260.125.314.010.008 50.21 ZXGD120.540.70129.632.050.7737.560.0310.039125.812.430.124.943.010.007 20.24 ZXGD130.700.6187.142.010.6230.850.0290.034117.242.410.156.222.080.005 00.24 ZXGD140.540.86159.261.860.8947.850.0420.03992.862.610.145.365.600.010 40.19 ZXGD150.560.70125.001.860.8244.090.0480.02960.422.330.135.583.740.010 40.28 ZXGD160.700.71101.432.010.8542.290.0360.039108.332.320.104.313.740.013 00.35 ZXGD170.700.5375.712.010.8441.790.0360.042116.672.320.125.173.740.007 80.21 ZXGD180.700.5984.292.010.9949.250.0360.03494.442.320.104.313.740.016 10.43 ZXGD190.700.5578.572.010.7838.810.0360.040111.112.320.104.313.740.009 80.26 ZXGD200.700.6592.862.010.7738.310.0360.036100.002.320.125.173.740.009 00.24 平均值0.640.65103.801.950.8242.360.0350.036105.532.400.135.403.450.008 00.23
3 討論
ZXGD由枳實、厚樸、薤白、桂枝、瓜蔞5味藥組成,主要用于治療胸痹等癥。為促進ZXGD中藥復方制劑的開發利用,本實驗從ZXGD基準樣品特征圖譜及多成分含量測定2個方面的關鍵質量屬性,全面分析了ZXGD物質基準的量值傳遞規律。
本研究在對特征圖譜及多成分含量測定方法建立過程中,分別考察了甲醇-水、乙腈-水、乙腈-磷酸水溶液等不同體系、不同比例的流動相系統,結果表明乙腈-0.05%磷酸水溶液為流動相,基線平穩、色譜峰分離良好;分別考察不同波長,全波長掃描結果表明在290 nm時各成分色譜行為良好,在214 nm時辛弗林色譜峰響應較好,雜質干擾小;分別考察不同柱溫,結果表明,30 ℃時辛弗林、肉桂酸色譜峰分離較好。因此,明確流動相為乙腈-0.05%磷酸水溶液,特征圖譜波長為290 nm,含量測定波長為290 nm(橙皮苷、肉桂酸、桂皮醛、厚樸酚與和厚樸酚)、214 nm(辛弗林),柱溫為30 ℃。
特征圖譜及多成分含量測定色譜峰均來自于枳實、厚樸、桂枝3味藥,薤白和瓜蔞的藥味信息未能很好的體現,可能是由于在本研究中的實驗條件下,薤白和瓜蔞的成分含量較低達不到定量限或洗脫程序不適合等因素導致。因此目前對薤白和瓜蔞2味藥的定量分析還存在困難,后期將采用適宜的方法如LC-MS、GC-MS等對該2味藥進一步分析,以較多地體現藥味信息[21-22],對ZXGD進行全方位的質量控制研究。
在對20批ZXGD基準樣品的含量測定和轉移率分析時,發現辛弗林、橙皮苷、肉桂酸和桂皮醛基本都在其均值的70%~130%,但是厚樸酚與和厚樸酚的含量卻出現了離散數據。在對厚樸飲片進行研究時發現,同一批厚樸藥材含量有高有低,因此,炮制出的同一批飲片含量也存在差異,而在制備ZXGD基準樣品時,每一批基準樣品僅投料厚樸飲片12 g,投料量較小,也有可能會導致厚樸飲片取樣不均,從而使得厚樸酚與和厚樸酚的含量出現離散數據。其次,厚樸酚與和厚樸酚為木脂素類成分,難溶于水,在基準樣品中含量較低,計算其均值的70%~130%就會出現相對更大的誤差[23],因此是否可考慮對含量高低不同的成分進行具體分析,而不是都把范圍限定在其均值的70%~130%,以減少誤差。在后期實驗中可進一步嚴格把控厚樸飲片質量,并增加基準樣品批次的制備,從而降低離散數據的影響。
對于ZXGD基準樣品的研究是其中藥復方制劑研究中的關鍵,同時也是經典名方中藥復方制劑“遵古”的體現,而物質基準是包含了基準樣品中飲片質量、制備工藝穩定性等信息的標準[24]。本研究通過對ZXGD物質基準的量值傳遞規律進行分析,明晰了飲片-物質基準的傳遞規律,能更好地指導原料飲片的質量控制,為確保ZXGD基準樣品的質量穩定提供有效手段,同時也為后續ZXGD復方制劑的研究,實現全過程的質量控制奠定有力基礎。
利益沖突 所有作者均聲明不存在利益沖突
[1] 東漢·張仲景.金匱要略 [M].何任, 何若蘋整理.北京: 人民衛生出版社, 2005: 31-32.
[2] 李楠楠, 石月萍.加減枳實薤白桂枝湯通過AC/cAMP通路對缺血再灌注大鼠心肌組織水通道蛋白表達的影響 [J].中國動脈硬化雜志, 2018, 26(3): 237-244.
[3] 姜曉旭.枳實薤白桂枝湯對ET-1誘發家兔冠脈痙攣干預及機制研究 [D].哈爾濱: 黑龍江中醫藥大學, 2017.
[4] 馬旬旬.黃連枳實薤白桂枝湯對痰阻心脈證冠心病心絞痛患者Hey、SOD、hs-CRP的影響[D].南京: 南京中醫藥大學, 2018.
[5] 劉宇, 邵金博, 郭立中.枳實薤白桂枝湯治療冠心病合并高脂血癥的療效及對內皮功能和脂代謝的影響 [J].中藥材, 2018, 41(2): 476-478.
[6] Tang Y, Cai H R, Zhan Z Y,.Herbal medicine (Zhishi Xiebai Guizhi Decoction) for unstable angina: Protocol for a systematic review and meta-analysis [J]., 2018, 97(52): e13965.
[7] 張長喜.枳實薤白桂枝湯治療功能性消化不良50例 [J].中國中醫藥現代遠程教育, 2015, 13(20): 45-46.
[8] 楊艷玲, 劉彩鳳, 黃嘉怡, 等.經典名方桃紅四物湯的物質基準量值傳遞分析 [J].中國中藥雜志, 2021, 46(4): 801-809.
[9] 彭梅梅, 郭爽, 陳琪, 等.基于特征圖譜和網絡藥理學的經典名方黃連湯質量標志物(Q-Marker)預測分析 [J].中草藥, 2021, 52(18): 5514-5523.
[10] 齊琪, 趙(王月)瑛, 張晴, 等.經典名方小承氣湯的物質基準量值傳遞研究 [J].中草藥, 2021, 52(10): 2927-2937.
[11] 袁海建, 李衛, 祝一飛, 等.枳實薤白桂枝湯HPLC指紋圖譜及10種指標成分含量測定研究 [J].中草藥, 2020, 51(9): 2448-2459.
[12] 閆紅, 余洪, 潘小丹, 等.枳實薤白桂枝湯合理中湯加減輔助治療穩定型心絞痛及對炎癥因子和血管內皮功能的影響 [J].中國實驗方劑學雜志, 2020, 26(17): 83-88.
[13] 李楠楠, 石月萍.加減枳實薤白桂枝湯通過AC/cAMP通路對缺血再灌注大鼠心肌組織水通道蛋白表達的影響 [J].中國動脈硬化雜志, 2018, 26(3): 237-244.
[14] 何學春.四妙勇安湯合枳實薤白桂枝湯治療冠心病臨床療效分析 [J].亞太傳統醫藥, 2014, 10(14): 108-109.
[15] 國家藥品監督管理局.公開征求古代經典名方中藥復方制劑及其物質基準申報資料要求意見[EB/OL].[2019-03-27].https://www.nmpa.gov.cn/xxgk/zhqyj/ zhqyjyp/20190327150 101694.html.
[16] 劉冬涵, 薛宇濤, 羅菊元, 等.經典名方苓桂術甘湯的物質基準量值傳遞分析 [J].中國中藥雜志, 2019, 44(24): 5421-5428.
[17] 成顏芬, 杜克群, 吳億晗, 等.基于化學特征與核心功效分析經典名方桃紅四物湯復方合煎與單煎差異研究 [J].中草藥, 2021, 52(19): 5879-5890.
[18] Sang Q N, Jia Q Q, Zhang H Y,.Chemical profiling and quality evaluation of Zhishi-Xiebai-Guizhi Decoction by UPLC-Q-TOF-MS and UPLC fingerprint [J]., 2021, 194: 113771.
[19] 國家中醫藥管理局.關于發布《古代經典名方目錄(第一批)》的通知[EB/OL].[2018-04-16].http://kjs.satcm.gov.cn/zhengcewenjian/2018-04-16/7107.html.
[20] 荊文光, 張權, 杜杰, 等.不同產地厚樸藥材中3種木脂素類成分含量測定及聚類分析 [J].世界科學技術—中醫藥現代化, 2018, 20(10): 1822-1827.
[21] 王宇卿, 黃涵.UPLC-Q-TOF/MS法分析瓜蔞薤白半夏湯中主要化學成分 [J].中國醫院藥學雜志, 2018, 38(19): 2017-2021.
[22] 李欣, 唐力英, 許靜, 等.基于UPLC-LTQ-Orbitrap高分辨質譜的中藥瓜蔞化學成分分析 [J].中國實驗方劑學雜志, 2019, 25(1): 201-210.
[23] 范琪.厚樸抗氧化活性成分的提取分離及其抗氧化活性測試研究 [D].重慶: 重慶大學, 2014.
[24] 國家藥品監督管理局.關于發布《中藥配方顆粒質量控制與標準制定技術要求》的通告(2021年第16號)[EB/OL].[2021-01-26].https:www.nmpa.gov.cn/xxgk/ ggtg/qtggtg/20 210210145453181.html.
Research on quantitative transmitting of classical prescription Zhishi Xiebai Guizhi Decoction substance benchmarks
XU Rui-jie, XUE Rong, MEI Xi,GONG Jing-wen, ZHANG Qian, LOU Yue, ZHAO Xiao-li, XU Jin-guo, YAN Guo-jun, LU Tu-lin, MAO Chun-qin
School of Pharmacy, Nanjing University of Chinese Medicine, Nanjing 210023, China
To establish the HPLC characteristic map of the reference samples of the classical prescription Zhishi Xiebai Guizhi Decoction (ZXGD, 枳實薤白桂枝湯) and to determine the content of its multi-components, to study the transfer rule of the substance benchmark value of ZXGD, for the follow-up study of Chinese medicine compound preparations lay the foundation.Twenty batches of ZXGD reference samples were prepared, and their characteristic map was established, its characteristic peaks was clarified and assigned to the characteristic peaks; Multi-component content determination on the reference samples of ZXGD was carried out, and the transfer law of main components were analyzed from the decoction pieces to the substance benchmark.The similarities of the characteristic maps of the 20 batches of ZXGD reference samples were all greater than 0.93, and a total of 11 characteristic peaks were matched, which were from Zhishi (, peaks 1, 3—5, 9), Houpo (, peaks 2, 10, 11), Guizhi (, peaks 6—8); The content range of each index component and the average transfer rate of decoction pieces-reference samples were 0.46%—0.85% and 103.80% for synephrine, respectively, hesperidin 0.58%—1.07% and 42.36%, cinnamic acid 0.025%—0.047% and 105.53%, cinnamaldehyde 0.09%—0.17% and 5.40%, magnolol and honokiol 0.005 6%—0.010 3% and 0.23%.The HPLC characteristic map and multi-component content determination are used to study the quantity value transfer law of ZXGD.The whole process quality control of the development and research of classical prescription ZXGD.
classic prescriptions; Zhishi Xiebai Guizhi Decoction; reference samples; substance benchmark; characteristic chromatogram; quantitative transmitting;;;; synephrine; hesperidin;cinnamon acid;cinnamaldehyde; magnolol; honokiol
R283.6
A
0253 - 2670(2022)09 - 2650 - 09
10.7501/j.issn.0253-2670.2022.09.007
2021-11-22
2018國家重點研發計劃項目(2018YFC1707000)
徐瑞杰,碩士研究生,主要從事中藥炮制及中藥飲片質量標準研究。E-mail: xuruijier@126.com
通信作者:毛春芹,正高級實驗師,主要從事新藥研發及中藥質量研究。E-mail:300555@njucm.edu.cn
陸兔林,教授,博士生導師,主要從事中藥炮制及中藥飲片質量標準研究。E-mail: ltl2021@njucm.edu.cn
[責任編輯 鄭禮勝]

