二甲雙胍聯合達格列凈治療T2DM合并NAFLD患者療效及血清二肽基肽酶4和C肽變化*
王詩淞,林輝雄,張泰勝,董儷雯,王英霞,林秋香
非酒精性脂肪性肝病(non-alcoholic fatty liver diseases,NAFLD)是與熱量過剩和代謝紊亂相關的最常見的慢性肝病,涵蓋肝脂肪變性、脂肪性肝炎、肝硬化甚至肝細胞癌的連續復雜的病理學過程[1,2]。NAFLD代表代謝綜合征的肝臟表現,其患病率不斷上升,當前我國發病率約為25%[3]。胰島素抵抗(insulin resistance,IR)是NAFLD的核心病理學發生基礎。隨著IR進展,易導致2型糖尿病(type 2 diabetes mellitus,T2DM)發生[4]。研究[5]顯示,T2DM合并NAFLD增加了肝臟脂肪變性向終末期肝病進展的風險。針對NAFLD尚缺乏特效的治療藥物。鈉-葡萄糖共轉運蛋白2抑制劑(sodium-glucose transporter protein 2 inhibitor,SGLT2i)作為一種新型降糖藥廣泛用于治療T2DM患者。多項研究[6,7]顯示,SGLT2i除了發揮降糖作用之外還能減輕體質量,降低肝臟脂肪含量。此外,SGLT2i能有效改善NAFLD患者肝組織學改變,延緩脂肪變病情進展[8]。本研究應用二甲雙胍聯合達格列凈治療T2DM合并NAFLD患者,評估了其療效和安全性,現報道如下。
1 資料與方法
1.1 一般資料 2018年9月~2021年9月我院收治的T2DM合并NAFLD患者98例,男60例,女38例;年齡為25~67歲,平均年齡為(46.5±4.9)歲。符合《非酒精性脂肪性肝病防治指南》[9]和《中國2型糖尿病防治指南》[10]的診斷標準。排除標準:1型糖尿病、妊娠期糖尿病或其他類型糖尿病;既往有大量飲酒史;合并惡性腫瘤;合并嚴重的肝、腎功能不全;自身免疫性肝病;既往有肝臟手術史;不耐受二甲雙胍或二甲雙胍聯合達格列凈治療者。患者簽署知情同意書,本研究獲得我院醫學倫理委員會審核通過。
1.2 治療方法 采用隨機數字表法將患者分為兩組,49例對照組患者接受鹽酸二甲雙胍(中美上海施貴寶制藥有限公司,國藥準字H20023370)500 mg口服,3次/d,治療24 w;49例觀察組患者在對照組治療基礎上加用達格列凈(阿斯利康制藥有限公司,國藥準字H20170119)10 mg口服,1次/d,治療24 w。
1.3 檢測與檢查 所有患者均采集清晨空腹靜脈血10 ml。使用日本OLYMPUS AU5400型全自動生化分析儀檢測血生化指標;使用TOSOH HLC-723全自動糖化血紅蛋白分析儀檢測糖化血紅蛋白(HbA1c);采用電化學發光法檢測血清空腹胰島素(FINS)水平,計算穩態模型胰島素抵抗指數(HOMA-IR),HOMA-IR=(FPG×FINS)/22.5;采用化學發光法檢測血清空腹C肽(鄭州人福博賽生物技術有限公司);采用ELISA法檢測血清可溶性二肽基肽酶4(sDPP-4)水平(Abcam公司);使用飛利浦Brilliance iCT 256層螺旋CT掃描儀空腹行腹部CT檢查,計算肝/脾CT比值。
2 結果
2.1 兩組肝功能指標比較 在治療24 w末,觀察組血清GGT水平顯著低于對照組,差異具有統計學意義(P<0.05,表1)。

表1 兩組肝功能指標比較
2.2 兩組肝/脾CT比值、血清空腹C肽和sDPP-4水平比較 在治療24 w末,觀察組肝/脾CT比值顯著高于對照組,而血清空腹C肽和sDPP-4水平均顯著低于對照組,差異均具有統計學意義(P<0.05,表2)。
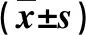
表2 兩組肝/脾CT比值、血清空腹C肽和sDPP-4水平比較
2.3 兩組血糖指標和胰島素抵抗指數比較 在治療24 w末,觀察組FPG、HbA1c和HOMA-IR水平均顯著低于對照組,差異均具有統計學意義(P<0.05,表3)。
2.4 兩組血脂水平比較 在治療24 w末,觀察組血清TC、TG和LDL-C水平均顯著低于對照組,而血清HDL-C水平顯著高于對照組,差異均具有統計學意義(P<0.05,表4)。
2.5 兩組不良反應發生情況比較 在治療期間,對照組未發生明顯的不良反應;觀察組發生輕度低血糖反應1例,尿路感染1例。
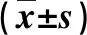
表3 兩組血糖指標和胰島素抵抗指數比較

表4 兩組血脂水平比較
3 討論
NAFLD與T2DM具有密切的內在聯系,IR作為T2DM與NAFLD共有的核心特征,是NAFLD與T2DM相互影響和促進的關鍵病理學基礎[11-13]。研究認為,NAFLD是代謝綜合征的肝臟表現,其治療應以積極控制體質量以及改善IR為核心策略[14]。作為一種胰島素增敏劑,盡管二甲雙胍能有效改善IR,但并不能顯著降低血清轉氨酶水平,對NAFLD患者肝組織學的影響也甚微。本研究觀察了在二甲雙胍治療基礎上聯合達格列凈治療T2DM合并NAFLD患者的效果,結果顯示聯合用藥可以有效降低血清轉氨酶水平、改善肝功能。肝/脾CT比值是應用CT檢查測量計算的定量指標。隨著肝脂肪變性的加劇,肝/脾CT比值減少,其已被越來越多地用于評估肝脂肪變性程度。C肽是胰島β細胞的分泌物。近年來研究發現空腹C肽是肝纖維化進展的獨立預測因子[15]。有研究者將T2DM合并NAFLD患者根據肝纖維化程度進一步分為進展性肝纖維化組和非進展性肝纖維化組,結果顯示兩組空腹C肽水平存在顯著性差異,進展性肝纖維化組空腹C肽水平明顯升高[16]。本研究聯用二甲雙胍和達格列凈治療患者可以顯著提高肝/脾CT比值、降低空腹C肽水平,提示達格列凈或能有效抑制肝脂肪變性和纖維化進展。
關于NAFLD發生、發展機制,最為接受的理論是國外學者提出的“二次打擊學說”,即以IR和脂代謝紊亂形成單純性肝脂肪變性的首次打擊;肝組織炎癥和纖維化改變導致脂肪肝發展為脂肪性肝炎或肝硬化的二次打擊[17,18]。代謝紊亂引起循環和肝臟中游離不飽和脂肪酸水平升高,過量的游離脂肪酸可在肝組織內轉化為甘油三酯等脂質,導致肝臟脂肪變性,進一步誘導NAFLD的形成。由此可見,改善IR和脂代謝平衡對減輕T2DM合并NAFLD患者肝臟脂肪變性具有重要的臨床意義。在本研究,與單獨應用二甲雙胍相比,聯用達格列凈治療可以顯著改善患者血脂代謝紊亂和IR水平,表現為有效降低了血清TC、TG、LDL-C水平和HOMA-IR,而增加了血清HDL-C水平。既往研究[19]表明,SGLT2i能增加尿糖排泄,并促進脂肪利用以抑制脂肪堆積,還能通過減少脂肪酸合成酶等表達,降低肝臟脂肪的合成。
研究[20]顯示,SGLT2i能改善大小鼠NAFLD模型IR并降低血清轉氨酶水平,延緩肝臟脂肪變性程度。此外,在原有降糖藥的應用基礎上加用達格列凈能明顯減輕IR水平,提高肝臟、肌肉等組織對胰島素的敏感性,減輕肝臟脂肪變性程度[8],與本研究結論相符合。本研究結果還顯示,二甲雙胍聯合達格列凈治療可以顯著降低T2DM合并NAFLD患者血清sDPP-4水平。DPP-4是一種細胞表面Ⅱ型跨膜蛋白,是體內胰高糖素樣生長因子1的降解酶。DPP-4的可溶性形式sDPP-4存在于血液循環,缺乏胞質尾和跨膜結構域,具有DPP-4酶活性。在小鼠,肥胖刺激肝細胞產生和分泌sDPP-4,促進脂肪組織炎癥和IR[21]。另有研究表明,在治療期間T2DM合并NAFLD患者肝酶的變化與血清sDPP-4變化呈正相關[22]。我們結合相關研究總結應用達格列凈顯著改善T2DM合并NAFLD患者IR的可能機制包括:降低血清sDPP-4水平,抑制sDPP-4引起的IR水平增加;減少游離脂肪酸水平和肝臟脂肪積累;通過減少炎癥細胞因子的分泌,從而間接改善IR;減輕肝纖維化。在不良反應方面,長期使用達格列凈會引起多尿、低血壓、泌尿系感染和低血糖反應。在本研究,我們聯合使用達格列凈并未顯著增加總體不良反應發生率,僅有個例發生輕度低血糖反應或尿路感染。
綜上所述,應用二甲雙胍聯合達格列凈治療T2DM合并NAFLD患者能有效控制血糖并糾正脂代謝紊亂,降低血清sDPP-4和胰島素抵抗水平,在改善肝脂肪變性方面顯示出有價值的苗頭,但這種聯合長期應用是否會帶來花費增加和不良反應等,仍值得深入探討。

