基于真實(shí)情境的深度學(xué)習(xí)與思維發(fā)展
王長艷 李伏剛 陳瑞雪


摘要:基于對化學(xué)深度學(xué)習(xí)的研究,在模擬侯氏制堿的情境中思考、分析碳酸鈉工業(yè)制備的原料、原理問題,建立認(rèn)識物質(zhì)和分析轉(zhuǎn)化的學(xué)科視角;實(shí)驗(yàn)探究碳酸鈉和碳酸氫鈉的性質(zhì)差異,思維有序地從定性和定量的角度分析混合物,提升真實(shí)情境下綜合復(fù)雜問題的解決能力,發(fā)展學(xué)生化學(xué)學(xué)科核心素養(yǎng)。
關(guān)鍵詞:制備Na2CO3;深度學(xué)習(xí);思維發(fā)展
文章編號:1008-0546(2022)08-0047-05?? 中圖分類號:G632.41?? 文獻(xiàn)標(biāo)識碼:B
doi:10.3969/j.issn.1008-0546.2022.08.010
化學(xué)深度學(xué)習(xí)的內(nèi)涵為:“在教師引領(lǐng)下,學(xué)生圍繞具有挑戰(zhàn)性的學(xué)習(xí)主題,開展以化學(xué)實(shí)驗(yàn)為主的多種探究活動,從宏微結(jié)合、變化守恒的視角,運(yùn)用證據(jù)推理與模型認(rèn)知的思維方式,解決綜合復(fù)雜問題,獲得結(jié)構(gòu)化的化學(xué)核心知識,建立運(yùn)用化學(xué)學(xué)科思想解決問題的思路方法,培養(yǎng)學(xué)生的創(chuàng)新精神和實(shí)踐能力,促進(jìn)學(xué)生核心素養(yǎng)的發(fā)展。[1]”化學(xué)深度學(xué)習(xí)的根本目標(biāo)是改變學(xué)生的學(xué)習(xí)方式,促進(jìn)化學(xué)學(xué)科核心素養(yǎng)發(fā)展。基于對化學(xué)深度學(xué)習(xí)的研究,在進(jìn)行元素化合物內(nèi)容教學(xué)時(shí),恰當(dāng)選取真實(shí)生產(chǎn)生活情境,課堂中以具體知識為載體,以帶有驅(qū)動性的問題引領(lǐng)學(xué)生進(jìn)行驅(qū)動思考、深度探究,將問題“情境化”,促使學(xué)生基于問題深度參與課堂學(xué)習(xí),提升真實(shí)情境下綜合復(fù)雜問題的解決能力,發(fā)展學(xué)生化學(xué)學(xué)科核心素養(yǎng)。
一、課程標(biāo)準(zhǔn)要求和教學(xué)內(nèi)容分析
《普通高中化學(xué)課程標(biāo)準(zhǔn)(2017年版2020年修訂)》對碳酸鈉和碳酸氫鈉內(nèi)容的教學(xué)要求是:結(jié)合真實(shí)情境中的應(yīng)用實(shí)例或通過實(shí)驗(yàn)探究,了解鈉及其重要化合物的主要性質(zhì),了解這些物質(zhì)在生產(chǎn)、生活中的應(yīng)用[2]。教材內(nèi)容安排主線為展示碳酸鈉和碳酸氫鈉的主要用途→實(shí)驗(yàn)比較碳酸鈉和碳酸氫鈉的溶解性→介紹碳酸鈉和碳酸氫鈉的主要物理性質(zhì)→實(shí)驗(yàn)對比碳酸鈉和碳酸氫鈉的熱穩(wěn)定性→科學(xué)史話介紹侯德榜和侯氏制堿法。教材內(nèi)容的編排給出了研究碳酸鈉和碳酸氫鈉性質(zhì)的基本方法——對比法,也給實(shí)際教學(xué)提供了豐富的情境素材,既可以從生活實(shí)際應(yīng)用入手進(jìn)行學(xué)習(xí),又可以從實(shí)驗(yàn)探究進(jìn)入學(xué)習(xí),還可以借助侯氏制堿法并結(jié)合工業(yè)生產(chǎn)深入學(xué)習(xí)。基于學(xué)生在初中學(xué)習(xí)過部分碳酸鈉和碳酸氫鈉的性質(zhì),在本節(jié)前一部分運(yùn)用對比法學(xué)習(xí)了氧化鈉與過氧化鈉的性質(zhì),碳酸鈉和碳酸氫鈉這部分教學(xué)內(nèi)容可以在深入了解兩種鹽各自性質(zhì)的基礎(chǔ)上進(jìn)一步開放思維,以哪些物質(zhì)之間的反應(yīng)可以生成Na2CO3引發(fā)思考,從元素找尋物質(zhì),多角度分析實(shí)際工業(yè)生產(chǎn)的需求;以測定實(shí)驗(yàn)室制備出的產(chǎn)品碳酸鈉含量引發(fā)師生間、生生間思維的碰撞,梳理出對于混合物進(jìn)行定性、定量分析的思路。
二、教學(xué)目標(biāo)和教學(xué)流程
(1)通過思考、分析碳酸鈉工業(yè)制備的原料、原理問題,進(jìn)一步建立認(rèn)識物質(zhì)、分析轉(zhuǎn)化的學(xué)科視角。
(2)通過實(shí)驗(yàn)探究碳酸鈉和碳酸氫鈉的性質(zhì)差異,進(jìn)而思維有序地從定性、定量的角度分析混合物,促進(jìn)科學(xué)探究與創(chuàng)新意識的化學(xué)學(xué)科核心素養(yǎng)的發(fā)展。
(3)通過對純堿工業(yè)的發(fā)展史和侯德榜個(gè)人事跡的介紹,感悟“實(shí)干興邦”的重要意義,落實(shí)科學(xué)態(tài)度和社會責(zé)任的化學(xué)學(xué)科核心素養(yǎng)。
本節(jié)課的情境線、問題線、學(xué)生認(rèn)識發(fā)展線設(shè)置如圖1所示。
三、教學(xué)過程
1.探秘侯氏制堿法
【展示】碳酸鈉和碳酸氫鈉的主要用途。
【提問】哪些物質(zhì)之間的反應(yīng)可以生成Na2CO3?
【回答】Na2O、Na2O2、NaOH都可以與CO2反應(yīng)生成 Na2CO3。
【思路外顯總結(jié)】(見圖2)
【追問】依據(jù)哪些因素思考圖2所示反應(yīng)是否能夠應(yīng)用于工業(yè)生產(chǎn)中?
【思考】從原料來源、成本、生產(chǎn)工藝、安全性等選擇NaOH與CO2反應(yīng)制備Na2CO3。
【展示】NaOH、Na2CO3成本價(jià)格。
【師】需要找到更加廉價(jià)易得的Na源。
【生】NaCl。
【提問】NaCl + NH3+ CO2+ H2O = NaHCO3↓+ NH4Cl此反應(yīng)能發(fā)生的原因是什么?
NaHCO3→ Na2CO3轉(zhuǎn)化可以實(shí)現(xiàn)嗎?
【思考回答】反應(yīng)能發(fā)生的原因是NaHCO3溶解度小,NaHCO3受熱質(zhì)量減少,預(yù)測NaHCO3受熱能分解,產(chǎn)物可以用澄清石灰水鑒別。
設(shè)計(jì)意圖:從物質(zhì)所含核心元素的角度尋找實(shí)現(xiàn)制備碳酸鈉的諸多反應(yīng),進(jìn)而分析Na2CO3工業(yè)制備的原料、原理問題,建立認(rèn)識物質(zhì)、分析轉(zhuǎn)化的學(xué)科視角,提升證據(jù)意識、科學(xué)探究意識。
【師】很好,以上我們分析的反應(yīng)原理就是侯氏制堿法的主要制備原理。
【展示】侯氏制堿法原理。
【師】侯氏制堿法又稱聯(lián)合制堿法,是我國化學(xué)工程專家侯德榜先生于1943年創(chuàng)立的。侯氏制堿法的創(chuàng)舉在于不僅可以獲得產(chǎn)品Na2CO3,還可以獲得產(chǎn)品 NH4Cl。
設(shè)計(jì)意圖:感悟侯氏制堿法的精妙,落實(shí)科學(xué)態(tài)度和社會責(zé)任的化學(xué)學(xué)科核心素養(yǎng)。
2.模擬侯氏制堿法制備Na2CO3
【展示】碳酸鈉實(shí)驗(yàn)室制備過程。(見圖3)
反應(yīng)原理:NH4HCO3+NaCl=NaHCO3↓+NH4Cl 2NaHCO3 Na2CO3+H2O+CO2↑
【提問】產(chǎn)品中碳酸鈉的含量是多少呢?產(chǎn)品可能存在哪些雜質(zhì)?
【回答】產(chǎn)品中可能存在沒有分解完全的 NaHCO3,還可能有NaCl、NH4Cl。
【繼續(xù)思考】依據(jù)資料NH4Cl溶解度大,受熱易分解,產(chǎn)品中可能有NaHCO3和NaCl。
設(shè)計(jì)意圖:從制備原理出發(fā)分析產(chǎn)品中可能存在的雜質(zhì),結(jié)合已有證據(jù)作出合理推斷。
【提問】如何知道產(chǎn)品中是否還存在NaCl 呢?
【回答】可以利用 AgNO3溶液鑒別產(chǎn)品中是否含有NaCl。
【展示說明】產(chǎn)品經(jīng)硝酸酸化后滴加 AgNO3溶液后產(chǎn)生白色沉淀,產(chǎn)品中存在NaCl。
【追問】如何知道產(chǎn)品中是否還存在沒有分解的 NaHCO3呢?
【回答】還可以繼續(xù)受熱分解檢測分解產(chǎn)物。
設(shè)計(jì)意圖:基于已有認(rèn)知、物質(zhì)性質(zhì)提出恰當(dāng)?shù)臋z驗(yàn)方法。
【師】還有沒有其他方法呢?我們再多了解一些 Na2CO3、NaHCO3的性質(zhì)。
【展示】碳酸鈉和碳酸氫鈉溶解性的比較實(shí)驗(yàn)。
【分組實(shí)驗(yàn)】Na2CO3溶液、NaHCO3溶液分別與稀鹽酸、Ba(OH)2溶液的反應(yīng)。
【說明】學(xué)生在分組實(shí)驗(yàn)中發(fā)現(xiàn),起始向Na2CO3溶液滴加稀鹽酸無明顯現(xiàn)象,繼續(xù)滴加產(chǎn)生氣泡,向 NaHCO3溶液滴加稀鹽酸即有氣泡產(chǎn)生;向 Na2CO3溶液、NaHCO3溶液中滴加 Ba(OH)2溶液均有白色沉淀生成。
【實(shí)驗(yàn)原理分析】
Na2CO3+2HCl=2NaCl + H2O + CO2↑
Na2CO3+ Ba(OH)2=BaCO3↓+2NaOH
NaHCO3+ HCl=NaCl + H2O + CO2↑
NaHCO3+ Ba(OH)2=BaCO3↓+ NaOH + H2O
設(shè)計(jì)意圖:通過教師演示、學(xué)生預(yù)測、分組實(shí)驗(yàn)進(jìn)一步認(rèn)識碳酸鈉、碳酸氫鈉的化學(xué)性質(zhì),發(fā)展科學(xué)探究核心素養(yǎng)。
3.產(chǎn)品成分鑒定
【師】現(xiàn)在我們對于Na2CO3和NaHCO3又多了一些認(rèn)識。
【提問】如果產(chǎn)品質(zhì)量是m克,如何知道其中是否還存在沒有分解的NaHCO3呢?
【分組思考】
【思考、分析】如果能知道產(chǎn)品中鹽酸反應(yīng)產(chǎn)生 CO2的量是不是可以確定出是否含有NaHCO3呢?
【回答】應(yīng)該可以。如果產(chǎn)品中含 NaHCO3,與鹽酸反應(yīng)釋放出 CO2氣體的質(zhì)量應(yīng)該與純凈的 Na2CO3不相等。
【追問】但是產(chǎn)品中有NaCl,NaCl 的質(zhì)量可以知道嗎?
【回答】雜質(zhì) NaCl 的質(zhì)量可以通過產(chǎn)品與AgNO3溶液沉淀獲得AgCl 的質(zhì)量確定下來。
【追問】還有其他方法嗎?
【回答】利用與Ba(OH)2溶液反應(yīng)獲得沉淀BaCO3的質(zhì)量也可以確定。
【師】我們想知道產(chǎn)品中是否還存在沒有分解的 NaHCO3,剛才大家的想法實(shí)際上一直在進(jìn)行比較,是與什么進(jìn)行對照的呢?
【回答】與純凈的Na2CO3進(jìn)行比較。
【師】物理性質(zhì)可以幫助我們確定產(chǎn)品中是否還存在沒有分解的NaHCO3嗎?
【回答】如果產(chǎn)品中雜質(zhì)少利用顏色、狀態(tài)、溶解性不易判斷。
設(shè)計(jì)意圖:基于碳酸鈉和碳酸氫鈉的物理性質(zhì)、化學(xué)性質(zhì)提出完成對混合物進(jìn)行定性說明NaHCO3存在、定量確定 Na2CO3含量的可行性,并在分析過程中完善認(rèn)識思路。
【思路外顯和總結(jié)】(見圖4)
【師】通過上面的分析我們可以感受到以上的鑒別方法在實(shí)際操作中也都存在操作復(fù)雜的問題,且雜質(zhì)如果含量不高不易獲得準(zhǔn)確結(jié)果,那么還有其他方法嗎?
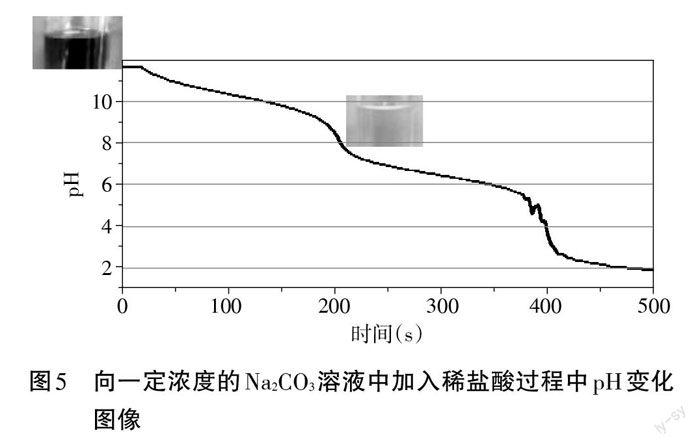
【展示】向一定濃度的 Na2CO3溶液中加入稀鹽酸過程中pH變化圖像(見圖5)。
【提問】依據(jù) pH 的圖形走勢,Na2CO3溶液與稀鹽酸是怎樣進(jìn)行反應(yīng)的?
【傾聽、思考、分析】Na2CO3溶液與稀鹽酸反應(yīng)是分段進(jìn)行的。
【展示】向產(chǎn)品溶液中加入稀鹽酸 pH 變化圖像(見圖6)。
【提問】依據(jù)pH的圖形走勢,若產(chǎn)品中含有NaHCO3則在滴入稀鹽酸發(fā)生反應(yīng)的兩個(gè)階段耗用鹽酸的體積大小關(guān)系是什么?
【分析、回答】若產(chǎn)品中不含有NaHCO3則分段所用稀鹽酸體積應(yīng)是一樣大的,若含有NaHCO3,第二階段用的稀鹽酸會更多。
設(shè)計(jì)意圖:以向一定濃度的Na2CO3溶液中加入稀鹽酸后pH 變化的圖像為證據(jù),分析Na2CO3溶液與稀鹽酸反應(yīng)的過程,進(jìn)而分析滴定法應(yīng)用于Na2CO3含量測定的可操作性。
【師】我們也有一些現(xiàn)代儀器分析方法可以幫助我們確定產(chǎn)品中是否含有NaHCO3。
【展示】利用紅外光譜儀、X-射線衍射儀測定產(chǎn)品中是否含有NaHCO3的方法。
【說明】NaHCO3結(jié)構(gòu)中獨(dú)有的氧氫結(jié)構(gòu)會在紅外光的入射下特定的位置產(chǎn)生吸收峰,據(jù)此可知是否含有NaHCO3(見圖7);每一種晶體物質(zhì)都具有特定的晶體結(jié)構(gòu),用X射線照射試樣,試樣中的物質(zhì)受激發(fā)后會在特定的位置出現(xiàn)吸收峰,通過樣品和純品的比對,就可以知道其中是否含有NaHCO3(見圖8)。
【提問】依據(jù)今天所學(xué)找出能夠?qū)崿F(xiàn) Na2CO3、 NaHCO3轉(zhuǎn)化的方法。
【回答】向 Na2CO3溶液中加入少量鹽酸可以生成 NaHCO3。NaHCO3固體受熱分解得到Na2CO3。NaHCO3與NaOH溶液反應(yīng)可以生成Na2CO3。
【師】還有其他方法嗎?
【展示】向飽和Na2CO3溶液中通入CO2。(見圖9)
【生】向飽和 Na2CO3溶液中通入 CO2也會生成 NaHCO3。NaHCO3溶解度小會在溶液中以固體形式析出。
設(shè)計(jì)意圖:從組成、性質(zhì)認(rèn)識 Na2CO3、NaHCO3相互轉(zhuǎn)化的方法,正鹽與酸式鹽相互轉(zhuǎn)化的一般規(guī)律。
四、教學(xué)效果及反思
碳酸鈉和碳酸氫鈉的學(xué)習(xí)基于教材內(nèi)容,在真實(shí)情境中設(shè)計(jì)符合學(xué)生認(rèn)知發(fā)展規(guī)律的遞進(jìn)問題,開展了有效的基于問題的驅(qū)動思考、深度探究,促進(jìn)了學(xué)科深度學(xué)習(xí)與學(xué)生思維發(fā)展。整節(jié)課思路清晰,具備以下特點(diǎn):
1.重視情境創(chuàng)設(shè),體現(xiàn)學(xué)科價(jià)值
“碳酸鈉和碳酸氫鈉”是繼“氧化鈉和過氧化鈉”之后學(xué)生需要掌握的另外兩種重要的鈉的化合物。本次學(xué)習(xí)以哪些物質(zhì)之間的反應(yīng)可以生成 Na2CO3引發(fā)思考,從元素找尋物質(zhì),多角度分析實(shí)際工業(yè)生產(chǎn)的需求;以測定實(shí)驗(yàn)室制備出的產(chǎn)品Na2CO3含量引發(fā)師生間、生生間思維的碰撞,梳理出對于混合物進(jìn)行定性、定量分析的思路。學(xué)生在教師創(chuàng)設(shè)的具有探究性、啟發(fā)性、生動性的情境中激發(fā)學(xué)習(xí)興趣,步步深入探究,凸顯了核心知識的應(yīng)用價(jià)值。
2.關(guān)注問題解決,構(gòu)建認(rèn)識思路
本次學(xué)習(xí)從物質(zhì)所含核心元素的角度尋找實(shí)現(xiàn)制備Na2CO3的諸多反應(yīng),進(jìn)而分析Na2CO3工業(yè)制備的原料、原理問題,建立認(rèn)識物質(zhì)、分析轉(zhuǎn)化的學(xué)科視角;基于Na2CO3和NaHCO3的物理性質(zhì)、化學(xué)性質(zhì)提出完成對混合物中NaHCO3是否存在的證明。學(xué)生的認(rèn)識思路在尋找性質(zhì)差異、對比純凈 Na2CO3、思索證據(jù)是否充分中逐步完善形成,在進(jìn)一步認(rèn)識 Na2CO3和 NaHCO3的相關(guān)性質(zhì)基礎(chǔ)上,建立了科學(xué)探究的思維模式。
3.致敬侯氏制堿,培植社會責(zé)任
本次學(xué)習(xí)的情境取自在實(shí)驗(yàn)室模擬侯氏制堿法制備Na2CO3。在教學(xué)過程中適時(shí)將侯氏制堿法、侯德榜先生的事跡介紹給學(xué)生,學(xué)生在課堂學(xué)習(xí)中感受中國化學(xué)化工專家為國家發(fā)展所作出的貢獻(xiàn),深悟自己身上承擔(dān)的社會責(zé)任,讓學(xué)科德育落地生根。
參考文獻(xiàn)
[1]胡久華,羅濱,陳穎.深度學(xué)習(xí):走向核心素養(yǎng)[M].北京:教育科學(xué)出版社,2019,2-3.
[2]中華人民共和國教育部.普通高中化學(xué)課程標(biāo)準(zhǔn)(2017年版2020年修訂)[S].北京:人民教育出版社,2020:33-35.
[3]商建波,楊玉琴.基于真實(shí)情境的深度學(xué)習(xí)——以人教版九年級化學(xué)“溶液的形成”為例[J].化學(xué)教學(xué),2020(12):35-40.

