源于Bacillus megaterium STB10的直鏈麥芽五糖生成酶酶學性質及其產(chǎn)物合成規(guī)律
韓 煦,班宵逢,李才明,顧正彪,李兆豐
(江南大學食品學院,江蘇 無錫 214122)
直鏈麥芽低聚糖(maltooligosaccharide,MOS)是由3~10 個葡萄糖(G1)單元通過-1,4-糖苷鍵連接而成的鏈狀低聚糖。其中,直鏈麥芽五糖(G5)由于其具有良好的加工適應性、較好的溶解度、適宜的甜度、較強的抗結晶性能及抑制淀粉回生能力等特性受到食品領域研究者的廣泛關注。此外,G5在醫(yī)療健康領域還具有重要的應用,其可用作為精確測定人體尿液或血清中-淀粉酶活性的診斷試劑,及腎衰竭患者的膳食營養(yǎng)補充劑,在疾病診斷、營養(yǎng)補充等方面發(fā)揮著重要作用。
G5 的酶法生產(chǎn)主要利用直鏈麥芽五糖生成酶(maltopentaose-forming amylase,MFA)作用于淀粉的-1,4-糖苷鍵,生成以G5為主的MOS混合物,并在此基礎上實現(xiàn)G5的分離與純化。目前,MFA在細菌、嗜溫和嗜熱真菌中均有發(fā)現(xiàn),其中,以在芽孢桿菌屬中發(fā)現(xiàn)的MFA為主。例如:Yoshigi等從含有可溶性淀粉的培養(yǎng)基中分離出1 株可以產(chǎn)MFA的蠟狀芽孢桿菌;Hmidet等發(fā)現(xiàn)了來源于A21的MFA。在此基礎上,隨著基因工程技術的發(fā)展,部分研究者嘗試對MFA的基因進行克隆測序,并構建其異源表達系統(tǒng),以期實現(xiàn)MFA的工業(yè)化生產(chǎn)。如:Shida等利用大腸桿菌表達系統(tǒng)對來源于sp.KO8940的MFA進行了克隆表達,該酶水解活力可達到33.8 U/mL。
雖然先前的研究進行了許多嘗試,但目前已被異源表達的MFA大多催化活力較低,還有待進一步提升。此外,這些MFA大多存在產(chǎn)物特異性差的問題,其水解淀粉后產(chǎn)物中G5的比例多集中在20%~40%之間,使得后續(xù)分離純化成本增高,限制了G5的工業(yè)化應用。因此,急需篩選出具有良好產(chǎn)物特異性的MFA以滿足G5的工業(yè)化生產(chǎn)。此外,天然菌株發(fā)酵生產(chǎn)MFA往往存在表達量較低、發(fā)酵周期長及安全性爭議等問題,在食品、醫(yī)藥等領域的應用受到限制。因此,需要在篩選出應用性能優(yōu)良基因的基礎上,實現(xiàn)其在食品級枯草芽孢桿菌的規(guī)模化制備,從而為MFA的工業(yè)化應用奠定基礎。
本研究篩選來源于巨大芽孢桿菌()STB10的()基因,前期研究顯示其可能具有較高的產(chǎn)物特異性,構建該基因的枯草芽孢桿菌表達系統(tǒng),實現(xiàn)MFA的胞外表達,并對其酶學性質及產(chǎn)物合成規(guī)律進行研究,以期為G5的酶法制備提供理論依據(jù)。
1 材料與方法
1.1 材料與試劑
巨大芽孢桿菌STB10、大腸桿菌JM109、枯草芽孢桿菌WB600、枯草芽孢桿菌-大腸桿菌穿梭質粒pST均保藏于本實驗室。
限制性內切酶I、DNA上樣緩沖液、核酸染色劑NA-Red、Tris乙酸鹽乙二胺二乙酸(Tris acetate-ethylene diamine tetraacetic acid,TAE)緩沖液(50×)、瓊脂糖、DNA Ladder、十二烷基硫酸鈉-聚丙烯酰胺凝膠電泳(sodium dodecyl sulfate-polyacrylamide gel electrophoresis,SDS-PAGE)試劑盒、SDS-PAGE蛋白上樣緩沖液、蛋白質分子質量標準、Bradford蛋白濃度測定試劑盒 上海碧云天生物技術研究所;Prime STAR HS DNA聚合酶、聚合酶鏈式反應(polymerase chain reaction,PCR)擴增Buffer 大連TaKaRa公司;質粒小量提取試劑盒、超級感受態(tài)制備試劑盒、硫酸卡那霉素、透析袋 生工生物工程(上海)股份有限公司;酵母粉、胰蛋白胨 英國Oxoid公司;直鏈麥芽三糖(G3)、直鏈麥芽四糖(G4)、直鏈麥芽五糖(G5)、直鏈麥芽六糖(G6)、直鏈麥芽七糖(G7)標準品 日本Hayashibara生物化學研究所;直鏈麥芽八糖(G8)、直鏈麥芽九糖(G9)標準品 法國Elicityl公司;-淀粉酶 無錫杰能科生物工程有限公司;-淀粉酶 大連美侖生物技術有限公司;馬鈴薯直鏈淀粉和支鏈淀粉 上海Sigma-Aldrich公司;其他試劑均為進口或國產(chǎn)分析純。
1.2 儀器與設備
ProFlexPCR系統(tǒng) 美國ABI公司;WD-9413B凝膠成像分析儀 北京市六一儀器廠;RJ-LD-50G低速大容量立式離心機 上海生析超生儀器有限公司;Centrifuge 5424臺式高速離心機 德國Eppendorf公司;Mini Protein 3蛋白電泳系統(tǒng) 美國Bio-Rad公司;AKTA primeplus蛋白質純化系統(tǒng) 美國通用電氣公司;FE28-Standard pH計 瑞士Mettler-Toledo公司;ZQZY-70BS空氣恒溫搖床 上海知楚儀器有限公司;UV2450紫外-可見光分光光度計 日本Shimadzu公司;SW22恒溫水浴搖床、TW12恒溫水浴槽 德國Julabo公司;GI54T高壓滅菌鍋 美國Zealway儀器有限公司;BPH-9042恒溫培養(yǎng)箱 上海一恒科學儀器有限公司;SWCJ-2FD凈化工作臺 蘇州凈化設備有限公司;GenPure UV-TOC/UF Xcad plus型超純水儀、905超低溫冰箱、高效陰離子交換色譜(high performance anion-exchange chromatography with pulsed amperometric detector,HPAEC-PAD)系統(tǒng) 美國Thermo Scientific有限公司。
1.3 方法
1.3.1的克隆、表達及酶純化
以巨大芽孢桿菌STB10基因組DNA為模板,以F和L為引物,PCR擴增出線性基因片段,使用碧云天I試劑盒對PCR產(chǎn)物進行消化。以質粒pST及消化后的線性片段為模板,以F和L為引物,PCR擴增出線性基因片段pST/。將消化后的pST/轉化到大腸桿菌JM109中培養(yǎng)富集,提取質粒測序驗證。將測序正確的質粒pST/轉化感受態(tài)枯草芽孢桿菌WB600,即得到能夠表達MFA的基因工程菌枯草芽孢桿菌WB600(pST/)。PCR體系參考Jiang Haimin等的方法。引物設計如下:F:5’-TTCAGCCCTGCCCAGGCCGATACAGTTAAC AATGGAACGCTAATGCA-3’,L:5’-GCCTATCCC TCACGCCTTACCTCTGGACATATATAGAAACTGAT CC-3’;F:5’-TTCAGCCCTGCCCAGGCC-3’,L:5’-GGCCTGGGCAGGGCTGAA-3’。
將活化后的基因工程菌枯草芽孢桿菌WB600(pST/)種子液以2%(/)比例接種到TB發(fā)酵培養(yǎng)基(酵母粉4 g/L,胰蛋白胨12 g/L,甘油5 g/L,KHPO2.32 g/L,KHPO?3HO 16.43 g/L;pH 7.0;含有20 μg/mL硫酸卡那霉素)中,于25 ℃發(fā)酵60 h后收集發(fā)酵液,4 ℃、10 000×離心15 min,收集上清液即得到MFA的粗酶液。采用疏水層析和離子交換層析對粗酶液進行分離純化。疏水層析使用HiTrap Phenyl HP柱,緩沖液A1為10 mmol/L Tris-HCl(pH 7.0),緩沖液B1為含有10%(/)飽和(NH)SO溶液的10 mmol/L Tris-HCl溶液(pH 7.0),粗酶液加入終體積分數(shù)為10%的飽和(NH)SO溶液待純化。在2 mL/min流速下,用5~6 個柱體積的緩沖液B1平衡疏水柱;預處理后的粗酶液上樣流速為2 mL/min;之后先用6~8 個柱體積的緩沖液B1平衡疏水柱,再分別用體積分數(shù)0%~100%的緩沖液A1、超純水、0.5 mmol/L NaOH溶液進行梯度洗脫,流速為1 mL/min。離子交換層析采用強陰離子HiTrap Q-HP柱,緩沖液B2為含有1 mol/L NaCl的10 mmol/L Tris-HCl(pH 7.0),并將經(jīng)疏水柱純化后含有目的蛋白的組分置于4 ℃在緩沖液A1中透析48 h。在2 mL/min流速下,用5~6 個柱體積的緩沖液A1平衡強陰離子柱;預處理后的一步純化酶液上樣流速為2 mL/min;之后先用6~8 個柱體積的緩沖液A1平衡強陰離子柱,再分別用體積分數(shù)0%~100%緩沖液B2、超純水與10 mmol/L NaOH溶液進行洗脫。收集各洗脫組分測定酶活力和SDS-PAGE驗證。
1.3.2MFA催化活力的測定
M FA 催化活力的測定采用3,5-二硝基水楊酸(3,5-dinitrosalicylic acid,DNS)法,參考Xie Xiaofang等方法并適當修改。用NaHPO-NaHPO緩沖液(10 mmol/L,pH 7.0)配制1 g/100 mL可溶性淀粉為底物,反應體系為0.1 mL酶液和0.9 mL底物,反應溫度50 ℃,反應時間15 min。通過葡萄糖標準曲線計算體系中還原糖含量,以每分鐘生成1 μmol還原糖(以葡萄糖計)所需的酶量定義為1 個酶活力單位(U)。
1.3.3MFA最適反應溫度及熱穩(wěn)定性的分析
通過測定不同溫度梯度下MFA的催化活力及不同溫度保溫一定時間下的殘余酶活力,以分析MFA最適反應溫度及熱穩(wěn)定性。
1.3.4MFA最適反應pH值及pH值穩(wěn)定性的分析
使用不同pH值緩沖液(CHO-NaCHO緩沖液(10 mmol/L,pH 3.0~6.0)、NaHPO-NaHPO緩沖液(10 mmol/L,pH 6.0~8.0)、甘氨酸-NaOH緩沖液(10 mmol/L,pH 8.0~12.0))配制1 g/100 mL可溶性淀粉底物,于50 ℃測定MFA水解活力以分析酶的最適反應pH值。使用不同pH值緩沖液稀釋MFA,并將酶液于4 ℃靜置3 h后,于50 ℃測定殘余酶活力以分析MFA的pH值穩(wěn)定性。
1.3.5 金屬離子對MFA活力及熱穩(wěn)定性的影響
參考相關文獻,金屬離子及EDTA濃度為0.5 mmol/L,設置不添加金屬離子保溫的酶液作為對照組。
1.3.6MFA動力學性質
參考相關文獻,根據(jù)Bradford的方法,使用上海碧云天的Bradford蛋白濃度測定試劑盒說明書測定MFA濃度,并以牛血清白蛋白作為標準品繪制標準曲線。底物為NaHPO-NaHPO緩沖液(10 mmol/L,pH 7.0)配制的0.1~10 mg/mL馬鈴薯直/支鏈淀粉溶液,MFA對直/支鏈淀粉的催化活力測定條件及方法如1.3.2節(jié)所述。采用Lineweaver-Burk雙倒數(shù)法計算MFA的米氏常數(shù)()、最大反應速率()、催化常數(shù)()和催化效率(/)等動力學參數(shù)。
1.3.7MFA反應模式分析
參考文獻[34-36]的方法并適當修改,以-淀粉酶和-淀粉酶為對照,使用NaHPO-NaHPO緩沖液(10 mmol/L,pH 7.0)配制0.25 g/100 mL徹底糊化的馬鈴薯直鏈淀粉與支鏈淀粉溶液為底物。將0.2 mL酶液和1.80 mL底物在50 ℃反應不同時間后于沸水浴中加熱30 min以終止反應。待反應體系冷卻至室溫后,取其中1.0 mL反應液稀釋一定倍數(shù),加入1.0 mL DNS溶液,采用1.3.2節(jié)方法計算還原糖含量。另取稀釋適當倍數(shù)的0.3 mL反應液,加入4.0 mL碘液(0.05 g/100 mL KI、0.005 g/100 mL I,pH 7.5),振蕩混合后避光靜置15 min后在660 nm(以直鏈淀粉為底物)和530 nm(以支鏈淀粉為底物)波長處測定吸光度以計算體系碘藍值。比較3 種酶水解淀粉底物時碘藍值隨還原糖含量的變化趨勢。
1.3.8MFA產(chǎn)物特異性分析
樣品制備:將10 U/g(以干基底物計)的MFA粗酶液與2%(/)麥芽糊精(DE4)底物溶液于40 ℃反應24 h后,取1 mL反應液于沸水浴中加熱30 min滅酶,取上清液稀釋一定倍數(shù)后過0.22 μm水系濾膜,用HPAECPAD分析產(chǎn)物含量。
HPAEC-PAD條件:CarboPac PA 200色譜柱,柱溫35 ℃,流動相分別為1 mol/L NaAc、0.25 mol/L NaOH及超純水,流速0.5 mL/min,進樣量10 μL。單糖質量分數(shù)的計算如式(1)所示:

1.3.9MFA產(chǎn)物合成規(guī)律分析
通過探究MFA水解直/支鏈淀粉的產(chǎn)物組成分析底物對產(chǎn)物合成的影響。底物為預先糊化的0.25 g/100 mL馬鈴薯直/支鏈淀粉溶液(pH 7.0),向反應體系中加入20 U/g(以干基底物計)的MFA,于40 ℃反應不同時間后取樣滅酶,制樣方法同1.3.8節(jié),用HPAEC-PAD測定MFA水解產(chǎn)物中單糖組分質量分數(shù)和底物轉化率。底物轉化率計算如式(2)所示:

1.4 數(shù)據(jù)處理與分析
使用Microsoft Office Excel 2019軟件對數(shù)據(jù)進行初步處理,使用Prism graphpad 7.0軟件作圖;使用SPSS 23.0版本中的Student’s檢驗程序和單因素方差分析(ANOVA)對數(shù)據(jù)進行顯著性分析(<0.05)。使用Clustal Omega(http://www.ebi.ac.uk/Tools/msa/clustalo)對序列進行比對,比對結果使用ESPript v3.0(http://espript.ibcp.fr/ESPript/cgi-bin/ESPript.cgi)作圖。
2 結果與分析
2.1 BmMFA的表達、分離和純化
食品級枯草芽孢桿菌無致病性,培養(yǎng)發(fā)酵條件簡單、菌體易于生長繁殖,是MFA分泌表達較為理想的系統(tǒng)。前期實驗中,已將目的基因克隆到大腸桿菌-枯草芽孢桿菌穿梭型質粒(pST質粒)中,并將該質粒轉入到食品級枯草芽孢桿菌WB600中,獲得基因工程菌枯草芽孢桿菌WB600(pST/)。
目前已報道的MFA發(fā)酵水平均不高,例如來源于GRS 313的MFA催化活力僅為98.3 U/mL。將基因工程菌枯草芽孢桿菌WB600(/)接種到TB發(fā)酵培養(yǎng)基中,于25 ℃培養(yǎng)60 h后,離心收集發(fā)酵上清液,測定其催化活力可達到196.57 U/mL,比活力達到588.54 U/mg,發(fā)酵上清液中蛋白含量為76.98 mg,表明MFA在枯草芽孢桿菌中成功進行了分泌表達,且發(fā)酵水平較高。采用疏水柱和強陰離子交換柱對粗酶液進行分離純化,圖1為MFA的SDS-PAGE驗證結果,經(jīng)兩步純化的目的條帶相對分子質量大小與酶的理論分子質量(56 kDa)符合。MFA與其他來源的MFA氨基酸序列比對結果如圖2所示。MFA的氨基酸序列與來源于sp.JAMB-204(JAMB,GenBank:
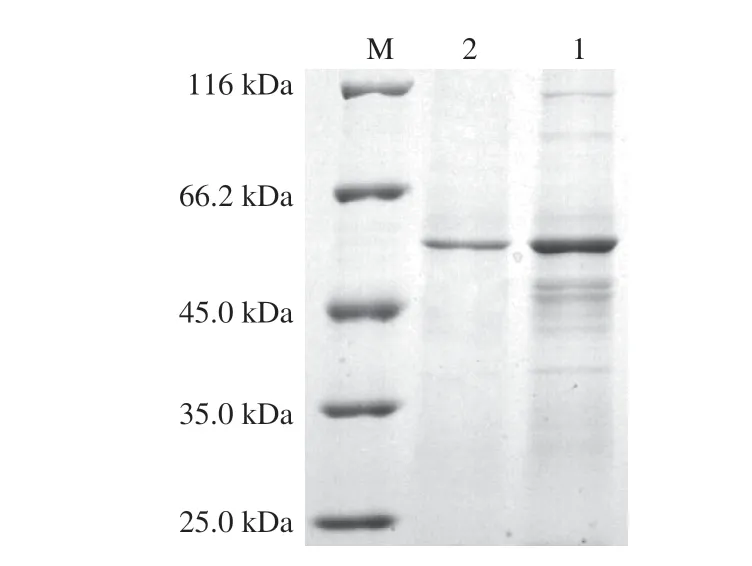
圖1 BmM FA的SDS-PAGE分析Fig.1 SDS-PAGE analysis of BmMFA purified by hydrophobic chromatography or ion chromatography

圖2 BmMFA與其他來源MFA氨基酸序列比對Fig.2 Amino acid sequence alignment of BmMFA with maltopentaose-forming amylases from other sources
BAF03567.1)、(,GenBank:AGK25234.1)、sp.(,GenBank:E24185.1)、sp.KO8940(KO,GenBank:BAA01600.1)及(,GenBank:AIV43244.1)的MFA相比對,氨基酸序列相似性為53.36%,表明其具有MFA的典型特征基因。
2.2 BmMFA的酶學性質分析
2.2.1 最適反應溫度及熱穩(wěn)定性圖3a結果表明,在不同的溫度下,MFA催化活力呈現(xiàn)先上升后下降的趨勢。在50 ℃時,MFA的催化活力達到最大值。酶的催化活力與反應溫度密切相關,溫度對酶的催化特性的影響主要體現(xiàn)在兩方面:一方面可歸屬于熱力學的正效應,當反應溫度逐漸升高時,酶的催化位點逐步暴露,單位時間內酶與底物結合幾率增大,酶的催化效率上升;隨著溫度的進一步提升,酶失活的負效應增強,底物對酶的保護作用不足以抵抗熱變性作用,導致酶發(fā)生解折疊作用,表現(xiàn)為其催化活力的降低。50 ℃為該酶的正負效應達到平衡的溫度,即該酶在50 ℃時具有最高的催化活力。
此外,還對MFA的熱穩(wěn)定性進行了研究,結果見圖3b。隨著溫度的上升,MFA的熱穩(wěn)定性呈現(xiàn)下降的趨勢,在酶的最適溫度50 ℃時,該酶的半衰期約為30 min,與其他來源的MFA相比,其熱穩(wěn)定性還有待進一步提升。因此,在工業(yè)上應用MFA時,反應溫度不宜過高。
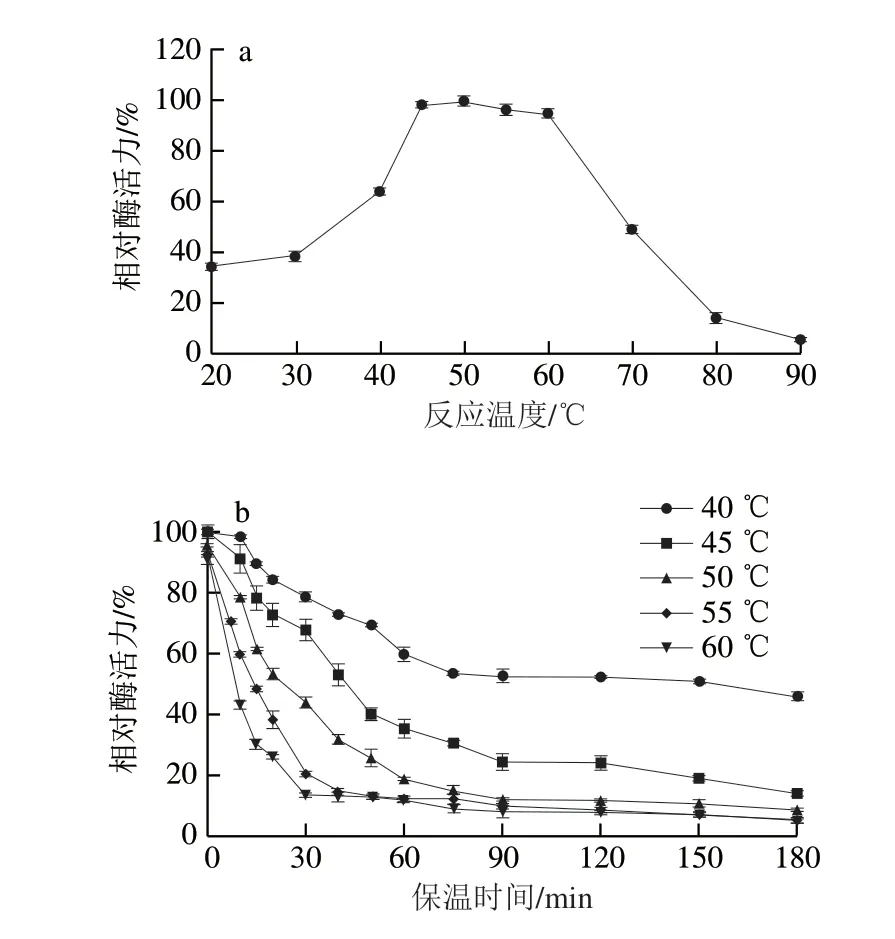
圖3 BmMFA的最適反應溫度(a)及熱穩(wěn)定性(b)Fig.3 Optimal reaction temperature (a) and thermostability (b) of BmMFA
2.2.2 最適反應pH值及pH值穩(wěn)定性
圖4a結果表明,在不同pH值下,MFA的催化活力和穩(wěn)定性呈現(xiàn)先上升后下降的趨勢,MFA的最適反應pH值為7.0。此外,研究還發(fā)現(xiàn),相同pH值下,MFA在甘氨酸-NaOH緩沖液中的催化活力高于NaHPO-NaHPO緩沖液。這可能是由于甘氨酸-NaOH緩沖液中的甘氨酸增強了酶與底物的親和力,并對酶分子構象具有一定的保護作用。
圖4b結果顯示,在pH 6~10下,MFA仍可保持超過80%的催化活力,表明其可適應較寬的pH值范圍,且該酶對堿性環(huán)境的耐受性強于酸性環(huán)境的耐受性。在pH 7.0時,該酶可保持最高程度的穩(wěn)定性,因此在工業(yè)上應用MFA時,適宜在pH值為中性的反應體系環(huán)境中。
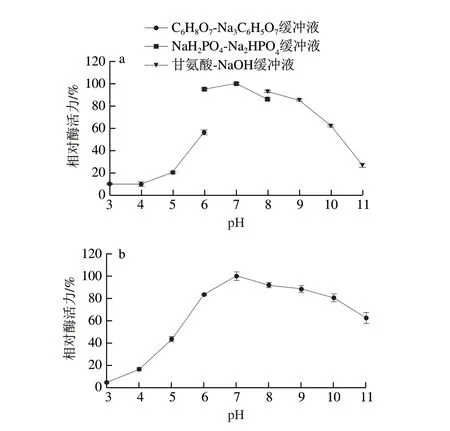
圖4 BmMFA的最適反應pH值(a)及pH值穩(wěn)定性(b)Fig.4 Optimal reaction pH (a) and pH stability (b) of BmMFA
2.2.3 金屬離子對酶活力和熱穩(wěn)定性的影響
如圖5所示,相比較于未添加金屬離子的對照組,F(xiàn)e、Mn、Cu、Zn顯著降低了MFA的催化活力(<0.05),表明MFA對重金屬離子較敏感。添加其他金屬離子時,MFA的催化活力可保持在80%以上,這表明MFA具有相對較強的離子耐受性。不僅如此,少量Ca還具有激活MFA的作用,表現(xiàn)為Ca提升了MFA的催化活力。

圖5 金屬離子或螯合劑對BmMFA活力的影響Fig.5 Effects of metal ions or EDTA on the activity of BmMFA
此外,實驗還研究了Ca、Mg、Na對MFA熱穩(wěn)定性的影響,結果如圖6所示。以未添加金屬離子的酶為空白對照,0.5 mmol/L Ca使MFA在55 ℃的半衰期由13 min提高到15 min,而Mg、Na則降低了MFA的熱穩(wěn)定性。說明在實際生產(chǎn)MOS時,可以適當添加Ca以保證MFA的應用效果。

圖6 金屬離子對BmMFA熱穩(wěn)定性的影響Fig.6 Effects of metal ions on the thermostability of BmMFA
2.2.4MFA的動力學分析
分別以馬鈴薯支鏈淀粉和直鏈淀粉為底物,分析MFA的動力學性質,結果如表1所示。動力學參數(shù)及/分別代表酶對底物的親和力及催化效率。結果顯示,以支鏈淀粉為底物時,MFA的值遠小于以直鏈淀粉為底物,說明MFA對支鏈淀粉的親和力顯著高于直鏈淀粉(<0.05)。此外,以支鏈淀粉為底物時,MFA的/值比以直鏈淀粉為底物時大,表明該酶對支鏈淀粉的催化效率更高。因此,在工業(yè)上應用MFA時,適宜選擇支鏈淀粉含量相對較高的底物。

表1 BmMFA作用于直鏈淀粉/支鏈淀粉的動力學參數(shù)Table 1 Kinetic parameters of BmMFA with amylose/amylopectin as substrate
2.2.5MFA催化反應模式分析
MFA催化模式的分析將有利于深入了解MFA的作用方式,從而為工業(yè)化應用MFA提供指導。淀粉酶根據(jù)反應模式的差異一般被分為內切酶和外切酶兩種。-淀粉酶作為一種典型的內切酶,可以隨機作用于淀粉分子內部的-1,4-糖苷鍵,產(chǎn)生不同聚合度麥芽低聚糖和含有-1,6-糖苷鍵極限糊精的混合物,其碘藍值快速下降。-淀粉酶是典型的外切酶,可以從淀粉的非還原末端開始水解淀粉,相對于被內切酶作用的底物,其多糖鏈的聚合度變化較為緩慢,表現(xiàn)為其碘藍值隨著還原末端數(shù)量的增加而緩慢下降。為確定MFA的反應模式,將-淀粉酶、-淀粉酶和MFA各自水解淀粉過程中的還原糖含量變化(以葡萄糖計)和淀粉鏈聚合度(碘藍值)變化之間的關系用圖7a(支鏈淀粉為底物)和圖7b(直鏈淀粉為底物)表示。結果顯示,MFA水解支/直鏈淀粉的碘藍值-還原糖含量趨勢更接近于-淀粉酶,這表明MFA水解淀粉時體現(xiàn)出內切酶的作用機制。

圖7 α-淀粉酶、β-淀粉酶和BmMFA作用于直/支鏈淀粉的反應模式Fig.7 Action patterns of AA,BA and BmMFA on amylopectin and amylose
內切型淀粉酶傾向于隨機作用多糖鏈分子內部的糖苷鍵,生成不同聚合度的低聚糖混合物,并且隨著反應時間的推移才會體現(xiàn)出特定的主產(chǎn)物優(yōu)勢。因此,使用MFA制備G5產(chǎn)品時,適宜通過延長反應時間以促進產(chǎn)物中G5的累積。
2.3 BmMFA的產(chǎn)物合成規(guī)律
2.3.1MFA的產(chǎn)物特異性
MFA產(chǎn)物特異性是區(qū)別于一般-淀粉酶的關鍵性質,產(chǎn)物特異性的高低直接影響MOS產(chǎn)量以及目標產(chǎn)物的分離成本。通過分析MFA水解麥芽糊精的產(chǎn)物組成情況,對該酶的產(chǎn)物特異性進行分析,結果見表2。麥芽糊精經(jīng)MFA充分作用后,其酶解產(chǎn)物為不同聚合度的MOS混合物,其中,G1~G7為MFA的主要產(chǎn)物;在G1~G7中,G5的占比最高,可達到42.08%,且與其他聚合度的MOS副產(chǎn)物相比,具有顯著差異(<0.05)。MFA水解麥芽糊精24 h后,底物轉化率達到76.61%,G5得率可以達到32.24%,與其他來源MFA相比,MFA具有較高的產(chǎn)G5的能力,表現(xiàn)出相對較強的G5產(chǎn)物特異性,適宜工業(yè)上酶法生產(chǎn)G5。
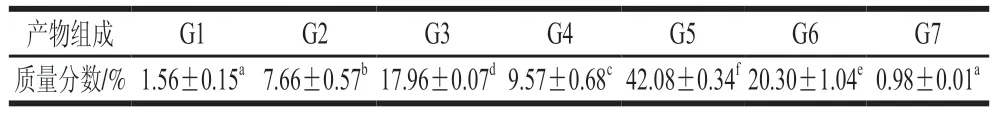
表2 BmMFA水解麥芽糊精產(chǎn)物比例Table 2 Product composition of BmMFA-hydrolyzed maltodextrin
2.3.2 底物結構對產(chǎn)物組成的影響
底物結構對MFA的產(chǎn)物合成具有重要的影響,通過分析酶解不同結構底物的產(chǎn)物組成情況,對實際生產(chǎn)時底物的篩選具有重要意義。MFA對支鏈淀粉的比活力為436.21 U/mg,對直鏈淀粉的比活力為339.83 U/mg。在相同加酶量及反應條件下,用MFA分別水解支/直鏈淀粉,其所得產(chǎn)物所占比例見圖8。兩組底物水解產(chǎn)物中G1~G5含量均隨反應時間的延長逐漸增加。在相同反應時間下,相比于直鏈淀粉,以支鏈淀粉為底物時MFA酶解產(chǎn)物中G5含量更高,以支鏈淀粉為底物時,MFA表現(xiàn)出更好的產(chǎn)物特異性。

圖8 BmMFA水解支鏈淀粉和直鏈淀粉的產(chǎn)物Fig.8 Products of BmMFA-hydrolyzing amylopectin and amylose
2.3.3 底物結構對反應程度的影響
MFA對反應程度及底物水解程度的高低對生產(chǎn)成本具有重要意義,以酶對底物的轉化率為指標,探究底物結構對酶水解反應程度的影響,結果見圖8。反應2 h,MFA對支鏈淀粉的轉化率為24.15%,是以直鏈淀粉為底物時轉化率的2.13 倍。這可能是因為在反應初期,支鏈淀粉的簇狀結構有利于酶與底物的結合。
反應進行到中后期(12~24 h),MFA水解支鏈淀粉的轉化率增速不及以直鏈淀粉為底物,這可能是由于隨著淀粉水解程度的增加,以支鏈淀粉為底物可能產(chǎn)生較多的極限糊精,MFA難以繼續(xù)作用于這些極限糊精,使得底物轉化率增速減慢。但總體而言,MFA以支鏈淀粉為底物時的轉化率高于以直鏈淀粉為底物;反應進行到24 h,以支鏈淀粉為底物時的轉化率比以直鏈淀粉高52.36%。這可能是由于MFA對支鏈淀粉具有更強的親和力。
3 結論
本研究實現(xiàn)了MFA在枯草芽孢桿菌表達系統(tǒng)中的分泌表達,并對其酶學性質和產(chǎn)物合成規(guī)律進行了研究。結果顯示,MFA的最適反應溫度為50 ℃,最適反應pH值為7.0,其具有相對較寬的pH值應用范圍;MFA傾向于內切酶的作用機制,以支鏈淀粉為底物時的親和力及催化效率較高;產(chǎn)物合成規(guī)律研究結果表明MFA具有較好的產(chǎn)物特異性,水解麥芽糊精24 h后產(chǎn)物中G5質量分數(shù)在42%以上,表現(xiàn)出了相對較強的工業(yè)化生產(chǎn)G5的應用潛力;底物為支鏈淀粉時更利于主產(chǎn)物G5的累積及酶對底物的水解程度。MFA酶學性質及產(chǎn)物合成規(guī)律的研究,為酶法制備G5的工業(yè)化應用提供了理論依據(jù)。

