糖皮質激素性骨質疏松癥骨代謝特征分析
藍旭華 張楊 林瀅 薛英 樊長萍 錢林 柯典閃 侯建明*
1.福建省立醫院,福建 福州 350001
2.福建醫科大學省立臨床醫學院,福建 福州 350001
骨質疏松癥(osteoporosis,OP)是一種以骨量減少和骨組織微結構破壞為特征、骨骼脆性增加和易發生骨折的全身性代謝性疾病[1-2]。目前,全球骨質疏松癥患者已超過2億[3],如此悄無聲息的疾病給社會、家庭及個人帶了沉重的負擔。糖皮質激素在臨床上被廣泛應用于各種免疫性、炎癥性、過敏性、血液系統等疾病及腫瘤化療期間,儼然是一把雙刃劍。長期超生理劑量的糖皮質激素一方面抗炎及免疫調節療效顯著[4],另一方面會導致各種不良反應,其中包括糖皮質激素性骨質疏松癥(glucocorticoid-induced osteoporosis,GIOP)[5-6]。長期使用糖皮質激素可誘導成骨細胞調亡、增加破骨細胞活化及減少腸道對鈣的吸收[7-8]。骨代謝生化指標包括骨形成及骨吸收指標,在骨質疏松癥的鑒別診斷、療效判斷及骨折風險預測方面具有重要的臨床意義。本研究選擇其中最有代表性的骨形成指標總I型膠原氨基酸延長肽(tPINP)、骨吸收指標β-膠原特殊系列(β-CTX)和反映骨代謝總體水平的骨鈣素(OG)作為研究指標。甲狀旁腺素(PTH)及活性維生素D是重要的鈣調激素[9-10],在維持體內鈣、磷水平及骨骼微環境穩態方面發揮重要作用。
1 對象與方法
1.1 研究對象
選取2019年6月至2021年6月收住福建省立醫院的88例研究對象,其中48例為GIOP患者,對照組為未服用糖皮質激素且骨密度正常的健康人群。收集所有受試者的臨床資料、血鈣(Ca)、血磷(P)、堿性磷酸酶(ALP)、血肌酐(Cr)、血清白蛋白(ALB)、25羥維生素D [25(OH)D]、甲狀旁腺素(PTH)、β-CTX、tPINP、OG及骨密度等結果。
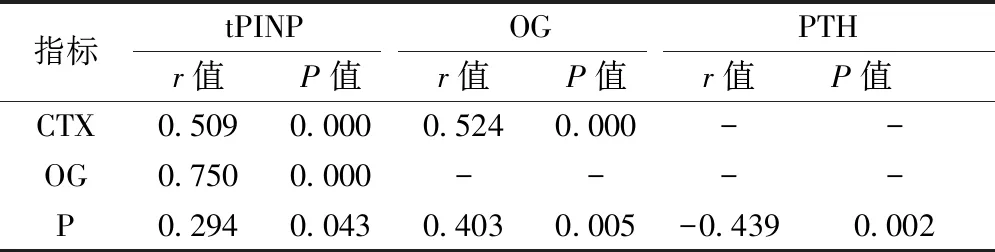
1.1.1納入標準:GIOP組為口服超生理劑量糖皮質激素至少1年的骨質疏松癥患者,按WHO推薦的骨質疏松癥診斷標準[11]:(1)依賴骨密度:骨密度T值≤-2.5為骨質疏松癥,Z值≤-2.0表示骨密度低于同種族同年齡預期(絕經前女性和50歲以內的男性建議采用Z值);(2)髖部或者椎體脆性骨折,不依賴骨密度;骨盆/肱骨近端或前臂遠端脆性骨折伴骨密度顯示低骨量(-2.5 1.1.2排除標準:患胃腸道疾病、神經肌肉疾病、心肺疾病、慢性腎臟病、血液系統疾病及庫欣綜合征、嗜鉻細胞瘤以及甲狀旁腺、甲狀腺、性腺功能減退、下丘腦垂體相關等內分泌疾病;口服抗癲癇藥、芳香化酶抑制劑、促性腺激素釋放激素類似物、抗病毒藥、甲狀腺素和噻唑烷二酮類藥物等。 清晨空腹采血,25(OH)D、PTH、β-CTX、tPINP、OG濃度采用電化學發光檢測,羅氏診斷試劑盒檢測。Ca、P、ALP、Cr、ALB采用全自動生化儀檢測。BMD應用美國Norland XR-36型雙能X線吸收法(DEXA)骨密度儀測量,記錄受試者身高、體重,檢測部位為腰椎2~4(L2~4)BMD及左側髖關節的股骨頸BMD(Neck-BMD)。 正常對照組:男性18例,女性22例,年齡31~74歲,平均年齡55歲,體質量指數(BMI)為(21.51±2.95)kg/m2,血肌酐為(63.95±15.12)mmol/L。GIOP組:男性19例,女性29例,年齡35~85歲,平均年齡58歲,BMI為(20.63±2.86)kg/m2,血肌酐為(66.60±19.10)mmol/L,使用糖皮質激素(氫化可的松、潑尼松、甲潑尼龍、地塞米松)超生理劑量至少1年,伴有滿月臉、向心性肥胖、皮膚菲薄、淤青瘀斑、血壓升高。兩組年齡、BMI和血肌酐差異無統計學意義。 GIOP患者的骨形成指標tPINP和血清ALB水平較正常對照組更低,而ALP、25(OH)D水平比對照組更高,差異均具有統計學意義(P<0.05)。見表1、表2。 表1 兩組生化指標及鈣調激素測定值對比Table 1 Serum biochemical index and calcium-regulating hormone in two groups 表2 兩組骨代謝指標測定值比較Table 2 Comparison of the measured values of bone metabolism indexes between the two GIOP組中,對PTH、25(OH)D、Ca、P與tPINP、OG、CTX進行Pearson相關分析,結果顯示骨代謝指標之間具有顯著正相關性,PTH與P呈負相關,PTH、25(OH)D與骨代謝指標、Ca、ALP無相關性,見表3。 表3 鈣調激素、生化指標與骨代謝指標相關性分析Table 3 Correlation analysis of calcineurin, biochemical indexes and bone metabolism indexes 維生素D屬于類固醇激素,其代謝產物1,25(OH)2D是內分泌激素,調節鈣磷代謝及骨基質礦化。25(OH)D水平的檢測有助于對代謝性骨病等繼發性骨質疏松癥的鑒別診斷。本研究發現與正常對照組相比,雖然GIOP組的25(OH)D水平更高,但兩組均值均小于30 μg/L,為維生素D不足。可見維生素D不足是GIOP患者的臨床特征之一。補充維生素D和鈣劑是治療GIOP的基石。維生素D在肝腎功能正常的情況下代謝為活性維生素D,促進腸鈣吸收,而老年人因為肝腎功能不全,所以推薦補充活性維生素D。鈣調激素PTH是由甲狀旁腺主細胞合成與分泌的,能夠促進骨吸收、重吸收尿鈣、減少尿磷吸收及調節維生素D的活化。本研究未發現GIOP組PTH有意義的變化,兩組的PTH都在正常范圍,因此對PTH的檢測無助于GIOP的鑒別。 骨代謝指標的測定有助于臨床醫生判斷骨代謝的類型、骨丟失速率、病情變化、骨折風險評估、治療方案選擇及療效監測等。有研究發現[12-13]關于GIOP的發病機制,長期應用糖皮質激素患者第一階段即第一年,主要是刺激破骨細胞增加引起骨吸收增強,在第二階段長期應用抑制了成骨細胞增殖分化并促進了骨細胞及成骨細胞的凋亡。本研究的對象為使用糖皮質激素1年以上的GIOP患者,結果證實了上述觀點。相對于正常組,GIOP的骨形成指標tPINP水平是降低的,骨形成是下降的,糖皮質激素可能抑制成骨細胞增殖分化及增加了凋亡[7,14]。骨代謝指標的檢測為GIOP和其他疾病引起的骨質疏松癥鑒別提供了重要依據。在GIOP藥物治療方面,促骨形成藥物特立帕肽是重組人甲狀旁腺素N端1-34片段,小劑量、間歇性使用該藥可以促進骨形成,減少骨折發生風險[11]。對于GIOP患者,早期可以用抑制破骨細胞機制的藥物,后續采用序貫療法,選擇促進骨形成或者抗凋亡機制的藥物,比如特立帕肽,增加骨密度,從而提高療效,減少骨折風險。 通過與正常對照組對比,發現GIOP患者的骨形成標志物tPINP是下降的。因此,筆者進一步尋找與tPINP變化相關的指標。經過Pearson相關分析顯示,本研究發現GIOP組tPINP與β-CTX、OG具有顯著正相關,推測長期應用糖皮質激素同時抑制了骨形成與骨吸收。PTH是甲狀旁腺合成并釋放的一種鈣調激素,可以升高血鈣降低血磷,促進骨代謝。本研究發現PTH與P呈負相關,支持PTH減少尿磷吸收而降低血磷。本研究還發現鈣調激素PTH、25(OH)D與各項骨代謝指標呈非線性相關,可見糖皮質激素對骨代謝平衡的影響遠超于PTH與維生素D的作用。只監測鈣調激素PTH、25(OH)D水平,并維持它們在正常水平,并不能有效提高GIOP患者的成骨細胞活性以及抑制破骨細胞的活性。GIOP患者骨形成和骨吸收間動態平衡的維護需要建立在更多骨參數監測的基礎上。 綜上所述,本研究闡明了GIOP患者存在骨形成標志物降低,支持成骨細胞的形成減少或凋亡增加是其重要的發病機制[2]。上述推論為GIOP的鑒別診斷與藥物治療選擇提供了更多潛在證據,針對應用抑制破骨細胞藥物療效欠佳的患者,可以序貫應用促進成骨細胞的活性或者抗成骨細胞凋亡藥物,進而提高療效以減少骨折風險。1.2 方法
1.3 統計學

2 結果
2.1 一般臨床資料比較
2.2 骨代謝指標、鈣調激素特征分析
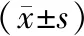
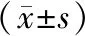
2.3 鈣調激素、Ca、P與骨代謝指標相關性分析
3 討論
3.1 鈣調激素25(OH)D和PTH在GIOP中的變化
3.2 GIOP骨代謝的臨床特征
3.3 GIOP患者生化指標、鈣調激素與骨代謝相關性分析

