蕎麥提取物對鋁在HCl溶液中的緩蝕作用
雷然,石成杰,黎世美,張旭,李向紅
(1.西南林業大學 西南地區林業生物質資源高效利用國家林業和草原局重點實驗室,云南 昆明 650224;2.西南林業大學 化學工程學院,云南 昆明 650224)
鋁由于易加工等性能應用于國民經濟各部門[1]。在pH=4~9之外,鋁易發生腐蝕[2]。鹽酸酸洗可除去腐蝕物,但同時腐蝕鋁基體。緩蝕劑可有效吸附于鋁/溶液界面起到緩蝕作用[3],芳香胺類[4]、氮雜環化合物[5]等被用作鋁的緩蝕劑,但其毒性大、污染環境。植物緩蝕劑因高效環保,為人們關注[6],止血草[7]、竹葉[8]、檳榔種子[9]、核桃青皮[10]、沙冰藜[11]等提取物在酸中對鋁緩蝕性能良好。
蕎麥(FagopyrumesculentumMoench.)在我國種植面積居世界第二[12],其中含有大量黃酮類等化合物[13],分子中的O、N等雜原子可表現出較好緩蝕效果[14]。因此,本文研究蕎麥提取物在HCl介質中對鋁的緩蝕性能及作用機理。
1 實驗部分
1.1 試劑與儀器
鋁片(厚度0.6 mm),含銅0.024%,鐵0.3%,鎂0.002 5%,硅0.15%,鈦0.001%;蕎麥,市售(產地云南省),干燥粉碎備用;無水乙醇、鹽酸、丙酮均為分析純。
SG 250 HPT型超聲波提取儀;SQP型電子天平;HWS-20型恒溫水浴箱;PARSTAT 2273型電化學工作站;Zeiss Sigma 300型掃描電子顯微鏡;SPA-400 SPM unit型原子力顯微鏡;Avatar-FTIR-360型紅外光譜儀。
1.2 FEME提取
稱取一定量粉碎后的蕎麥于500 mL 燒杯中,提取溶劑為60%的乙醇溶液,蕎麥粉末與提取溶劑的料液比為1∶30(質量體積比),進行超聲波提取,60 ℃ 提取20 min,工作頻率59 kHz。提取液經過濾、抽濾后進行減壓濃縮,濃縮至小體積,再進行真空干燥,得到固體蕎麥提取物(FEME)。
1.3 實驗方法
1.3.1 失重法 將鋁切割成25.0 mm×20 mm×0.6 mm的鋁片,進行砂紙逐漸打磨處理,砂紙型號分別為120#、600#和1 500#,打磨好丙酮脫脂后干燥、密封保存備用。
利用玻璃掛鉤將稱量處理好的鋁片試樣懸掛浸沒于50 mL添加和未添加FEME的1.0 mol/L的HCl溶液中,然后置于水浴鍋中,恒溫反應一定時間,取出鋁片,洗滌、烘干、稱重,并計算腐蝕前后的質量損失。失重法緩蝕率(ηw)和腐蝕速率(v)可按照式(1)和式(2)進行計算[15]。
(1)
(2)
式中W0——鋁片在未添加FEME的HCl介質中的質量差,g;
W——鋁片在含有FEME的HCl介質中的質量差,g;
S——1塊鋁片表面積,m2;
t——腐蝕浸泡時間,h。
1.3.2 電化學法 利用電化學工作站進行電化學測試,參比電極為飽和甘汞電極,輔助電極為Pt電極(1.0 cm × 1.0 cm),由聚酰胺樹脂和環氧樹脂以1∶2比例灌封的鋁電極作為工作電極(測試面積為1.0 cm × 1.0 cm),測試前,打磨處理好工作電極并將工作電極浸入1.0 mol/L HCl溶液中2 h進行測試。電化學極化曲線檢測范圍為 -250~250 mV,掃描速率為0.5 mV/s,緩蝕率(ηP)按下式計算[16]:
(3)
其中,icorr(0)和icorr(inh)分別為工作電極在不含和含有FEME的1.0 mol/L HCl介質中的腐蝕電流密度。
電化學阻抗譜圖(EIS)的測試頻率在0.01~105Hz范圍內,其緩蝕率(ηR)根據下式計算[17]。
(4)
1.4 鋁片測試
1.4.1 掃描電子顯微鏡(SEM)和原子力顯微鏡(AFM)測試 在20 ℃下,將鋁片分別恒溫浸泡于不含及含有500 mg/L FEME的1.0 mol/L的HCl溶液中,2 h后取出,洗凈干燥,利用掃描電子顯微鏡和原子力顯微鏡進行表面形貌和狀態測試表征。
1.4.2 紅外光譜測試 將蕎麥粉末(FEM)、FEME和加入FEME于1.0 mol/L的HCl溶液中浸泡鋁片緩蝕后的鋁片表面物質利用KBr壓片法分別進行紅外光譜測試,波數掃描范圍為400~4 000 cm-1。
2 結果與討論
2.1 失重法測試FEME對鋁在1.0 mol/L HCl中的緩蝕性能
圖1a為不同溫度下1.0 mol/L HCl溶液中,緩蝕率(ηw)和FEME濃度的關系曲線圖。圖1b為不同溫度下1.0 mol/L HCl溶液中,腐蝕速率(v)和FEME的濃度關系曲線圖。


圖1 不同溫度下,1.0 mol/L HCl溶液中緩蝕率(ηw)和 腐蝕速率(v)與FEME濃度的變化關系曲線Fig.1 The curves of corrosion inhibition (ηw) and corrosion rate (v) versus FEME concentration in 1.0 mol/L HCl solution at different temperaturesa.ηw-c曲線;b.v-c曲線
由圖1a可知,ηw隨FEME濃度的增加而增大,溫度為30 ℃,FEME的濃度為500 mg/L時,ηw最大,可達86.7%,但隨著溫度進一步升高,ηw降低,說明溫度較高不利于FEME在鋁表面的吸附,相對較低溫度下,腐蝕抑制作用更明顯。
由圖1b可知,未添加FEME的1.0 mol/L HCl溶液中,鋁的腐蝕速率較大,腐蝕嚴重,加入FEME后,不同溫度下鋁片在鹽酸介質中的腐蝕速率都明顯減緩,并且在同一溫度下,腐蝕速率也隨FEME濃度增大而減小,當FEME的濃度為 500 mg/L 時,腐蝕速率降至 7.86(20 ℃),12.9(25 ℃),15.3(30 ℃),36.7(35 ℃),54.54(40 ℃),116.55 g/(m2·h)(45 ℃),說明FEME對鋁在鹽酸介質具有較好的緩蝕效果。
2.2 FEME在鋁表面的吸附等溫式
根據Langmuir吸附等溫式擬合FEME在 1.0 mol/L HCl介質中緩蝕后的失重法實驗數據[18],結果見圖2。
(5)
式中c——緩蝕劑濃度,mg/L;
K——吸附平衡常數,L/mg;
θ——表面覆蓋度,數值與ηw近似。
FEME在鋁表面的標準吸附Gibbs自由能(ΔG0)可根據式(6)進行計算[18]:
(6)
式中 R——氣體常數,8.314 J/(K·mol);
csolvent——溶劑水的濃度(在此處取其近似值1.0×106mg/L);
T——熱力學溫度,K。
ECMO生命支持治療中,血栓形成的因素有:部分血細胞被管道破壞,ECMO管在血管內的存在導致局部血液循環不良以及患者長期臥床,活動能力受限。護理人員需嚴密觀察患者四肢肌力及活動情況,末梢循環情況及意識情況,警惕血栓的形成。可按摩患者四肢,預防血栓形成;一旦發現血栓形成,需立即通知醫生根據病情調整肝素用量。
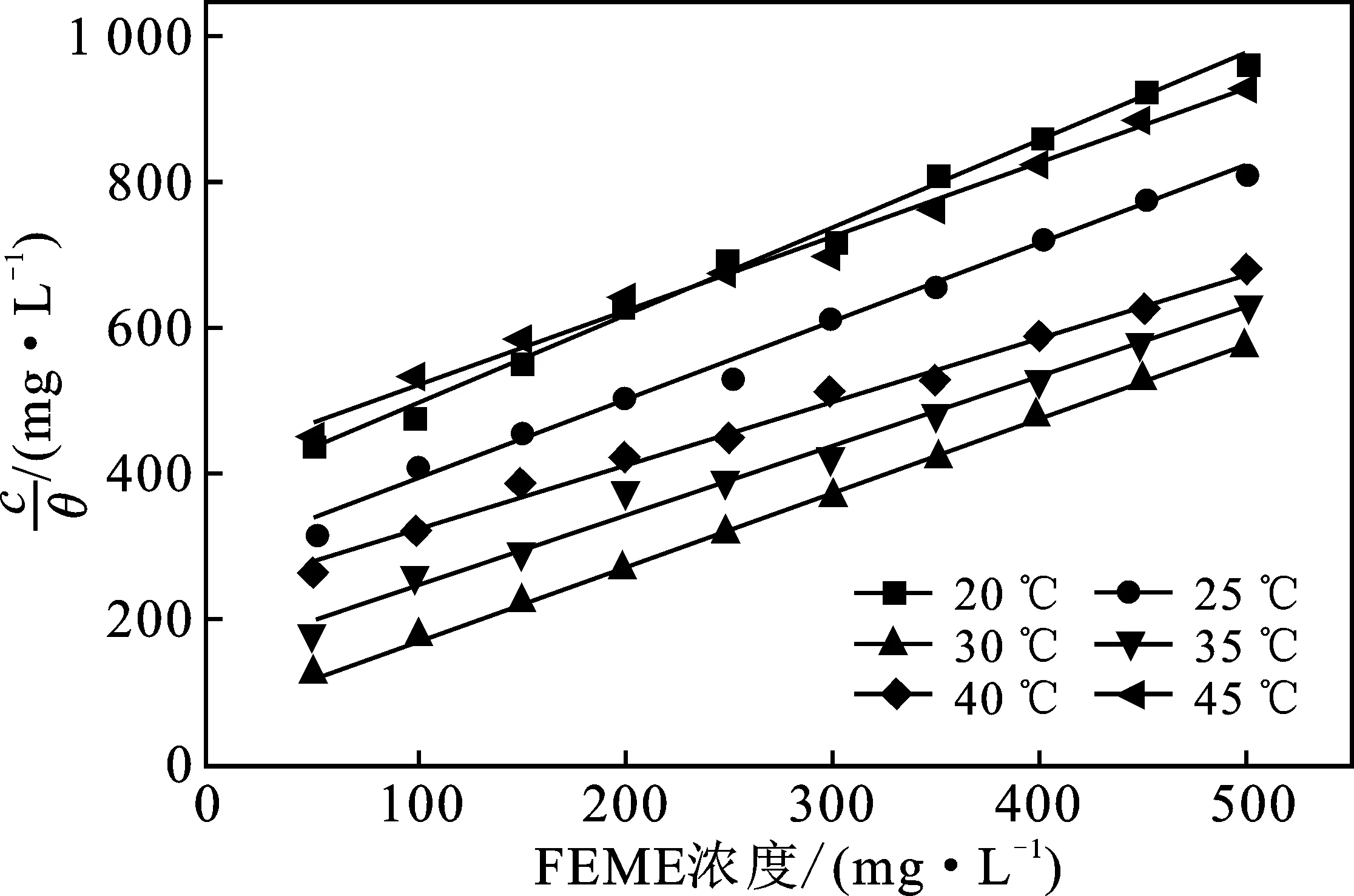
圖2 不同溫度下1.0 mol/L鹽酸溶液中 c/θ-c的擬合直線Fig.2 The fitted straight line of c/θ-c in 1.0 mol/L HCl solution at different temperatures
由圖2可知,c/θ和c在不同溫度下都具有較好的直線關系。由表1可知,線性系數(r2)和直線斜率均接近1,表明FEME在鋁表面的吸附符合Langmuir吸附等溫式。K在30 ℃時達到最大,為14.81×10-3L/mg,說明FEME此時在鋁表面吸附強度最強,緩蝕作用最明顯,但隨溫度升高,K減小,吸附過程為放熱反應,FEME在鋁表面隨溫度升高吸附能力減弱。標準吸附自由能(ΔG0)計算結果為-19~-25 kJ/mol,ΔG0為負值,表明FEME是自發吸附于鋁表面的,絕對值在20~40 kJ/mol范圍內(25,30,35,40,45 ℃),說明FEME由靜電力和化學鍵結合共同作用吸附于鋁表面,吸附行為為物理吸附和化學吸附相結合的吸附類型,溫度為20 ℃時,ΔG0= -19.22 kJ/mol,主要以物理吸附為主[19]。

表1 c/θ-c和標準吸附Gibbs自由能的線性擬合參數Table 1 The linear fitting parameters of c/θ-c and standard adsorption Gibbs free energy
2.3 動電位極化曲線分析
圖3為20 ℃時鋁在含有不同濃度的FEME的1.0 mol/L HCl介質中的動電位極化曲線。

圖3 20 ℃時鋁在含有不同濃度的FEME的 1.0 mol/L HCl介質中的動電位極化曲線Fig.3 Potential polarization curves of aluminum in 1.0 mol/L HCl medium containing different concentrations of FEME at 20 ℃
由圖3可知,陽極極化曲線隨FEME濃度的增加變化不明顯,而陰極極化曲線在加入FEME后,隨著FEME濃度的增加,腐蝕電流密度減小,說明FEME在1.0 mol/L HCl介質中對鋁主要是通過阻礙陰極析氫反應而起到腐蝕抑制作用。通過陰極曲線明顯的Tafel直線區域可說明工作電極的反應由活化極化控制[20],進一步表明FEME吸附在陰極上,從而阻礙了腐蝕反應的進行。
表2為Tafel線性外推法擬合的電化學參數。
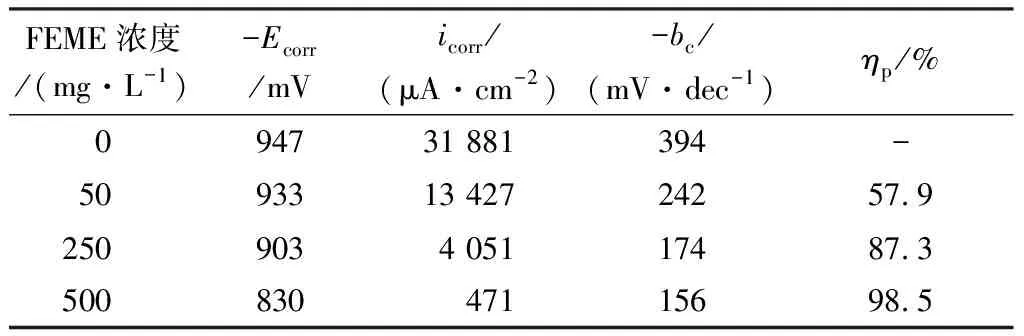
表2 20 ℃時鋁在含有不同濃度的FEME的 1.0 mol/L HCl介質中的動電位極化曲線參數Table 2 Parameters of potentiodynamic polarization curves for aluminum in 1.0 mol/L HCl medium containing different concentrations of FEME at 20 ℃
由表2可知,在添加FEME前后,腐蝕電位(Ecorr)變化不大,說明FEME沒有改變鋁在 1.0 mol/L HCl介質中對鋁的腐蝕反應機理,但腐蝕電流密度(icorr)隨著FEME濃度的增大而顯著下降,當FEME濃度在500 mg/L時,緩蝕率(ηP)可達到98.5%,再次說明FEME在鋁表面進行有效吸附而起到良好的緩蝕作用。
2.4 FEME的電化學阻抗譜(EIS)
圖4a為20 ℃時,鋁在含有不同濃度的FEME的1.0 mol/L HCl介質中的Nyquist圖。
由圖4a可知,高頻區的容抗弧和低頻區的感抗弧組成橢圓圖形,高頻區未出現完整半圓是因為反應過程中鋁電極表面粗糙所致,產生彌散效應[21]。隨著FEME濃度的增加,高頻區容抗弧直徑增大,且形狀不變,說明添加FEME后,鋁在1.0 mol/L HCl介質中腐蝕反應的電阻增大,且隨FEME濃度的增加,電阻越大,從而阻礙腐蝕反應進行,起到緩蝕作用。由圖4b和4c可知,隨著FEME濃度的增加,鋁的阻抗模量增加,相位角值更高,進一步說明加入FEME后達到了緩蝕的效果,且隨著FEME濃度的增大緩蝕作用越明顯。
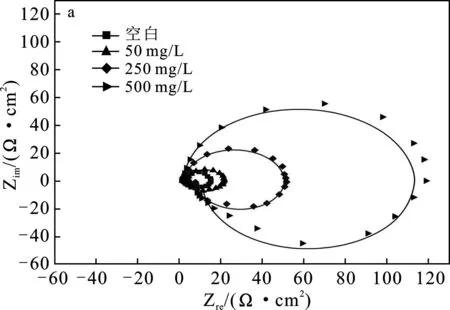
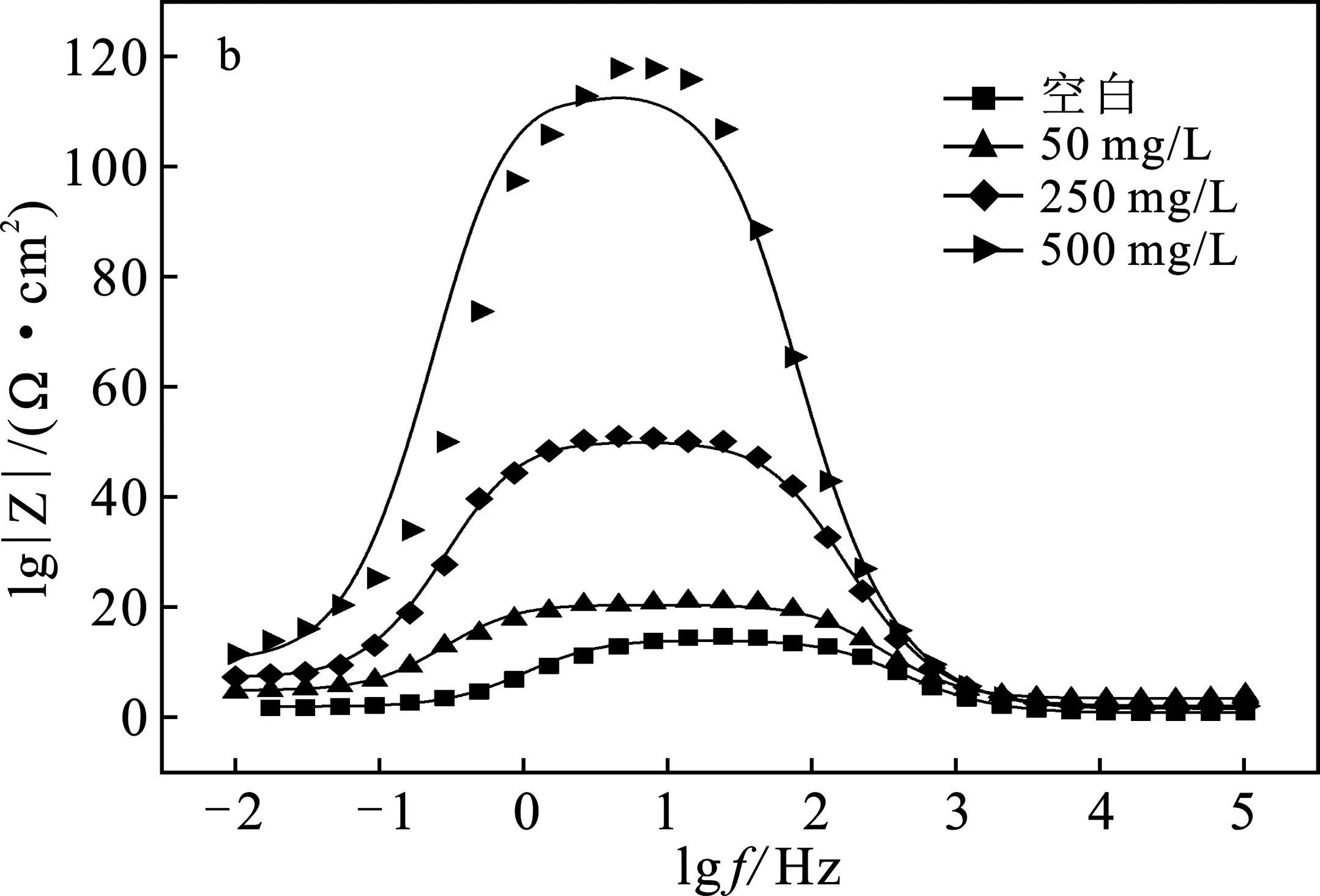

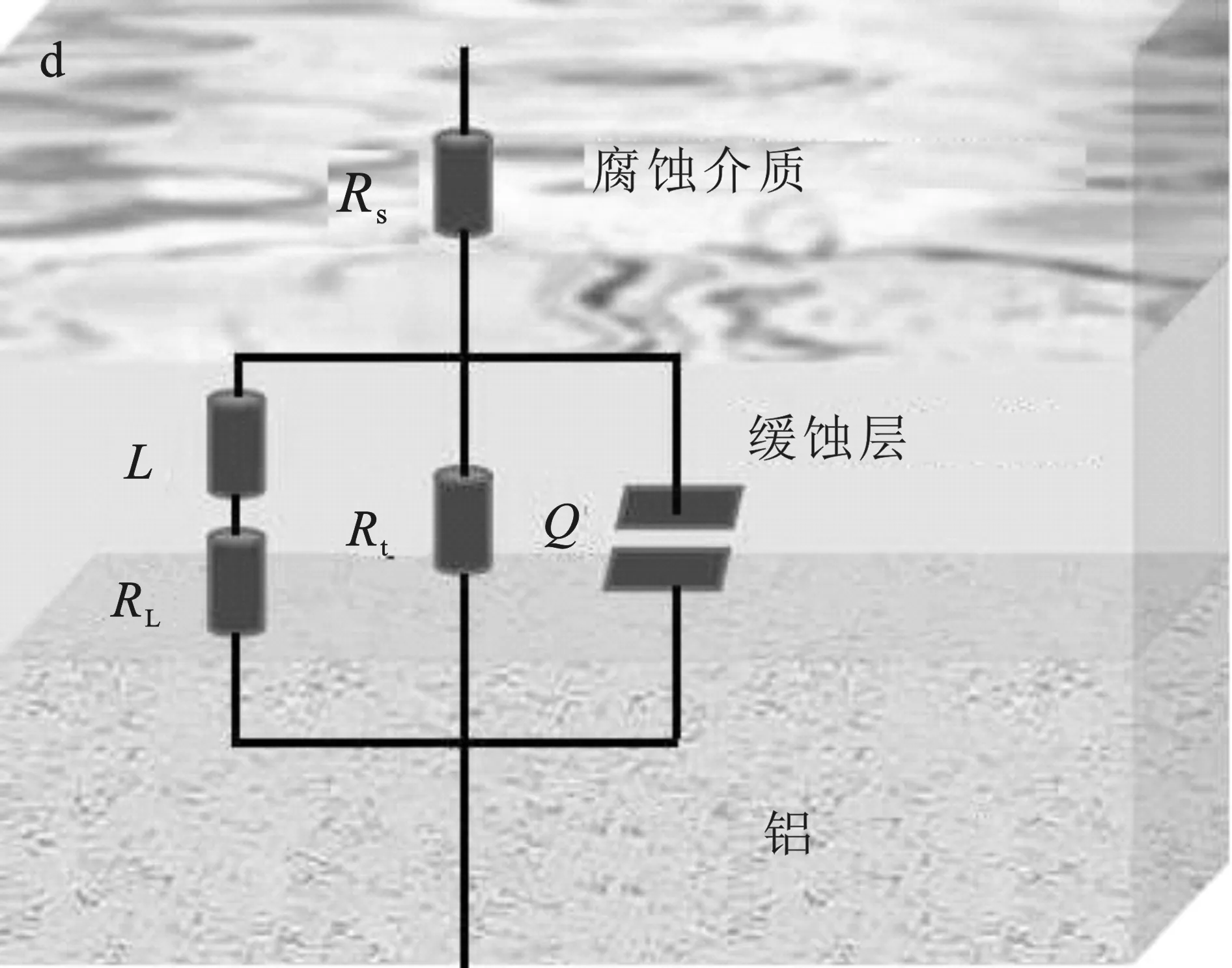
圖4 20 ℃下鋁在不同濃度的FEME的 1.0 mol/L HCl溶液中的阻抗譜圖Fig.4 Impedance spectra of aluminum in 1.0 mol/L HCl solution with different concentrations of FEME at 20 ℃a.Nyquist圖;b.Bode模量;c.Bode相位角圖;d.等效電路圖
采用圖4d所示的等效電路圖對EIS數據進行擬合,其中Q為常相位角元件(包含彌散效應系數a),Rs為測試溶液的電阻,Rt為鋁/酸界面發生腐蝕反應的電荷轉移電阻。
EIS擬合參數見表3,鋁/酸溶液的界面雙電層電容(Cdl)與Q存在如下關系式[22]:
(7)
其中,fmax為Nyquist圖譜上虛軸(Zim)最大值時的最大特征頻率(Hz)。
由表3可知,實驗數據擬合卡方方差(χ2)非常小,說明所選有效電路圖擬合參數的誤差很小,電路圖與阻抗數據擬合相關性較好。彌散系數(a)接近1,說明鋁電極與溶液界面的彌散效應較小,隨著FEME濃度增加,電荷轉移電阻(Rt)增大,說明FEME能夠有效控制了腐蝕過程中的電荷轉移,即FEME濃度增大時,緩蝕率增大,當FEME濃度為500 mg/L時,緩蝕率達到88.2%,此規律與失重法和極化曲線得出的結果一致,說明在1.0 mol/L HCl介質中FEME對鋁的緩蝕作用明顯。與未添加FEME的HCl溶液相比,添加FEME后,Q和Cdl都下降,且隨FEME濃度的增大降幅增大,這可能是緩蝕劑分子取代水分子而吸附在鋁表面。
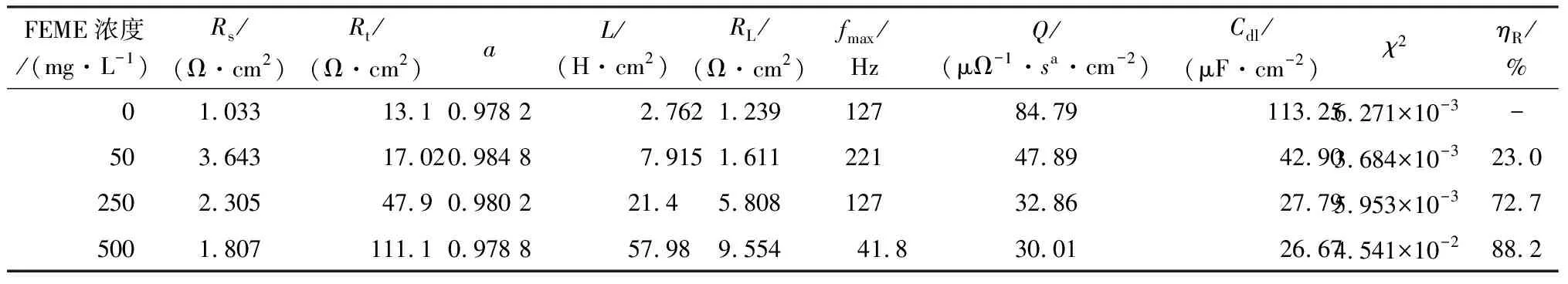
表3 20 ℃時鋁在含有不同濃度FEME的1.0 mol/L HCl溶液中的EIS擬合參數Table 3 EIS fitting parameters for aluminum at 20 ℃ in 1.0 mol/L HCl solution containing different concentrations of FEME
2.5 SEM微觀形貌分析
圖5為10 μm下鋁表面的SEM微觀形貌圖。

圖5 鋁表面浸泡前后的SEM圖片Fig.5 SEM images of aluminum surfaces
圖5a為砂紙打磨處理后的鋁片表面的微觀形貌,可以觀察到打磨痕跡和整體平整的鋁片表面。由圖5b可知,20 ℃時,鋁片在1.0 mol/L HCl溶液中浸泡后表面被嚴重腐蝕,腐蝕產物具有較大疏松孔隙,HCl可通過孔隙進入鋁基體,導致進一步腐蝕。在1.0 mol/L HCl溶液中加入500 mg/L FEME后,鋁表面較為平整(見圖5c),說明加入FEME后,由于緩蝕劑的鋁表面吸附,減緩了HCl對鋁的腐蝕,表明FEME對鋁的腐蝕抑制作用良好。
2.6 AFM表面狀態分析
圖6為鋁表面的AFM表面形貌圖。
由圖6a可知,打磨好未浸泡的鋁片表面起伏度小,砂紙打磨留下的起伏痕跡清晰可見,鋁片表面平整。鋁片在1.0 mol/L HCl溶液中浸泡2 h后(圖6b)表面起伏度非常大,表面變得相當粗糙,腐蝕程度嚴重。當在HCl溶液中加入500 mg/L FEME,浸泡鋁片2 h后,由圖6c可知,鋁片表面起伏度明顯減小,腐蝕程度有所改善,表面產生覆蓋層,整體較為光滑。AFM形貌粗糙度參數見表4,Ra、Rq、P-V分別表示平均表面粗糙度、均方根表面粗糙度和最大起伏度。


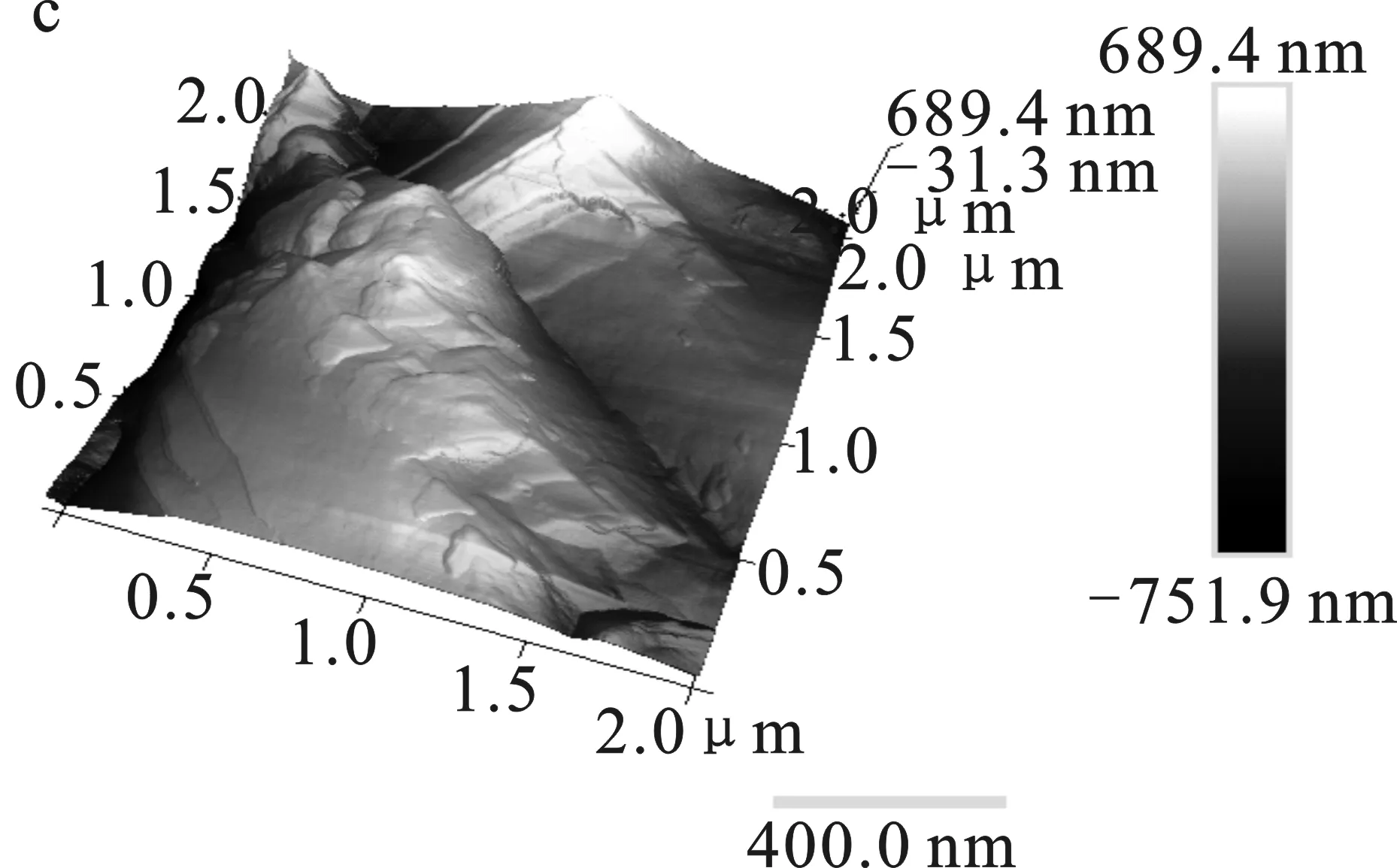
圖6 鋁表面浸泡前后的AFM圖Fig.6 AFM diagram of aluminum surface
由表4可知,鋁在1.0 mol/L HCl溶液中浸泡 2 h 后,Ra、Rq、P-V比浸泡前的數值明顯增大,當加入FEME緩蝕劑后,Ra、Rq、P-V都急劇變小,與AFM微觀形貌圖表觀變化一致,表明FEME的加入抑制了HCl對鋁的腐蝕。
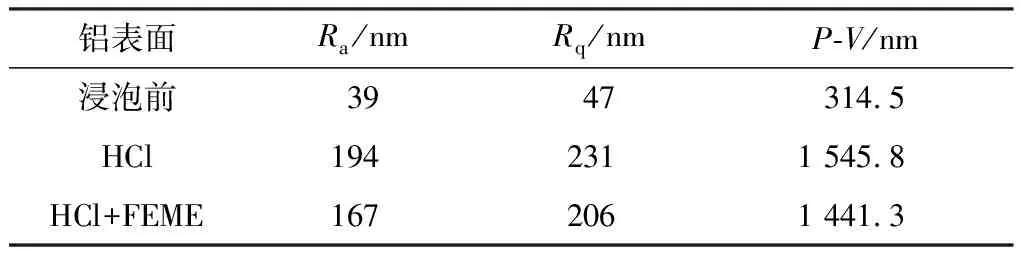
表4 鋁表面AFM微觀結構粗糙度參數Table 4 AFM microstructure roughness parameters of aluminum surface
2.7 紅外光譜表征


圖7 蕎麥、蕎麥提取物和鋁表面吸附層的紅外光譜圖Fig.7 Infrared spectra of FEM,FEME and aluminum surface adsorption layer
2.8 腐蝕及緩蝕作用機理
鋁在HCl溶液中為析氫腐蝕,反應式如下:
2Al+6HCl→2AlCl3+3H2
(8)
腐蝕反應的陽極反應機理如下:
Al+H2O(AlOH)(ads)+H++e-
(9)
(AlOH)(ads)+5H2O+H+
[Al(H2O)6]3++2e-(10)
[Al(H2O)6]3+Al3+·6H2O
Al3++6H2O (11)
Al3++H2O[Al(OH)]2++H+
(12)
陽極腐蝕反應產物[Al(OH)]2+與HCl溶液中的Cl-發生如下反應:
[Al(OH)]2++Cl-[Al(OH)Cl]+
(13)
當Cl-濃度增加時,陽極反應平衡右移,腐蝕速率增大,如反應式(13)所示。
鋁在HCl中的腐蝕的陰極反應機理如下:
Al+H+(AlH+)(ads)
(14)
(AlH+)(ads)+e-(AlH)(ads)
(15)
(AlH)(ads)+H++e-Al+H2
(16)
蕎麥提取物中主要化學成分為黃酮類化合物(見圖8a),黃酮類化合物中含有大量O原子,O原子的孤對電子可與Al的空p軌道發生配位作用而吸附在Al的表面。另外,黃酮類化合物的中央三碳鏈的羰基和相鄰酚羥基可與Al3+形成配合物(圖8b),從而形成腐蝕抑制膜層,進而有效抑制HCl對Al的腐蝕,所以FEME在HCl溶液中對Al起到了良好的緩蝕作用。


圖8 黃酮(a)和Al3+與黃酮形成的配合物(b)的結構式Fig.8 The structural formula flavonoid(a) and complexe formed by Al3+ and flavonoid(b)
3 結論
(1)FEME對鋁在1.0 mol/L HCl溶液中對鋁有明顯的緩蝕作用,緩蝕性能隨著FEME濃度的增大而增大,且最大緩蝕率(ηw)達到了86.7%。FEME在鋁表面的吸附符合Langmuir吸附等溫式,吸附類型主要為物理吸附和化學吸附相結合的混合吸附型,但20 ℃下,ΔG0=-19.22 kJ/mol,主要以物理吸附為主。
(2)FEME為以抑制陰極析氫反應為主的陰極抑制型緩蝕劑,隨著FEME濃度的增大,電荷轉移電阻增大,腐蝕反應阻力增大,腐蝕速率降低,緩蝕性能增強,鋁表面粗糙程度和起伏度明顯減小。超聲波提取法對蕎麥進行充分提取,FEME中主要成分為黃酮類化合物,大量O原子與Al有效結合,從而吸附于鋁表面進而達到緩蝕效果。

