亞低溫聯合高壓氧對一氧化碳中毒遲發性腦病患者認知功能的影響
張明明 張瑛琪 陳 瑩 張 彬 籍文強 張 歲
1.河北醫科大學第一醫院急診科,河北石家莊 050031;2.河北醫科大學第一醫院肝病中心,河北石家莊 050031
急性一氧化碳中毒遲發型腦病(delayed encephalopathyafteracutecarbonmonoxidepoisoning,DEACMP)是急性一氧化碳中毒發生的最嚴重的后遺癥,該病致殘率和病死率高,治療難度大,癥狀主要有認知和神經功能受損、精神錯亂、失認、暫時性空間識別能力下降、錐體外系癥狀等,多數患者以認知功能障礙為首發癥狀,嚴重影響患者的生活質量[1]。近年來,研究報道[2-3],血清神經元特異性烯醇化酶(neuron specific enolase,NSE)、S100β 是中樞神經系統損傷的敏感性和特異性生化標志物。目前,目標溫度管理越來越受到臨床關注,亞低溫治療已成為顱腦損傷的一種有效的腦保護措施[4-6],亞低溫聯合高壓氧在重型顱腦損傷疾病方面取得了較好的臨床療效[7-9]。因此,本研究通過亞低溫聯合高壓氧對DEACMP 血清NSE、S100β及認知功能方面進行探索,旨在為綜合治療DEACMP提供新的理論依據。
1 資料與方法
1.1 一般資料
收集2018 年10 月至2020 年12 月河北醫科大學第一醫院急診科收治的DEACMP 患者70 例,按照隨機數字表法將其分為觀察組和對照組,各35 例。觀察組:男25 例,女10 例;年齡60~78 歲,平均(65.7±5.5)歲。對照組:男23 例,女12 例;年齡61~77 歲,平均(66.1±4.3)歲。兩組性別、年齡比較,差異無統計學意義(P >0.05),具有可比性。本研究獲得醫院倫理委員會批準,且患者家屬均簽署知情同意書。
1.2 納入標準
①符合一氧化碳中毒遲發型腦病診斷標準,有明確急性一氧化碳中毒病史;②有2~60 d 的假愈期;③頭CT 或頭顱核磁共振檢查提示腦白質損害;④以智能障礙、精神癥狀和震顫麻痹為主的典型臨床表現。
1.3 排除標準
①影像學顯示為其他疾病導致的昏迷;②伴有肝、腎等重要臟器器質性病變;③既往存在認知障礙、精神疾病。
1.4 治療方法
兩組均給予營養神經、清除自由基及對癥治療等基礎上,對照組給予高壓氧治療(高壓氧艙,中國,YC-2270),觀察組給予亞低溫(亞低溫治療儀,YZB/奧0136-2009)+高壓氧治療。
1.4.1 高壓氧治療方法 患者入高壓氧艙后升壓20 min,治療壓力0.22 MPa,面罩氧30 min,間歇10 min 后再繼續吸氧30 min,減壓30 min 后出艙。1 次/d,10 d為1 個療程,連續治療9 個療程(3 個月),無脫落患者。
1.4.2 亞低溫治療方案 入院后即讓患者進行亞低溫治療:采用降溫毯全身及冰帽頭部降溫,溫度控制在30~32℃,低溫過程密切監測生命體征,持續5 d,復溫采用自然復溫。
1.5 觀察指標
1.5.1 療效判定 痊愈:臨床癥狀、體征消失,生活基本或完全自理;顯效:臨床癥狀、體征減輕,生活部分自理;無效:癥狀、體征無明顯變化,生活不能自理。總有效率=(痊愈+顯效)例數/總例數×100%[10]。
1.5.2 精神狀態及生活能力評價 兩組治療前及治療后3 個月,采用簡易精神狀態檢查量表(mini-mental state examination,MMSE)及日常生活能力量表(activities of daily living,ADL)評定患者認知功能及日常生活能力。MMSE 判定標準:最高分為30 分,正常為27~30 分,認知功能障礙為<27 分;癡呆嚴重程度分級方法:輕度MMSE 為≥21 分,中度MMSE 為10~20 分,重度為≤9 分。ADL 判定標準:100 分表示正常,≤40 分有ADL 功能重度損害,41~60 分為中度損害,≥61 分為輕度損害。
1.5.3 NSE、S100β 水平 兩組治療前后,抽取患者空腹靜脈血5 ml,采用酶聯免疫吸附法檢測血清NSE、S100β 水平變化(試劑盒均購自深圳市新產業生物工程股份有限公司)。
1.6 統計學方法
采用SPSS 20.0 軟件對所得數據進行統計分析。符合正態分布的計量資料以均數±標準差()表示,采用t 檢驗。計數資料以例數或百分比表示,采用χ2檢驗。以P <0.05 為差異有統計學意義。
2 結果
2.1 兩組臨床效果比較
治療3 個月后,觀察組治療總有效率高于對照組,差異有統計學意義(P <0.05)。見表1。
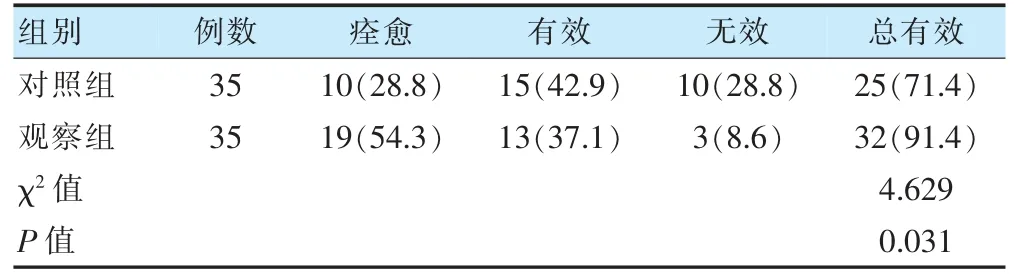
表1 兩組臨床效果比較[例(%)]
2.2 兩組治療前后NSE、S100β 水平比較
兩組治療前NSE、S100β 比較,差異無統計學意義(P >0.05)。兩組治療后NSE、S100β 水平低于治療前,且觀察組低于對照組,差異有統計學意義(P <0.05)。見表2。
表2 兩組治療前后NSE、S-100β 水平比較(μg/L,)
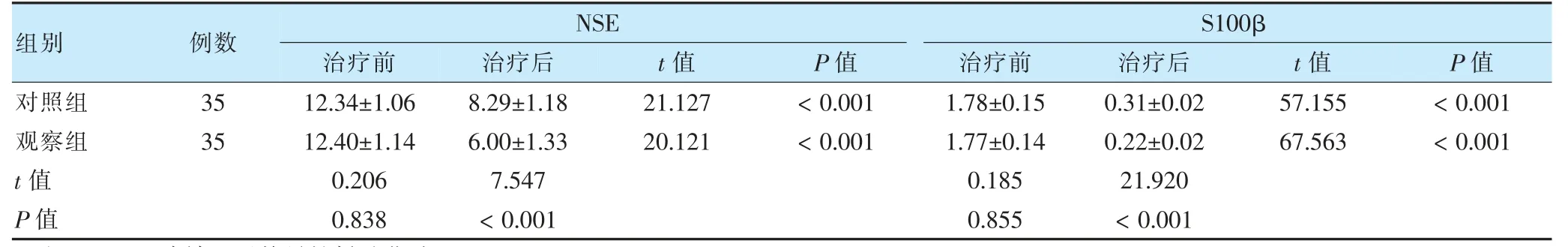
表2 兩組治療前后NSE、S-100β 水平比較(μg/L,)
注 NSE:血清神經元特異性烯醇化酶
2.3 兩組治療前后MMSE、ADL 評分比較
兩組治療前MMSE、ADL 評分比較,差異無統計學意義(P >0.05)。兩組治療后MMSE、ADL 評分高于治療前,且觀察組高于對照組,差異有統計學意義(P <0.05)。見表3。
表3 兩組治療前后MMSE、ADL 評分比較(分,)
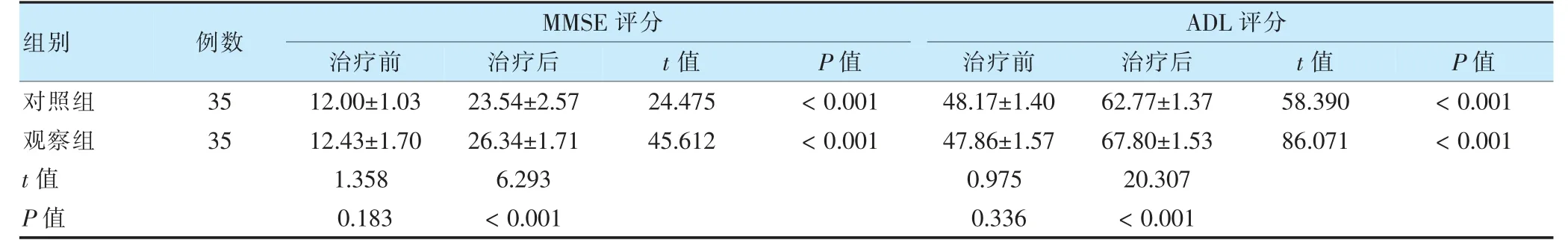
表3 兩組治療前后MMSE、ADL 評分比較(分,)
注 MMSE:簡易精神狀態檢查量表;ADL:日常生活能力量表
3 討論
DEACMP 是急性一氧化碳中毒患者完全康復后,經過一定時間“假愈期”出現的以神經系統和精神癥狀為主要表現的缺氧性腦病,表現為癡呆、譫妄、步態細碎不穩、失語、失讀或再次喪失勞動能力、人格怪異、手足徐動癥等,生活不能自理,給社會和家庭造成巨大負擔。目前DEACMP 治療以高壓氧為主,輔以腦保護及對癥支持治療,療效欠佳,預后差,故尋找其有效治療方法改善DEACMP 預后尤為重要。亞低溫療法安全有效、不良反應輕微,是目前廣泛應用于多個疾病領域的一種腦保護治療策略[11-15]。李亞斌等[7]報道亞低溫聯合早期高壓氧治療重型顱腦損傷不僅可有效降低顱內壓,改善腦組織缺氧狀況,還可以明顯改善患者的預后,兩者聯合療效更為顯著,值得臨床推廣;張志偉等[16]報道亞低溫聯合高壓氧治療重型顱腦損傷患者明顯改善其顱內壓,促進其腦功能與神經功能恢復,提升其生活質量,具有良好遠期療效;黃勁超等[17]報道顱腦損傷患者血清NSE 和S100β 升高,亞低溫治療能降低其含量,改善患者的預后。故本研究應用亞低溫聯合高壓氧對DEACMP 患者NSE、S100β 水平及認知功能方面進行探討,以便為綜合治療DEACMP提供參考依據。
目前,DEACMP 發病機制可能的學說有缺血缺氧、血管因素、血流變異常、自由基、細胞凋亡、細胞自噬、免疫反應、興奮性氨基酸學說等[18],其中缺血缺氧學說是發生DEACMP 的首要原因,中樞系統神經元對缺血缺氧尤為敏感,血清NSE 和S100β 是與腦損傷有關的生化標志物,血清NSE 水平與腦損傷呈正相關,是一種存在于神經元內、神經元分泌細胞中的酸性可溶性蛋白,是臨床評價神經元損傷最靈敏的指標[19];S100β 主要存在于中樞神經系統的星形膠質細胞的胞液中,是由Moore1965 年首次從牛腦中分離出來的一種酸性鈣結合蛋白,對于判定患者腦損傷嚴重程度及預后具有輔助作用[20]。本研究顯示,亞低溫聯合高壓氧聯合治療后的觀察組NSE、S100β 水平低于單一高壓氧對照組,差異有統計學意義(P <0.05),提示亞低溫聯合高壓氧能明顯減輕腦損傷,促進中樞神經系統恢復;觀察組MMSE、ADL 評分高于單一高壓氧對照組,并且觀察組總有效率明顯高于對照組,提示亞低溫療法的介入可提高患者認知功能障礙及日常生活能力,明顯改善患者康復進程和病情預后。
有研究報道[21],NSE、S100β 對評估腦梗死患者認知功能具有重要的臨床意義,NSE、S100β 水平越高,認知功能損害越嚴重,本研究與上述研究結果一致,亞低溫療法介入的觀察組較對照組血清NSE、S100β水平變化小,腦損傷程度輕,從而認知功能損害輕,分析可能的原因:腦部是由神經元和膠質細胞共同組成的信息網絡,膠質細胞過多分泌可影響神經元的反應,繼而損害腦部神經。中樞神經系統對缺氧最為敏感,腦缺氧引起腦神經元功能損傷,血腦屏障通透性隨之增加,NSE 釋放入腦脊液及血中進入血液循環,同時增加膠質細胞的壓力,使其過度分泌S100β 并對神經元產生不良作用,最終導致顱內壓增高、腦內微循環障礙和腦功能衰竭[22-25],而亞低溫療法的應用,減少腦細胞代謝率,改善腦內血液循環,降低顱內壓,減輕腦水腫的程度,促進神經元的生成,改善預后[26-28]。
綜上所述,亞低溫聯合高壓氧治療DEACMP,能有效保護腦細胞損傷,提高患者認知功能及日常生活能力,改善其生活質量,促進患者的恢復,改善預后,值得臨床推廣應用,在以后的工作中需加大樣本量及研究時間,以取得更客觀的研究結果。

