四氫姜黃素對MCF-7細胞增殖、凋亡及轉移的作用
張 敏,華 樺,曾安琪,劉 俐,劉 芳,趙軍寧,
(1.成都中醫藥大學,四川 成都 610075;2.四川省中醫藥科學院轉化藥理與臨床應用研究所,四川省中醫藥轉化醫學中心,四川省道地藥材系統開發工程技術研究中心,四川省道地藥材形成原理與品質評價工程研究中心,中醫藥轉化醫學四川省重點實驗室,國家中醫藥管理局中藥質量生物評價重點研究室,四川 成都 610041;3.四川大學,四川 成都 610041)
乳腺癌是一種發生于乳腺上皮組織的惡性腫瘤,其發病率逐年上升并愈發年輕化[1-4]。乳房并非維持生命的重要器官,但乳腺癌細胞易失去細胞間的黏附能力,極易增殖擴散,短時間內迅速轉移、生長到其他器官如骨髓、淋巴等,最后危及患者生命[5-8]。姜黃素類為中藥姜黃的主要有效成分,目前已有研究證實姜黃素能抑制膀胱癌、乳腺癌、肺癌等腫瘤細胞的生長[9-10]。四氫姜黃素 (tetrahydrocurcumin)為姜黃素在體內的主要代謝產物,具有抗腫瘤作用[11-14],但其作用機制尚不清楚。本研究探索了四氫姜黃素對MCF-7乳腺癌細胞增殖、凋亡、轉移的作用及其機制,為四氫姜黃素后續開發奠定實驗基礎。
1 材料
1.1 細胞 人乳腺癌細胞(MCF-7)由上海中國科學院干細胞庫提供,目錄號TCHu74。
1.2 試劑與藥物 四氫姜黃素由四川省中醫藥科學院藥學研究所提供,批號2018090,純度≥98%。二甲基亞砜(DMSO)(批號EZ6688D182)購自美國Sigma-Aldrich公司;磷酸緩沖鹽溶液(PBS)(批號8119244)購自美國Gibco公司;胎牛血清(批號1909505)購自杭州四季青生物工程材料有限公司;胰酶(批號14J22C67)購自美國HyClone公司;細胞增殖毒性檢測試劑盒(Cell Counting Kit-8,CCK8,批號14I07A60)、HRP-羊抗兔IgG(批號BST14KBL54)、HRP-羊抗小鼠IgG(批號BST14J0A50)均購自武漢博士德生物工程有限公司;結晶紫染色液(批號C0121)購自上海碧云天生物技術有限公司;Annexin V-FITC/PI 細胞凋亡檢測試劑盒(批號20200624)購自江蘇凱基生物技術股份有限公司;β-肌動蛋白(β-Actin)(批號HL0305)購自杭州華安生物技術有限公司;基質金屬蛋白酶9(MMP-9)(批號GR3204084-11)、基質金屬蛋白酶2(MMP-2)(批號GR3244972-1)、B淋巴細胞瘤-2(Bcl-2)(批號GR3219584-4)、BCL-2-Associated X的蛋白質(Bax)(批號GR380247-20)均購自英國Abcam公司。
1.3 儀器 BSC-1304ⅡA2細胞生物安全柜(蘇州安泰空氣技術有限公司);美國311水套式二氧化碳培養箱(美國Thermo公司);1820型酶標儀(賽默飛世爾科技有限公司);ME204/02電子天平[梅特勒-托利多儀器(上海)有限公司];YM100 A滅菌鍋(上海三申醫療器械有限公司);DHG-9070A型電熱恒溫鼓風干燥箱(上海精宏實驗設備有限公司);C2500低溫離心機(湖南湘儀實驗儀器廠);090-135008倒置顯微鏡(德國徠卡公司)。
2 方法
2.1 四氫姜黃素對MCF-7細胞增殖的影響
2.1.1 CCK8實驗 將對數生長期的MCF-7細胞用完全培養液配成細胞懸液,以每孔8 000、6 000、4 000個細胞接種于3塊96孔板中,放置于5% CO2、37 ℃培養箱中培養24 h,待細胞貼壁至80%~90%時,加入不同濃度(0、0.78、1.56、3.12、6.25、12.5、25、50、100、200 μmol/L)四氫姜黃素藥液進行干預,每孔100 μL。分別培養24、48、72 h,棄去舊培養基,每孔加入新鮮培養基100 μL后,再避光加入10 μL CCK8溶液,37 ℃ 孵育1 h,酶標儀檢測450 nm波長處吸光度(A)值。根據公式計算細胞增殖抑制率,Graphpad計算半數抑制濃度(IC50)。細胞增殖存活率=[(A實驗-A空白)/(A對照-A空白)]×100%。
2.1.2 克隆形成實驗 取對數生長期細胞,完全培養基重懸后計數,細胞以500/mL密度分別加入6孔板中,放置于5% CO2、37 ℃培養箱培養24 h后,加入濃度為0、6.25、12.5、25、50、100 μmol/L四氫姜黃素藥液,每3天換1次藥液至第10天。實驗結束時棄去舊培養基,加入1 mL甲醇固定15 min后棄去甲醇,再加入2 mL結晶紫避光固定30 min,結晶紫回收后PBS清洗孔板2次后晾干拍照。
2.2 四氫姜黃素對MCF-7細胞凋亡的影響
2.2.1 MCF-7細胞形態變化 取對數生長期細胞計數后,按1×105/mL密度接種于6孔板,放置于5% CO2、37 ℃培養箱培養24 h后,棄去培養基,加入濃度為0、25、50、100 μmol/L四氫姜黃素藥液,分別于0、48 h在200倍顯微鏡下觀察細胞形態并拍照。
2.2.2 流式細胞術檢測MCF-7細胞凋亡情況 用不含EDTA胰酶消化收集細胞,PBS洗滌細胞2次,500 μL預冷Binding Buffer懸浮細胞,加入5 μL Annexin V-FITC混勻后,再加入5 μL Propidium lodide混勻,室溫避光反應15 min,檢測細胞凋亡情況。
2.3 四氫姜黃素對MCF-7細胞轉移的影響
2.3.1 劃痕實驗 取對數生長期細胞,將細胞懸液密度調為5×105/mL后接種于6孔板,放置于5% CO2、37 ℃培養箱培養24 h后進行劃痕;將0、25、50、100 μmol/L四氫姜黃素藥液(含2%血清的培養基配制)依次加入孔板中,每孔2 mL,放入放置于5% CO2、37 ℃培養箱孵育48 h后棄去舊液,用PBS清洗2次,再加入600 μL PBS,40倍顯微鏡下觀察拍照。Image J 軟件分析細胞遷移距離。
2.3.2 Transwell實驗 在對數生長期細胞中加入無血清培養基計數后調整密度為4×104/μL;用無血清培養基分別配置0、25、50、100 μmol/L四氫姜黃素藥液,每孔加入50 μL藥液和50 μL細胞懸液;將5個Transwell小室放入6孔板中,小室下加入600 μL含血清培養基,小室中加入50 μL無血清藥液和50 μL無血清細胞培養基,放置于5% CO2、37 ℃培養箱孵育48 h后,棄小室下方培養基,用棉簽輕輕旋轉擦拭小室,1 mL甲醇固定后,每孔加入1 mL結晶紫染液染色,用PBS清洗3次后用棉簽輕輕旋轉擦拭小室中液體,于通風櫥中晾干,將小室底部圓片取出放在滴有中性樹膠(滴載玻片中心)的載玻片上,蓋上蓋玻片,于100倍顯微鏡下拍照。
2.4 蛋白質印跡(Western blot)實驗 將細胞接種于培養皿中,待貼壁后加入相應濃度的四氫姜黃素藥液(0、25、50、100 μmol/L),48 h后用刮刀將各組細胞收集于離心管中,加入RIPA細胞裂解液,冰浴30 min后,加入等量4×SDS Loading buffer,進行凝膠電泳后,置于轉膜儀轉膜后,加封閉液封閉1 h,用一抗(Bcl-2、Bax、MMP2、MMP9)孵育(4 ℃)過夜,放置于搖床用TBST清洗4次,15 min更換1次TBST,二抗孵育(37 ℃)1 h,發光液曝光10 min,顯影,進行Bcl-2、Bax、MMP-2、MMP-9蛋白表達分析。

3 結果
3.1 四氫姜黃素對MCF-7細胞增殖的影響
3.1.1 CCK8實驗 如圖1所示,實驗各時間點四氫姜黃素 6.25、12.5、25、50、100、200 μmol/L劑量組細胞存活率,與空白對照組(0 μmol/L)比較均降低(P<0.05,P<0.01)。根據其IC50值提示后續試驗藥物作用濃度為0、6.25、12.5、25、50、100 μmol/L,實驗時間為48 h。
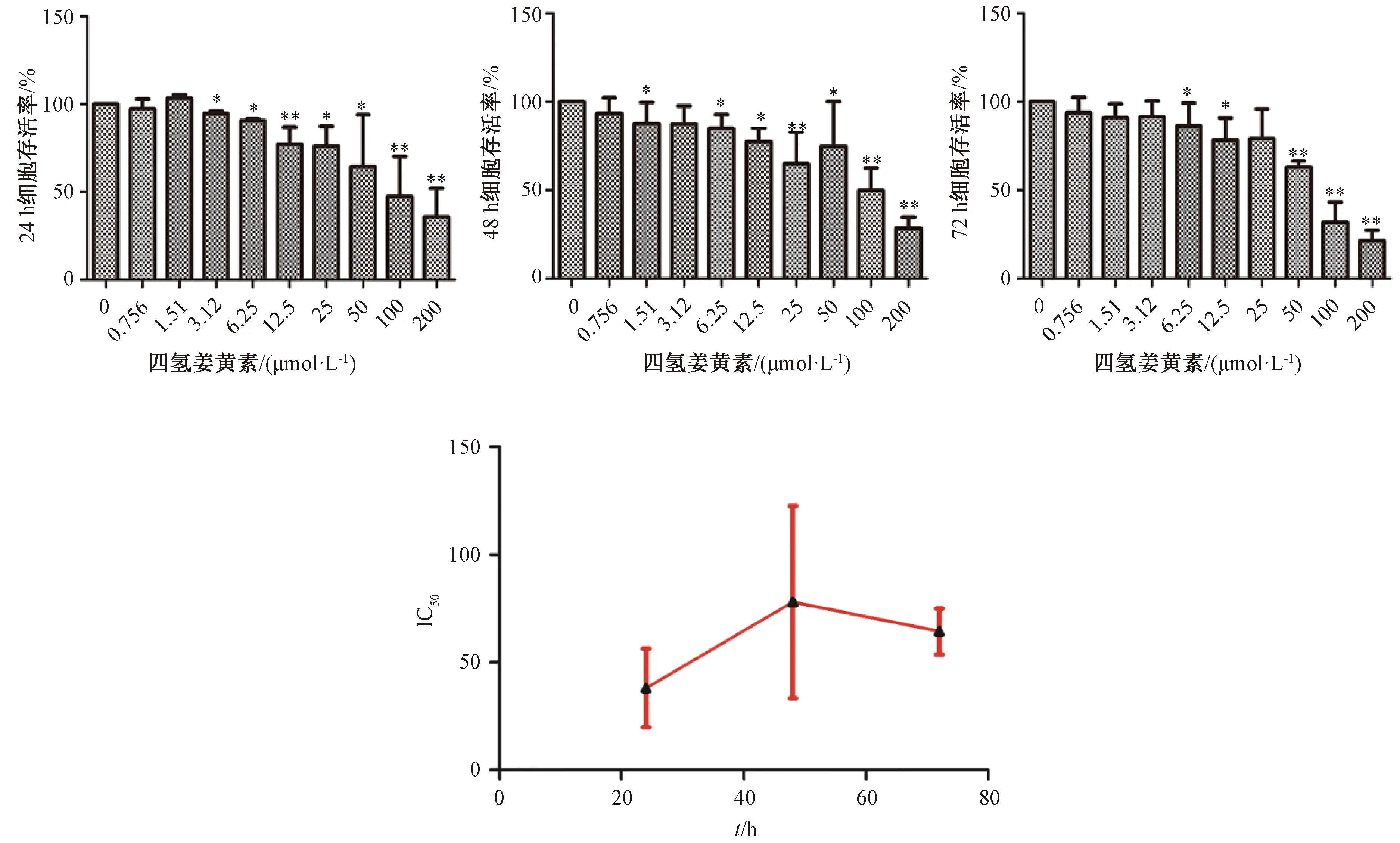
注:與空白對照組(0 μmol/L)組比較,*P<0.05,**P<0.01。圖1 四氫姜黃素對MCF-7細胞增殖的影響
3.1.2 克隆形成實驗 如圖2所示,與空白對照組比較,四氫姜黃素25、50、100 μmol/L劑量組MCF-7細胞克隆形成數減少(P<0.01),四氫姜黃素對MCF-7細胞具有抑制作用。
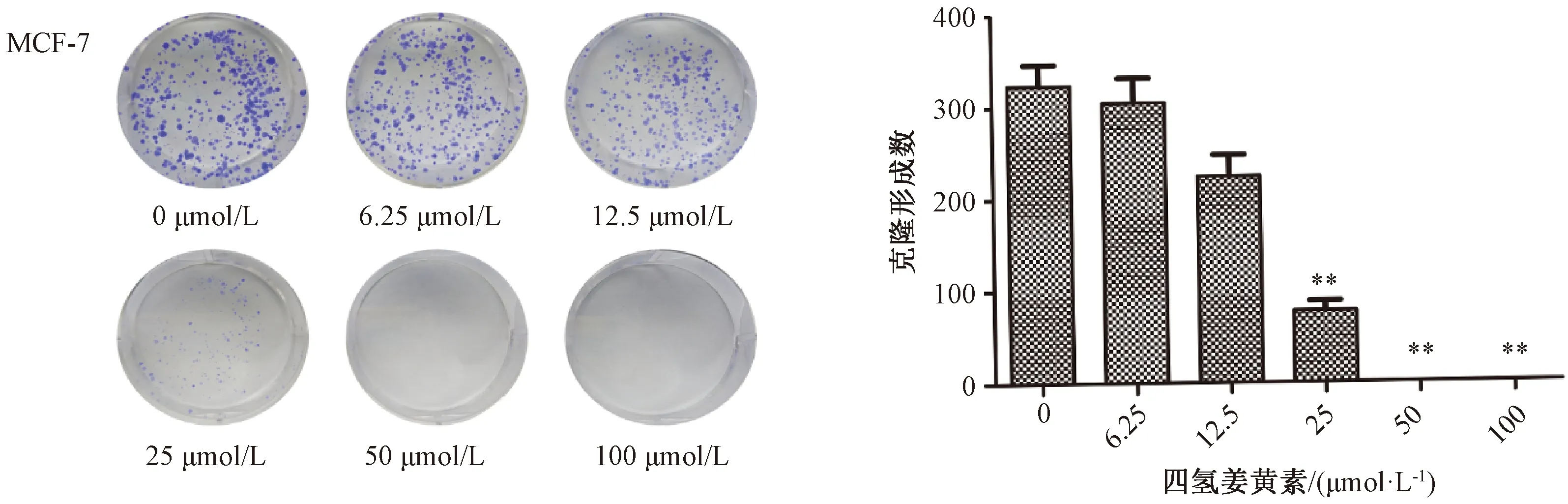
注:與空白對照組(0 μmol/L)組比較,**P<0.01。圖2 四氫姜黃素對MCF-7克隆形成的影響
3.2 四氫姜黃素對MCF-7細胞凋亡的影響
3.2.1 細胞形態 如圖3所示,與空白對照組比較,四氫姜黃素作用48 h后細胞生長緩慢,細胞數量減少,細胞形態發生改變,胞內出現空泡,大量細胞碎片漂浮于培養液表面。

圖3 四氫姜黃素對MCF-7細胞形態的影響(×200)
3.2.2 流式細胞術實驗 如圖4所示,與空白對照組比較,四氫姜黃素50、100 μmol/L劑量組MCF-7細胞凋亡率升高(P<0.05,P<0.01),四氫姜黃素能促進MCF-7細胞凋亡。

注:與空白對照組(0 μmol/L)組比較,*P<0.05,**P<0.01。圖4 四氫姜黃素對MCF-7細胞凋亡的影響
3.3 四氫姜黃素對MCF-7細胞轉移的影響
3.3.1 劃痕實驗 如圖5所示,與空白對照組比較,四氫姜黃素25、50、100 μmol/L劑量組細胞遷移率降低(P<0.01)。
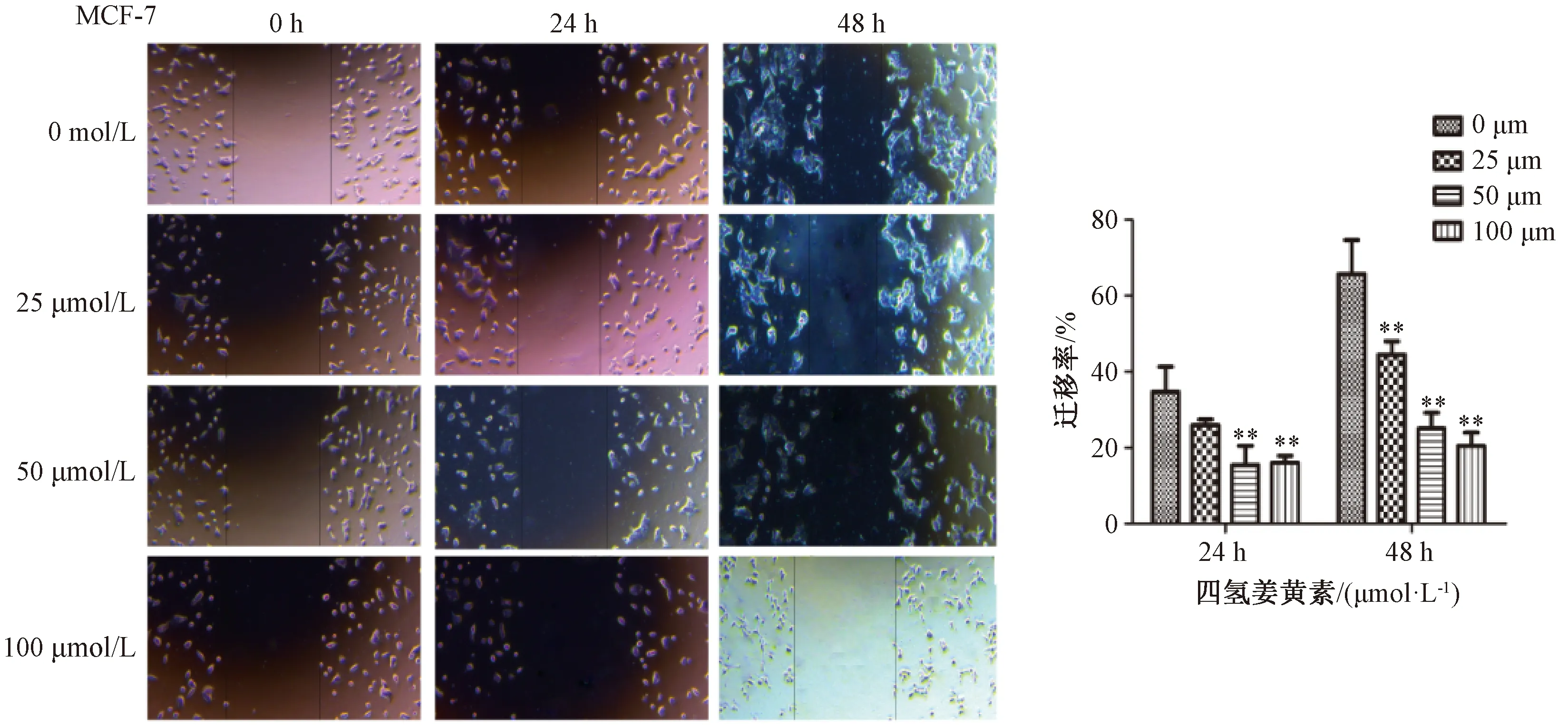
注:與空白對照組(0 μmol/L)組比較,**P<0.01。圖5 四氫姜黃素對MCF-7細胞遷移的影響
3.3.2 Transwell實驗 如圖6所示,與空白對照組比較,四氫姜黃素25、50、100 μmol/L劑量組穿透小室隔膜到達上層小室的底面的細胞數減少(P<0.01)。
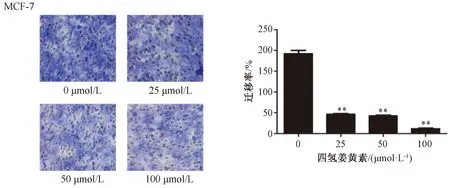
注:與空白對照組(0 μmol/L)組比較,**P<0.01。圖6 四氫姜黃素對MCF-7細胞遷移的影響
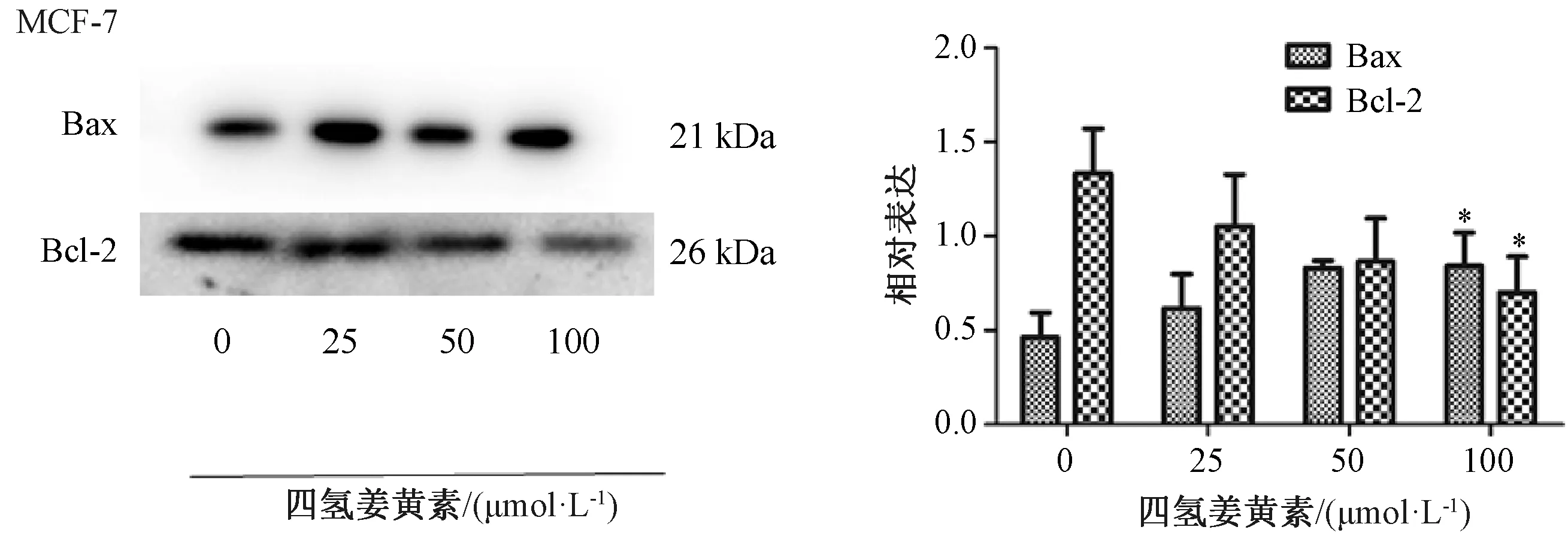
注:與空白對照組(0 μmol/L)組比較,*P<0.05。圖7 四氫姜黃素對MCF-7細胞Bax、Bcl-2蛋白表達的影響
3.4 Western blot實驗 如圖7所示,與空白對照組比較,四氫姜黃素100 μmol/L劑量組MCF-7細胞中Bcl-2蛋白表達降低(P<0.05),Bax蛋白表達升高(P<0.05),提示四氫姜黃素能促進MCF-7的凋亡。如圖8所示,四氫姜黃素100 μmol/L劑量組MCF-7細胞MMP2、MMP-9蛋白表達均降低(P<0.05),表示四氫姜黃素能抑制MCF-7細胞的轉移。
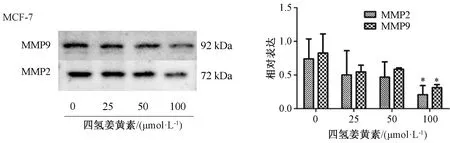
注:與空白對照組(0 μmol/L)組比較,*P<0.05。圖8 四氫姜黃素對MCF-7細胞MMP2、MMP9蛋白表達的影響
4 討論
乳腺癌是女性中常見的惡性腫瘤之一,發病率和致死率高,具有起病隱匿、發展快、早期診斷率低等特征,嚴重危害女性健康。腫瘤的轉移依靠癌細胞的遷移和侵襲兩大關鍵途徑,阻斷這些途徑是抗腫瘤治療的重要方法,因此,抑制細胞轉移及增殖是預防和治療惡性腫瘤的重要研究方向[11]。近年來,中醫藥在腫瘤的治療中通過穩定癌灶、減輕放化療副作用及改善患者預后等多種方式起到良好抗腫瘤效果[15]。腫瘤的遷移與侵襲是腫瘤向遠端轉移和增殖的第一步,腫瘤細胞必須要穿透細胞外基質、基底膜組成的組織屏障才能完成轉移[16-17]。MMP-9以酶原的形式分泌,被激活后形成Ⅳ型膠原酶,通過降解、破壞靠近腫瘤表面的細胞外基質中的Ⅳ型、Ⅴ型膠原和明膠,然后腫瘤細胞沿著缺失的基底膜向周圍組織浸潤,最終導致腫瘤的侵襲和轉移[18-20]。MMP-2是金屬蛋白酶家族中與腫瘤關系最為密切的因子之一。MMP-2是一種鋅離子依賴的蛋白水解酶,由腫瘤細胞和間質細胞以酶原形式分泌,經水解后激活,能特異性地降解基底膜的主要成分—Ⅳ型膠原,還可降解Ⅴ、Ⅵ、Ⅹ型膠原、FN和明膠,同時通過對細胞外基質的改建,促進腫瘤新生血管的形成,促進腫瘤的侵襲和轉移,從而影響預后[18-23]。
本研究中,CCK8與克隆實驗結果顯示四氫姜黃素對MCF-7細胞的增殖具有抑制作用;流式細胞術實驗及Western blot實驗結果顯示,四氫姜黃素能誘導細胞凋亡;劃痕實驗、Transwell實驗及Western blot實驗結果表明四氫姜黃素能抑制細胞的遷移。綜上所述,四氫姜黃素對MCF-7乳腺癌細胞的增殖、轉移具有一定的抑制作用,可促進MCF-7乳腺癌細胞的凋亡,其作用機制可能是通過抑制細胞MMP2、MMP9的表達從而抑制MCF-7細胞遷移。本研究為四氫姜黃素在預防和/或治療乳腺癌轉移提供了實驗依據,具有進一步研究的價值。

