早發型新生兒敗血癥危險因素及炎癥指標分析
方巧巧,王艷芬,2,李林科
(1.山西醫科大學兒科醫學系,山西 太原 030001;2.山西醫科大學第三醫院,山西 太原 030032)
新生兒敗血癥是指病原體侵入新生兒血液循環并生長、繁殖,產生毒素而引起的全身性炎癥反應[1],是威脅新生兒生命的嚴重疾病。臨床診斷新生兒敗血癥的金標準是血培養或無菌體腔液培養出致病菌,但此項檢查結果報告不及時、陽性率低,易漏診、誤診,延誤治療[2]。新生兒敗血癥根據發病時間可分為早發型敗血癥(出生72h內)和晚發型敗血癥(出生72h后)[3],其中早發型敗血癥起病隱匿,進展快,多器官易受累,對新生兒危害大,且無典型的臨床表現,早期識別非常困難。故研究早發型敗血癥的獨立危險因素對其早期臨床表現的識別和干預具有指導作用。本研究將2017—2021年山西醫科大學第三醫院兒科新生兒病房收治的100例早發型新生兒敗血癥作為感染組,隨機選取同期100例非敗血癥患兒作為對照組,回顧性分析患兒及其母親的臨床資料,以及患兒生后不同時齡段炎癥指標特點,以期發現該病的獨立危險因素及有早期診斷價值的炎癥指標,為臨床早期診斷及干預提供依據。
1研究對象與方法
1.1研究對象
選取2017—2021年山西醫科大學第三醫院兒科新生兒病房收治的100例發病時間≤3日齡的早發型新生兒敗血癥患兒作為感染組,并隨機抽取同期新生兒病房收治的100例無感染征象且出院已排除敗血癥的患兒作為對照組。該研究方案經過倫理審查。納入標準:①感染組符合新生兒敗血癥的診斷標準且發病時間≤3日齡;②對照組選取臨床無感染征象,血培養陰性,且出院時排除敗血癥診斷(如新生兒高膽紅素血癥、新生兒濕肺、新生兒低血糖等非感染性疾病患兒);③血培養、血常規、C反應蛋白(C-reactive protein,CRP)、降鈣素原(procalcitonin,PCT)檢測資料齊全;④患兒家屬簽署知情同意書。
排除標準:①入院前已使用抗生素;②嚴重先天性畸形;③先天性遺傳代謝疾病;④臨床資料不全的病例。
1.2診斷標準
參考中華醫學會兒科學分會新生兒學組《2019版新生兒敗血癥診斷及治療專家共識》[3]:①確診敗血癥組即患兒有臨床表現,血培養或腦脊液(或其他無菌腔液)培養致病菌。②臨床診斷敗血癥組即有臨床異常表現,同時滿足下列條件中任何一項:血液非特異性檢查≥2項陽性;腦脊液檢查為化膿性腦膜炎改變;血液中檢出致病菌DNA。根據發病時間,新生兒敗血癥又分為早發型敗血癥(early onset sepsis,EOS)及晚發型敗血癥(late onset sepsis,LOS),EOS一般發病時間≤3日齡,LOS一般發病時間>3日齡[3]。
1.3資料收集
回顧性收集患兒的出生體重、性別、有無發熱、有無宮內窘迫、窒息、搶救史、有無吸氧,并采集患兒生后不同時齡段炎癥指標等資料;回顧性收集患兒母親的妊娠年齡、分娩方式、有無流產、有無子癇前期、有無妊娠期糖尿病等妊娠合并癥,是否有羊水糞染、胎膜早破,有無產前發熱等臨床資料。
1.4統計學方法

2結果
2.1早發型新生兒敗血癥影響因素分析
2.1.1單因素分析
母親相關因素中胎膜早破、羊水糞染、產前發熱、子癇前期、妊娠期糖尿病在兩組間差異均有統計學意義(P<0.05);新生兒相關因素中性別、早產、患兒發熱、宮內窘迫、窒息、搶救史、吸氧在兩組間差異均有統計學意義(P<0.05),見表1、表2。

表1 早發型新生兒敗血癥母親相關危險因素[n(%)]

表2 早發型新生兒敗血癥新生兒相關危險因素[n(%)]
2.1.2多因素分析
以早發型新生兒敗血癥作為因變量,將上述分析結果中有統計學意義的單因素如胎膜早破、羊水糞染、產前發熱、子癇前期、妊娠期糖尿病、新生兒性別、早產、患兒發熱、宮內窘迫、窒息、搶救史、吸氧作為自變量引入,進行二元Logistic回歸分析,結果顯示:胎膜早破、產前發熱、子癇前期、患兒發熱、早產是早發型新生兒敗血癥的獨立危險因素(P<0.05),見表3。

表3 早發型新生兒敗血癥多因素Logistic回歸分析結果
2.2生后不同時齡段各實驗室指標的ROC曲線及診斷價值分析
在患兒出生后不同的實際小時齡,感染組與對照組炎癥指標如白細胞計數(white blood counts,WBC)、PCT、CRP比較,差異均有統計學意義(P<0.05),見表4。以3項炎癥指標繪制ROC曲線,計算AUC、靈敏度、特異度、約登指數及截斷值,見圖1,AUC差異均有統計學意義(P<0.05);ROC曲線顯示,生后不同時齡段各實驗室指標有不同的最佳截斷值,其中出生12~24h PCT有最大AUC,為0.983,敏感性為0.984,特異性0.991;出生24~48h CRP有最大的AUC,為0.992,敏感性為0.981,特異性為0.972,見表5。
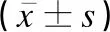
表4 生后不同時齡段感染組和對照組實驗室指標比較

表5 3項實驗室指標在患兒生后不同時齡段診斷早發型新生兒敗血癥的評價參數
3討論
3.1概述
新生兒敗血癥是新生兒發病和死亡的主要原因,該病臨床表現無特異性、血培養陽性率低,臨床早期診斷極為困難,尤其是早發型敗血癥進展快,死亡率高,需早期識別并及時治療。通常產前或產時懷疑有感染危險因素的新生兒在等待血培養結果的同時使用抗生素進行預防性治療,這又不可避免地導致抗生素的過度使用,進而使耐藥菌的不斷增加[4],故早期正確識別早發型新生兒敗血癥的危險因素顯得尤為重要。
本研究單因素分析結果表明,胎膜早破、羊水糞染、產前發熱、子癇前期、妊娠期糖尿病、新生兒性別、早產、患兒發熱、宮內窘迫、窒息、搶救、吸氧是早發型新生兒敗血癥的影響因素;多因素Logistic回歸分析結果表明,胎膜早破、產前發熱、子癇前期、患兒發熱、早產是早發型新生兒敗血癥的獨立危險因素。
3.2早發型新生兒敗血癥與胎膜早破的關系
胎膜早破是指分娩前胎膜的全層(絨毛和羊膜)自然破裂,其對懷孕和分娩的不利影響包括增加早產率、新生兒死亡率、產婦宮內感染和產褥感染率等[5]。胎膜早破增加了病原菌從產道進入羊膜囊的機會,導致絨毛膜羊膜炎、胎兒損害及窒息,從而導致早發型新生兒敗血癥。本研究中,發現胎膜早破是早發型新生兒敗血癥的獨立危險因素,這一結論與Gebremedhin 等人[6]的研究一致。胎膜早破的時間長短與早發型敗血癥是否存在直線相關是目前研究的熱點。Alemu等[7]研究指出:胎膜早破時間越長,發生早發型新生兒敗血癥的風險越高,胎膜早破18小時及以上的孕婦所生新生兒發生敗血癥的幾率是胎膜早破18小時以內新生兒的2.8倍。但本文未將胎膜早破的具體時間納入,無法驗證胎膜早破時間長短與早發型新生兒敗血癥是否存在相關性,有待今后擴大樣本量進一步探索研究。
3.3早發型新生兒敗血癥與子癇前期的關系
子癇前期是一種累及母體各器官系統功能的妊娠期高血壓疾病,表現為妊娠20周后新發的高血壓(收縮壓≥140mmHg 或舒張壓≥90mmHg)伴隨至少一個器官或系統的功能障礙,出現蛋白尿、心力衰竭、胎兒生長受限等,病情多呈不斷進展的過程,嚴重影響母親和新生兒的健康,是新生兒患病和死亡的重要原因[8]。子癇前期的病因尚未明確闡述,然而很大一部分歸因于免疫功能失調和炎癥增加,炎癥細胞因子破壞胎盤信號,并穿過胎兒循環,改變胎兒和新生兒的易感性,這可能使子癇前期母親的新生兒患早發型敗血癥的風險增加[9]。本研究結果表明子癇前期是早發型新生兒敗血癥的獨立危險因素,這與Harrison等人[10]的結果一致。目前國內外對于子癇前期對早發型敗血癥的研究仍較少,子癇前期是否為新生兒早發型敗血癥的獨立危險因素仍存在爭議,尚需進一步擴大樣本量進行研究。
3.4生后不同時齡段炎癥指標對早發型新生兒敗血癥的診斷價值
血培養結果的獲得在大多數醫療機構需要72h,早發型新生兒敗血癥治療的關鍵時間在生后72h內,故早期診斷需要其他實驗室指標提供依據,本研究將感染組和對照組炎癥指標進行比較,繪制ROC曲線,發現炎癥指標在出生后不同時齡段有不同的最佳截斷值,其中生后12~24h PCT最大的AUC為0.983,敏感性為0.984,特異性0.991;生后24~48h CRP最大的AUC為0.992,敏感性為0.981,特異性為0.972。PCT是一種急性期反應蛋白,健康人血液中PCT含量微乎其微,在受到炎癥刺激,特別是細菌感染的情況下,細菌內毒素釋放,引起炎癥反應,從而導致PCT水平顯著升高,PCT于4~6h升高,12~24h達高峰,已成為識別細菌感染和指導抗生素治療的標志物[11]。Memar等人[12]研究指出:由于PCT具有更好的敏感性和特異性,建議PCT作為早發型新生兒敗血癥的良好診斷標志物,有助于快速和早期診斷,以啟動早期抗生素治療。CRP也是臨床上常用且經濟、快速的檢測指標,在機體發生炎癥時,CRP通常會升高,CRP是肝臟對炎癥刺激作出反應而產生的,因此被認為是一種急性期蛋白,Wu等[13]發現,CRP可以作為一種快速、經濟的預測指標,以更好地指導抗生素的使用。
3.5小結
綜上所述,通過分析早發型新生兒敗血癥的相關危險因素及生后不同時齡段實驗室指標的特點,發現胎膜早破、產前發熱、子癇前期、患兒發熱、早產均會增加早發型新生兒敗血癥的風險,盡早識別危險因素并監測生后12~24h PCT及CRP的變化,有助于降低早發型新生兒敗血癥發生,改善其預后。本研究的局限在于樣本量少,不能做更精確的時齡分組研究如每6小時一組,炎癥指標檢測需多次采血,費用高,家長經濟負擔重、心理壓力大,可期待無創或更多微創檢測技術應用于臨床后再進一步研究。

