早期胃食管結合部癌行內鏡黏膜下剝離術后非治愈切除的危險因素分析
黃小杰,林曉露,梁瑋,林瀛,程輝,楊士杰,林海寧,鄭煒平,鄧萬銀
(1. 福建中醫藥大學中西醫結合學院,福建 福州 350122; 2. 福建省立醫院消化內鏡中心,福建 福州 350001)
胃食管結合部(gastroesophageal junction,GEJ)癌指GEJ上下5 cm以內的腫瘤[1]。既往GEJ癌在我國和日本等發病率較低,但隨著幽門螺桿菌感染率的下降,GEJ癌發病率較過去40年增加了2.5倍,并呈逐年上升的趨勢[2]。內鏡黏膜下剝離術(endoscopic submucosal dissection,ESD)是早期胃癌的首選治療方式,其提高了早期胃癌患者治愈性切除率,并使治愈性切除在特殊部位(如GEJ)的腫瘤成為可能[3]。與早期胃癌相比,ESD治療早期GEJ癌的治愈性切除率低、手術時間較長、手術難度較大[4]。為了減少不必要的內鏡下治療,在選擇治療方案之前需要評估非治愈性切除的可能。目前關于早期GEJ癌非治愈性切除的危險因素尚不清楚,因此,本研究旨在評估與ESD術后產生非治愈性切除的相關的預測因素。
1 對象與方法
1.1 病例資料
選擇2016年10月至2020年9月于福建省立醫院消化內鏡中心行胃鏡檢查時檢出的早期GEJ癌患者114例,均行ESD術。其中,男93例,女21例,平均年齡(63.1±7.6)歲。
納入標準:年齡≥18歲;GEJ上方5 cm和下方5 cm以內的腫瘤;病理提示腺癌、高級別上皮內瘤變;有完整的臨床資料。排除標準:超聲內鏡或CT顯示腫瘤進展或可疑轉移;多發原位癌;殘胃癌;病理類型為鱗癌、低級別上皮內瘤變。本研究方案獲得我院倫理委員會批準。
1.2 數據收集
收集患者性別、年齡、腫瘤直徑、腫瘤形態、病理類型、浸潤深度以及是否合并潰瘍,是否脈管浸潤,是否治愈性切除,是否追加手術治療等。所有胃鏡圖片均由1名10年以上經驗豐富的內鏡醫師進行評估,評估內容包括:腫瘤直徑,參照胃鏡先端部直徑目測計算;Paris分型[5],分為隆起型病變(0-Ⅰ)、平坦型病變(0-Ⅱ)和凹陷型病變(0-Ⅲ);周邊黏膜炎癥狀態;是否存在潰瘍或者潰瘍后疤痕;是否存在黏膜下纖維化及纖維化程度;是否并發深在性囊性胃炎。具體示例如圖1所示。

A:隆起型(0-Ⅰ)GEJ癌;B:背景黏膜炎癥狀態;C:賁門一淺凹潰瘍,底覆白苔;D:輕度纖維化,在藍色的黏膜下層中出現白色的網狀結構;E:重度纖維化,黏膜下層與白色的固有肌層分界不清;F:超聲胃鏡提示合并深在性囊性病變
1.3 ESD手術方案及病理取材
操作均由具備10年以上ESD手術經驗的醫師完成,所有患者均予全麻下行ESD,氬氣刀予病灶周圍標記(術前據白光內鏡和窄帶成像放大內鏡明確分界線),黏膜下注射使病灶隆起,環狀切開黏膜,行病灶黏膜下剝離,最后創面預防電凝止血。
1.4 樣本處理和診斷
所有ESD術后標本間隔2 mm取材,所有病理切片均由本院1位10年以上經驗豐富的病理科主任醫師對其組織類型、浸潤深度、水平切緣、垂直切緣和淋巴血管侵犯等進行評估診斷。
診斷內容主要如下。早期GEJ癌:局限于黏膜層或黏膜下層,而不論有無淋巴結轉移的GEJ癌。早期癌分類:未分化型包括低分化腺癌、黏液腺癌、印戒細胞癌;分化型包括中、高分化的管狀腺癌、乳頭狀腺癌[6]。整塊切除:病灶在內鏡下整塊切除,并獲得單塊標本。完全切除:水平和垂直切緣均為陰性的整塊切除。治愈性切除:病灶整塊切除,直徑≤2 cm、垂直切緣與水平切緣陰性、無合并潰瘍且無脈管浸潤的分化型黏膜內癌;相對治愈性切除:病灶整塊切除、垂直切緣與水平切緣陰性、無脈管浸潤且滿足下列條件的早期GEJ癌:直徑>2 cm,無潰瘍的分化型黏膜內癌;直徑≤3 cm,可伴潰瘍的分化型黏膜內癌;直徑≤2 cm,無潰瘍的未分化型黏膜內癌;直徑≤3 cm,分化型淺層黏膜下癌[7];非治愈性切除:指除治愈性切除和相對治愈性切除以外的內鏡下切除。
根據術后病理檢查等結果將患者分為治愈性切除組和非治愈性切除組,對其性別、年齡、腫瘤直徑、腫瘤形態、病理類型、浸潤深度以及是否合并潰瘍等進行比較。
1.5 統計學方法
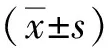
2 結果
2.1 兩組臨床病理參數比較
114例患者,整塊切除率為99.1%(113/114),完全切除率為89.5%(102/114),非治愈性切除率為17.5%(20/114)。兩組在性別、年齡、病變形態、病灶位置、深在性囊性胃炎、背景炎癥方面差異均無統計學意義(P均>0.05),而腫瘤直徑、黏膜下浸潤、潰瘍、病理類型、黏膜下纖維化差異有統計學意義(P均<0.05)。見表1。

表1 內鏡下治愈性切除組與非治愈性切除組臨床病理特征比較 例(%)

續表
2.2 內鏡下非治愈性切除相關危險因素的多因素分析
將表1中有統計學差異的指標納入Logistic回歸分析,結果顯示,腫瘤直徑(OR=4.421,P=0.008)、黏膜下浸潤(OR=8.352,P<0.001)、潰瘍(OR=24.769,P<0.001)和未分化癌(OR=7.583,P=0.012)為非治愈性切除的獨立危險因素。見表2。

表2 非治愈性切除相關危險因素的多因素分析
2.3 危險因素數量與非治愈性切除發生率的相關性分析
獨立危險因素的數量與術后非治愈性切除發生率相關(rs=0.492,P<0.01)。見表3。

表3 非治愈性切除的影響因素
2.4 術后隨訪
20例非治愈性切除患者中,3例失訪,平均隨訪時間(32.8±16.1)個月,4例為eCura C-2級,2例追加外科手術,其中1例經手術病理證實為淋巴結轉移。在未追加全胃切除術的隨訪患者中,未發現復發病例。
3 討論
本研究114例接受ESD治療的早期GEJ癌患者中,非治愈性切除率為17.5%(20/114)。日本一項多中心回顧性研究結果顯示,早期GEJ癌的完整切除率為82.5%(307/372)[2]。研究顯示,早期GEJ癌的整塊切除率為100%,非治愈性切除率為21%[8]。本研究結果與其相似。
深在性囊性胃炎是一種相對少見的疾病,其特征是胃腺增生,囊性向下生長到黏膜下層。這種情況往往可能導致內鏡下的隆起表現,從而影響內鏡下判斷浸潤深度的過估情況存在。本研究中24.6%(28/114)病例伴有黏膜下囊性病變,與非治愈性切除無明顯相關(P>0.05)。研究發現,背景炎癥狀態是黏膜下囊性病變的獨立危險因素(OR=2.683,P=0.030)[9]。所以,臨床上選擇是否做ESD治療的時候應考慮是否伴發深在性囊性胃炎及周邊炎癥存在對判斷浸潤深度的影響。
腫瘤直徑(>2 cm)是非治愈性切除的獨立危險因素,可能與病變大操作難度大、邊界定義困難等相關。Gotoda等[10]研究表明,病變大小與淋巴結轉移風險相關。Jang等[11]對82例賁門(GEJ線以上1cm及GEJ線以下2 cm)早期癌患者進行回顧性分析,結果顯示,病灶直徑>2 cm、黏膜下層浸潤導致治愈性切除率降低。本研究中浸潤至黏膜下層的非治愈性切除患者共11例,可能與術中粘連及病變巢狀黏膜下深層浸潤等相關。研究報道,早期GEJ癌黏膜下層浸潤導致淋巴結侵犯風險由2.2%上升至17.9%[10]。一項納入44例早期GEJ癌患者的回顧性研究表明,非治愈性切除病例中未分化癌、黏膜下浸潤及淋巴脈管浸潤多見[12],也證實黏膜下浸潤可作為獨立危險因素。
本研究結果顯示,潰瘍是非治愈性切除的獨立危險因素。研究表明,潰瘍可造成黏膜下層結構不清、剝離困難及術前浸潤深度判斷困難,導致非完全切除[13]。未分化癌生長方式與分化癌有所不同,尤其是印戒細胞癌,容易出現淋巴結轉移、腹膜轉移及遠處轉移。因此,對于未分化癌,ESD的選擇應該更加慎重及需要較大的安全側緣。此外,本研究發現危險因素越多的患者,其ESD術后非治愈性切除的風險越高。由Hatta等[14]建立的eCura系統對早期胃癌ESD術后患者依據危險因素權重積分進行危險分層和指導術后隨訪和治療,分級越高的患者非治愈性切除的風險越高,eCura C-2級患者均需進一步外科手術。本研究20例非治愈性切除患者中,4例為eCura C-2級,2例追加外科手術,其中1例經手術病理證實為淋巴結轉移,顯示腫瘤直徑(>2 cm)、黏膜下浸潤、未分化癌3個危險因素。由于本研究病例數較少,故僅研究危險因素數量與ESD術后非治愈性切除的關系,未采用eCura評分系統進一步深入分析。因此,如術前發現患者有多個危險因素,臨床醫師應更傾向采用外科根治術。
本研究存在的局限性主要如下:首先,本研究為回顧性、非隨機且單中心,存在一定的選擇偏差;其次,非治愈性切除患者平均隨訪時間較短,不能確定非治愈性切除拒絕外科手術患者的臨床結果。
綜上所述,腫瘤直徑(>2 cm)、黏膜下浸潤、潰瘍、未分化癌是非治愈性切除的預測因素。此外,隨著危險因素的增加,非治愈性ESD的風險也隨之增加。對于有多個危險因素的患者,在考慮ESD之前,臨床醫師應該仔細選擇合適的GEJ癌治療方法。

