碳納米管用于水合物法捕集CO2的研究進展
陳佳豪,王 芳,黃澤皚,曹玥晗,周 瑩,2
(1.西南石油大學 新能源與材料學院,碳中和研究院,四川 成都 610500;2.西南石油大學 油氣藏地質及開發工程國家重點實驗室,四川 成都 610500)
自《巴黎協定》提出各國應對全球氣候變化的行動安排后,面對國際嚴峻的碳減排形勢[1],中國明確提出力爭在2060年前實現“碳中和”的目標[2]。碳捕集、利用與封存(Carbon capture,utilization and storage,CCUS)技術是將捕集和分離后的CO2直接加以利用或封存,以實現CO2減排的關鍵技術,按工業鏈流程分為碳捕集、輸送、利用與封存等環節[3-4],2025~2060年各環節預計成本如表1所示[5-6]。碳捕集成本約占CCUS技術工業鏈總成本的70%以上,成為影響CCUS技術商業化的關鍵因素。隨著綠色、低能耗碳捕集技術的發展,預計到2035年,碳捕集成本為70~320元/噸,2060年降至20~130元/噸。火電廠等排放的煙氣作為工業碳排放的主要來源,其CO2濃度(物質的量分數,下同)為15%~20%[3-5],捕集難度較大,因此發展綠色高效碳捕集技術迫在眉睫。

表1 2025~2060年CCUS各環節成本Table 1 Cost of each link of CCUS from 2025 to 2060
傳統碳捕集方法包括吸收法、吸附法、低溫分離法、金屬氧化物法和膜分離法等[5],近年來水合物法由于其成本低、綠色環保、能耗低及過程無副產物的優點[3],受到了國際能源部門和研究者的廣泛關注。不同碳捕集方法的優點、缺點和技術成熟度如表2所示[7-9],目前,已工業化應用的化學吸收法和物理吸附法吸收效率高,處理量大,但吸收劑消耗大、能耗較高;低溫分離法最大的缺點是只適用于高濃度的CO2處理。相比之下,通過水合物法捕集火電廠排放源煙氣中CO2的操作條件溫和、碳捕集成本大大降低且綠色環保,展現出了良好的工業應用前景[5]。然而,水合物生長速率慢、CO2分離效率和分離因子低等缺點成為制約水合物法捕集CO2技術發展的關鍵。以碳納米管(CNTs)為代表的納米多孔材料由于具有納米尺寸結構和大量表面活性位點,在水合物生長過程中發揮了動力學促進劑的作用,可有效強化水合物生成的動力學特性。

表2 碳捕集方法對比 Table 2 Comparison of carbon capture methods
本文對CNTs及功能化CNTs(—COOH、—OH、—NH2、Cu和Ag納米粒子等修飾)在氣體溶解期、水合物誘導期和水合物生長期等各階段的作用進行綜述,分析CNTs在水合物生長中的作用機制及應用前景,以期對同類技術研究提供參考借鑒。
1 水合物法捕集CO2技術及其促進劑
水合物法分離氣體技術于20世紀40年代首次提出,NIKITIN等[10]利用SO2水合物從氖中成功分離了氬氣,隨后KANG等[11]于2000年提出了通過水合物法分離煙氣中CO2的理念,其原理為利用不同氣體的水合物相平衡不同來實現氣體分離和提純。近年來水合物利用技術發展迅速,樊栓獅等[9]提出了水合物膜分離技術,可有效提高分離效率,CHEN等[12]研究了不同CO2水合物的拉曼光譜,宗杰等[13]致力于開發新型水合物利用技術等。促進劑的研發對于改善水合物法分離氣體技術尤為重要,不同類型的促進劑如表3所示[8-9,14-15]。目前促進劑分為熱力學促進劑與動力學促進劑,熱力學促進劑可通過占據水合物籠型孔穴降低其熱力學相平衡條件,有機物小分子如四氫呋喃(THF)等可作為熱力學促進劑參于水合反應;動力學促進劑可提高動力學反應速率,如表面活性劑、多孔材料和納米材料等均可作為動力學促進劑加快水合速率,同時可以提高儲氣量和氣體分離效率[16-18]。盡管傳統型促進劑的加入部分解決了水合物法水合速率慢、儲氣量低和分離效率差的問題,但有機物促進劑有毒性、表面活性劑產氣阻礙CO2在氣液界面滲透與溶解的問題依舊限制了水合物技術快速發展,亟待開發綠色高效促進劑[19-20]。

表3 不同類型的促進劑Table 3 Different types of accelerators
CNTs因其多孔結構及化學特性在氣體吸附[21-25]和影響水合物生長[26-28]方面展現出了良好的工業應用前景。2010年,PARK等[29]首次報道了多壁碳納米管(MWCNTs)在CH4水合物體系中的應用,發現在MWCNTs的作用下CH4消耗量比純水中高出3倍,MWCNTs有效提高了CH4氣體儲存量,展示出CNTs促進CH4水合物生長的優勢并備受關注,同時體現出用于CO2水合物的良好應用前景。
2 CNTs對CO2水合物生長的影響
CO2水合物與CH4水合物相似,其生長是非平衡過程,生長階段可分為氣體溶解期、水合物誘導成核期、水合物快速生長期和穩定期,如圖1所示[30]。第一階段為CO2在氣-液界面溶解傳質,由于CO2與CNTs間的范德華相互作用,CNTs提高了CO2吸附能力,增大了CO2吸附量,促進了CO2在溶液中的吸附溶解;第二階段是水分子誘導成核期,界面處的水合物結構為CO2與水的組合提供了模板,氣液混合引起界面的晶體結構向液體內部擴散,導致大量成核,CNTs為水合物成核提供了更多的成核位點;第三階段是快速生長期,水合物微晶在誘導時間后大量聚集并加速生長,最終形成水合物晶體,伴隨溶液黏稠度增加,此階段釋放出大量熱量[30];第四階段水合物生長速率逐漸減緩,水合物已大量生成,晶體結構趨于穩定。

圖1 水合物生長過程Fig.1 Hydrate growth process
2.1 CNTs對CO2吸附溶解的影響
CO2吸附溶解階段為CO2在氣-液界面吸附溶解的傳質過程。當環境條件高于水合物相平衡條件時,氣體首先被溶液吸附飽和,而起始環境條件低于相平衡條件時,溶解與成核所需時間大幅縮短,促使水合物在氣-液接觸界面生成。
2.1.1 CNTs對CO2吸附能力的影響
CNTs表面吸附作用歸因于分子間范德華力,林志忠等[17]利用蒙特卡羅模擬(MC)方法研究了CNTs管徑對CO2/N2吸附分離的影響,不同的壓力使得CO2/N2分別與CNTs產生不同作用力,從而實現了CO2/N2混合氣體的選擇性吸附,CO2和N2吸附量同時隨壓力升高不斷增加或先增加后趨于飽和。曹偉等[20]利用分子動力學(MD)方法計算了CO2/CH4與CNTs壁面之間的吸附能,發現相互作用隨管徑擴大而增大,CO2與壁面的相互作用明顯強于CH4與壁面的相互作用,表明CNTs對CO2的吸附效果更強,而混合氣吸附容量相比純組分有所減少,CH4減少量大于CO2,表明CNTs更傾向于吸附CO2。ZHAO等[31]通過密度泛函理論(DFT)計算并研究了不同類型的CNTs吸附CO2的吸附能及吸附作用,發現CO2在CNTs外側的吸附作用較弱,吸附能大約為2 J/mol,CO2距離管壁表面32~35 nm。CINKE等[32]通過CNTs吸附實驗發現對CO2的吸附為物理吸附,吸附能大約為0.24 eV,利用二階摩爾勒-粒子微擾理論進一步證明CO2吸附于管側。張超等[33]利用去正則蒙特卡洛模擬(GCMC)法探究了管壁層數及間距對吸附能力的影響,結果表明單壁碳納米管(SWCNTs)的吸附能力最強,隨管壁層數的增加,吸附能力逐漸減弱,壁面間距越大,吸附能力越強。
CNTs的表面修飾改性可改善氣體吸附特性,通過加入強氧化酸[34]、氧化試劑(H2O2)[35],利用等離子體[36]、加熱處理[37]等技術,利用官能團(—COOH、—OH、—NH2和—C==O)對CNTs管壁進行修飾,可提高CNTs在水溶液中的分散性和浸潤性,改善了CNTs對相對分子量小的極性氣體分子的吸附性能[38]。隨著CNTs管徑增大,CO2吸附量先增大后趨于平衡。由此可見,CO2在CNTs促進劑溶液中吸附能力越大,越有利于氣-液界面傳質,水合物成核幾率隨之提高,可有效縮短成核誘導時間,提高水合物生長速率。
2.1.2 CNTs對CO2溶解度的影響
CO2溶解符合低溫吸收特性,溶解度隨著溫度的降低而增大,25.5 ℃時的動態溶解平衡的溶解度大約為30.6 mol/m3[39]。IIJIMA[40]發現CNTs材料為良好的氣體吸附材料是由高比表面積和中空結構決定的,吸附性能主要由CNTs的吸附位點、比表面積、表面官能團、純度和孔徑大小所決定[41-42],從而決定了CO2氣體吸附量。
ZENG等[43]采用MC方法研究了離子液體(IL)復配CNTs對CO2/N2混合氣體的吸附性能,發現CNTs中IL的存在增強了對CO2的吸附,產生高濃度CO2的吸附歸因于CO2與IL之間的強相互作用,并且在混合氣體中,IL@CNTs對CO2的吸附選擇性更高。SU等[44]研究了氨丙基三乙氧基硅烷修飾MWCNTs對CO2吸附,發現CO2吸附量隨水汽含量(物質的量分數,0~7%)的提高而增加,說明水汽可有效提高MWCNTs對CO2氣體的吸附性能,從而促進CO2溶解,為籠型CO2水合物團簇提供客體分子。PASIEKA等[45]研究了MWCNTs及胺功能化的MWCNTs對CO2水合物的影響,發現由于CO2比CH4進入液相的傾向更大,MWCNTs對CO2溶解飽和值和溶解速率影響不大,溶解的CO2與胺功能化MWCNTs管壁發生了化學反應,一定物質的量分數的MWCNTs促進水合物生成,過量反而對生長速率產生抑制作用。
2.2 CNTs對誘導成核的影響
CNTs表面缺陷的修飾(共價官能團、非共價官能團和金屬納米粒子等)可為水合物生長提供成核位點,縮短水合物的誘導期[27,46]。水合物的誘導成核期影響因素較多[47],如主體分子(水)、客體分子(CO2)、驅動力(溫度、壓力)、促進劑類型、攪拌情況和溶液黏稠度等[48],CNTs管壁和表面官能團與CO2產生吸附作用,親水性官能團可與水形成氫鍵,吸引水分子聚集,促進水合物團簇的生成。WANG等[49]通過MD計算發現尿素分子上的氧原子可以作為氫受體,通過氫鍵誘導水分子形成五邊形水合物結構,說明尿素有誘導水合物成核的效果。ZHAO等[50]使用SWCNTs分離了溶解于水的CO2/H2混合氣體,由于CO2的潛在平均力差值比相應水合物中的H2低,實現了CO2在SWCNTs中的高選擇性吸附,并在水溶液中觀察到SWCNTs誘導準一維(Q1D)多邊形CO2水合物的自發形成現象。
LI等[51]發現MWCNTs存在下CO2水合物的誘導時間縮短至12.5 min。雖然CO2水合物生成會釋放熱量,但MWCNTs具有高導熱系數和熱容,使熱量得以及時傳遞,而較大的比表面積為CO2水合物的多相成核提供了合適位置,但對儲氣量無太大影響。NASHED等[52]將MWCNTs-COOH復配SDS后,水合物的初始生長速率提升了23.4%,同時儲氣量達到最高。盛淑美等[53]使用不同物質的量分數的MWCNTs分離CO2/CH4水合物,發現隨著MWCNTs物質的量分數的增加,誘導時間逐漸變短,同時儲氣量增加,這一觀點與Li等[51]得出的MWCNTs物質的量分數對儲氣量無影響的結論不同。
CNTs可縮短水合物誘導期,加快水合物生長,然而官能團如—COOH、—OH對CO2水合物生長成核的機制并未明確,因此后續研究可從水合物誘導成核、反應動力學、異相成核及成核位點等角度探究CNTs對水合物晶體成核的作用機制。
2.3 CNTs對生長速率的影響
由圖1可知,水合物的生長期是快速反應期,水合物在短時間內大量生成至反應結束。在水合物的快速生長階段,氣體濃度、促進劑含量和反應條件至關重要,由于水合物為放熱反應,快速生長期的溫度升高[54],不利于反應持續進行,CNTs可通過及時傳遞熱量加速反應進行。LI等[51]發現在高熱導率的納米顆粒(TiO2、SiO2和MWCNTs)作用下,水合物生長速率大幅提升,此外NASHED等[52]證明了MWCNTs-COOH與水分子間的氫鍵促進了CO2水合物快速生成。
金屬納米粒子的修飾可顯著提高CNTs的導熱性能,促進水合物快速生成[55-56]。SONG等[57]制備了以Cu和Ag納米粒子嫁接的CNTs,用于水合物動力學實驗,結果表明,Ag嫁接CNTs使水合物生成時間縮短至125.1 min,相比于Cu減少12.0%;CH4氣體儲氣量提高至93.3%,相比于Cu提高了3.0%;甲烷回收率高達78.9%。
張保勇等[58]采用不同質量分數的MWCNTs復配SDS溶液分離CO2/CH4混合氣,其中0.1% MWCNTs采用0.05%(質量分數)SDS分散后將CO2回收率提升至40.87%,分離因子達到3.23,較高質量分數的MWCNTs對水合物生長起促進作用,提高了CO2/CH4混合氣的氣體消耗量。RENAUT等[59]研究了氧功能化MWCNTs對TBAB-水CO2半粘合酸鹽體系的影響,MWCNTs僅在誘導時間1 h內增加了氣體消耗率,1 h后影響減弱,氣體消耗率最大提高15%。
由表4可知,適當含量的MWCNTs可提高CO2水合物的生長速率、縮短誘導時間以及增加CO2消耗量,過量的MWCNTs會表現出抑制的效果。CNTs中典型水合物的形成方式如圖2所示,由于在CNTs管徑孔隙中形成了納米限域效應,LIU等[60]提出當CO2進入充滿水的CNTs中時,CO2被管壁及附著水大量吸附(I),隨著CO2濃度的增加,進一步置換孔隙中的水(II-IV),大量CO2水合物晶體在管壁夾縫的孔隙外形成。以CNTs為代表的多孔材料可以通過納米限域效應促進水合物的形成,其作用歸因于納米孔隙約束條件下的氫鍵作用和空間不均勻性[61],但水合物形成機理需進一步通過原位表征實驗驗證。
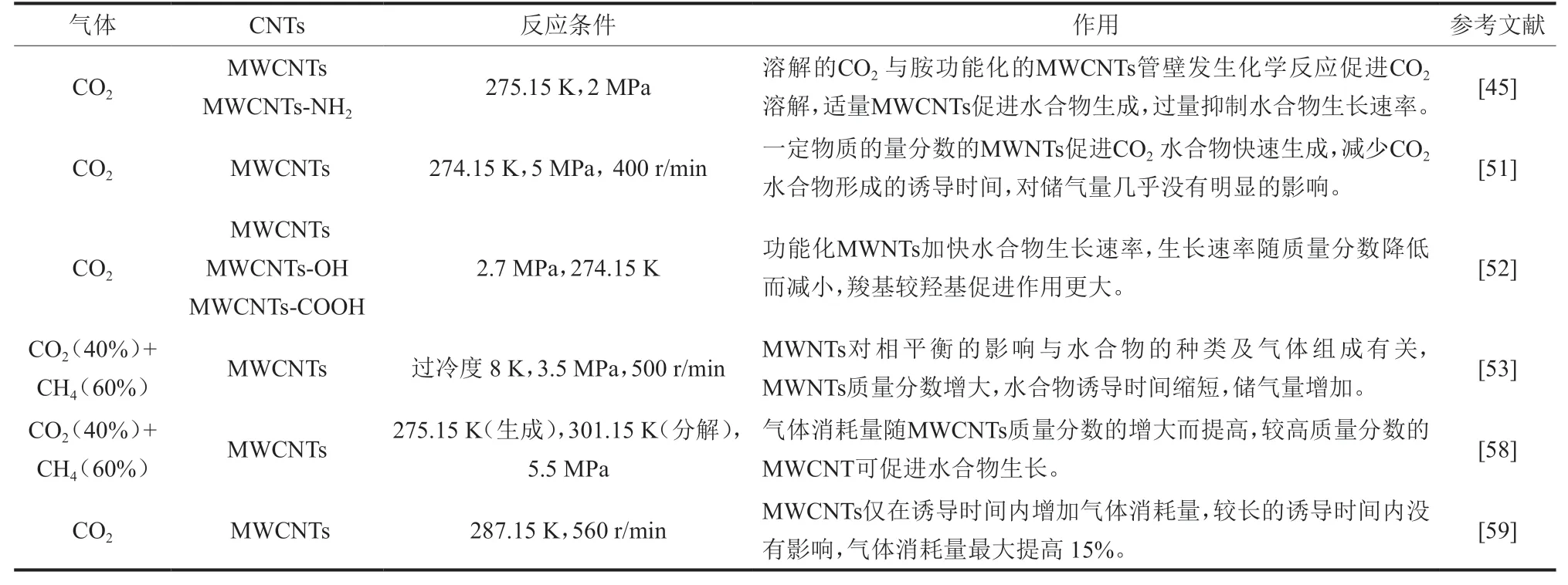
表4 不同CNTs用于CO2水合物的作用比較Table 4 Comparison of effects of different CNTs on CO2hydrate

圖2 基于SWCNTs的CO2水合物的形成方式Fig.2 CO2hydrate formation based on SWCNTs
3 水合物法捕集CO2應用前景
與天然氣水合物技術相比,CO2水合物的相平衡條件較低,較易生成,因此水合物法捕集CO2有望在水合物利用技術方面取得重大突破。水合物法捕集CO2技術具有儲氣量高、工藝簡單和操作條件溫和等特點,目前在天然氣水合物置換開采[62]、儲運[63]及氣體分離領域[64]表現出良好的應用潛力。天然氣水合物置換開采既能將CO2轉化為水合物穩定封存于海底,又能從水合物中開采天然氣,在減輕溫室效應的同時可穩固海床、減少地質災害、避免環境污染,并實現CO2的減排和CH4清潔能源的獲取。此外,由于水合物儲氣量巨大,僅需0.8 m3的水便可存儲約170 m3的CO2,可大大節約運輸空間、降低成本。另外,利用氣體水合物相平衡的特性可有效實現合成氣(H2與CO2)[65]、沼氣(CH4與CO2)[66]、煙道氣(N2與CO2)[16]等含低濃度CO2混合氣的分離與提純,有望在分離氣體領域實現工業化應用。
但目前此技術仍存在諸多問題:(1)CO2水合物生長速率慢,迫切需要開發高效、綠色動力學促進劑,以及滿足低濃度CO2水合物生成的多元復配促進劑(熱力學促進劑、動力學促進劑和離子液體等);(2)高壓低溫環境及反應條件相對苛刻,間歇式反應使得工業應用不成熟,研究仍處于中試或實驗室階段;(3)水合物結晶中夾帶濃縮液,后期分離較為困難。為有效解決分離效果差的問題,2007年,LINGA等[67]提出了水合物結合膜分離法分離煙氣中CO2的混合工藝,如圖3所示。以物質的量分數為1%的THF作為添加劑,在273.75 K、2.5 MPa條件下,使用CO2濃度為17.0%的煙氣生成水合物。經多級分離后,可提純CO2濃度至94.0%[68];XU等[69]研發了水合物法聯合化學吸收法連續分離氣體的工藝裝置,如圖4所示。可通過從合成氣中分離CO2,目前該工藝裝置每日處理氣體量為521 m3,CO2捕獲率可達99.0%以上。
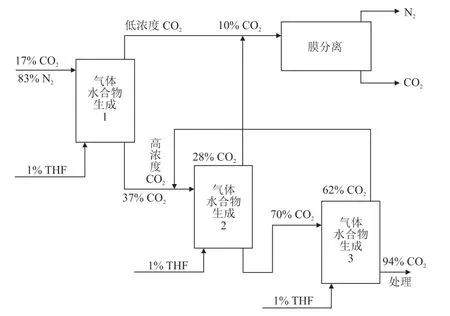
圖3 水合物結合膜分離法分離煙氣中CO2的混合工藝流程Fig.3 Mixing process flow for separating CO2from flue gas by hydrate combined with membrane separation method

圖4 水合物法聯合化學吸收法分離CO2的工藝流程Fig.4 Process flow of CO2separation by hydrate method combined with chemical absorption method
4 結語與展望
本文綜述了CNTs及功能化CNTs在CO2水合物領域的應用,并分析了其對氣體溶解階段、水合物誘導成核階段和水合物快速生長階段的影響,展望了水合物技術用于捕集CO2的應用前景。CNTs對CO2水合物不同生長階段的作用效果主要如下:(1)CNTs的納米多孔結構及表面修飾親水性官能團與CO2產生的范德華相互作用,使得CO2在溶液中吸附溶解,可有效強化CO2在氣-液界面吸附溶解的傳質過程;(2)CNTs表面官能團及金屬納米粒子修飾為水合物異相成核提供豐富的成核位點,CNTs的納米限域效應可縮短水合物的誘導時間,加快CO2水合物微晶的形成;(3)CNTs優良的導熱性能有利于在水合物快速生長期過程的熱量傳遞,進一步加快水合物晶粒的生長與聚集,從而加快水合物大量形成。
為實現水合物法捕集CO2技術邁向工業化,應從以下方面著力研究:(1)開發低能耗、綠色環保可回收的動力學促進劑(如CNTs等多孔納米材料)或研發多元復配促進劑(如二元/三元動力學促進劑、熱力學促進劑和離子液體等),在降低水合物生成的相平衡條件的同時,提高CO2水合物生長速率;(2)優化水合物捕集分離工藝,并聯合其它處理方法提高CO2分離效率;(3)進行工業成本經濟測算,適當展開大型中試實驗,為工業化應用提供參考。

