老年輕度認知障礙患者睡眠障礙與認知功能的關系
李鐘梅,冉 麗,蔣 依,郭志偉,母其文
(1.南充市中心醫院 影像科,四川 南充 637000;2. 西南醫科大學 臨床醫學院,四川 瀘州 646000)
睡眠是人體重要的生理功能,是維持良好精神狀態的保證。多種形式的睡眠障礙(sleep disorders,SD)與認知功能下降有關,是老年患者發生認知障礙的危險因素之一。輕度認知功能障礙(mild cognitive impairment, MCI)是個人日常認知功能的損害超過年齡和教育程度的預期,但不會影響日常生活活動的癥候群,是介于正常老年化和癡呆的一種臨界狀態。雖然MCI不同于癡呆癥,后者會破壞患者的日常功能并產生更嚴重的認知缺陷,但有記憶障礙的MCI患者已被證明發展為癡呆癥的風險較高。MCI患者SD的患病率是認知正常老年人群的3倍以上[1]。SD會影響患者生活質量,加速認知功能衰退,增加癡呆的患病風險[1]。本研究對MCI患者的認知功能和睡眠狀況進行評價,并研究兩者之間的關系,探討SD對MCI患者認知功能的影響,為及時干預SD、延緩MCI患者認知功能減退提供一定的臨床依據。
1 資料與方法
1.1病例選擇 選取2018年11月至2019年1月四川省南充市某社區的MCI患者171例,其中男性61例,女性110例。納入標準:①符合2018中國癡呆與認知障礙診治指南[2]中MCI的診斷標準。②年齡60~<80歲。③蒙特利爾認知評估量表基礎版(Montreal cognitive assessment-basic,MoCA-B)評分情況:小學及以下學歷評分≤19分,中學學歷≤22分,大學學歷≤24分;簡明精神狀態量表(mini-mental status examination,MMSE)評分:文盲者評分>17分,小學學歷評分>20分,初中及以上評分>24分;臨床癡呆評定量表(clinical dementia rating,CDR)評分=0.5;日常生活能力量表(activity of daily living scale, ADL)評分≥26分;功能活動問卷(functional activities questionnaire, FAQ)評分≥9分。④配合研究涉及的相關檢查,簽署知情同意書。排除標準:①其他導致認知障礙的疾病,如腦血管病、腦積水、腦腫瘤及顱內感染等;②嚴重的內科疾病,如心肺功能不全、肝腎功能不全等慢性消耗性疾病;③精神分裂癥等精神障礙性疾病;④藥物或酒精等物質濫用史;⑤嚴重的頭部外傷史;⑥服用可引起認知障礙的藥物;⑦嚴重視力、聽力障礙或其他嚴重影響檢查的情況。
1.2方法
1.2.1一般資料 記錄患者的人口學資料,包括性別、年齡、受教育水平等。
1.2.2總體睡眠評價 采用匹茲堡睡眠質量指數(Pittsburgh sleep quality index,PSQI)量表評估患者的總體睡眠情況,該量表包括18個測評項目,歸納為7個子項目,包括主觀睡眠質量、入睡時間、睡眠時間、睡眠效率、夜間睡眠障礙、催眠藥物使用及日間功能障礙,每項評分0~3分,總分0~21分,分值越高,代表睡眠質量越差。根據測評結果進行分組,評分≥7分為MCI伴SD組(MCI-SD組),評分<7分為MCI不伴SD組(MCI-NSD組)[3]。
1.2.3認知功能評估 ①MoCA-B:一種比較靈敏、可靠的工具量表,包括10個子項目,評分越高,表明總體認知能力越好。②MMSE:簡便易實行且應用廣泛的評估總體認知功能的量表,包括5個子項目,評分越高,表明受試者總體認知能力越好。③聽覺詞匯學習測驗(auditory verbal learning test,AVLT):評估患者的記憶功能,記錄延遲回憶與再認詞語個數,每對一個記一分,分值越高提示記憶功能越好。④波士頓命名測試(Boston naming test,BNT):評估患者的語言功能,20秒內正確命名該圖形則給分,分值越高提示語言功能越好。⑤動物語言流暢性(animal verbal fluency test,AFT):評估患者語言功能, 要求被試者在1 分鐘內說出或寫出盡可能多的某一類屬的詞, 每說對一詞得1分, 得分越高表示越流暢。⑥形狀連線測試(trail making test, TMT):評估患者的執行功能,記錄測試題A、B的總耗時數,耗時越長提示執行功能越差。
2 結 果
2.1人口學資料 在171例MCI患者中, MCI-SD組70例(40.9%),MCI-NSD組101例。兩組性別、年齡、受教育水平等差異無統計學意義(均P<0.05),見表1。

表1 兩組人口學資料比較
2.2兩組總體睡眠情況比較 MCI-SD組PSQI量表總分及各子項目評分均明顯高于MCI-NSD組,主觀睡眠質量更差、入睡時間更長、睡眠時間更短、睡眠效率更低、SD更重、使用催眠藥物更多、日間功能障礙更明顯,見表2。
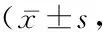
表2 兩組PSQI量表及其子項目比較分)
2.3認知功能 與MCI-NSD組相比,MCI-SD組MoCA-B、MMSE、BNT評分明顯降低,TMT-A總耗時數明顯增加(均P<0.05),見表3。
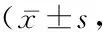
表3 兩組認知功能比較分)
2.4MCI-SD組認知功能與睡眠狀況的相關性分析 Pearson相關性分析發現,MCI-SD組入睡時間與MMSE總分呈負相關,與TMT-A總耗時數呈正相關;睡眠效率與MMSE總分呈負相關;PSQI總分與MoCA-B及MMSE總分呈負相關,與TMT-A總耗時數呈正相關,見表4。

表4 MCI-SD組認知功能與睡眠狀況的相關性分析
2.5MCI合并SD的危險因素分析 以是否患有SD為因變量,性別、年齡、受教育水平、MoCA-B、MMSE、AVLT、BNT、VFT總分、TMT總耗時數為自變量進行多因素Logistic回歸分析,結果發現BNT、TMT-A總耗時數是MCI患者合并SD的獨立危險因素(均P<0.05),見表5。

表5 MCI患者合并SD的危險因素分析
3 討 論
睡眠可促進神經元的恢復和重塑,而睡眠剝奪損害認知功能[4]。有研究發現,睡眠質量差與額葉皮層灰質體積減小有關,同時SD也增加了額葉、顳葉和頂葉區域萎縮率[5]。因此,SD不僅損害身體健康,同時破壞大腦的認知功能,降低患者的生活質量。認知障礙患者,如MCI患者可表現出SD,改善SD有助于延緩患者認知功能的進行性衰退。
國外一項研究發現,40%的阿爾茨海默病(AD)患者存在SD[6]。MCI患者的SD研究相對較少,意大利一項納入431例老年患者的研究發現,MCI各類型的SD與AD患者SD的發病率大致相同[7]。本研究采用PSQI量表評價總體睡眠狀況,以PSQI總分≥7分判定為SD,結果發現40.9%的MCI患者存在SD,表明SD是MCI患者常見的臨床癥狀。PSQI量表涵蓋主觀睡眠質量、入睡時間、睡眠時間、睡眠效率、夜間睡眠障礙、催眠藥物及日間功能障礙共7個方面,我們發現,MCI-SD組上述表現明顯重于MCI-NSD組,表明MCI患者的SD表現在多方面受損。這與郭鵬等[8]的研究結果相似。
本研究發現,MCI-SD組總體認知、語言及執行功能均較MCI-NSD組明顯降低。已有研究發現過類似結果,Lim等[9]的前瞻性研究發現:SD程度與老年癡呆發生率及認知功能下降密切相關。睡眠明顯影響MCI患者語言及執行功能的原因可能包括:SD嚴重影響多種神經遞質的代謝(如γ-氨基丁酸、環磷酸腺苷), 從而嚴重影響突觸的可塑性[10]。一些細胞活性降解產物,如β淀粉樣蛋白(Aβ)低聚體和淀粉樣蛋白沉積, 可導致神經通路及細胞內外離子紊亂, 從而引起神經元損傷[11]。動物和人類腦脊液中Aβ水平存在晝夜生理波動,清醒和睡眠減少時增加,SD患者多個腦區Aβ沉積均增加[12-13], 從而導致認知功能障礙,影響MCI患者的語言及執行功能。同時本研究發現,MCI患者的語言及執行功能也影響著睡眠,語言及執行功能越差導致SD的可能性越大。因此,睡眠和認知功能障礙之間存在密切聯系,目前研究支持SD通過多種途徑參與認知障礙的發生和發展,并有助于早期預測癡呆類型的發展,同時認知功能下降加重SD,兩者之間存在雙向關系[14]。
本研究結果顯示,MCI患者的PSQI總分及入睡時間與總體認知功能及執行功能相關,睡眠效率與總體認知功能相關。一項社區人群的前瞻性研究[15]也發現了類似結果,即睡眠效率降低與認知功能下降風險的增加密切相關。對上述結果的原因分析有以下幾個方面:①乙酰膽堿可通過作用乙酰膽堿受體來調節海馬體中的神經元興奮性[16],參與學習記憶及認知注意。MCI伴SD患者的認知損害可能與乙酰膽堿的異常合成分泌有關。②認知功能與大腦的血流量及分布密切相關,大腦半球局部供血不足,將會導致認知功能障礙。前額葉皮質是調節執行功能的重要結構[17],MCI伴SD患者由于入睡時間延長、睡眠質量不佳會引起前額葉皮質的血流量明顯下降[18],從而造成執行功能的損害。③腦皮質尤其是內側額葉皮質的萎縮,影響慢波睡眠對睡眠紡錘波的協調,由此損害夜間記憶整合,從而導致遺忘[19]。入睡時間延長及睡眠效率減低,可能引起大腦顳頂區神經網絡變化以及使影響夜間記憶整合的睡眠紡錘波減少[7],從而影響認知功能。④慢性睡眠剝奪可能直接引起注意力、學習、記憶力及執行功能的下降[20]。入睡時間延長及睡眠效率減低可使實際睡眠減少而導致慢性睡眠剝奪。
本研究存在一些局限性,未對患者進行隨訪。綜上,MCI患者中SD的發生率較高;MCI伴SD患者的SD體現在多個方面;MCI伴SD患者的認知與睡眠相互影響。臨床醫師應高度關注MCI伴SD患者,對MCI患者的認知功能和睡眠狀況定期進行評價,及早干預SD、從而延緩MCI的惡化,提高患者的生活質量,減輕照護負擔。

