新生兒高促甲狀腺素血癥圍產期危險因素分析
張彩營 ,奎正平 ,王 瓊 ,趙小龍 ,侯曉梅 ,齊志業 1,
(1)昆明醫科大學第一附屬醫院兒科;2)新生兒遺傳代謝病篩查中心;3)產科,云南 昆明 650032)
近年來,隨著新生兒遺傳代謝病篩查工作的開展,越來越多的先天性甲狀腺功能減低癥(congenital hypothyroidism,CH)患兒得到早期診斷和治療[1]。而新生兒遺傳代謝病篩查過程中,促甲狀腺素(thyroid stimulating hormone,TSH)篩查陽性新生兒最終診斷為CH 的患兒相對較少,更多的新生兒診斷為高促甲狀腺素血癥(hyperthyrotropinemia,HT)[2]。目前國內尚無針對HT 的規范治療方案,隨訪過程中亦存在治療不足或過度治療情況[3],并有罹患CH,影響兒童生長發育的可能[4]。國內外關于新生兒CH 圍產危險因素分析較多[5],關于HT 相關危險因素的報道并不多見[6],國內尚未見相關報道。本研究通過病例對照研究探討與新生兒HT 相關的母親和新生兒圍產危險因素,為判斷HT 的預后、制定新生兒隨訪計劃提供指導。
1 資料與方法
1.1 病例資料
選擇2016 年1 月至2020 年12 月在昆明醫科大學第一附屬醫院分娩并接受遺傳代謝病篩查的新生兒為研究對象。對TSH 篩查陽性新生兒進行召回,使用美國Abbott ARCHITECT i2000SR 型全自動免疫分析儀,采用化學發光法完善甲狀腺功能檢查。胎齡 < 34 周或出生體重 < 2 000 g 的新生兒在出生后28 d 或出院時復查甲狀腺功能[7]。TSH 增高、游離甲狀腺素(free thyroxine,FT4)正常者診斷為HT;TSH 增高,FT4 降低者診斷為CH。TSH 的參考范圍為(0.35~4.94)μIU/mL,FT4的參考范圍為(0.70~1.48)ng/dL。召回復查新生兒中,診斷為HT 的新生兒作為病例組,甲狀腺功能檢查正常新生兒作為對照組。所有進行的檢測均獲得新生兒監護人知情同意,并簽署知情同意書。
1.2 研究方法
自行設計調查問卷,并通過預調查進行修改和完善。根據調查問卷內容由經過統一培訓的調查人員查閱產科診療記錄收集臨床數據,并由質量控制人員對收集的資料進行審核,缺失數據通過電話隨訪進行補充。使用統一的軟件進行雙錄入審核,以保證錄入信息的準確性。調查內容包括社會人口學資料、不良孕產史、妊娠期合并癥、新生兒分娩信息及患病情況等。高齡產婦定義為分娩年齡 ≥35 歲[8];不良孕產史包括既往有胚胎停育、死胎、死產、自然流產、不良生育史等病史;妊娠期并發癥[8]、胎兒宮內窘迫[9]的診斷指標參考文獻;新生兒根據出生體重分為低出生體重(< 2 500 g)、正常出生體重(2 500 g~3 999 g)和巨大兒(≥4 000 g),根據胎齡分為早產(胎齡 <37 周)和足月(37 周≤胎齡 < 42 周)。
1.3 統計學處理
采用SPSS 26.0 軟件進行統計學分析。計數資料采用例數及百分比(%)表示。單因素分析采用χ2檢驗,按α=0.10 的水平將單因素分析篩選出的變量納入Logistic 回歸模型。以P< 0.05 為差異有統計學意義。
2 結果
2.1 研究對象基本情況
2016 年1 月至2020 年12 月共完成新生兒遺傳代謝病篩查36 024例,其中TSH 篩查陽性276例,篩查陽性率0.77%。篩查陽性新生兒召回過程中,失訪19例,新生兒死亡5例。完成甲狀腺功能檢查252例,其中母親高齡43例(17.1%),早產39例(15.5%),低出生體重52例(20.6%),需轉兒科治療136例(54.0%)。最終診斷HT 109例,HT 發病率30.3/萬,診斷CH 16例,CH 發病率4.4/萬。甲狀腺功能正常127例。
2.2 新生兒HT 圍產期危險因素的單因素分析
新生兒HT 圍產因素的單因素分析結果表明,病例組高齡產婦和早產的比例均為23.9%(26例),顯著高于對照組(P< 0.05),見表1。

表1 新生兒HT 圍產因素的單因素分析 [n(%)]Tab.1 Univariate analysis of perinatal risk factors for neonatal hyperthyrotropinemia
2.3 新生兒HT 圍產期危險因素的多因素Logistic 回歸分析
對單因素分析中P< 0.10 的因素納入多因素Logistic 回歸模型。變量賦值及多因素分析中變量的參考類別見表2。結果表明,高齡產婦(OR=2.320,95%CI:1.099~4.897)和早產(OR=2.960,95%CI:1.354~6.473)是新生兒HT 發生的危險因素,見表3。
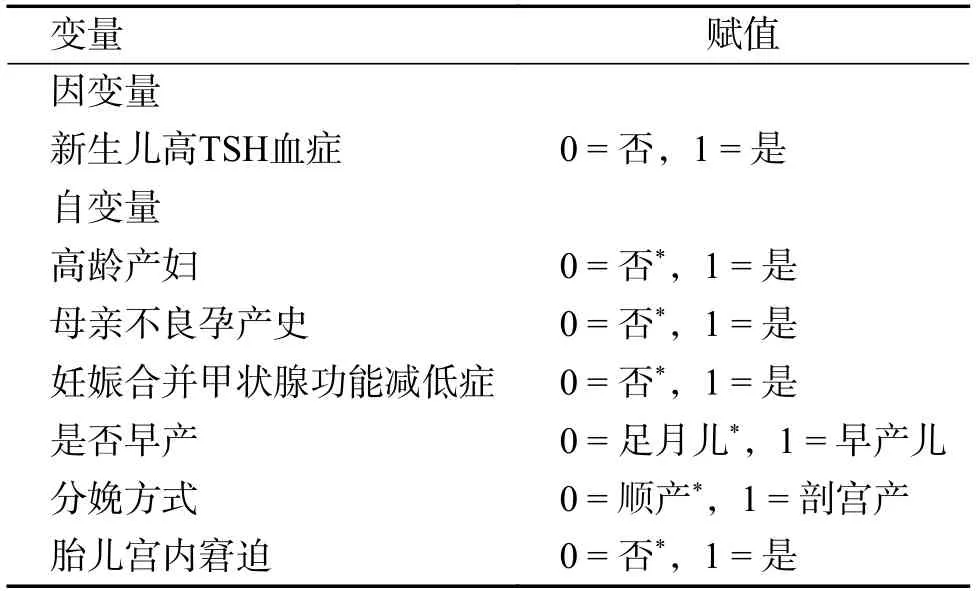
表2 變量賦值表Tab.2 Variable assignment

表3 新生兒HT 危險因素的Logistic 回歸分析Tab.3 Multivariate logistic regression analysis of perinatal risk factors for neonatal hyperthyrotropinemia
3 討論
HT 是涵蓋亞臨床甲狀腺功能減低癥、甲狀腺素不敏感綜合征和TSH 不敏感綜合征的一組疾病[3],可能的病因包括下丘腦-垂體-甲狀腺軸發育不成熟、TSH 對促甲狀腺激素釋放激素敏感性增加、新生兒體內存在抗甲狀腺抗體、甲狀腺發育異常和甲狀腺過氧化物酶或TSH 受體基因突變等[6]。國外關于新生兒HT 危險因素的研究結果并不一致,部分研究結果提示新生兒HT 與母親年齡、妊娠期甲狀腺疾病、新生兒民族、性別、胎齡、分娩方式、出生體重和出生后患病情況等有關[6,10]。我國先天性甲狀腺功能減低癥篩查中,CH 發病率約為4.13/萬[1],HT 發病率約為5.2/萬[11]。本研究中,CH 發病率與以往研究接近,但HT 發病率明顯增高,這可能和本研究中TSH篩查陽性新生兒早產(15.5%)、低出生體重(20.6%)和需進一步轉兒科治療(54.0%)的比例較高而導致新生兒暫時性TSH 增高有關。
Raj S 等[12]的研究提示,隨著母親年齡的增長,新生兒臍帶血TSH > 20.1 mIU/L 的比例明顯增高。中國天津的前瞻性出生隊列研究表明,新生兒TSH 水平與母親年齡呈現正相關關系[13],這些新生兒最終診斷為HT 的概率也明顯增高。本研究結果中,高齡母親所生新生兒發生HT 的風險增加2.320 倍。高齡母親血清可溶性fms 樣酪氨酸激 酶-1(soluble FMS-like tyrosine kinase-1,sFLT1)濃度更高[14]。sFLT1 可與血管內皮生長因子(vascular endothelial growth factor,VEGF)結合,拮抗VEGF 促血管生成作用,并影響胚胎期甲狀腺組織的發育,導致新生兒TSH 增高[15]。同時,高齡母親下丘腦-垂體-甲狀腺軸功能減退,釋放TSH 功能減弱,影響胎兒甲狀腺發育,導致新生兒自身甲狀腺素分泌減少而負反饋調節TSH 增高[16]。
國內關于新生兒TSH 參考區間的研究[17]結果表明,新生兒FT4 水平與胎齡呈正相關,而TSH 水平與胎齡呈負相關;意大利一項回顧性隊列研究[18]提示新生兒TSH 與早產存在明顯的負相關關系,均表明早產是HT 的危險因素。本研究結果也表明,和足月兒相比,早產兒HT 的發生風險增加了2.960 倍。甲狀腺是胚胎發育的第一個內分泌腺,并隨著孕周的增加而逐漸增大。至胚胎第11 周,胎兒甲狀腺開始合成甲狀腺素,但其主要來源于仍依賴母體轉運。孕中期開始,胎兒自身合成甲狀腺素逐漸增多,直至孕36 周達到足月兒水平[19]。而為了滿足胎兒生長發育需求,其TSH 水平也逐漸增加,并且持續高于母體水平[19]。早產兒宮內生長受限,下丘腦-垂體-甲狀腺軸功能和甲狀腺發育不成熟[20],使得其在新生兒早期甲狀腺素和TSH 水平明顯低于足月兒。而出生后腸道吸收碘和甲狀腺聚碘、合成和碘化功能較差[21],加之對甲狀腺素的生理需求增加,導致早產兒TSH 延遲增高,HT 發生率增高。
多項研究表明,母親合并妊娠期甲狀腺疾病可影響新生兒甲狀腺功能[5,22],這可能和母親抗甲狀腺藥物治療和妊娠合并甲狀腺功能減低癥孕婦血清促甲狀腺激素受體抗體(thyroid-stimulating hormone receptor antibodies,TRAbs)受到抑制[23],而甲狀腺過氧化物酶抗體(thyroid peroxidase antibody,TPOAb)濃度增高[24],導致發生HT 的風險增加有關。本研究將母親妊娠合并甲狀腺功能減低癥納入回歸分析,提示母親合并妊娠甲狀腺功能減低癥和HT 的發生風險之間存邊界顯著性(P=0.090),但差異無統計學意義(P> 0.05),這可能和本研究未將母親甲狀腺功能的具體檢測指標(如TSH、FT4 或TPOAB 水平)進行分層分析有關。以往研究表明,經陰道分娩或胎兒宮內窘迫可導致新生兒體內兒茶酚胺濃度增高,影響下丘腦-垂體-甲狀腺軸激素的合成和分泌,從而導致新生兒TSH 增高[25]。但有研究[26]并未發現二者之間相關性,與本研究結果一致,具體原因尚不清楚。因此,關于圍產期因素和新生兒HT 之間的關系仍有待進一步研究。
本研究采用病例對照設計對新生兒HT 的圍產期危險因素進行分析,發現母親高齡和早產是新生兒HT 的危險因素,避免高齡分娩和早產是預防新生兒HT 的重要手段。本研究存在一定的局限性:樣本量小,可能降低統計功效;回歸分析模型并未納入全部與新生兒HT 相關的混雜因素,比如母親甲狀腺功能相關指標、母親體質指數、妊娠期心理壓力和環境有害物質暴露[15]等;新生兒HT 可能與遺傳因素有關[27],本研究并未將研究對象中有甲狀腺相關遺傳病病史的新生兒排除。因此,關于母親和新生兒圍產危險因素與新生兒HT 的相關性仍需大樣本前瞻性出生隊列研究進行檢驗。