硒化綠豆抗性淀粉制備工藝優化及抗氧化活性分析
趙姝婷, 全志剛, 王 娟, 劉德志, 王一飛 武云嬌, 蘇有韜, 王維浩,2, 曹龍奎,2,3
(黑龍江八一農墾大學食品學院1,大慶 163319) (黑龍江八一農墾大學國家雜糧工程技術研究中心2,大慶 163319) (黑龍江省天然產物模擬移動床色譜分離技術創新中心3,大慶 163319)
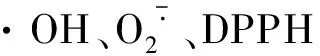
本實驗以綠豆抗性淀粉(MB-RS4)為原料,采用硝酸-亞硒酸鈉法對MB-RS4進行硒化,得到硒化綠豆抗性淀粉[MB-RS4Se(Ⅳ)],并對硒化條件進行優化;通過光學顯微鏡、偏光十字顯微鏡和掃描電鏡觀察MB-RS4Se(IV)光學性質及表觀形態,體外測定抗氧化活性及相關性分析,為開發以抗性淀粉為原料的功能性食品提供了參考。
1 材料與方法
1.1 材料與試劑
1.2 儀器與設備
DGA-9080A電熱恒溫鼓風干燥箱,Aldpha1-2LD plus真空冷凍干燥機,透析袋(Mw:1 000 u);S-570掃描電子顯微鏡,NP-800TRF型偏光顯微鏡,N-800M光學顯微鏡,SPECTROstar Nano酶標儀,Specord 200紫外分光光度計。
1.3 方法
1.3.1 綠豆RS4的制備
根據李蒙娜等[13]的方法并作適當修改。將淀粉與檸檬酸按照干基比5∶2混合,加入適量蒸餾水攪拌均勻,用氫氧化鈉調節混合體系pH至3.5左右,室溫靜置12 h,于40 ℃烘干。取出干燥樣品粉碎過60目篩,取篩下物于150 ℃酯化4 h,反應產物用無水乙醇洗滌3次,37 ℃烘干至含水量為8%,即得MB-RS4。
根據王麗波等[14]的方法并作適當修改。用50 mL體積分數為0.5%的HNO3溶液溶解樣品(1.0 g),在室溫下攪拌30 min,加入1.0 gNa2SeO3和0.7 gBaCl2,將混合物在66 ℃攪拌反應3.5 h。冷卻至室溫滴加1 mol/L的NaOH溶液調節pH至7~8。加入0.5 gNa2SO4除去溶液中的雜質Ba2+,4 000 r/min離心15 min,取上清液后透析出反應產生的無機鹽和多余的Na2SeO3、濃縮、醇沉,凍干即得MB-RS4Se(Ⅳ)。
(1)
式中:m1為綠豆RS4Se(Ⅳ)的質量/g;m為綠豆RS4的質量/g。
根據國家標準[15]選用分光光度法測MB-RS4Se(Ⅳ)中硒含量[16]。用移液管分別吸取0.1、0.2、0.4、0.8、1.6 mL的硒標準溶液至25 mL容量瓶,加入2 mL鄰苯二胺(2%)用HCl定容并調節pH至2,避光反應1 h,最后用5 mL甲苯萃取,在334 nm處測定有機相吸光度,測得硒標準曲線方程y=19.380 21x-0.042 04,線性相關系數R2=0.995 7,其中:y為硒含量(mg),x為吸光度。
5 mg樣品中加入2 mL HNO3,4 ℃放置過夜。將樣品加熱至燒杯中無橙黃色煙霧生成,冷卻至室溫加入6 mol/L的鹽酸8 mL繼續加熱至無白色煙霧生成,轉移至25 mL容量瓶,根據標準曲線測定方法測定樣品溶液吸光度,并用式(2)計算樣品中硒含量。

(2)
式中:ρ為有機相中硒的質量濃度/mg/mL,由標準曲線方程得出;V1為定容后待測溶液體積(25 mL);V2為有機相總體積(5 mL);V3為萃取前待測溶液體積(2 mL);m為MB-RS4Se(Ⅳ)質量(5 mg)。
1.3.5 MB-RS4·Se(Ⅳ)工藝條件研究1.3.5.1 MB-RS4·Se(Ⅳ)制備工藝單因素實驗
將樣品溶解于一定體積分數的HNO3(0.1、0.3、0.5、0.7、1%)中,并在室溫下處理30 min,改變樣品與Na2SeO3的物料比(1∶0.6、1∶0.8、1∶1.0、1∶1.2、1∶1.4),反應溫度(40、50、60、70、80 ℃)和反應時間(2、3、4、5、6 h)進行實驗。
以HNO3(A)、物料比(B)、反應溫度(C)、反應時間(D)為自變量,通過Box-Behnken設計四因素三水平的響應面實驗,再分別以硒含量和MB-RS4·Se(Ⅳ)得率為響應值,考察各因素對于響應值的影響程度,響應面實驗因素水平見表1。

表1 Box-Behnken響應面實驗設計因素與水平
1.3.6 光學特征及體外抗氧化性分析1.3.6.1 光學顯微鏡測定
將樣品溶于30%甘油中,混合均勻后取一滴滴在載玻片上,蓋上蓋玻片無氣泡后置于光學顯微鏡下觀察,調整物鏡倍數和焦距,直至能清晰看到顆粒形態和偏光十字即可,保存圖片。
1.3.6.2 掃描電子顯微鏡(SEM)測定
根據Asad等[18]的方法并作適當修改對樣品的形貌和微觀結構進行研究。將樣品置于雙面膠帶噴金,于50.0 kV收集圖像。
1.3.6.3 羥基自由基清除能力
羥自由基通常以反應Fe2++H2O2=Fe3+OH-+·OH產生[19]。參照Huang等[20]的方法并作適當修改,測定樣品對羥基自由基清除能力。按式(3)計算羥基自由基清除率。
(3)
式中:A0為空白對照在510 nm的吸光度;A1為待測樣品在510 nm的吸光度。
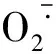
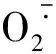
(4)
式中:A0為空白對照在330 nm的吸光度;A1為待測樣品在330 nm的吸光度。
1.3.6.5 ABTS自由基清除能力
ABTS自由基清除能力參照Li等[22]的方法并作適當修改。按式(5)計算ABTS自由基清除率。
(5)
式中:A1為0.2 mL樣品稀釋液+1.2 mLABTS稀釋液;A2為0.2 mL樣品稀釋液+1.2 mL無水甲醇;A0為0.2 mL無水甲醇+1.2 mLABTS稀釋液。
1.3.6.6 總抗氧化能力測定
采用鐵離子還原能力法測定樣品的總抗氧化能力,參照Huang等[23]的方法并作適當修改,每個樣品平行測定3次。
1.4 數據處理與分析
所有實驗均設置3組平行,數據用平均值±標準差表示,采用SPSS Statistics 25和Excel 2020對數據進行顯著性分析及相關性分析,采用Design Expert 11進行響應面分析,以P<0.05表示差異顯著,使用Origin 2019b進行繪圖。
2 結果與分析
2.1 單因素實驗結果與分析
由圖1知,4 h時得率達到最大值23.35%,硒含量為2.04 mg/g。隨著反應時間的延長,得率降低。結果表明,合成MB-RS4Se(Ⅳ)與時間密切相關,時間短底物MB-RS4與Na2SeO3反應不充分,時間過長會促進MB-RS4降解,導致得率降低[25]。
圖1中硝酸體積分數對產物得率及硒含量的影響較大,硝酸體積分數達到0.5%,得率及硒含量達到最大值;但硝酸體積分數超過0.5%,得率及硒含量呈下降趨勢,是因為在較高濃度的硝酸存在下(硝酸屬于強酸,可導致降解,不利于硒化反應),MB-RS4的羥基被氧化或者斷鏈等因素有關[26]。因此選擇硝酸體積分數為0.5%。
由圖1知MB-RS4和亞硒酸鈉的質量比從1∶0.6到1∶1.4過程中反應未飽和,隨反應物的增加反應趨于正反應階段,但當質量比達到1∶1后,反應底物MB-RS4完全轉化,再加入過量的亞硒酸鈉,反應則向逆反應方向進行,產物得率及硒含量則降低。這可能是由于飽和結合位點引起的非特異性攝取[25]。因此選擇最佳物料比為1∶1。
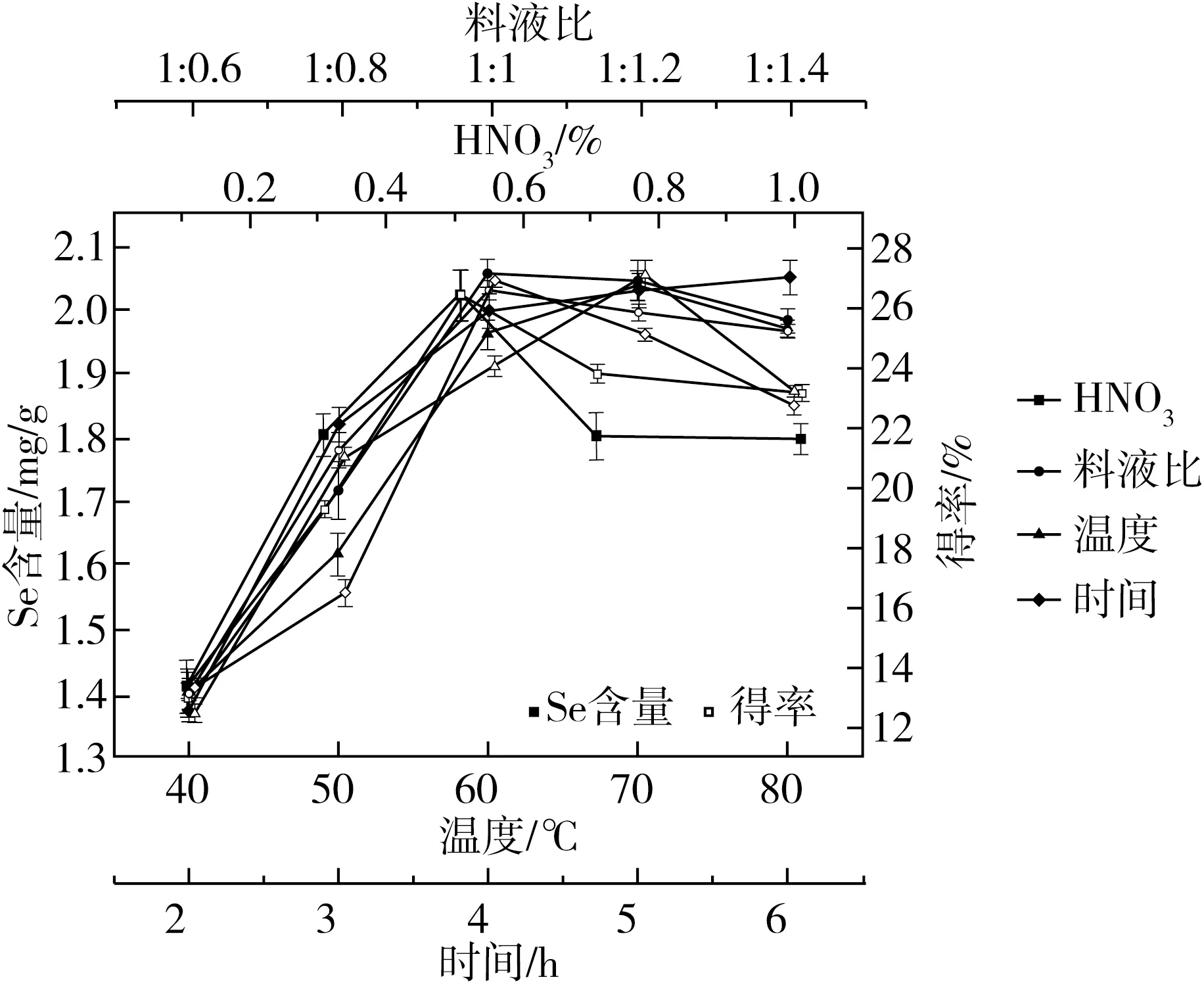
圖1 單因素實驗結果
2.2 響應面實驗結果與分析
2.2.1 硒化MB-RS4的Box-Behnken響應面實驗結果

表2 Box-Behnken實驗設計與結果
利用Design-Expert 11軟件對實驗數據進行多元回歸擬合,得到二次多項回歸方程:
Se含量=2-0.40A-0.021B-1.57C-1.63D-0.095AB+0.25AC+0.16AD-0.13BC+0.14BD+4.8CD-0.85A2-0.93B2+1.58C2+1.54D2
MB-RS4·Se(Ⅳ)得率=27.30+1.91A-1.37B-1.69C+0.35D-2.19AB+2.85AC-1.25AD-0.61BC+2.49BD+2.57CD-1.55A2-4.35B2-5.08C2-0.71D2
對回歸方程進行方差分析,見表3。其中,F值可用來檢驗各變量對響應值影響的顯著性的高低,F值越大,則相應變量的顯著程度越高。當模型的顯著性檢驗概率P<0.05時,認為該模型具有統計學意義。由表3知,2個模型的P值均小于0.01,表明模型對響應值有極顯著影響,且失擬相P值均大于0.05(即不顯著),表明2個模型都具有高度的擬合度,并且實驗誤差很小,能夠準確描述各因素與響應值之間的關系,即可以用這2個模型對硒化的得率和硒含量進行分析和預判。
表3 響應Se含量及MB-RS4Se(IV)得率 擬合回歸方程的方差分析結果

表3 響應Se含量及MB-RS4Se(IV)得率 擬合回歸方程的方差分析結果
方差來源MB-RS4?Se(IV)得率擬合Se含量擬合F值P值顯著性F值P值顯著性回歸模型73.21<0.000 1??4 028.64<0.000 1??A97.50<0.000 1??1 455.20<0.000 1??B49.88<0.000 1??328.33<0.000 1??C76.22<0.000 1?7.740.014 7?D3.240.093 22 498.86<0.000 1??AB42.44<0.000 1??276 4.96<0.000 1??AC72.17<0.000 1??17 975.45<0.000 1??AD13.910.002 2?790 7.28<0.000 1??BC3.270.091 9508 4.19<0.000 1??BD55.10<0.000 1??5 484.37<0.000 1??CD58.70<0.000 1??173 9.59<0.000 1??A234.39<0.000 1??231 0.74<0.000 1??B2272.02<0.000 1??9 540.82<0.000 1??C2371.37<0.000 1??3.900.068 3D27.230.017 7?634.78<0.000 1??失擬項0.200.982 80.820.640 5R20.986 50.998 9R2Adj0.973 10.999 5信噪比28.287220.951
實驗數據的殘差和響應面設計如圖2a所示,圖2b為不同水平條件MB-RS4·Se(Ⅳ)響應值的殘差正態分布概率圖, 29組響應值較為合理地分布于一條直線兩側,且其方差無偏差顯示,本實驗的實驗值與預測值非常接近,表明本實驗所建立的模型成功地加強了4個變量參數與響應之間的關系。通過建模擬合,對內部殘差與29組實驗運行數據進行分析,如圖2c所示,所有數據點都位于極值之間,所有杠桿點都小于2,處于樣本空間中心,表明實驗模型中沒有有效誤差存在,如圖2d所示,相反,由圖2e知,Cook’D的值在確定的范圍內,說明29組實驗數據中沒有影響模型的觀察值,通過回歸診斷分析,說明本實驗建立的MB-RS4·Se(Ⅳ)改性工藝模型準確性較高,可以用于綠豆酯化淀粉的硒化改性制備。
實驗數據的殘差和響應面設計如圖3所示,圖3a為不同水平條件MB-RS4·Se(Ⅳ)響應值的殘差正態分布概率圖, 29組響應值較為合理地分布于一條直線兩側,且其方差無偏差顯示,本實驗的實驗值與預測值非常接近,如圖3b所示,表明本實驗所建立的模型成功地加強了4個變量參數與響應之間的關系。通過建模擬合,對內部殘差與29組實驗運行數據進行分析,如圖3c所示,所有數據點都位于極值之間,所有杠桿點都小于2,處于樣本空間中心,表明實驗模型中沒有有效誤差存在,如圖3d所示,相反,由圖3e知,Cook’D的值在確定的范圍內,說明29組實驗數據中沒有影響模型的觀察值,通過回歸診斷分析,說明本實驗建立的MB-RS4·Se(Ⅳ)改性工藝模型準確性較高,可以用于MB-RS4的硒化改性制備。
2.2.5 最優條件確定和驗證
應用響應面最優分析方法對回歸模型分析,確定最優工藝條件為:HNO3體積分數0.46%,物料比1∶0.98,反應溫度66.56 ℃,反應時間3.5 h,Se含量為2.22 mg/g,MB-RS4Se(Ⅳ)得率為26.293 5%。為適應實際生產需求對工藝參數優化,在HNO3體積分數0.5%,物料比1∶1,反應溫度66 ℃,反應時間3.5 h下進行反應,經3次重復實驗得到Se含量為2.21 mg/g,MB-RS4Se(Ⅳ)得率為26.450 6%。
2.3 MB-RS4和MB-RS4Se(Ⅳ)光學特征及抗氧化分析
2.3.1 光學特征分析
由圖4可知,綠豆淀粉中交替存在結晶區和非結晶區,偏光十字出現“馬耳他十字”。綠豆淀粉顆粒大部分呈現橢圓形,少數為球形,表面光滑,有典型的偏光十字[30,31]。通過檸檬酸酯化處理綠豆淀粉后,綠豆淀粉分子鏈在酸熱運動下,分子中心晃動,原子尺寸數量級的空穴增多并伴隨著顆粒結構坍塌[29],通過光學顯微鏡和掃描電鏡觀察可以發現MB-RS4出現了不同程度的交聯、抱團現象,形成了形狀不規則、結晶結構破壞和偏光十字逐漸消失的MB-RS4。在此基礎上對MB-RS4進行硒化改性得到MB-RS4·Se(Ⅳ),MB-RS4·Se(Ⅳ)顆粒結構破碎,呈現不規則的碎片狀態,偏光十字完全消失,是由于引入Se4+時MB-RS4斷鏈發生降解,導致MB-RS4形態碎片化嚴重。
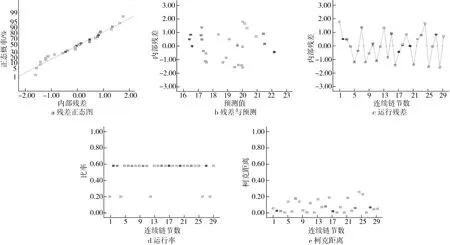
圖2 MB-RS4Se(Ⅳ)得率準確性分析
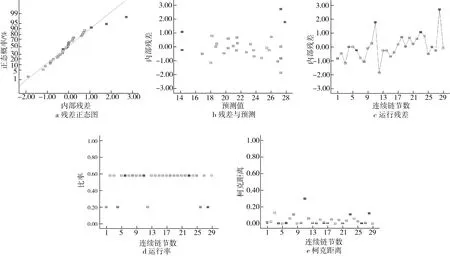
圖3 MB-RS4Se(Ⅳ)硒含量準確性分析

注:光學顯微鏡放大倍數為目鏡10×;物鏡20×。圖4 MBS (1)、MB-RS4 (2)、MB-RS4Se(Ⅳ)(3) 光學顯微鏡(a)、偏光十字顯微鏡(b)、掃描電鏡(c)
2.3.2 抗氧化活性及相關性分析
硒化前后MB-RS4和VC的還原能力如圖5d所示,硒化前的吸光度保持在0.1~0.2,硒化后吸光度隨質量濃度升高而增加,當質量濃度達到10mg/mL時,吸光度值接近陽性對照VC。說明MB-RS4的還原能力幾乎沒有,硒化后的MB-RS4還原能力大幅度增加。
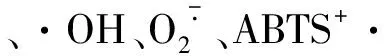


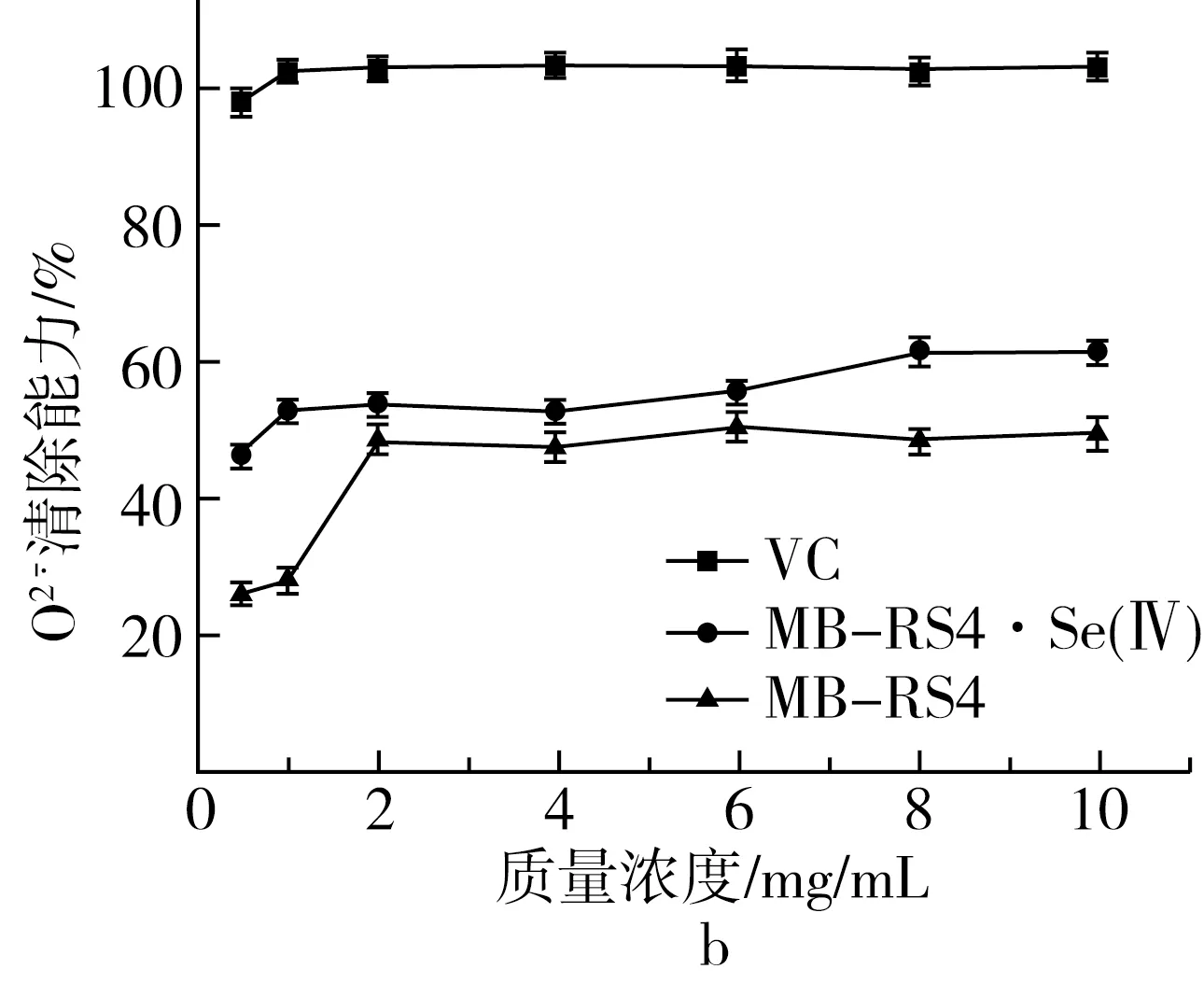


圖5 MB-RS4、MB-RS4Se(Ⅳ)和VC對 ABTS+·清除能力及總還原能力
表4 MB-RS4、MB-RS4Se(Ⅳ)和VC IC50值及其相關性
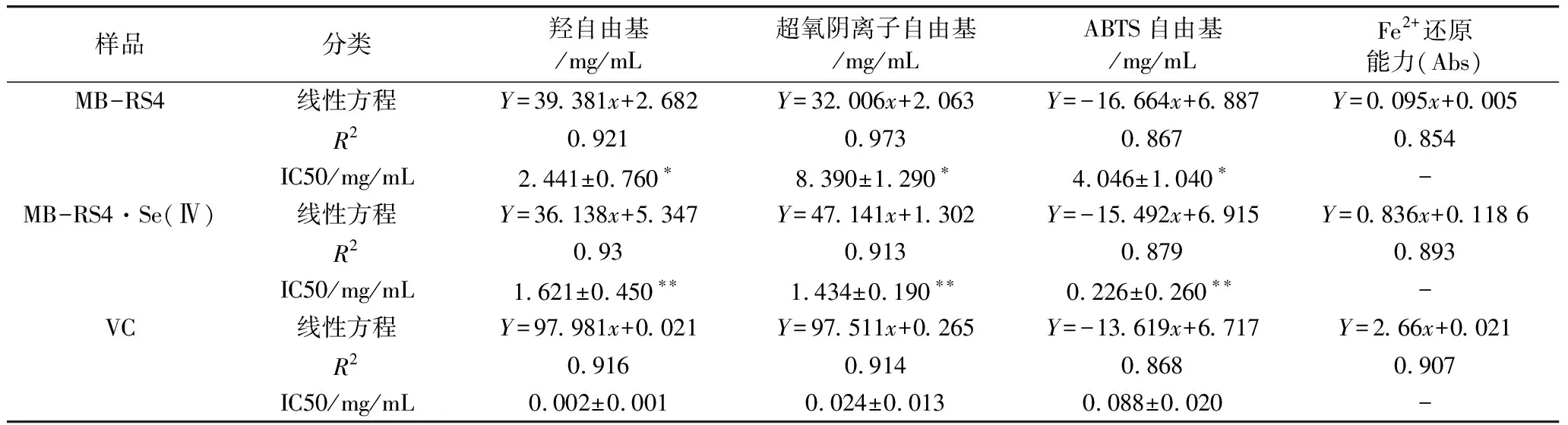
表4 MB-RS4、MB-RS4Se(Ⅳ)和VC IC50值及其相關性
樣品分類羥自由基/mg/mL超氧陰離子自由基/mg/mLABTS自由基/mg/mLFe2+還原能力(Abs)MB-RS4線性方程Y=39.381x+2.682Y=32.006x+2.063Y=-16.664x+6.887Y=0.095x+0.005R20.9210.9730.8670.854IC50/mg/mL2.441±0.760?8.390±1.290?4.046±1.040?-MB-RS4·Se(Ⅳ)線性方程Y=36.138x+5.347Y=47.141x+1.302Y=-15.492x+6.915Y=0.836x+0.118 6R20.930.9130.8790.893IC50/mg/mL1.621±0.450??1.434±0.190??0.226±0.260??-VC線性方程Y=97.981x+0.021Y=97.511x+0.265Y=-13.619x+6.717Y=2.66x+0.021R20.9160.9140.8680.907IC50/mg/mL0.002±0.0010.024±0.0130.088±0.020-
注:IC50值表示自由基清除率為50%的有效質量濃度,*為顯著,**為極顯著。
2.3.3 抗氧化能力表型分析
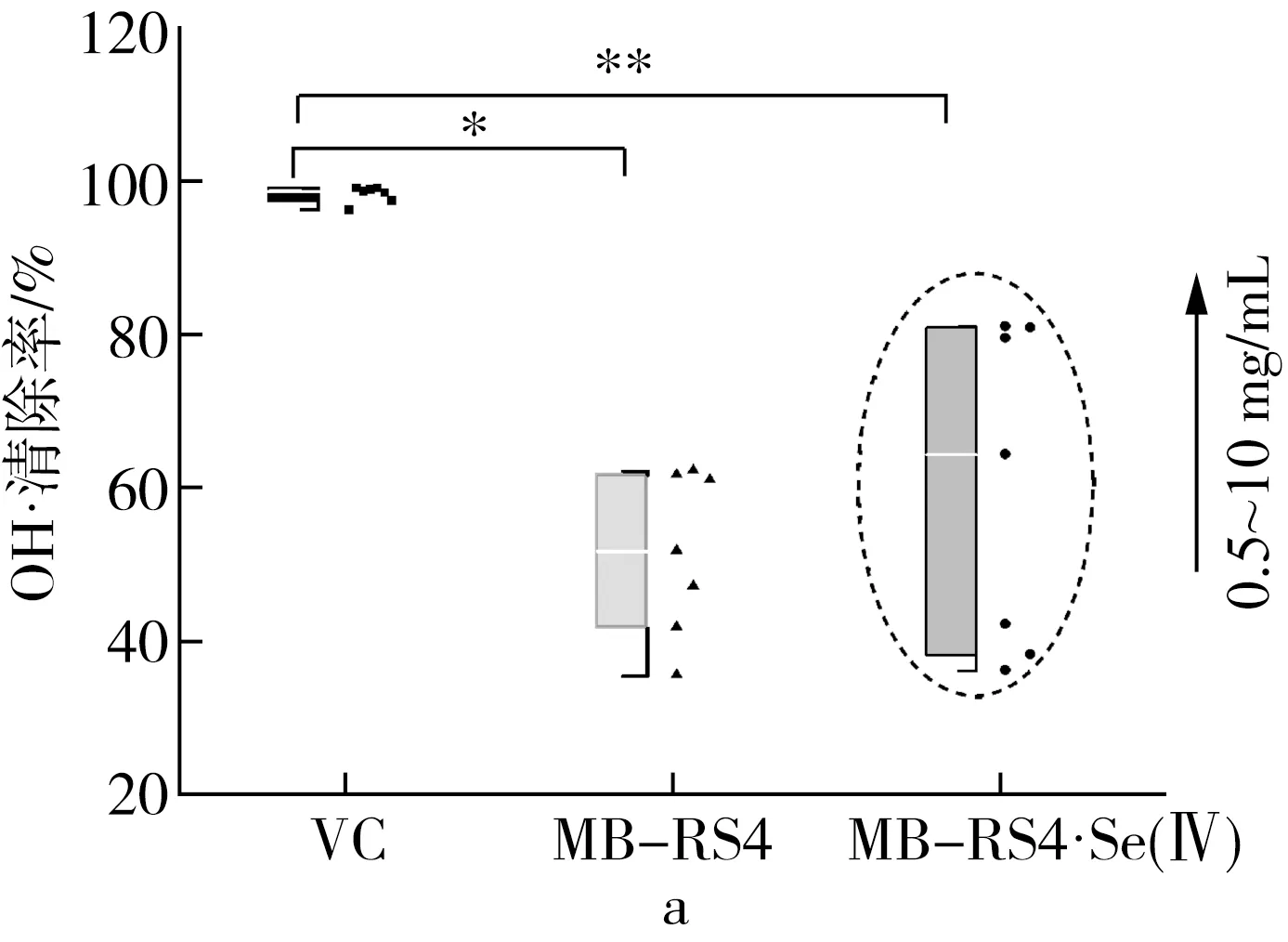
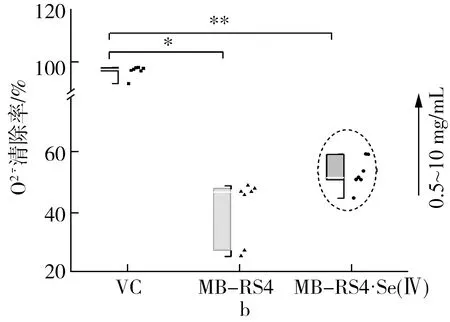
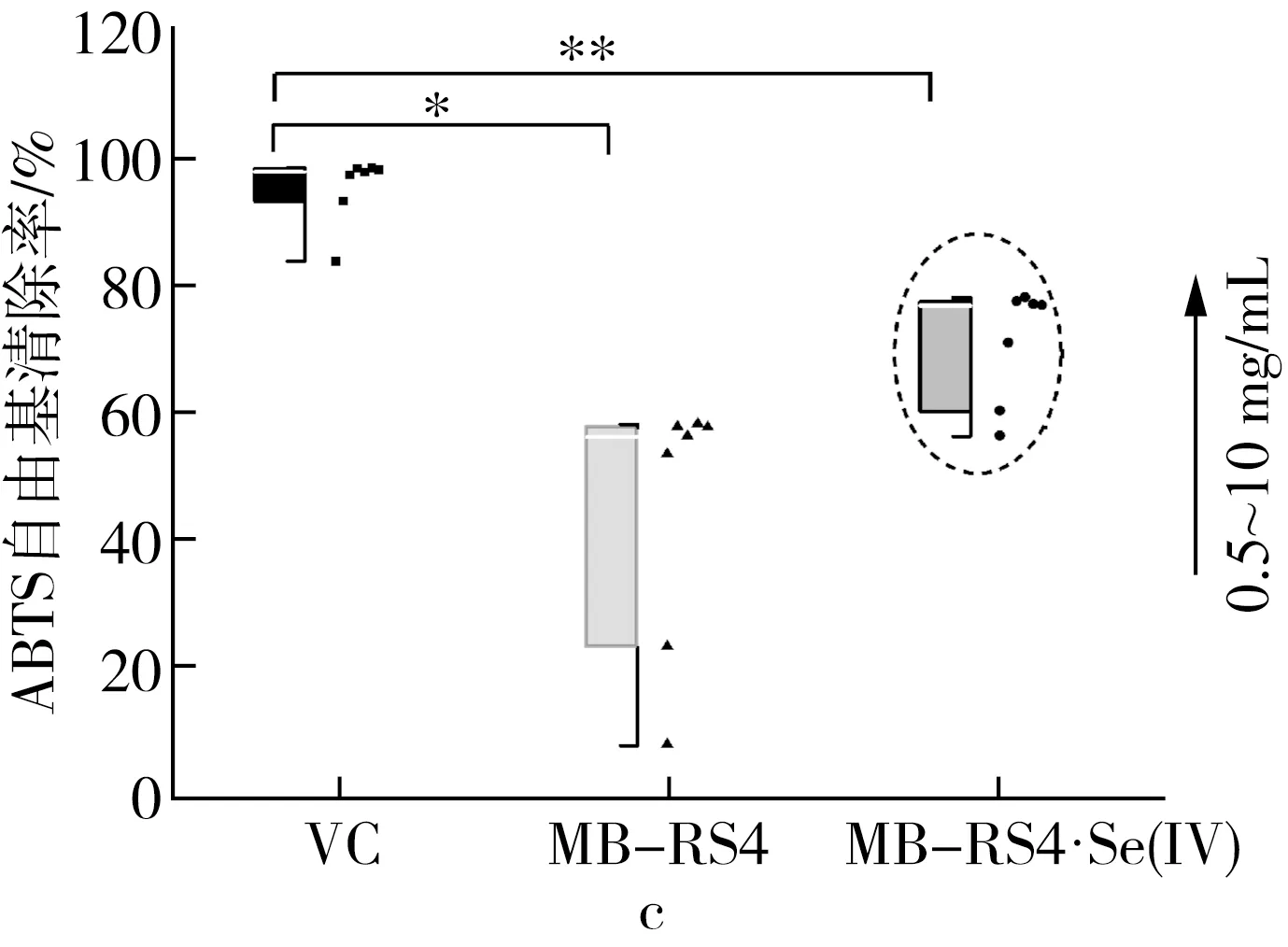
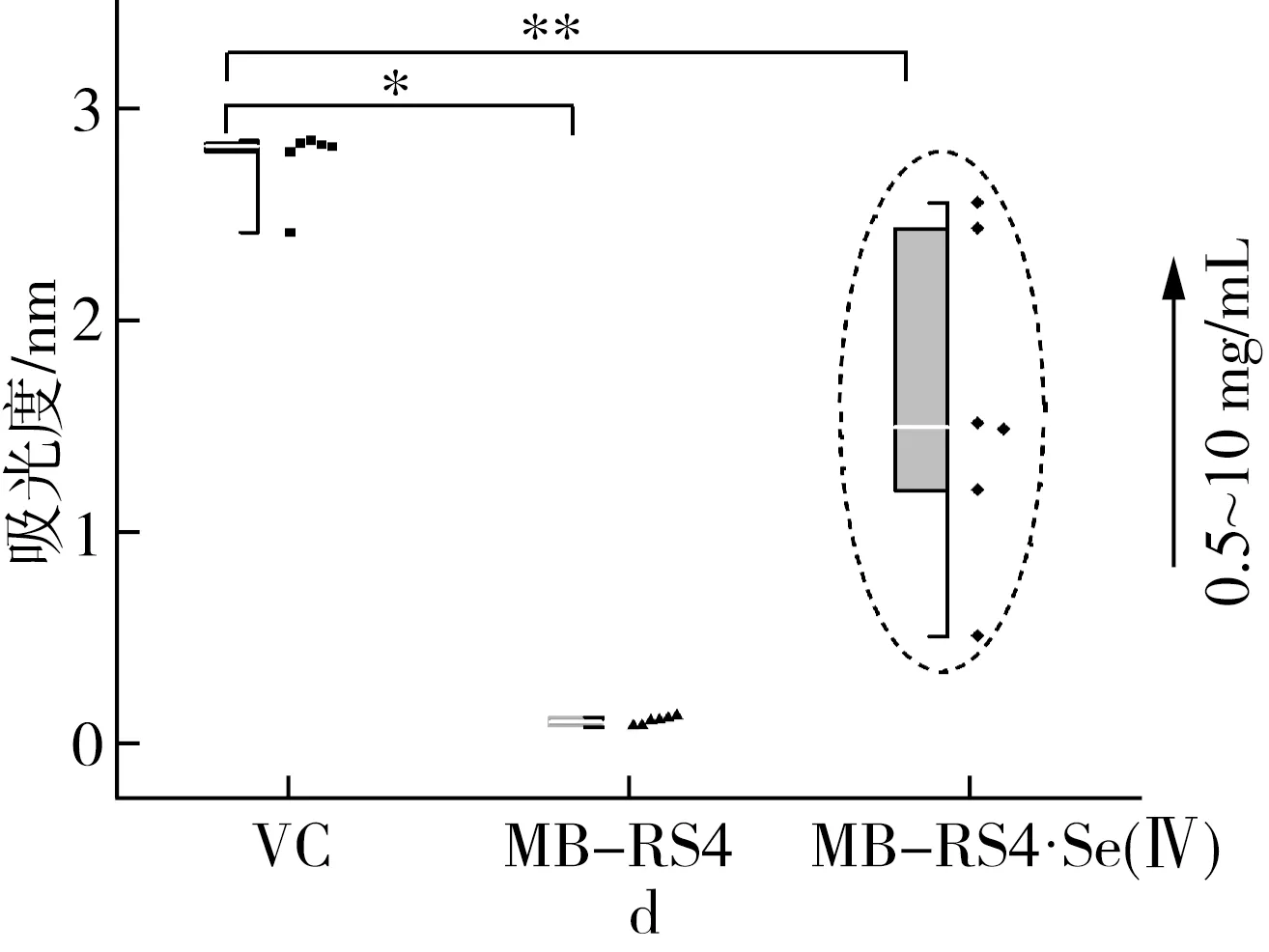
注:*為P≤0.05,**為P≤0.01。

