鹽酸多柔比星脂質體聯合利妥昔單抗治療復發難治性非霍奇金淋巴瘤的臨床研究*
邱流進 劉軒 肖威
非霍奇金淋巴瘤(NHL)屬于一種惡性淋巴細胞腫瘤性疾病,臨床表現包括消瘦、皮膚病變、發熱、盜汗等,嚴重者可導致全身功能障礙,預后較差[1]。近年來,NHL 的治療取得了較大進展,但一線化療后仍有50%~60%的患者出現耐藥或復發[2],現臨床針對復發難治性NHL 尚無統一的治療標準。鹽酸多柔比星脂質體可通過抑制DNA 聚合酶,阻礙核酸形成,進而阻斷腫瘤細胞進一步分化,以達到抗腫瘤的效果[3-4]。利妥昔單抗是一種單克隆抗體,作用于B 細胞以減輕細胞毒性,在淋巴瘤的治療中具有顯著效果[5]。目前,鹽酸多柔比星脂質體與利妥昔單抗聯合治療復發難治性NHL 的研究較少,本研究就此進行研究,旨在為臨床提供數據支持。現報道如下。
1 資料與方法
1.1 一般資料 選取2018 年1 月-2019 年12 月贛州市腫瘤醫院收治的168 例復發難治性NHL 患者。納入標準:(1)均符合復發難治性NHL 診斷標準,即經標準化療方案2 周后腫瘤縮小<50%或者疾病進展,或達完全緩解但半年內復發,或兩次及以上復發[6];(2)預計生存期超過3 個月;(3)經病理學或細胞學檢查確診。排除標準:(1)并發其他惡性腫瘤;(2)免疫系統功能異常;(3)主要臟器功能障礙;(4)妊娠期或哺乳期女性;(5)對本研究所用藥物存在禁忌證。使用隨機數字表法將患者分為對照組和試驗組,各84 例。本研究經醫院倫理委員會審批批準,患者知情同意,自愿加入本研究。
1.2 方法 對照組患者給予鹽酸多柔比星脂質體注射液(生產廠家:石藥集團歐意藥業有限公司,批準文號:國藥準字H20113320,規格:5 mL∶10 mg)治療,靜脈滴注,20 mg/m2,每2 周1 次。試驗組在對照組基礎上加用利妥昔單抗注射液(生產廠家:上海羅氏制藥有限公司,批準文號:國藥準字J20170034,規格:1 g∶10 mL)治療,靜脈滴注,375 mg/m2,1 次/周。兩組均持續治療6 周。
1.3 觀察指標及判定標準(1)比較兩組的臨床療效。療效判斷,疾病進展:腫瘤病灶擴大25%以上或發現新病灶;疾病穩定:病灶縮小25%~50%;部分緩解:病灶縮小50%以上,且維持28 d 以上;完全緩解:病灶消失,且維持28 d 以上[7]。總有效=完全緩解+部分緩解。(2)比較兩組患者的卡氏評分(KPS 評分)。于治療前后進行KPS 評分,評分范圍0~100 分,評分越低,生存質量越差[8]。(3)比較兩組免疫功能指標。在治療前后,采集患者4 mL 空腹靜脈血,經離心處理(3 200 r/min,10 min,半徑8 cm),收集上清液,冷藏待測。采用免疫補濁法檢測體液補體C3、C4 及免疫球蛋白A(IgA)、免疫球蛋白M(IgM)、免疫球蛋白G(IgG),操作均遵循試劑盒說明書(江蘇邁源生物科技有限公司)進行。(4)比較兩組患者不良反應發生情況。
1.4 統計學處理 采用SPSS 25.0 統計學軟件。計數資料用率(%)表示,采用χ2檢驗;計量資料用()表示,組間比較采用獨立樣本t 檢驗,組內比較采用配對t 檢驗。以P<0.05 為差異有統計學意義。
2 結果
2.1 兩組一般資料比較 兩組患者一般資料比較,差異均無統計學意義(P>0.05),具有可比性,見表1。

表1 兩組一般資料比較
2.2 兩組臨床療效比較 試驗組總有效率高于對照組,差異有統計學意義(χ2=4.052,P=0.044),見表2。

表2 兩組臨床療效比較[例(%)]
2.3 兩組免疫功能比較 治療前,兩組患者補體C3、C4 和IgA、IgM、IgG 比較,差異均無統計學意義(P>0.05)。治療后,兩組補體C3、C4 均低于治療前,且試驗組均低于對照組,差異均有統計學意義(P<0.05)。治療后,兩組患者IgA、IgM、IgG 與治療前比較,差異均無統計學意義(P>0.05);兩組治療后IgA、IgM、IgG 比較,差異均無統計學意義(P>0.05)。見表3。
表3 兩組免疫功能比較[g/L,()]
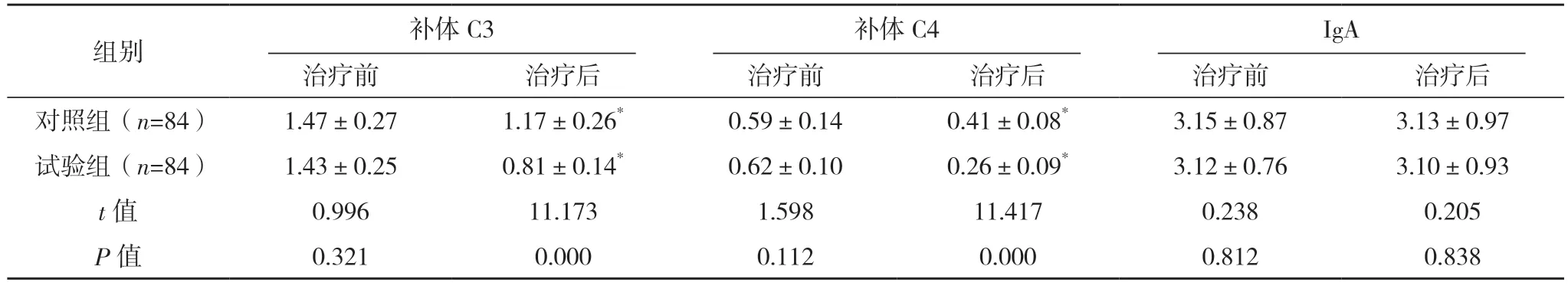
表3 兩組免疫功能比較[g/L,()]
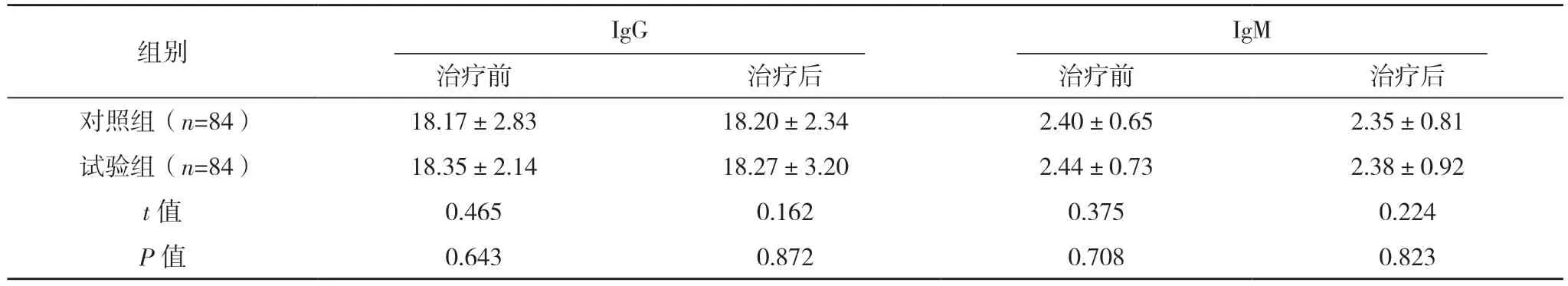
表3 (續)
2.4 兩組KPS 評分比較 治療前,兩組KPS 評分比較,差異無統計學意義(P>0.05);治療后,兩組KPS 評分均高于治療前,且試驗組高于對照組(P<0.05)。見表4。
表4 兩組KPS評分比較[分,()]
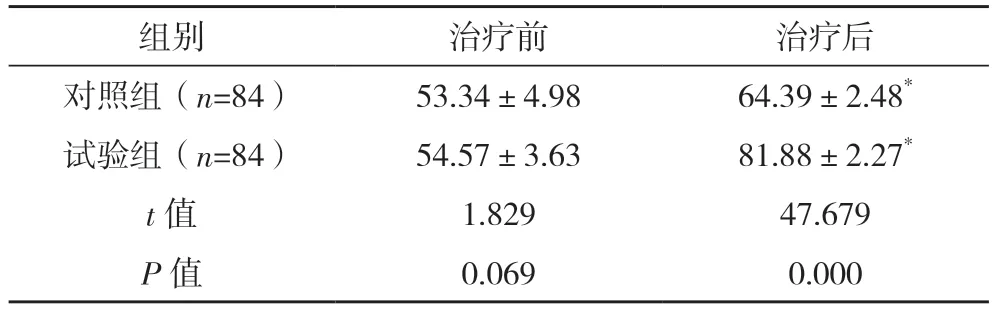
表4 兩組KPS評分比較[分,()]
*與治療前比較,P<0.05。
2.5 兩組治療期間不良反應發生情況比較 試驗組治療期間不良反應總發生率低于對照組,差異有統計學意義(χ2=4.568,P=0.033),見表5。

表5 兩組治療期間不良反應發生情況比較[例(%)]
3 討論
NHL 起源于淋巴結或淋巴組織,其發病率隨年齡增長而增加,嚴重危害人類健康。臨床治療常用CHOP 化療方案,但也只有50%~60%的患者可完全緩解,且其中約有一半病例會有復發情況,病情逐漸進展至復發難治性NHL[9]。由于此時的患者多已接受過標準化化療,身體狀況已較差,無法再耐受大劑量化療或放療[10]。以往亦有研究報道顯示,針對復發難治性NHL 患者采用CHOP 化療方案,其完全緩解率僅為5%~10%[11]。故而尋求高效、低毒的其他治療方案具有積極的臨床意義。鹽酸多柔比星脂質體是以脂質體作為載體的新一代藥物,具有抑制腫瘤活性、靶向性強、血液循環時間長等特點,常用于白血病、淋巴瘤的治療中[12]。文獻[13]研究結果顯示,鹽酸多柔比星脂質體可發揮與化療類似的治療效果,且毒副作用明顯低于化療。利妥昔單抗是通過基因工程研發所得,已被美國食品藥品監督管理局批準為治療惰性淋巴瘤的首選藥物。文獻[14]研究結果表明,利妥昔單抗治療復發難治性NHL 的效果高達78.05%。可見該藥物對阻止復發難治性NHL 的病情進展具有一定效果。為驗證鹽酸多柔比星脂質體與利妥昔單抗聯合能否進一步提高療效,本研究建立對照試驗進行分析。
本研究試驗組治療后臨床效果優于對照組,同時,試驗組KPS 評分高于對照組,可見鹽酸多柔比星脂質體與利妥昔單抗聯合可有效提高療效,改善患者生存質量。鹽酸多柔比星是蒽環類抗腫瘤抗菌藥物,其利用脂質體作為移動載體,靶向性選擇腫瘤細胞,可嵌合于DNA 雙螺旋結構中,以阻止DNA 復制,干擾mRNA 轉錄,最終抑制蛋白表達[15]。CD20 抗原通常在正常漿細胞、造血干細胞和其他正常組織中不表達,因此不會與抗體競爭性結合,而利妥昔單抗可與CD20 抗原特異性結合,并通過抗體及補體依賴性細胞毒性消滅淋巴瘤細胞[16]。因此,兩種藥物聯合從不同的機制發揮協同抗腫瘤作用,提高治療效果。本研究結果還顯示,兩種治療方式均對機體免疫球蛋白影響不大,但會減少機體補體水平,且聯合治療補體水平降低更明顯,分析原因為補體C3 和C4 在腫瘤進展過程中有重要作用,免疫功能下降伴隨著體液免疫功能的增強,使補體C3 和C4 表達增高,而利妥昔單抗的藥效取決于補體C3、C4,從而降低補體水平[17]。另試驗組治療期間不良反應總發生率更低,說明聯合治療安全性較高,這可能是由于該聯合治療可提高整體效果,促進患者恢復,相應的減少不良反應的發生。
綜上所述,鹽酸多柔比星脂質體聯合利妥昔單抗治療復發難治性NHL 患者,效果確切,可有效減少不良反應發生率,改善生存質量,同時對機體免疫球蛋白無影響,臨床應用價值較高。

