DC-CIK療法聯(lián)合伽馬刀治療局部淋巴結(jié)轉(zhuǎn)移性食管癌患者的療效
張百樂 張建東 丁巖
食管癌(esophageal cancer,EC)常表現(xiàn)為消瘦脫水、吞咽困難等,其發(fā)病率、死亡率較高,是八大惡性腫瘤之一[1]。隨著疾病進展,EC患者會出現(xiàn)局部淋巴結(jié)轉(zhuǎn)移,鎖骨淋巴結(jié)轉(zhuǎn)移病灶多與周圍組織粘連,侵犯神經(jīng),縱隔淋巴結(jié)轉(zhuǎn)移病灶常壓迫食管、氣管、喉返神經(jīng)等,引發(fā)進食梗阻、呼吸困難、聲音嘶啞等[2]。目前,臨床多以手術(shù)、放化療、生物療法等手段治療EC,雖可取得一定臨床療效,但單獨應(yīng)用效果有限[3]。伽馬刀對腫瘤細(xì)胞殺傷力較大,可有效促進腫瘤細(xì)胞凋亡,但治療后易復(fù)發(fā)[4]。樹突狀細(xì)胞聯(lián)合細(xì)胞因子誘導(dǎo)的殺傷細(xì)胞(DC-CIK)療法是將化學(xué)和生物治療結(jié)合的一種新型抗腫瘤治療模式,其在EC的治療方面越來越受到臨床重視[5]。本研究嘗試以DC-CIK療法聯(lián)合伽馬刀治療局部淋巴結(jié)轉(zhuǎn)移性EC患者,觀察其臨床療效及對免疫功能的影響,旨在為臨床治療EC提供參考。
1 資料與方法
1.1 一般資料 選取南陽市第一人民醫(yī)院2018年2月至2019年10月收治的108例局部淋巴結(jié)轉(zhuǎn)移性EC患者,隨機數(shù)字表分為對照組54例、聯(lián)合組54例。兩組性別、年齡、病程、腫瘤分期、腫瘤位置等一般資料比較,差異無統(tǒng)計學(xué)意義(P>0.05),見表1。
表1 兩組患者一般資料比較[n(%),(±s)]

表1 兩組患者一般資料比較[n(%),(±s)]
項目 對照組(n=54)聯(lián)合組(n=54) 統(tǒng)計值 P值性別 0.037 0.847男28(51.85) 29(53.70)女26(48.15) 25(46.30)年齡(歲) 52.24±3.62 53.19±4.07 1.282 0.203病程(月) 13.74±2.87 12.96±2.48 1.511 0.134腫瘤分期 0.348 0.555Ⅱ期 31(57.41) 34(62.96)Ⅲ期 23(42.59) 20(37.04)腫瘤位置 0.148 0.700頸段 25(46.30) 27(50.00)胸上段 29(53.70) 27(50.00)
1.2 選取標(biāo)準(zhǔn) 納入標(biāo)準(zhǔn):符合局部淋巴結(jié)轉(zhuǎn)移性EC相關(guān)診斷標(biāo)準(zhǔn)[6];無溝通交流障礙;臨床分期Ⅱ~Ⅲ期;卡氏功能狀態(tài)評分>60分;患者同意本文采用的治療方案,并簽署知情同意承諾書。排除標(biāo)準(zhǔn):對本研究相關(guān)藥物過敏;伴有心、肺、腎等嚴(yán)重功能不全;全身免疫性反應(yīng);治療依從性差;精神狀態(tài)異常。
1.3 治療方法 對照組采用伽馬刀治療,聯(lián)合組采用DC-CIK聯(lián)合伽馬刀治療。
1.3.1 伽馬刀 5次/周,治療操作均由伽馬刀專科醫(yī)師進行。患者取仰臥位(可根據(jù)病灶部位及其周圍組織調(diào)整),選取SGS-Ⅰ型立體定向伽馬刀(深圳渤海科技有限公司),根據(jù)患者具體病情給予初始劑量50~60 Gy,病灶區(qū)給予總劑量50%進行照射,病灶周圍以4 Gy/次進行10~12次照射(使用總劑量40~48 Gy)。
1.3.2 DC-CIK療法 采集患者外周靜脈血,采用血液成分分離機(鄭州飛龍醫(yī)療設(shè)備有限公司)分離單個核細(xì)胞,使用磷酸鹽緩沖液(ScienCell)洗滌2~4次,37 ℃下置于培養(yǎng)瓶中孵育2 h,移除懸浮細(xì)胞至GT-T601培養(yǎng)袋中。加入30 mL GT-T551培養(yǎng)液[重組人粒細(xì)胞巨噬細(xì)胞刺激因子(GM-CSF,廈門特寶生物工程有限公司)、白細(xì)胞介素-4(IL-4,Pepro-tech公司) 含量均為1 000 U/mL] 至培養(yǎng)瓶中,于培養(yǎng)箱(5% CO2,37 ℃)內(nèi)培養(yǎng),每3 d進行一次換液并擴充相關(guān)細(xì)胞因子,第6天加入注射用重組人干擾素(IFN-γ,上海凱茂生物醫(yī)藥有限公司),誘導(dǎo)DC細(xì)胞成熟。CIK細(xì)胞的培養(yǎng):向培養(yǎng)袋中加入GT-T551培養(yǎng)液(GM-CSF、IFN-γ含量均為1 000 U/mL),24 h后加入CD3單克隆抗體(50 ng/mL,古巴分子免疫學(xué)中心)和重組人白介素-2(rhIL-2,1 000 U/mL,北京四環(huán)生物制藥有限公司),每3 d進行一次換液并補充rhIL-2。第8天收獲成熟DC細(xì)胞,按照5∶1與CIK細(xì)胞繼續(xù)培養(yǎng),第14天獲得DC-CIK細(xì)胞。以生理鹽水沖洗2~4次后靜脈回輸,1×109個/次,1次/d,連續(xù)5 d。兩組均以3周為1個周期,共治療2個周期。
1.4 檢測方法
1.4.1 免疫功能指標(biāo)(CD3+、CD4+、CD4+/CD8+) 于清晨采集患者空腹?fàn)顟B(tài)下外周血,采用流式細(xì)胞術(shù)測 定 外 周 血CD3+、CD4+、CD4+/CD8+水 平,并 計 算CD4+/CD8+比值,檢測儀器為CytoFLEX流式細(xì)胞儀(美國貝克曼庫爾特公司)。
1.4.2 血清血小板反應(yīng)蛋白-1(TSP-1)、基質(zhì)金屬蛋白酶-9(MMP-9)、血管內(nèi)皮生長因子(VEGF)、鈣結(jié)合蛋白(S100A4)水平 取上述血液標(biāo)本,以3 500 r/min轉(zhuǎn)速離心處理,10 min后取血清,采用酶聯(lián)免疫吸附試驗測定血清TSP-1、MMP-9、VEGF、S100A4水平,相關(guān)試劑盒分別購自上海酶研生物科技有限公司 (TSP-1、MMP-9、VEGF)、南京賽泓瑞生物科技有限公司(S100A4)。
1.5 療效判定標(biāo)準(zhǔn) 治療2個周期后參照相關(guān)評價標(biāo)準(zhǔn)[7]評估療效,分為完全緩解(CR)、部分緩解(PR)、疾病穩(wěn)定(SD)、疾病進展(PD)。其中CR:基線病灶完全消失且維持30 d以上;PR:基線病灶縮小≥50%及以上,未出現(xiàn)新病灶,且維持30 d以上;SD:基線病灶縮小<50%或增大<25%,未出現(xiàn)新病灶,且維持30 d以上;PD:基線病灶增大≥25%或有新病灶出現(xiàn)。客觀緩解率(ORR)=(CR+PR)例數(shù)/總例數(shù)×100%。
1.6 觀察指標(biāo) ①臨床療效。②治療前、治療2個周期后免疫功能指標(biāo)(CD3+、CD4+、CD4+/CD8+)。③治療前、治療2個周期后血清TSP-1、MMP-9、VEGF、S100A4水平。④隨訪2年,1年、2年生存率。
1.7 統(tǒng)計學(xué)方法 以SPSS 22.0對結(jié)果進行分析。計數(shù)資料以率[n(%)]表示,行χ2檢驗,計量資料以均數(shù)±標(biāo)準(zhǔn)差(±s)表示,行t檢驗,等級資料采用秩和檢驗,P<0.05表示差異有統(tǒng)計學(xué)意義。
2 結(jié)果
2.1 兩組患者臨床療效比較 兩組ORR比較,聯(lián)合組79.63%高于對照組61.11%(P<0.05),見表2。

表2 兩組患者臨床療效比較[n(%)]
2.2 兩組患者免疫功能指標(biāo)比較 治療2個周期 后 聯(lián) 合 組CD3+、CD4+、CD4+/CD8+明 顯 高 于 對 照 組(P<0.05),見表3。
表3 兩組患者免疫功能指標(biāo)比較(±s)
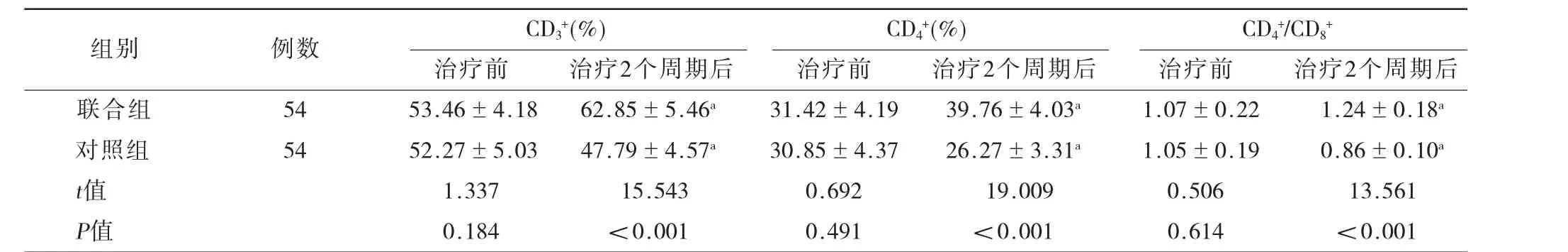
表3 兩組患者免疫功能指標(biāo)比較(±s)
注:CD3+、CD4+、CD4+/CD8+=免疫功能指標(biāo);與同組治療前比較,aP<0.05。
組別 例數(shù) CD3+(%) CD4+(%)治療前 治療2個周期后 治療前 治療2個周期后 治療前 治療2個周期后聯(lián)合組 54 53.46±4.18 62.85±5.46a 31.42±4.19 39.76±4.03a 1.07±0.22 1.24±0.18a對照組 54 52.27±5.03 47.79±4.57a 30.85±4.37 26.27±3.31a 1.05±0.19 0.86±0.10a t值 1.337 15.543 0.692 19.009 0.506 13.561 P值 0.184 <0.001 0.491 <0.001 0.614 <0.001 CD4+/CD8+
2.3 兩組患者血清TSP-1、MMP-9、VEGF、S100A4水平比較 治療2個周期后聯(lián)合組血清TSP-1水平高于對照組,MMP-9、VEGF、S100A4水平低于對照組(P<0.05),見表4。
表4 兩組患者血清TSP-1、MMP-9、VEGF、S100A4水平比較(±s)

表4 兩組患者血清TSP-1、MMP-9、VEGF、S100A4水平比較(±s)
注:TSP-1=血小板反應(yīng)蛋白-1,MMP-9=基質(zhì)金屬蛋白酶-9,VEGF=血管內(nèi)皮生長因子,S100A4=鈣結(jié)合蛋白;與同組治療前比較,P<0.05。
組別 例數(shù) TSP-1(ng/mL) MMP-9(ng/mL)治療前 治療2個周期后 治療前 治療2個周期后聯(lián)合組 54 82.74±7.43 171.63±9.78a 161.41±12.03 102.38±10.07a對照組 54 84.16±8.25 152.24±8.11a 158.76±13.05 121.76±11.83a t值 0.940 11.215 1.097 9.167 P值 0.349 <0.001 0.275 <0.001組別 例數(shù) VEGF(ng/L) S100A4(μg/mL)治療前 治療2個周期后 治療前 治療2個周期后聯(lián)合組 54 897.45±59.33 483.67±25.73a 6.74±1.68 2.52±0.51a對照組 54 884.17±51.76 561.84±30.08a 6.83±1.54 3.87±0.64a t值 1.239 14.512 0.290 12.123 P值 0.218 <0.001 0.772 <0.001
2.4 兩組患者生存率比較 隨訪2年,聯(lián)合組失訪5例,對照組失訪4例。聯(lián)合組1年、2年生存率高于對照組(P<0.05),見表5。

表5 兩組患者生存率比較[n(%)]
3 討論
隨著醫(yī)學(xué)科技進步,EC治療手段不斷被完善,但其5年生存率僅15%左右,且易復(fù)發(fā),嚴(yán)重威脅患者生命健康[8]。因此優(yōu)化EC治療方案以提高生存率仍是臨床研究重點方向[9]。
伽馬刀采用多線束、多野、多源三維空間聚焦,射線呈錐形分布,具有射線集中、局部劑量高等特點,可對腫瘤細(xì)胞產(chǎn)生較大殺傷力,且對周圍正常組織照射較少,可保護周圍組織及器官;但伽馬刀治療常伴隨嘔吐、惡心等胃腸道不良反應(yīng),對患者身心帶來極大痛苦[10]。
DC-CIK療法是一種過繼性細(xì)胞免疫療法,其中DC細(xì)胞具有較強抗原呈遞作用,可誘導(dǎo)抗原特異性T細(xì)胞功能,激活自然殺傷T細(xì)胞腫瘤識別能力;CIK細(xì)胞具備抗原活性及抗腫瘤活力,可殺死腫瘤細(xì)胞,增強機體免疫細(xì)胞功能,具有殺傷力強、增殖快、殺瘤譜廣等特點[11]。DC細(xì)胞、CIK細(xì)胞共培養(yǎng)得到DC-CIK細(xì)胞,可有效提高機體免疫系統(tǒng)功能,提高殺死腫瘤細(xì)胞的能力[12]。本研究結(jié)果顯示,與對照組相比,聯(lián)合組ORR、1年及2年生存率較高,CD3+、CD4+、CD4+/CD8+水平較高,表明DC-CIK療法可在伽馬刀殺傷腫瘤細(xì)胞、減輕腫瘤負(fù)荷基礎(chǔ)上,進一步殺死隱匿腫瘤細(xì)胞,并增強機體免疫應(yīng)答反應(yīng),緩解毒副損傷,從而延長患者生存期,提高臨床療效及生存質(zhì)量。
有研究表明S100A4高表達可影響細(xì)胞周期,引發(fā)細(xì)胞惡變導(dǎo)致腫瘤發(fā)生;還可抑制細(xì)胞間黏附作用,加速降解、重塑細(xì)胞外基質(zhì)及血管生成,從而加重腫瘤轉(zhuǎn)移風(fēng)險[13]。TSP-1屬于血管生成抑制因子,其高表達可抑制血管內(nèi)皮細(xì)胞增殖及血管生成,而VEGF屬于血管生成促進因子,與TSP-1機制相反[14]。有研究表明MMP-9參與炎癥反應(yīng)、血管形成、創(chuàng)傷修復(fù)等多種病理生理過程,且在腫瘤細(xì)胞侵襲及轉(zhuǎn)移中發(fā)揮重要作用[15]。本研究中,聯(lián)合組血清TSP-1 水平高于對照組,MMP-9、VEGF、S100A4水平低于對照組,表明聯(lián)合組治療方案可增強細(xì)胞間黏附作用,抑制血管生成,有效抑制腫瘤細(xì)胞轉(zhuǎn)移,進一步抑制EC疾病進展。
綜上所述,采用DC-CIK療法聯(lián)合伽馬刀治療局部淋巴結(jié)轉(zhuǎn)移性EC患者,可顯著提高機體免疫系統(tǒng)功能,增強對腫瘤細(xì)胞的殺傷力,緩解臨床毒副反應(yīng),進一步提高臨床療效、延長生存期。

