大孔吸附樹脂分離純化益心泰總黃酮工藝的優化
鄒蘇蘭, 李 雅, 李姿銳, 柳 蘭, 陸慧玲, 郭志華
(湖南中醫藥大學,湖南 長沙 410208)
心血管疾病已經發展成為嚴重威脅人類健康的第一殺手,近年來心血管系統疾病的發病率和死亡率高居不下[1]。研究表明心臟功能與代謝有著密不可分的聯系,代謝衰竭被認為在心力衰竭的發病機理中起著核心作用[2],這與中醫治療心力衰竭的理念不謀而合。
益心泰復方是湖南中醫藥大學附屬第一醫院臨床科研方,具有益氣活血、利水消腫之功效,對心氣虧虛、血瘀水停型心衰患者療效確切。益心泰復方由黃芪、丹參、紅花等7味中藥組成,方中以黃芪為君藥,補氣升氣,利水消腫;丹參和紅花共為臣藥,輔助黃芪活血通經、祛瘀止痛[3],全方共奏益氣活血、利水消腫之功效,臨床用于治療心氣虧虛、血瘀水停型心衰患者。毛蕊異黃酮、毛蕊異黃酮葡萄糖苷、芒柄花素、芒柄花苷、羥基紅花黃色素A為益心泰總黃酮中主要藥效成分,具有保護心血管、抗氧化、降血脂、抗腫瘤等藥理作用。動物實驗表明,益心泰總黃酮有效組分可以明顯改善心肌梗死后心力衰竭癥狀、心功能、超微結構[4]。
本實驗采用Plackett-Burman設計[5-6]和Box-Behnken響應面設計[7-8],確定大孔吸附樹脂分離純化益心泰總黃酮的關鍵工藝參數并建立數學模型,最后通過Monte Carlo法計算獲得基于概率的設計空間[9-10],以期為益心泰總黃酮的分離純化應用奠定基礎。
1 材料
黃芪(批號19082607)、丹參(批號19050806)、紅花(批號19092004)、澤瀉(批號19080202)、茯苓(批號19091009)、豬苓(批號19071209)、葶藶子(批號18112505)均購于湖南新匯制藥股份有限公司,經湖南中醫藥大學中藥鑒定教研室龔力民副教授鑒定為正品,均符合2020年版《中國藥典》一部附錄規定。UV755B紫外可見分光光度計(上海佑科儀器儀表有限公司);CP114電子天平(上海奧豪斯儀器有限公司);H1850R高速離心機(湘潭湘儀儀器有限公司)。蘆丁對照品(批號100080-201811,上海源葉生物科技有限公司)。色譜純甲醇(美國Tedia公司);優級純甲酸;分析純甲醇;Al(NO3)3、NaNO2、NaOH等其他試劑均為分析純。
2 方法與結果
2.1 總黃酮含量測定
2.1.1 對照品溶液制備 取蘆丁對照品10.50 mg,置于10 mL量瓶中,70%乙醇溶解定容至1.05 mg/mL,即得。
2.1.2 供試品溶液制備
2.1.2.1 上樣液 取處方量藥材(黃芪30 g、丹參15 g、紅花5 g、澤瀉10 g、豬苓15 g、葶藶子15 g、茯苓15 g),第1次以10倍量70%乙醇80 ℃水浴回流提取60 min,第2次加8倍量70%乙醇80 ℃水浴回流提取30 min,濾過,合并濾液,減壓濃縮后冷凍干燥,得到凍干粉。取適量至10 mL量瓶中,70%乙醇溶解定容,即得。
2.1.2.2 洗脫液 乙醇洗脫液減壓濃縮后,冷凍干燥得到凍干粉,取適量至10 mL量瓶中,70%乙醇溶解定容,即得。
2.1.3 檢測波長確定 取對照品溶液1.0 mL、供試品溶液2.0 mL,置于10 mL量瓶中,加入0.5 mL 5%NaNO2搖勻,靜置6 min,加入0.5 mL 10%Al(NO3)3,靜置6 min,加入4 mL 4%NaOH溶液搖勻,70%乙醇定容,靜置10 min,在200~700 nm波長處掃描。結果,對照品、供試品溶液最大吸收波長分別為505、500 nm,故選擇505 nm作為檢測波長。
2.1.4 線性關系考察 取對照品溶液0、0.1、0.2、0.3、0.4、0.5、0.6 mL至10 mL量瓶中,加入0.5 mL 5%NaNO2,搖勻,靜置6 min,加入0.5 mL 10%Al(NO3)3,靜置6 min,加入4 mL 4%NaOH搖勻,70%乙醇定容,靜置10 min,在505 nm波長處測定吸光度。以對照品溶液質量濃度為橫坐標(X),吸光度為縱坐標(A)進行回歸,得方程為A=12.59X-0.029 6(r=0.999 1),在0.010 0~0.060 0 mg/mL范圍內線性關系良好。
2.1.5 精密度試驗 取對照品溶液0.5 mL,置于10 mL量瓶中,按“2.1.4”項下方法顯色,在505 nm波長處測定吸光度6次,測得其RSD為0.15%,表明儀器精密度良好。
2.1.6 重復性試驗 平行制備6份供試品溶液,按“2.1.4”項下方法顯色,在505 nm波長處測定吸光度6次,測得其RSD為1.56%,表明該方法重復性良好。
2.1.7 穩定性試驗 取供試品溶液適量,按“2.1.4”項下方法顯色,于0、0.5、1、1.5、3、6、12、24 h在505 nm波長處測定吸光度,測得其RSD為2.35%,表明溶液在24 h內穩定性良好。
2.1.8 加樣回收率試驗 取各成分含量已知的供試品溶液9份,每份1 mL,精密加入80%、100%、120%對照品溶液,按“2.1.4”項下方法顯色,在505 nm波長處測定吸光度,計算回收率。結果,蘆丁平均加樣回收率分別為99.63%、98.89%、99.45%,RSD分別為2.01%、1.03%、1.13%。
2.2 上樣液制備 取凍干粉5.00 g至500 mL量瓶中,70%乙醇溶解定容,制得10 mg/mL供試品溶液,取0.5 mL,加入0.5 mL 5%NaNO2,搖勻,靜置6 min,加入0.5 mL 10%Al(NO3)3,靜置6 min,加入4 mL 4%NaOH搖勻,70%乙醇定容,靜置10 min,在505 nm波長處測定吸光度,測得總黃酮質量分數為9.08%。
2.3 樹脂篩選 MAR吸附分離技術是在中藥有效成分的精制分離和復方中藥制劑的純化中常用的提取純化工藝,它是通過靜態吸附作用從中藥及其復方提取液中有選擇性地吸附其中的有效部分,去除無效部分[11-12],在理化性質、選擇性、吸附能力等方面有著無可取代的優勢,并且易洗脫、可循環使用[13-14],同時其種類多,在結構、極性、孔徑等性能指標上均有所差異。D-101型大孔吸附樹脂是一種非極性吸附劑,比表面積為400 m2/g,適合極性或弱極性化合物(皂苷類、黃酮類)分離純化[15];AB-8型為一種弱極性的大孔吸附樹脂,比表面積為480~520 m2/g,王春民等[16]報道,它對黃芩總黃酮的效果最好;HPD-100型大孔吸附樹脂是苯乙烯型非極性共聚體,適用范圍廣,可用于皂苷、黃酮、萜類等天然產物及植物的提取分離;易海燕等[17]發現,它對藤茶總黃酮的吸附效果最佳。因此,本實驗選擇對黃酮吸附性強、解吸性好的AB-8、D-101、HPD-100大孔吸附樹脂,進行單因素試驗。
2.3.1 樹脂預處理與再生
2.3.1.1 預處理 將AB-8、D101、HPD-100大孔吸附樹脂用無水乙醇浸泡24 h以充分溶脹后,95%乙醇沖洗,至洗出液加5倍量蒸餾水時無白色渾濁,蒸餾水洗至無醇味,密封保存,備用。
2.3.1.2 再生 將使用過的樹脂用無水乙醇洗脫至無色后,5%鹽酸浸泡3~4 h,水洗至中性,5%NaOH浸泡3~4 h,水洗至中性。
2.3.2 靜態吸附性能考察 準確稱取經預處理好的3種樹脂(相當于干樹脂2.00 g),置于100 mL具塞錐形瓶中,分別精密加入質量濃度為0.911 2 mg/mL上樣液30 mL,室溫振搖吸附,于1、2、4、6、10、24 h吸取上清液,測定吸光度,計算靜態吸附量和吸附率,公式分別為吸附量=(上樣液中總黃酮質量濃度×樣液體積-水洗液中總黃酮質量濃度×水洗液體積)/樹脂質量、吸附率=[(上樣液中總黃酮質量濃度×樣液體積-水洗液中總黃酮質量濃度×水洗液體積)/上樣液中總黃酮質量濃度×樣液體積]×100%,結果見表1~2。由此可知,3種樹脂靜態吸附10 h后均基本達到飽和,其中HPD-100吸附量最大,吸附率最高。

表1 樹脂靜態吸附量測定結果

表2 樹脂靜態吸附率測定結果
2.3.3 靜態解吸性能考察 準確稱取經預處理好的3種樹脂(相當于干樹脂2.00 g),置于100 mL具塞錐形瓶中,精密加入0.911 2 mg/mL上樣液30 mL,室溫振搖吸附24 h,精密加入50%、70%、90%乙醇各40 mL,充分振搖6 h后靜置24 h,收集乙醇洗脫液,按“2.1.4”項下方法顯色,測定吸光度,計算解吸量和解吸率,公式分別為解吸量=醇洗液中總黃酮質量濃度×醇洗液體積/樹脂質量、解吸率=[醇洗液中總黃酮質量濃度×醇洗液體積/(上樣液中總黃酮質量濃度×樣液體積-水洗液中總黃酮質量濃度×水洗液體積)]×100%,結果見表3。由此可知,HPD-100樹脂靜態吸附能力最強。

表3 樹脂靜態解吸量及解吸率測定結果
2.4 評價指標確定 本實驗選擇總黃酮質量分數和總黃酮洗脫率作為評價指標,公式分別為總黃酮質量分數=洗脫液中黃酮質量/洗脫液干物質質量、總黃酮洗脫率=(洗脫液中黃酮質量/上柱液黃酮質量)×100%。
2.5 Plackett-Burman設計 總黃酮分離純化工藝魚骨圖見圖1,可知主要涉及藥材、環境、樹脂、吸附、解吸、除雜。由于本實驗處于同一實驗環境,采用同一批藥材提取,故不考慮環境和藥材因素,另外樹脂因素在單因素試驗中已進行考察,最終選擇上樣液體積(A)、水洗體積流量(B)、上樣液體積流量(C)、乙醇洗脫量(D)、乙醇體積分數(E)、乙醇洗脫流量(F)、水洗體積(G)進行Plackett-Burman設計,確定關鍵工藝參數(CPPs),共12組實驗,因素水平見表4,通過Minitab軟件進行數據處理,結果見表5,方差分析見表6~7。

圖1 總黃酮分離純化工藝魚骨圖

表4 Plackett-Burman設計因素水平
由表6可知,上樣液體積流量(C)、乙醇體積分數(E)、水洗體積(G)對總黃酮質量分數有顯著影響(P<0.05);由表7可知,上樣液體積(A)、水洗體積(G)對總黃酮洗脫率有顯著影響。因此,選擇因素A、C、E、G作Box-Behnken響應面設計。
2.6 Box-Behnken響應面設計 在Plackett-Burman設計結果基礎上,選擇上樣液體積(A)、上樣液體積流量(B)、水洗體積(C)、乙醇體積分數(D)作為影響因素,總黃酮質量分數(Y1)、洗脫率(Y2)作為評價指標,Box-Behnken響應面設計優化分離純化工藝,因素水平見表8,結果見表9。

表5 Plackett-Burman設計結果

表6 Plackett-Burman設計總黃酮質量分數方差分析

表7 Plackett-Burman設計總黃酮洗脫率方差分析

表8 Box-Behnken響應面設計因素水平

表9 Box-Behnken響應面設計結果

總黃酮質量分數方差分析見表10,可知模型P<0.000 1,達到極顯著水平;失擬項P>0.05,表示方程擬合度良好;因素A、B、AB、BC、BD有顯著影響(P<0.05)。響應面分析見圖2。

圖2 總黃酮質量分數各因素響應面圖
總黃酮洗脫率方差分析見表11,可知模型P<0.05,達到極顯著水平;失擬項P>0.05,表明方程擬合度良好;因素A、B、C、AD、BC、C2、D2有顯著影響(P<0.05),響應面分析見圖3。
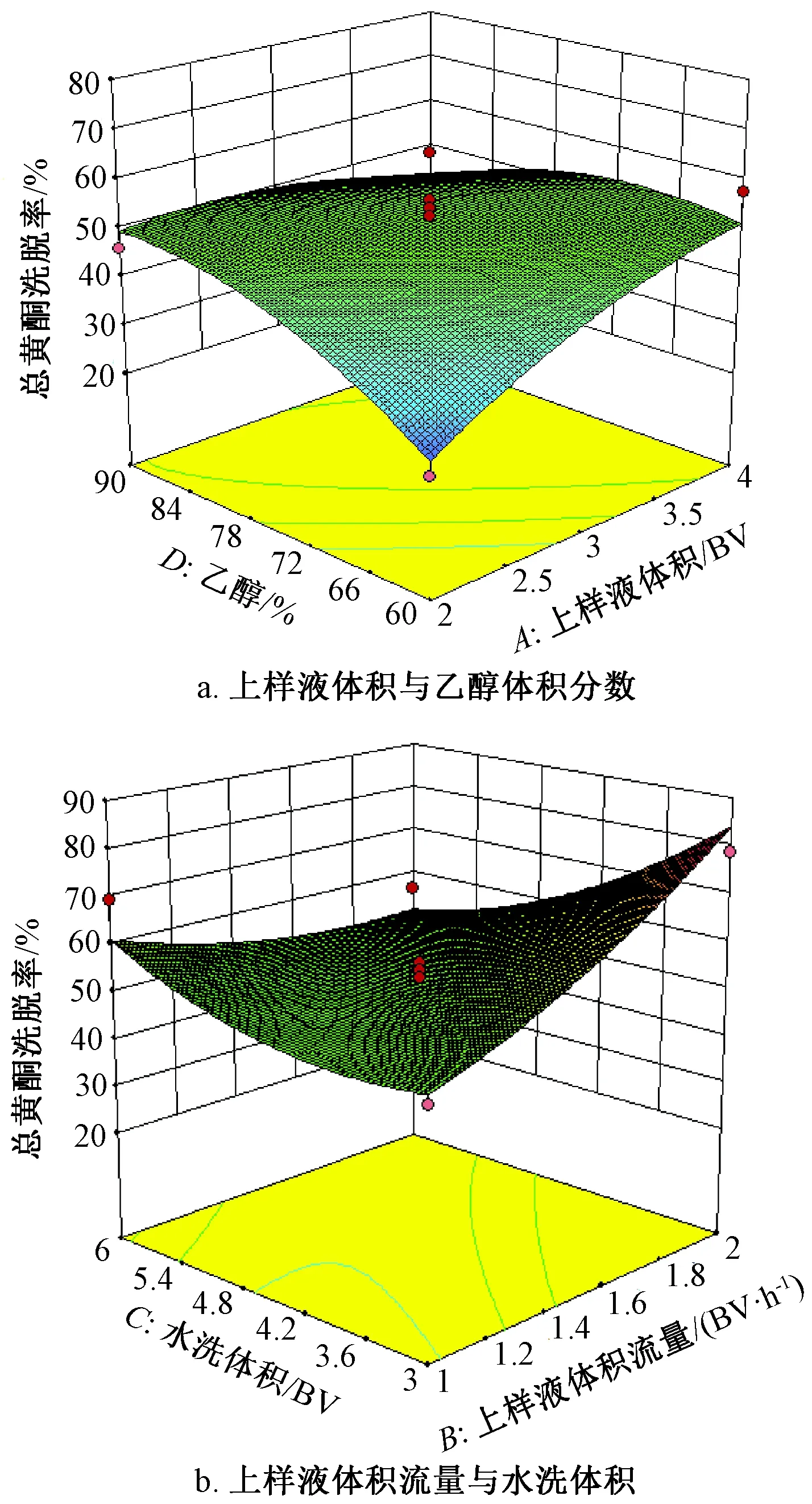
圖3 總黃酮洗脫率各因素響應面圖
2.7 設計空間建立 根據Design-Expert 10.0軟件得到的2個數學模型開發設計空間,通過查閱文獻和近年來相關管理辦法,希望大孔吸附樹脂分離純化的總黃酮質量分數、洗脫率均大于50%,故設置兩者優化標準為50%,目標范圍為大于50%。采用Monte Carlo法獲取基于達標概率的設計空間,首先進行仿真模擬實驗,獲得實驗測定誤差來計算達標概率,以總黃酮質量分數、洗脫率同時滿足優化標準為其達標,模擬次數設置為5 000次,假定所有的檢測量服從正態分布,均值取單組實驗的檢測量,目標正態分布的標準差取相同條件重復實驗所得檢測量的標準差,再采用實驗窮舉法對每個工藝參數進行窮舉,步長取0.05得到的設計空間見圖4。最終確定,最優操作空間為上樣液體積3 BV,乙醇體積分數75%,水洗體積3.0~4.8 BV,上樣液體積流量1.3~2.0 BV/h。

表10 Box-Behnken響應面設計總黃酮質量分數方差分析

表11 Box-Behnken響應面設計總黃酮洗脫率方差分析
對設計空間進行3批驗證試驗,結果見表12。由此可知,當相關參數落在設計空間內時,可保證總黃酮分離純化工藝的穩定性,對指導實際生產過程具有重大參考意義,符合質量源于設計(QbD)理念。
表12 驗證試驗結果
3 討論
相較于傳統的單因素實驗,Plackett-Burman設計是一種兩水平的試驗設計方法,它可以用最少試驗次數篩選并確定對結果影響比較顯著的因素,對于受多種因素影響的實驗來說,它可以科學客觀地篩選出顯著性的因素,可以避免不必要的資源浪費[18]。Box-Behnken響應面分析法能夠在因素和響應值之間建立模型,不僅僅可以通過相關數據進行擬合,篩選出最佳工藝,而且對實驗的預測性較好,信息量大,精確度高[19]。人用藥品注冊技術標準國際協調會(ICH)Q8是將QbD定義為一套系統的基于充分的科學知識和質量風險管理的研究方法,從預先確定的目標出發,強調對產品工藝的理解以及工藝控制。

注:圖中數字為工藝參數落在相應區域時關鍵評價指標未能達標的概率,數字越大,不達標可能性越大;綠色區域為設計空間,顏色由綠到紅表示在相應工藝條件下,響應值不符合要求的概率逐漸增大。
本研究采用Plackett-Burman設計篩選出樣液體積、上樣液體積流量、水洗體積及乙醇體積分數為大孔吸附樹脂分離純化益心泰總黃酮工藝中的CPPs;結合Box-Behnken設計建立了大孔吸附樹脂分離純化益心泰總黃酮的CPPs與關鍵評價指標的數學模型,最后通過Monte Carlo法計算獲得基于概率的設計空間,最終得到的推薦的工藝參數的操作空間為上樣液體積3.5~4.0 BV,水洗體積3~3.2 BV,上樣液體積流量1.8~2.0 BV/h。基于QbD理念的總黃酮分離純化的設計空間,是通過了解和控制關鍵工藝參數,確保產品質量,使分離純化工藝在研發階段獲得了充分的工藝知識,質量屬性和工藝參數可靠,分離純化工藝流程始終能在保證益心泰總黃酮質量的范圍內運行,可以最大限度減少失敗的成本,保證總黃酮質量分數及總黃酮洗脫率都能達到有效分離純化的條件。

