一測多評法同時測定連翹歸尾顆粒中3種成分
遆安航, 李思思, 陳 瑾, 翟康欣, 譚麗媛, 張淑蓉
(山西中醫藥大學,山西 晉中 030600)
連翹歸尾煎出自《景岳全書》,由連翹、歸尾、甘草、金銀花、紅藤組成,功效清熱解毒、活血消腫[1],可治療乳癰、口疽、頰瘍、牙癰、豬丹毒等[2],方中連翹、金銀花為君藥,具有清熱解毒、散結消腫作用[3]。課題組前期發現,該方在體內外實驗中均顯示對乳腺癌細胞的抑制作用,為了更有效地開展后期研究,保證實驗樣本前后的一致性,已將其改制成顆粒劑[4]。
為了降低檢測成本,同時結合中藥中多種成分相互作用、復雜多變等特點[5],采用一測多評法測定多指標成分含量已成為發展趨勢和研究熱點[6]。因此,本實驗建立該方法同時測定連翹歸尾顆粒中連翹酯苷A、綠原酸、連翹苷的含量[7],以期為該制劑質量控制和評價提供參考。
1 材料
1.1 儀器 數顯電熱套購自金壇市杰瑞爾電器有限公司(型號HDM500-10450);中藥材粉碎機購自廣州真麥機械設備有限公司(型號LG-50);恒溫水浴鍋購自上海比朗儀器制造有限公司(型號HH-2);旋轉蒸發儀購自鞏義市英峪弘源儀器廠(型號RE-5205);超聲波清洗機購自杭州法蘭特超聲波科技有限公司(型號SB-5200 DTDN);高效液相色譜儀購自杭州瑞析科技有限公司(型號Waters e2695)、上海諾析儀器有限公司(型號Agilent 1260);電動噴霧器購自武漢藥科新技術開發有限公司(型號CS-1020E);電子天平(十萬分之一)購自瑞士梅特勒-托利多公司(型號AE240)。
1.2 試劑與藥物 連翹歸尾顆粒(批號201020、201121、201222)及各陰性顆粒均為自制。綠原酸(批號110753-201716,純度>98%)、連翹酯苷A(批號111810-201606,純度>98%)、連翹苷(批號110821-200610,純度>98%)對照品及連翹(批號120908-201216)、金銀花(批號121060-201608)、甘草(批號120904-201605)、大血藤(批號121353-201704)對照藥材均購自中國食品藥品檢定研究院。乙腈為色譜純(河南薩默生物科技有限公司);甲酸、甲醇為分析純;水為娃哈哈純凈水。
2 方法與結果
2.1 色譜條件 Thermo Scientific BDS HYPERSIL C18色譜柱(150 mm×4.6 mm,5 μm);流動相乙腈(A)-0.1%甲酸(B),梯度洗脫(0~6 min,5%~9%A;6~9 min,9%~12%A;9~22 min,12%~14%A;22~35 min,14%~24%A;35~40 min,24%~26%A);體積流量1.0 mL/min;柱溫25 ℃;檢測波長278 nm;進樣量10 μL。
2.2 溶液制備
2.2.1 供試品溶液 精密稱取本品粉末(過6號篩)2 g,置于具塞錐形瓶中,加20%乙醇10 mL,密塞,浸泡40 min,稱定質量,超聲(功率250 W、頻率45 kHz)處理45 min,放冷,20%乙醇補足減失的質量,搖勻,濾過,0.45 μm微孔濾膜過濾,即得。
2.2.2 對照品溶液 精密稱取連翹酯苷A、連翹苷、綠原酸對照品適量,置于5 mL量瓶中,50%甲醇定容至刻度,搖勻,即得(三者質量濃度分別為0.538、0.066、0.222 mg/mL),在4 ℃下保存。
2.2.3 陰性樣品溶液 將缺連翹、缺金銀花和大血藤陰性樣品研成粉末,過6號篩,分別精密稱取2 g,按“2.1.2”項下方法制備,即得。
2.3 專屬性考察 取“2.2”項下供試品、對照品、陰性樣品溶液適量,在“2.1”項色譜條件下進樣測定,結果見圖1。由此可知,各成分色譜峰均能達到基線分離,表明該方法專屬性良好。
2.4 線性關系考察 分別精密量取“2.2.2”項下對照品溶液4、8、16、24、32、40 μL,置于2 mL量瓶中,50%甲醇定容至刻度,搖勻,得不同質量濃度,在“2.1”項色譜條件下進樣測定。以對照品峰面積為縱坐標(Y),質量濃度為橫坐標(X)進行回歸,得方程分別為連翹酯苷AY=888 061X-51 410(r=0.999 9),線性范圍1.08~10.76 μg/mL;連翹苷Y=747 692X-3 710(r=1.000 0),線性范圍0.13~1.32 μg/mL;綠原酸Y=1 798 549X-26 262(r=0.999 9),線性范圍0.44~4.44 μg/mL,均呈現良好的線性關系。
2.5 精密度試驗 精密量取“2.2.2”項下對照品溶液16 μL,置于2 mL量瓶中,50%甲醇定容至刻度,搖勻,在“2.1”項色譜條件下進樣測定6次,測得連翹酯苷A、連翹苷、綠原酸峰面積RSD分別為0.16%、0.07%、0.48%,表明儀器精密度良好。
2.6 重復性試驗 將同一批本品(批號201020)研成粉末,過6號篩,精密稱取6份,每份2 g,按“2.2.1”項下方法制備供試品溶液,在“2.1”項色譜條件下進樣測定,測得連翹酯苷A、連翹苷、綠原酸含量RSD分別為2.88%、2.22%、2.65%,表明該方法重復性良好。
2.7 穩定性試驗 將本品(批號201020)研成粉末,過6號篩,精密稱取2 g,按“2.2.1”項下方法制備供試品溶液,置于4 ℃冰箱中保存,每隔4 h取出,在“2.1”項色譜條件下進樣測定,測得連翹酯苷A、連翹苷、綠原酸峰面積RSD分別為0.58%、1.03%、2.47%,表明溶液在24 h內穩定性良好。
2.8 加樣回收率試驗 將各成分含量已知的本品(批號201020)研成粉末,過6號篩,精密稱取1 g,置于錐形瓶中,精密加入適量對照品溶液,平行9份,按“2.2.1”項下方法制備供試品溶液,在“2.1”項色譜條件下進樣測定,計算回收率[8],結果見表1。
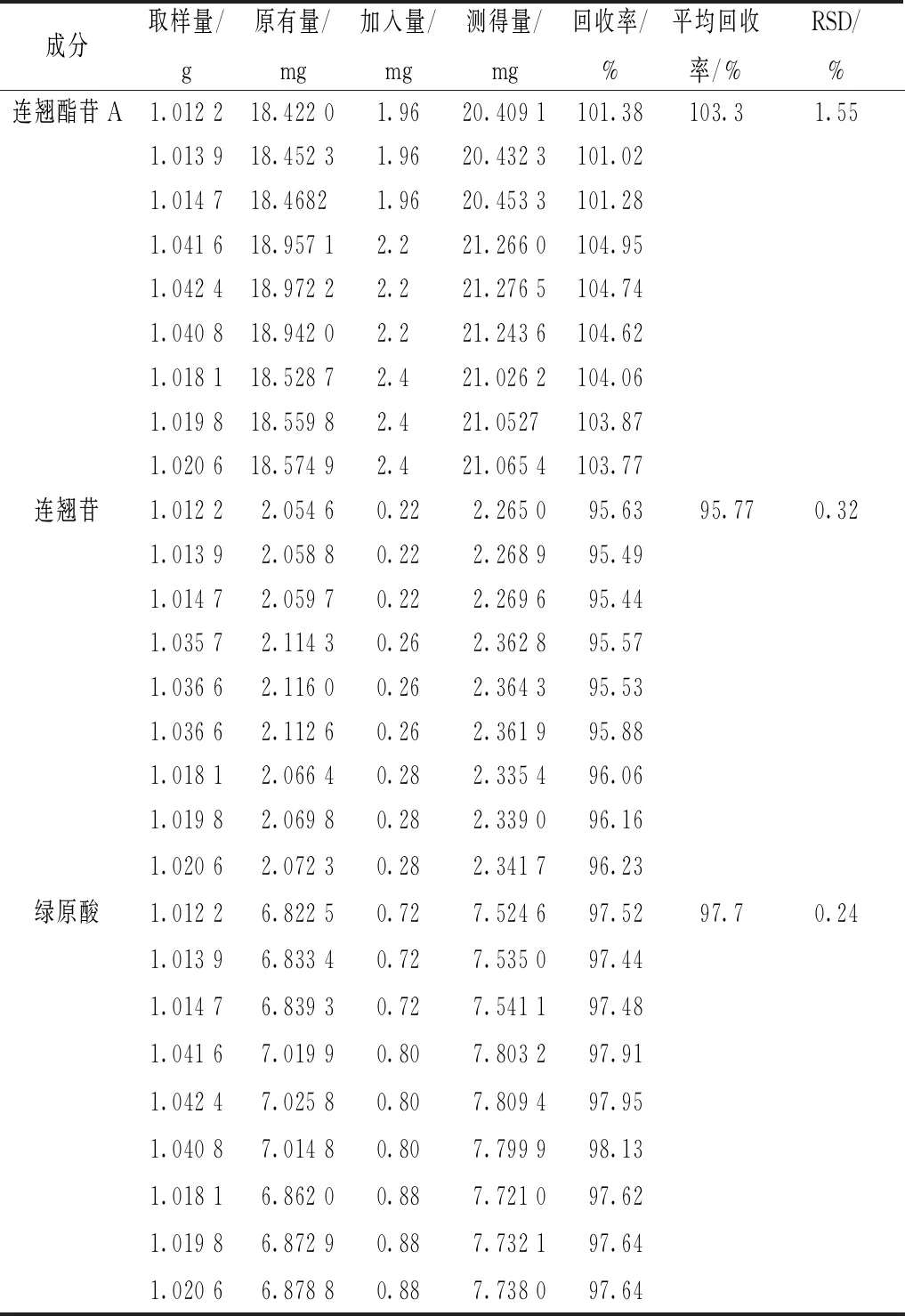
表1 各成分加樣回收率試驗結果(n=9)
2.9 相對校正因子計算 精密量取“2.2.2”項下對照品溶液5、10、15、20、30 μL,置于2 mL量瓶中,50%甲醇定容至刻度,搖勻,得不同質量濃度,在“2.1”項色譜條件下進樣測定,以連翹酯苷A為內標,計算其他2種成分相對校正因子fk/s[9],公式為fk/s=fk/fs=(CkAs)/(CsAk),其中Ck為其他成分含量,Ak為其他成分峰面積,Cs為內標含量,As為內標峰面積,結果見表2。
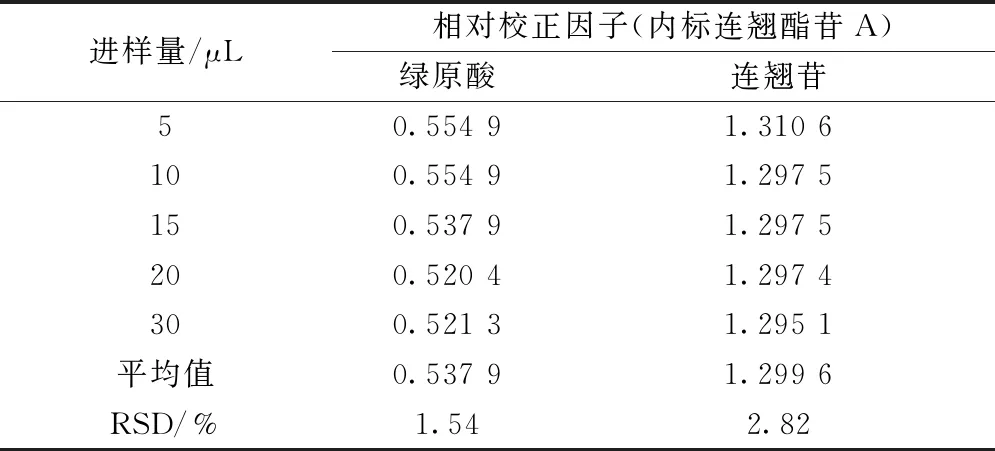
表2 各成分相對校正因子
2.10 不同儀器、色譜柱對相對校正因子的影響 分別采用Agilent 1260型、Waters e2695型色譜儀,以及Thermo Scientific BDS HYPERSIL C18、Hypersil BDS C18色譜柱(150 mm×4.6 mm,5 μm),按“2.9”項下方法計算相對校正因子,平行6次,結果見表3,可知均無明顯影響(RSD<3%)。
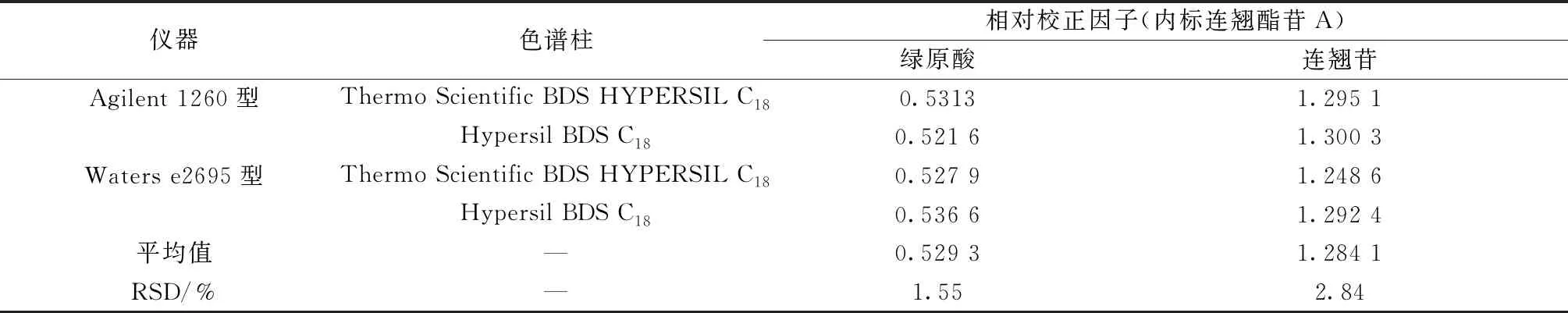
表3 不同儀器、色譜柱對相對校正因子的影響
2.11 色譜峰定位 考察了“2.10”項下儀器、色譜柱對相對保留時間的影響,結果見表4,可知均無明顯影響(RSD<3%)。

表4 不同儀器、色譜柱對相對保留時間的影響
2.12 樣品含量測定 取3批樣品,按“2.2.1”項下方法制備供試品溶液,各平行3份,在“2.1”項色譜條件下進樣測定,分別采用外標法、一測多評法計算含量,結果見表5。由此可知,2種方法所得結果接近[相對誤差(RE)<1%],表明一測多評法可用于含量測定。
3 討論
現代藥理研究表明,連翹酯苷A、連翹苷具有抗菌、抗衰老等作用[10-12],綠原酸具有抗內毒素、抗腫瘤等作用[13-14],均與連翹歸尾煎功能主治相符。由于連翹酯苷A在HPLC色譜圖中的出峰位置位于綠原酸和連翹苷的中間,并且性質較穩定,故本實驗以其為內標進行含量測定。
本實驗考察了流動相乙腈-0.2%甲酸、乙腈-0.1%甲酸的分離效果,發現以乙腈-0.1%甲酸洗脫時各成分基線分離較好,符合實驗要求。
4 結論
目前,有關一測多評法的報道大多是測定同一味藥中同一種類成分的含量[15-16],而本實驗測定了連翹歸尾顆粒中不同種類成分的含量,并且該方法具有專屬度高、重復性好、穩定性強、快速簡便、節約成本等優點,可為該制劑質量控制和評價提供參考依據。

