淺談環氧乙烷滅菌作為特殊過程在半月板縫合器產品中的過程確認
楊韓麗
(上海傲派醫療科技有限公司,上海 200000)
半月板縫合器產品屬于無菌植入性醫療器械。按照GMP要求,企業應選擇適宜的方法對該類產品進行滅菌,明確滅菌工藝和產品無菌保證水平(SAL),并提供滅菌確認的相關研究資料。本次研究在符合生產質量管理規范要求下[1],結合本公司的半月板縫合器產品,描述了半月板縫合器產品滅菌工藝的選擇及滅菌確認過程。
1 滅菌工藝的選擇
1.1 滅菌方法的研究
無菌醫療器械是一種無活微生物的產品。該類醫療器械滅菌方法的選擇是產品設計工藝研究的重要環節,目前可充分參考YY/T 1265—2015、YY/T 1267—2015和YY/T 0884—2013等標準考慮材料與滅菌方法的相容性,并考慮滅菌方法對產品成品(包括包裝材料)的適宜性及影響[2]。除此之外,設計開發過程還可以借鑒市場上已有同類產品的滅菌方式,通過對比分析并輸出文件資料確定產品最終滅菌方法。
1.2 滅菌方法的選擇
半月板縫合器產品主要在經皮或內窺鏡下軟組織修復手術中作為縫合閉合器使用,主要用于半月板修復重建手術[3]。產品主要由固定棒(聚醚醚酮或其他高分子材料)、縫線(超高分子量聚乙烯或其他材料)、插入器組件(不銹鋼)和手柄(ABS)等組成,產品結構如圖1所示,且采用單層吸塑盒與Tyvek片材包裝。半月板縫合器產品的原材料與常用滅菌方式的相容性總結如表1[4-5]所示。根據YY/T 1431—2016《外科植入物 醫用級超高分子量聚乙烯紗線》的附錄A.5,超高分子量聚乙烯材質縫線推薦使用環氧乙烷滅菌,同時分析該滅菌方式對半月板縫合器各組成原材料、包裝材料、產品結構、產品性能和使用方式等的影響,以及通過國家藥品監督管理局數據查詢,取得注冊證的同類產品大多是環氧乙烷滅菌,最終可得到環氧乙烷滅菌方法適宜半月板縫合器滅菌的結論。

圖1 產品結構圖
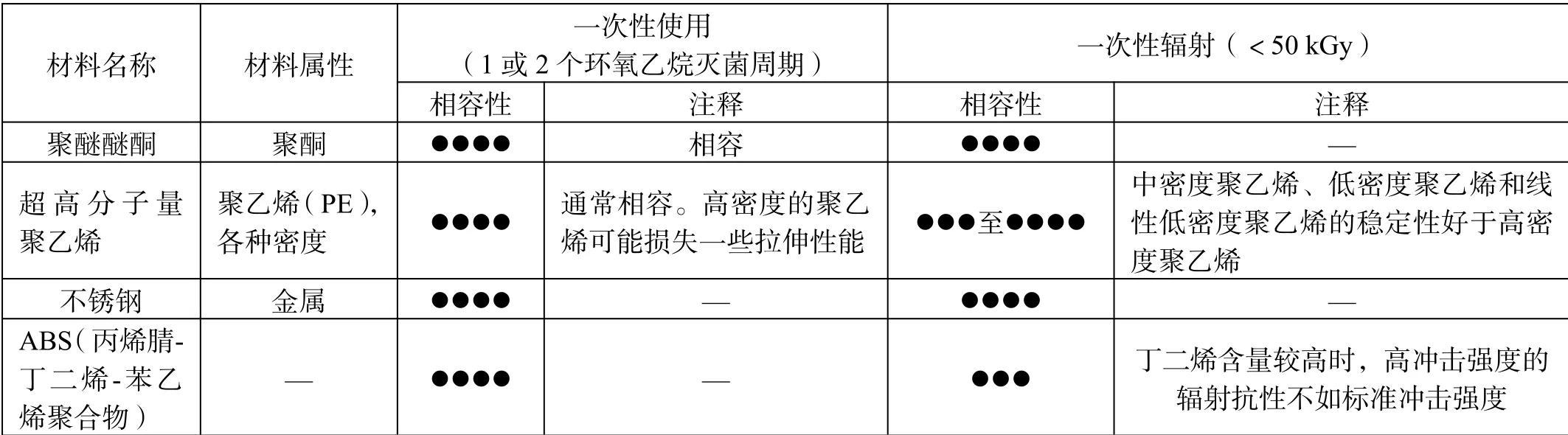
表1 原材料與常用滅菌方式的相容性
2 滅菌過程確認
2.1 滅菌確認的目的
滅菌確認的目的是證明預期滅菌工藝所設定的滅菌工藝過程及參數,能夠保證半月板縫合器產品達到公認的無菌保證水平(SAL,等于10-6)[6]及產品性能安全有效。
2.2 滅菌機構的選擇
醫療器械制造商往往將滅菌過程作為特殊過程并委托給有能力的環氧乙烷滅菌機構。在正式委托前,需根據質量管理體系要求對滅菌機構進行供方審核,并查驗滅菌機構的營業執照及質量體系證書(ISO 11135)等資料,確認資質。同時核查滅菌機構是否按照GB 18279或ISO 11135系列標準的要求對滅菌設備進行定期確認并查看文件資料。簽訂滅菌委托質量協議后,在委托期間,每年至少進行一次審核。
2.3 產品定義和技術評審
根據GB/T 18279.2—2015/ISO/TS 11135-2:2008第7章要求,產品在滅菌確認前需對產品進行產品定義和技術評審。產品定義是為了了解待滅菌產品的基本信息條件,并通過基本信息條件判定產品是否可劃分為一個環氧乙烷產品族。技術評審是對新產品或改進的產品及已確認的產品和/或用于確認現存的環氧乙烷過程的過程挑戰裝置(PCD)進行比較[7]。本次研究僅針對半月板縫合器的首次滅菌確認,故技術評審僅針對同一注冊單元內各規格型號,比較出內部過程挑戰裝置。
2.3.1 產品定義
半月板縫合器產品定義包括產品的本身、初包裝、其他任何附件、說明書及初包裝內的其他物品,還包括產品預期功能說明及現有制造和滅菌過程[7]。產品定義過程還應考慮GB/T 18279.2—2015/ISO/TS 11135-2:2008中7.1.1要求。通過產品定義的方式評估半月板縫合器,從產品結構類似、包裝方式一致、預期用途一致、制造過程一致、為一次性使用、裝載方式一致等方面,可得到結論:一個注冊單元內半月板縫合器產品各規格可劃分為一個環氧乙烷產品族進行滅菌確認。
2.3.2 技術評審
對半月板縫合器產品進行技術審核,宜從產品結構、產品生物負載、加工方式、產品包裝、產品裝載評估各規格型號,從比較中選擇最難的內部過程挑戰裝置的規格。新產品首次滅菌確認可參考GB/T 18279.2—2015/ISO/TS 11135-2:2008要求。上海傲派醫療科技有限公司半月板縫合器產品通過技術評審,無法判斷出最難的內部過程挑戰裝置,故依據結構方面的差別,最終選出2種不同規格的產品作為內部過程挑戰裝置1號(IPCD-1)和內部過程挑戰裝置2號(IPCD-2),在短周期進行抗性對比得出最難滅菌的內部過程挑戰裝置。
2.4 滅菌確認
滅菌確認可以證明某一特定過程能夠持續和有效地生產出符合無菌保證水平要求的產品[7]。滅菌確認由多個階段組成:安裝鑒定(IQ)和運行鑒定(OQ)、性能鑒定(PQ)[7]。
2.4.1 安裝鑒定(IQ)和運行鑒定(OQ)
上海傲派醫療科技有限公司產品滅菌確認是委托有資質的機構共同完成,其中安裝和運行鑒定由滅菌機構實施,但醫療器械制造商需監控審核。
滅菌機構提供的安裝鑒定報告,上海傲派醫療科技有限公司需按照GB/T 18279.2—2015/ISO/TS 11135-2:2008中9.1要求審核滅菌機構設備的安裝是否符合適用的規范和要求[7]。滅菌機構提供的運行鑒定報告,上海傲派醫療科技有限公司需按照GB/T 18279.2—2015/ISO/TS 11135-2:2008中9.2要求審核,重點包含溫濕度分布測試、柜室泄漏測試、抽真空速率以及柜室壁溫研究[7]。
審核過程中需理解各項要求的審核目的,便于更好地理解滅菌確認過程。
2.4.2 性能鑒定(PQ)
性能鑒定包括進行超出常規監視范圍外的嚴格的微生物和物理測試,以證明滅菌過程的有效性和再現性。性能鑒定通常是在安裝和運行鑒定完成后開始的。接受準則宜包括滅菌過程參數和微生物挑戰符合規范[7]。
2.4.2.1 性能鑒定——微生物鑒定
微生物性能鑒定(MPQ)通常采用至少有一個參數設置低于正常生產參數值的滅菌過程來實施。最經常調整的參數是氣體作用時間、氣體濃度和過程溫度。選擇用于微生物性能鑒定的過程比建立的常規過程參數更具有挑戰性(就能達到無菌可能性方面)[7]。微生物挑戰通俗可以理解為產品在規定的滅菌參數下均能保證無菌,為了滿足滅菌過程殺滅率的保守性確定,上海傲派醫療科技有限公司半月板縫合器選擇常用的過度殺滅法:選擇較短的EO暴露時間(遠遠少于半周期循環時間),按照已確認的產品滅菌裝載(根據滅菌柜和滅菌托盤規劃)放置IPCD和正常生產的產品(產品規格從技術評審可知)、按照GB 18279.1—2015/ISO 11135-1:2007標準中附錄C放置EPCD,運行一個短周期。半月板縫合器如上文2.3.2所述,IPCD選擇有2種,如圖2、圖3所示。

圖2 IPCD-1示意圖

圖3 IPCD-2示意圖
EPCD的選擇有3種,生物指示劑(BI)包裝在一層、兩層、三層復合薄膜包裝內,形式如圖4、圖5、圖6所示。

圖4 EPCD-1示意圖

圖5 EPCD-2示意圖

圖6 EPCD-3示意圖
運行短周期預期達到的結果,EPCD陽性率高于或等于IPCD陽性率[8],從而選擇出合適的EPCD和最難滅菌的IPCD,且產品測試結果必須顯示無菌。才能證明產品負載的抗性低于PCD的抗性。上海傲派醫療科技有限公司滅菌確認短周期運行結果:產品測試均無菌,IPCD-1為最難滅菌產品,EPCD-1為最合適的日常監測用挑戰裝置。
2.4.2.2 性能鑒定——物理性能鑒定
物理性能鑒定應證明:①過程再現性,應包括至少3次連續的、有計劃的鑒定運行,且滿足所有規定的接受準則;②負載滿足擬定的常規過程規范規定的接受準則[9]。上海傲派醫療科技有限公司半月板縫合器物理性能鑒定選用的半周期法,是保守性滅菌過程方法——過度殺滅法常采用的方法之一。總共運行3次連續的試驗,結果為生物指示劑全部滅活,以確認最小暴露時間。規定的暴露時間至少為此最小時間的2倍[6]。半月板縫合器根據微生物鑒定中最后的選擇,半周期3次循環中,按照已確認的滅菌裝載放置EPCD與IPCD以及溫濕度監控儀(或滅菌柜自帶),預期結果為IPCD和EPCD內生物指示劑全部滅活,才能證明產品在日常滅菌過程中能夠達到10-6無菌保證水平。上海傲派醫療科技有限公司3次半周期結束,完全達到了預期結果,且核查過程參數均維持在規定范圍內。
2.4.3 整周期
在性能鑒定后,需運行至少2次整周期,預期效果為:①過程參數符合規定的滅菌參數過程規范;②PCD無微生物生長;③產品的性能、穩定性和包裝完整性在2次滅菌后能符合產品既定的質量要求。此處提及一點,上海傲派醫療科技有限公司產品由于裝載一致,故主要從產品性能和包裝考慮,選擇了具有不同產品性能要求的代表規格運行整周期。整周期結論,上海傲派醫療科技有限公司半月板縫合器產品的PCD無微生物生長,且產品性能和包裝在兩次滅菌后不影響產品質量,過程參數滿足既定規范。
3 總結
產品滅菌除上述環氧乙烷滅菌確認外還包含環殘解析驗證、日常放行規范、保持滅菌過程有效性等需符合GMP要求,此研究不一一贅述。環氧乙烷滅菌確認是個特殊且復雜的確認過程,依據GB 18279.1—2015/ISO 11135-1:2007標準規定的流程和《醫療器械生產質量管理規范》規定的要求,完成產品環氧乙烷滅菌過程中各流程的確認。以本文的半月板縫合器產品為例,需知悉在實際滅菌確認過程中不同產品要具體分析其滅菌細節,且和滅菌委托機構保持有效溝通。隨著醫療器械行業的快速發展,質量管理體系核查愈來愈嚴格,企業需在產品設計開發過程中充分考慮滅菌方法和確定滅菌供應商,并對產品滅菌過程進行嚴格的確認和核查,提高企業滅菌確認的技能。

