帕金森病患者日間過度嗜睡與帕金森病癥狀的相關性
唐文靜,羅永杰,2
(1.西南醫科大學臨床醫學院,四川 瀘州 646000;2.四川省醫學科學院·四川省人民醫院神經內科,四川 成都 610072)
日間過度嗜睡(excessive daytime sleepiness,EDS)作為帕金森病(Parkinson’s disease)患者常見的睡眠障礙之一,是指患者在白天日常生活工作中,出現不恰當的、難控制的入睡,其在帕金森病人群中的發病率高達54%[1]。EDS由于時間、場景的不確定性給帕金森病患者造成嚴重的生命威脅,一項社會研究調查發現,約11%的帕金森病患者在近5年發生過不同程度的交通事故[2]。國內外大量研究發現,男性、高齡、認知功能障礙、睡眠障礙、多巴胺受體激動劑的使用等是EDS的易感因素[3]。目前國內對帕金森病患者合并EDS的關注度不夠,兩者相關性的研究較少,且存在較大的局限性和片面性,EDS與帕金森病癥狀間的相關性還需進一步證實。本研究應用量表評估方法,探討帕金森病患者EDS的特點及其與帕金森病癥狀的相關性,為帕金森病伴EDS的早識別、早診斷、早治療提供臨床依據,現報道如下。
1 資料與方法
1.1 一般資料 本研究收集2016年7月至2021年7月在四川省人民醫院神經內科就診的帕金森病患者157例。納入標準:(1)年齡>18歲;(2)符合2015年的國際運動障礙協會對帕金森病的新臨床診斷標準[4];(3)患者或家屬知情,并簽署知情同意書。排除標準:(1)帕金森疊加綜合征及繼發性帕金森綜合征等;(2)作息時間倒錯,服用麻醉鎮靜類藥物,嚴重心、腦、肺等疾病所致繼發性EDS;(3)嚴重癡呆、膀胱功能障礙、視聽障礙等不能配合本研究的疾病。根據Epworth嗜睡量表(ESS)評分結果將患者分為EDS組與非EDS組(NEDS組),同時采用帕金森病相關國際量表評估患者癥狀。本研究獲得四川省人民醫院倫理委員會批準。
1.2 調查內容 (1)基本資料:性別、年齡、發病年齡等基本資料;(2)運動癥狀:應用國際運動障礙協會統一帕金森病評定量表第三部(MDS-UPDRS-Ⅲ)評估患者運動癥狀,采用Hoehn-Yahr分期評分(H-Y分期)進行分期;(3)非運動癥狀:采用匹茲堡睡眠質量指數(PSQI)、ESS、快動眼睡眠行為障礙篩查量表(RBDSQ)評估睡眠質量;采用漢密爾頓焦慮量表(HAMA)、漢密爾頓抑郁量表(HAMD)評估情緒狀況;采用簡易精神狀態檢查量表(MMSE)評估認知功能;采用疲勞嚴重程度量表(FSS)評估疲勞狀況;采用膀胱過度活動癥狀評分(OABSS)評估膀胱功能;采用額葉功能評定表(FAB)評估額葉功能;詢問患者是否存在嗅覺減退;詢問患者是否存在消化系統癥狀、便秘、怕冷/熱等,以評估患者自主神經功能情況;(4)EDS評估:采用ESS評估,評分≥10分定義為EDS[5]。
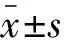
2 結 果
2.1 兩組帕金森病患者臨床特點比較 本研究共收集157例帕金森病患者,其中男性83例(52.87%)、女性74例(47.13%),平均年齡65.15歲。兩組UPDRS-Ⅲ分值、H-Y分期、FSS分值、OABSS分值、HAMA分值、HAMD分值、MMSE分值、FAB分值、自主神經功能合并癥情況比較差異均有統計學意義(P<0.05)。而兩組性別、發病年齡、PSQI分值、嗅覺減退例數、快動眼睡眠障礙例數比較差異均無統計學意義(P>0.05)。見表1。
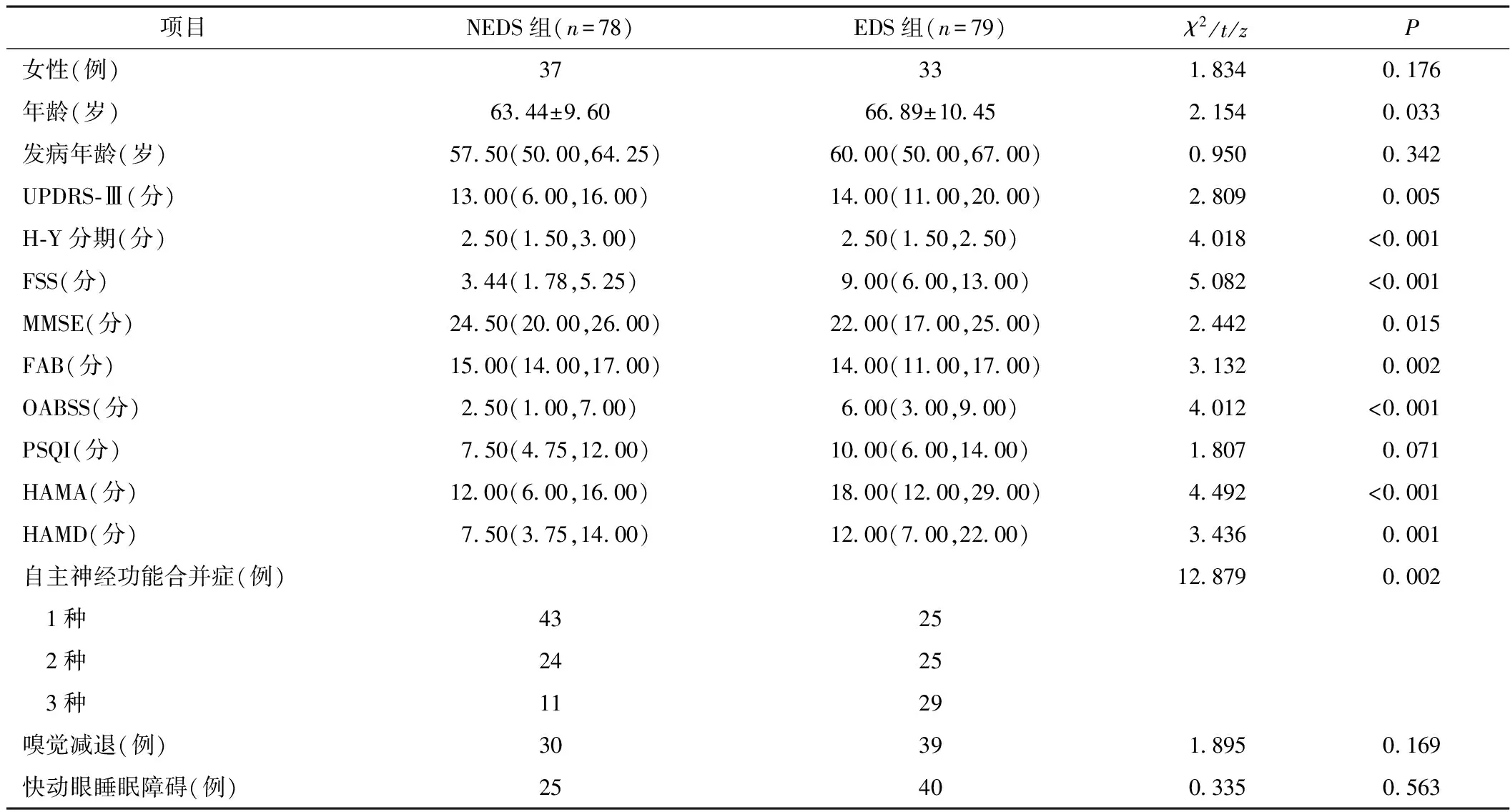
表1 兩組帕金森病患者臨床特點的單因素分析
2.2 影響帕金森病患者EDS的logistic回歸分析 將單因素分析中有統計學意義的因素納入多因素logistic回歸分析,所有數據進入回歸分析前按照國際評分量表進行分組[6-8]。其中UPDRS-Ⅲ無明確分類標準,以中位數14分進行變量賦值。結果顯示高H-Y分期、疲勞是帕金森病患者EDS的獨立危險因素(P<0.05)。見表2。

表2 影響帕金森病患者EDS的logistic回歸分析
3 討 論
帕金森病患者多合并諸多非運動癥狀,EDS是帕金森病患者常見的睡眠障礙表現形式。有研究表明,EDS可在帕金森病運動癥狀出現前10年發生,對于帕金森病發病有一定的警示性作用[9]。EDS不僅會增加帕金森病患者在日常生活中出現意外的風險,還會加重帕金森病患者的其他癥狀,給家庭帶來沉重的負擔。目前,國內外對于帕金森病癥狀與EDS之間關系的研究存在諸多爭議。耿海威等[10]的研究著重于分析EDS與藥物的相關性,但并未將其他帕金森病癥狀納入分析。另一項研究顯示,帕金森病的EDS癥狀與性別、認知功能有關,但忽略了患者自主神經功能、額葉功能、疲勞等的影響,且樣本量較小,代表性不足[11]。本研究借助國際量表,首次增加了額葉功能評估、膀胱過度活動癥狀評估,以全面分析EDS與帕金森病癥狀之間的相關性,更具有代表意義。
在本研究中,50.32%的帕金森病患者存在EDS,與既往的研究結果基本一致[1]。單因素分析顯示,帕金森病合并EDS與運動癥狀、認知功能、情緒障礙、自主神經功能、疲勞、額葉功能、膀胱過度活動癥狀均有關。其中年齡、認知障礙、情緒障礙、自主神經功能障礙等結果與既往的研究結果類似[12,3]。
本研究logistic回歸分析顯示,高H-Y分期是帕金森病合并EDS的獨立危險因素之一,高H-Y分期的帕金森病患者發生EDS的概率是低H-Y分期的2.078倍(P=0.041)。目前的觀點認為多巴胺在睡眠-覺醒周期中發揮作用,與喚醒有關,該功能取決于多巴胺的濃度和受體的靈敏度[13-14]。而隨著帕金森病病程的進展,人體自身的多巴胺功能減退,因此高H-Y分期的帕金森病患者會出現更嚴重的運動癥狀與非運動癥狀。Suzuki等[15]研究顯示,H-Y分期4期的帕金森病患者的EDS癥狀明顯比1、2、3期患者更嚴重。帕金森病患者在H-Y分期4期時,多巴胺能神經元的變性壞死和α-突觸核蛋白異常聚集累及中腦,導致其運動障礙,而在H-Y分期3期時其睡眠障礙已經出現[16]。另外,從下丘腦側區釋放的食欲素也與EDS相關,Amara等[17]發現帕金森病患者的食欲素細胞明顯減少,尤其是晚期的帕金森病患者,食欲素水平更低,進一步增加睡眠失調和猝倒發作風險。logistic回歸分析還顯示,疲勞是帕金森病合并EDS的另一獨立危險因素,伴疲勞的帕金森病患者發生EDS的概率是無疲勞患者的3.878倍(P<0.001)。帕金森病患者的運動癥狀,如震顫、僵硬、異動等,可加重疲勞現象。有研究發現,帕金森病的疲勞與背側紋狀體灰質體積減小有關,紋狀體則參與多巴胺信息的傳遞。因此疲勞與EDS具有間接關系[18],這與本研究結論一致。
本研究中,EDS組患者額葉功能評分更低,膀胱過度活動癥狀評分更高。周慧等[19]通過靜息態功能磁共振成像(rs-fMRI)對帕金森病患者進行靜態腦功能檢測發現,帕金森病伴EDS的神經網絡機制可能是額葉神經元的自發放電,EDS的節律調控中樞為丘腦,額葉參與其中,可見兩者在解剖區域具有一定的重疊性。另外,夜尿的增多可直接影響患者夜間睡眠體驗,進而導致帕金森病患者EDS癥狀加重。值得注意的是,本研究并未得出性別、夜間睡眠障礙分值與EDS有關,可能為分組標準、統計學方法不同所致。
綜上所述,EDS可與帕金森病患者長期共存,顯著增加了患者及護理人員的困擾和負擔。鑒于EDS與諸多帕金森病癥狀均具有相關性,建議在臨床工作中,應多從整體癥狀考慮,制定針對性的治療方案,從而改善患者的EDS癥狀,提高患者及其家人的生活質量。

