明膠納米顆粒穩定的Pickering乳液的制備及表征
王欣欣,吳霞,李德富,穆暢道,葛黎明
(四川大學 化學工程學院,四川 成都,610065)
傳統由表面活性劑穩定的乳液,存在表面活性劑用量較多、成本高、生物毒性較大和不穩定等問題。由固體顆粒不可逆地吸附在兩相界面上以改變空間位阻來實現穩定的Pickering乳液,具有優良的抗聚集、抗絮凝和奧氏成熟等優點,近年來被廣泛應用于生物醫藥、食品、化妝品等領域[1-2]。目前,Pickering乳液的研究多集中在無機顆粒上,這些無機或合成的固體顆粒存在著潛在的健康風險,大多被應用于石油、化工等領域。當前,研究人員致力于研發以廣泛來源于動植物、低/無毒可食、可生物降解和生物相容性好的膠體粒子穩定的Pickering乳液[3]。明膠是一種蛋白質生物聚合物,由天然膠原部分水解得到。它價格低廉,具有良好的生物相容性、生物降解性,在制備食品級膠體粒子方面具有很大的潛力。然而,明膠具有強親水性且能與水形成可逆凝膠,難以制備穩定且單分散的明膠納米顆粒[4]。此外,在先前大多數的研究中,制備明膠基Pickering乳液往往需要加入對人體有毒害的戊二醛[5]等交聯劑對明膠進行疏水改性,大大限制了其在食品、化妝品等領域的應用。京尼平是一種天然環烯醚萜類化合物,在中藥中廣泛用作利膽劑和消炎劑[6]。據報道,京尼平的毒性較戊二醛的毒性低5 000~10 000倍,常被用來替代傳統的小分子醛交聯劑,是一種生物相容性好和低毒性的蛋白質交聯劑[7]。因此,京尼平可被用于制備安全無毒的明膠納米顆粒。
基于此,本研究以明膠為基料,通過2次去溶劑結合京尼平交聯固化明膠法制備得到明膠納米顆粒,并表征其微觀形貌、三相接觸角、粒徑和Zeta電位。然后以明膠納米顆粒為乳化劑制備Pickering乳液,研究了明膠納米顆粒的濃度、乳化轉速、乳化時間、pH值和鹽濃度對制備的Pickering乳液的影響,獲得明膠納米顆粒穩定的Pickering乳液的最佳制備工藝。
1 材料與方法
1.1 材料與試劑
B型明膠(醫用級,膠強度為Bloom 240 g)、玉米油(AR級),上海阿拉丁生化科技股份有限公司;丙酮(AR級)、NaOH(AR級)、鹽酸(AR級)、NaCl(AR級),成都市科隆化學品有限公司;京尼平(HPLC, >98%),臨川之信生物科技有限公司。
1.2 儀器與設備
Ultra Turrax T25均質乳化機,德國IKA公司;FE 28-XX pH計,梅特勒-托利多(上海)有限公司;ST 16R高速冷凍離心機、Nicolet iS10傅里葉變換紅外光譜儀,美國Thermo Fisher Scientific公司;Helios G4 UC掃描電子顯微鏡,美國FEI公司;SPM-9600原子力顯微鏡,日本Shimadzu公司;Nano-ZS ZEN3600激光粒度儀,英國Malvern公司;OCAH光學接觸角測量儀,德國DATAPHYSICS公司;PH-100-DB800U-1PL光學顯微鏡,鳳凰光學集團有限公司;MCR302模塊化智能型旋轉流變儀,奧地利Anton Paar公司。
1.3 明膠納米顆粒的制備
將1.250 g明膠于45 ℃下溶解于25.0 mL去離子水中得到明膠溶液。然后緩慢加入25.0 mL丙酮,靜置以待溶液分層。取上層乳白色液體復溶于25.0 mL去離子水中,之后使用NaOH溶液將其pH值調為12.0。將上述混合液于50 ℃下持續攪拌,并以1.0 mL/min的速度滴加75.0 mL丙酮。接著加入0.125 0 g京尼平粉末,于50 ℃下繼續攪拌5 h。將混合液于10 000 r/min下離心35 min后使用去離子水清洗下層沉淀3次。最后將明膠納米顆粒分散于去離子水中,緩慢揮發掉殘余的丙酮。
1.4 明膠納米顆粒的表征
1.4.1 掃描電子顯微鏡(scanning electron microscope, SEM)觀察
將明膠納米顆粒懸浮液滴加到導電膠上,真空干燥24 h,在樣品表面噴金后使用掃描電子顯微鏡觀察明膠納米顆粒的微觀形貌。
1.4.2 原子力顯微鏡(atomic force microscope, AFM)觀察
將10 μL明膠納米顆粒懸浮液滴于云母片上,真空干燥24 h后使用原子力顯微鏡觀察明膠納米顆粒的微觀形貌。
1.4.3 三相接觸角測定
將1片干凈的玻璃片浸入100 mg/L的明膠納米顆粒懸浮液中,靜置10 s后取出,于真空干燥箱中緩慢蒸發掉液體,重復操作3次。將干燥后的玻璃片放置于正己烷中,利用光學接觸角測量儀測定明膠納米顆粒的三相接觸角。
1.4.4 紅外光譜分析
分別將2 mg明膠和冷凍干燥的明膠納米顆粒與200 mg KBr充分研磨,壓片后利用傅里葉變換紅外光譜(Fourier transform infrared spectroscopy, FTIR)儀測定其FTIR光譜。設置掃描的波數范圍為400~4 000 cm-1,掃描頻率為4 cm-1/s。
1.4.5 粒徑分布和Zeta電位測定
配制質量濃度為100 mg/L的明膠納米顆粒懸浮液,然后使用激光粒度儀于25 ℃下測定明膠納米顆粒的粒徑。配制質量濃度為100 mg/L的明膠納米顆粒懸浮液,使用0.1 mol/L的HCl溶液和NaOH溶液將其pH值分別調至2.0、4.0、6.0、8.0、10.0、12.0后使用激光粒度儀于25 ℃下測定明膠納米顆粒在不同pH值下的Zeta電位。
1.5 明膠納米顆粒穩定的Pickering乳液的制備
以明膠納米顆粒為乳化劑,分別研究明膠納米顆粒的濃度、乳化時間、乳化轉速、水相pH值和鹽濃度對制備的Pickering乳液的影響。
1.5.1 明膠納米顆粒濃度的影響
分別配制質量濃度為10.0、15.0、20.0 mg/mL的明膠納米顆粒懸浮液,按照明膠納米顆粒懸浮液與玉米油體積比為1∶4加入玉米油,然后使用均質機于13 000 r/min下乳化90 s,制備得到明膠納米顆粒穩定的Pickering乳液。
1.5.2 乳化時間的影響
將質量濃度為20.0 mg/mL的明膠納米顆粒懸浮液與玉米油按體積比為1∶4混合,然后使用均質機于13 000 r/min下乳化30、60、90、120 s,制備得到明膠納米顆粒穩定的Pickering乳液。
1.5.3 乳化轉速的影響
將質量濃度為20.0 mg/mL的明膠納米顆粒懸浮液與玉米油按體積比為1∶4混合,然后使用均質機于7 000、10 000、13 000、16 000 r/min下乳化90 s,制備得到明膠納米顆粒穩定的Pickering乳液。
1.5.4 水相pH值的影響
配制質量濃度為20.0 mg/mL的明膠納米顆粒懸浮液,分別調節其pH值為6.0、8.0、10.0、12.0。按照明膠納米顆粒懸浮液與玉米油體積比為1∶4加入玉米油,然后使用均質機于13 000 r/min下乳化90 s,制備得到明膠納米顆粒穩定的Pickering乳液。
1.5.5 鹽濃度的影響
配制質量濃度為20.0 mg/mL的明膠納米顆粒懸浮液,分別加入0、25、50、75 mmol/L的NaCl溶液,調節其pH值為8.0。按照明膠納米顆粒懸浮液與玉米油體積比為1∶4加入玉米油,然后使用均質機于13 000 r/min下乳化90 s,制備得到明膠納米顆粒穩定的Pickering乳液。
1.6 明膠納米顆粒穩定的Pickering乳液的表征
1.6.1 Pickering乳液的微觀形貌觀察及粒徑統計
將制備的Pickering乳液分散在去離子水中,取少量滴在載玻片上,然后使用光學顯微鏡觀察Pickering乳液的微觀形貌,并通過Nano-measure軟件統計其粒徑。
1.6.2 Pickering乳液的流變性能測試
使用模塊化智能型旋轉流變儀測定Pickering乳液的流變性能。采用平行板流變模式(plate-plate mode, PP25),并在1 Hz下對樣品進行應變掃描,測量溫度為25 ℃。
2 結果與討論
2.1 明膠納米顆粒的制備及表征
通過2次去溶劑結合京尼平交聯固化明膠法制備得到的明膠納米顆粒呈光滑且致密的球形,分散性好,直徑約為150 nm,如圖1-a和圖1-b所示。由原子力顯微鏡的三維高度圖可知,明膠納米顆粒的平均垂直高度約為15 nm,明顯小于其直徑,表明明膠納米顆粒為軟顆粒,有利于制備穩定的Pickering乳液[8]。
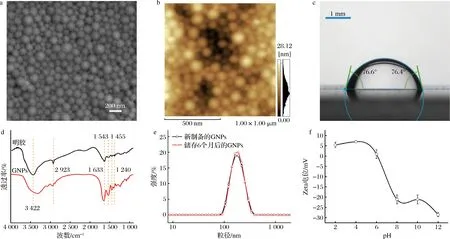
a-SEM圖;b-AFM圖;c-接觸角測量圖;d-FT-IR圖;e-粒徑分布圖;f-Zeta電位圖1 明膠納米顆粒的SEM圖,AFM圖,接觸角測量圖,FT-IR圖,粒徑分布圖,Zeta電位Fig.1 SEM images, AFM images, contact angel, FT-IR spectra, size distribution and Zeta potential characterization of gelatin nanoparticles
固體顆粒的表面潤濕性直接影響Pickering乳液的類型和穩定性,根據WILLIAMS等[9]提出的“液滴捕獲法”測得明膠納米顆粒的三相接觸角θow為76.6°。表明明膠納米顆粒具有較強的親水性能,適合用于制備水包油(O/W)型Pickering乳液[10],如圖1-c所示。

由圖1-e可知,利用激光粒度儀測定新制備的明膠納米顆粒的粒徑為(186.7±0.065) nm,其略大于SEM和AFM的測試結果。主要是因為分散在水中的明膠納米顆粒充分溶脹,導致其粒徑增大。儲存6個月后的明膠納米顆粒的粒徑為(186.9±0.028) nm,結果表明2次去溶劑結合京尼平交聯固化明膠法能制備出穩定的明膠納米顆粒。
納米顆粒的Zeta電位影響著其自身的儲存穩定性,也決定著其制備的乳液穩定性[18]。明膠納米顆粒在不同pH值下的Zeta電位如圖1-f所示。當pH≤4.0時,明膠納米顆粒帶6.0 mV的正電荷;隨著pH值的不斷增加,明膠納米顆粒所帶的正電荷減少,當pH值為6.0左右時,明膠納米顆粒表面所帶的凈電荷為0,即達到明膠納米顆粒的等電點;隨著pH值的繼續增大,明膠納米顆粒帶負電荷,且所帶的負電荷隨著pH值的增加而逐漸增大。當pH值為12時,明膠納米顆粒的Zeta電位為-28.5 mV。因此明膠是1種兩性電解質,含有大量酸性氨基酸(含有羧基)和堿性氨基酸(含有氨基)。明膠分子中的氨基和羧基等官能團通過得失電子以分別在較高pH值溶液中帶負電荷,而在較低pH值溶液中帶正電荷。
2.2 明膠納米顆粒的濃度對Pickering乳液的影響
不同濃度明膠納米顆粒穩定的Pickering乳液的直觀圖如圖2-a所示。當明膠納米顆粒的質量濃度大于15.0 mg/mL時,制備的Pickering乳液在倒置后仍然能夠承受自身質量而不流動,表明其形成了半固體凝膠狀Pickering乳液。由圖2-b和圖2-c可知,10.0、15.0、20.0 mg/mL明膠納米顆粒穩定的Pickering乳液的液滴直徑分別為(92.50±3.62)、(74.53±4.53)和(43.67±3.37) μm。隨著明膠納米顆粒濃度的增加,制備的Pickering乳液液滴尺寸不斷減小,液滴的均勻性不斷提高。隨著顆粒濃度的增大,油水界面吸附的固體顆粒數量增多,多余的顆粒可以在水相中輕微絮凝,形成三維網絡結構,進而增強乳液的穩定性。綜合乳液的穩定性及其液滴直徑,確定制備Pickering乳液的最佳顆粒質量濃度為20.0 mg/mL。

a-穩定的Pickering乳液;b-Pickering乳液的光學顯微鏡圖;c-平均粒徑圖2 不同濃度的明膠納米顆粒穩定的Pickering乳液,Pickering乳液的光學顯微鏡圖及平均粒徑Fig.2 Images, optical micrographs and average emulsion particle size of Pickering emulsions prepared using different concentration of gelatin nanoparticles
2.3 乳化時間對Pickering乳液的影響
在不同乳化時間下制備的Pickering乳液如圖3所示。僅有乳化90 s制備的Pickering乳液在倒置情況下能夠承受自身質量而不流動。當乳化時間從30增加到90 s時,乳液液滴尺寸不斷減小,與文獻報道的情況相符[19]。乳化時間的增加有利于顆粒在體系中的分散,同時能幫助其遷移到油水界面上進行鋪展,形成的液滴尺寸也有所減小[20]。繼續增加乳化時間至120 s時,液滴的尺寸增大。這可能是由于持續的能量輸入造成已吸附在界面處的顆粒的重排,乳液發生相反轉或形成多重乳液[21],進而破壞了乳液的穩定性。因此,確定乳化的最佳時間為90 s。

a-穩定的Pickering乳液;b-Pickering乳液的光學顯微鏡圖;c-平均粒徑圖3 明膠納米顆粒在不同乳化時間下穩定的Pickering乳液,Pickering乳液的光學顯微鏡圖及平均粒徑Fig.3 Images, optical micrographs and average emulsion particle size of Pickering emulsions prepared under different emulsification time
2.4 乳化轉速對Pickering乳液的影響
低乳化轉速下制備的Pickering乳液有油相析出,高乳化轉速下制備的乳液在倒置后不能承受自身質量而發生流動,均不能形成穩定的乳液。由圖4可知,在13 000 r/min乳化轉速下能夠制備穩定的Pickering乳液。

a-穩定的Pickering乳液;b-Pickering乳液的光學顯微鏡圖;c-平均粒徑圖4 明膠納米顆粒在不同乳化轉速下穩定的Pickering乳液,Pickering乳液的光學顯微鏡圖及平均粒徑Fig.4 Images, optical micrographs and average emulsion particle size of Pickering emulsions prepared under different emulsification speed
當均質乳化轉速小于13 000 r/min時,乳液的液滴尺寸較大。表明均質轉速過低,輸入體系的能量小,很難打破兩相界面使納米顆粒吸附在油水界面,形成穩定的乳液。然而,當乳化轉速提高到16 000 r/min時,制備的乳液液滴分散不均勻,很多固體顆粒發生堆疊形成聚集體。轉速過大使得顆粒間的外力增強,將原來已吸附于兩相界面處的顆粒發生異動并重排,部分顆粒游離于水相中,發生聚集及堆疊。在乳化轉速為13 000 r/min下制備的乳液的液滴分散相對均一,尺寸為(41.71±0.86) μm。綜合乳液的穩定性和液滴的顯微鏡圖確定乳化的最佳轉速為13 000 r/min。
2.5 水相pH值對Pickering乳液的影響
如圖5所示,當水相pH為12.0時制備的乳液發生了油水相分離。明膠納米顆粒在界面上的吸附效率強烈依賴其表面所帶電荷或溶液的離子強度。在pH值較高的條件下,過多NaOH的加入極大程度地改變了體系的離子強度,屏蔽了顆粒表面的電荷量,影響其溶脹程度[22]。而顆粒在界面處的溶脹程度會影響到其是否能穩定吸附,故pH過高時無法形成穩定的Pickering乳液,由此可見顆粒的溶脹性能與乳液的穩定性關聯較大。當水相pH值為6時,接近明膠納米顆粒的等電點,均質乳化后制備的乳液立即發生大范圍的相分離。此外,通過京尼平與明膠發生席夫堿反應制備的明膠納米顆粒在酸性條件下由于席夫堿的斷裂而遭到不同程度的破壞,從而影響明膠納米顆粒的表面潤濕性。結果表明,酸性及過堿性環境不利于制備明膠納米顆粒穩定的Pickering乳液。然而,在pH為8時能夠制備乳液液滴直徑為(55.00±5.06) μm的穩定的Pickering乳液。帶電的軟顆粒在界面上表現出類似軟凝膠的行為,從而導致更加穩定的乳液的形成。而電中性軟顆粒包覆液滴表面所形成的吸附層非常脆弱,因而不能依此制備出穩定的乳液。穩定的Pickering乳液的制備依賴水相pH值,本研究最佳的水相pH值為8.0。

a-穩定的Pickering乳液;b-Pickering乳液的光學顯微鏡圖;c-平均粒徑圖5 明膠納米顆粒在不同pH下穩定的Pickering乳液,Pickering乳液的光學顯微鏡圖及平均粒徑Fig.5 Images, optical micrographs and average emulsion particle size of Pickering emulsions prepared under different pH
2.6 鹽濃度對Pickering乳液的影響
水相中的電解質會在一定程度上影響顆粒的聚沉,從而影響到乳液的形成[23]。由圖6可知,在NaCl濃度為0、25、50和75 mmol/L下制備的Pickering乳液液滴直徑分別為(42.51±1.91)、(50.81±1.75)、(44.43±1.05)、(47.99±1.45) μm。乳液液滴直徑隨著體系中NaCl濃度的增加而略微增加,這歸因于離子官能團的水合作用。當水化斥力與范德華引力相比較弱時,粒子就會聚集,從而影響乳液的穩定性[24]。從圖6-b可以看出,當NaCl濃度為50 mmol/L時,制備的Pickering乳液液滴的粒徑分布相對較均勻。基于以上研究結果,明膠納米顆粒穩定的Pickering乳液的最佳制備工藝參數為:顆粒質量濃度20.0 mg/mL,乳化時間90 s,乳化轉速13 000 r/min,水相pH 8.0,NaCl濃度50 mmol/L。

a-穩定的Pickering乳液;b-Pickering乳液的光學顯微鏡圖;c-平均粒徑圖6 明膠納米顆粒在不同濃度的NaCl中穩定的Pickering乳液,Pickering乳液的光學顯微鏡圖及平均粒徑Fig.6 Images, optical micrographs and average emulsion particle size of Pickering emulsions prepared under different concentration of NaCl aqueous solution
2.7 Pickering乳液的流變性能研究
由于乳液的流變性可作為食品結構感知的指示,因此對最佳工藝下制備的Pickering乳液的流變性能進行測試,如圖7所示。
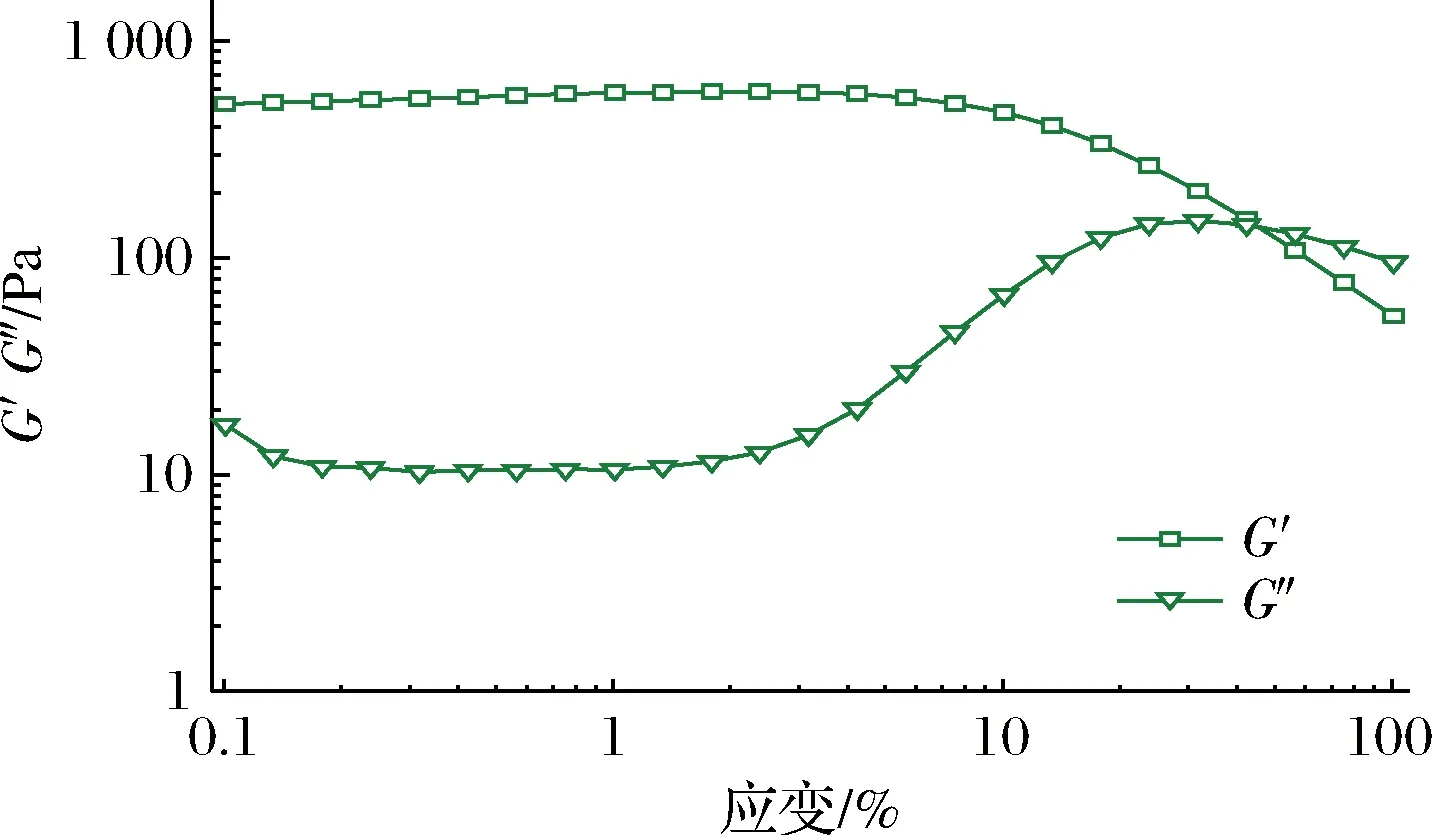
圖7 最佳工藝下制備的Pickering乳液的儲能模量(G′)和損失模量(G″)的應變依賴性曲線Fig.7 Storage modulus (G′) and loss modulus (G″) of Pickering emulsion prepared under the optimum process
在低剪切應變時,Pickering乳液的儲能模量(G′)大于損耗模量(G″),表明Pickering乳液在此階段具有彈性或類似固體的行為;隨著剪切應變力的增加,G′不斷減小,G″不斷增大。當剪切應變大于40%時,G″與G′相交,表明已達到液體和固體的臨界點。對Pickering乳液施加的應變繼續增大時,G″高于G′。這是由于Pickering乳液在高剪切應變力下,乳液內部結構發生重組或乳液液滴發生了流動[25]。結果表明,在最佳工藝下制備的Pickering乳液具有良好的穩定性,其添加到食品中可以為食物提供形態可塑性和感官特性,在食品領域具有廣闊的應用前景。
3 結論
通過二次去溶劑結合京尼平交聯固化明膠法制備得到的明膠納米顆粒的粒徑為(186.7±0.065) nm,等電點約為6,三相接觸角為76.6°。以明膠納米顆粒為乳化劑,通過均質乳化技術制備穩定的Pickering乳液的最佳制備條件為:明膠納米顆粒的質量濃度為20.0 mg/mL,乳化時間為90 s,乳化轉速為13 000 r/min,水相pH值為8.0,NaCl濃度為50 mmol/L。最優條件下制備的Pickering乳液的液滴粒徑為(44.43±1.05) μm。最佳工藝下制備的Pickering乳液具有良好的穩定性,在食品領域具有廣闊的應用前景。

