馬乳酒樣乳桿菌馬乳酒樣亞種ZW3的毒理學安全性評價
張陽,賈龍剛,耿偉濤,袁媛,楊帆,張寅靜,樊柏林,王艷萍*
(1.天津科技大學食品科學與工程學院,天津 300457;2.諾佰克(武漢)生物科技有限公司,湖北 武漢 430090;3.湖北省疾病預防控制中心湖北省應用毒理學重點實驗室,湖北 武漢 430079)
益生菌被定義為對人類或其他動物宿主健康具有有益影響的活的微生物[1-2]。許多研究表明,益生菌在緩解或預防人類疾病方面具有有益作用,如便秘[3]、腸易激綜合征[4]、炎癥性腸病[5]和神經退行性疾病[6]等。此外,研究發現很多益生菌具有恢復和維持腸道健康或平衡口腔微生物群落的功能[7-8]。許多有潛力的益生菌菌株也被分離篩選出來,有望被添加到食品或微生態藥物中,給人類帶來健康益處,預防或治療人類疾病[9-10]。與此同時,對菌株進行全面系統的安全性評價也非常重要,這是菌株作為功能性原料被廣泛使用的前提和基礎。
kefir是一種黏稠、含微碳酸、對健康有許多益處的傳統發酵乳,是益生菌的良好來源[11-13]。在前期研究中,從西藏采集的kefir粒中分離篩選出一株馬乳酒樣乳桿菌馬乳酒樣亞種ZW3,它具有高產胞外多糖(exopolysaccharide,EPS)[14-15]、顯著改善乳制品質地、延長乳品保質期的特性[16]。功能實驗證實,ZW3具有調節腸道微生物群、改善抑郁樣行為障礙、減少免疫炎癥[17]等功效。馬乳酒樣乳桿菌馬乳酒樣亞種ZW3是一種很有潛力的食品原料或功能成分,可應用于食品工業和疾病預防及治療領域。然而目前國內外關于馬乳酒樣乳桿菌馬乳酒樣亞種的綜合毒理學評價研究報道較少。因此,本研究旨在通過大鼠急性經口毒理實驗、細菌回復突變實驗、哺乳動物紅細胞微核實驗和體外哺乳類細胞染色體畸變實驗,評估馬乳酒樣乳桿菌馬乳酒樣亞種ZW3的遺傳毒性、致突變、潛在致癌作用及食用安全性,為其應用作食品原料提供參考。
1 材料與方法
1.1 菌株及主要試劑
馬乳酒樣乳桿菌馬乳酒樣亞種ZW3:天津科技大學微生物資源與開發實驗室分離鑒定;馬乳酒樣乳桿菌馬乳酒樣亞種ZW3凍干菌粉(活菌濃度6×1010CFU/g):諾佰克(武漢)生物科技有限公司;血液稀釋液、溶血劑:上海東湖生物醫學有限公司;疊氮鈉、瓊脂粉(生物純):美國Amresco公司;環磷酰胺(cyclophosphamide,CP):德國 Baxter Oncology GmbH 公司;敵克松、1,8-二羥基蔥醌蔥:德國Dr.EhrenstorferGmbH公司;DME/F12 1∶1(體積比)無血清培養液、磷酸鹽緩沖液(pH值7.2~7.4):美國 HyClone公司;葡萄糖-6-磷酸鹽(分析純):美國SIGMARLife Science公司;2-氨基菊、絲裂霉素 C(mitomycin C,MMC)、秋水仙素:美國默克公司;L-組氨酸(分析純)、D-生物素(分析純):阿拉丁試劑(上海)有限公司;氯化鉀、氯化鎂、二甲基亞砜(dimethyl sulfoxide,DMSO)、氯化鈉、葡萄糖、硫酸鎂、磷酸二氫鈉、磷酸氫二鉀、檸檬酸、磷酸氫鈉(均為分析純):國藥集團化學試劑有限公司;煙酰胺腺嘌呤二核苷酸磷酸(nicotinamide adenine dinucleotide phosphate,NADP)(分析純):上海麥克林生化科技有限公司。
1.2 實驗動物
急性經口毒理實驗選擇7~8周齡、SPF級的SD大鼠20只,雌雄各半,體重:180 g~220 g。哺乳動物紅細胞微核實驗選擇7~12周齡、SPF級的昆明小鼠50只,雌雄各半,體重:25 g~35 g。實驗動物均由湖北省實驗動物研究中心提供。
1.3 實驗細胞株
中國倉鼠卵巢細胞株(CHO-K1細胞株):中國典型培養物保藏中心(武漢大學);5株鼠傷寒沙門氏菌菌株(組氨酸缺陷型 TA97a、TA98、TA100、TA102和TA1535):美國 moltox公司。
1.4 主要儀器設備
MEK-6318K型自動血球計數儀:日本光電工業株式會社;MCO-18AIC(UV)CO2培養箱:日本 SANYO公司;SW-CJ-2F超凈工作臺:蘇州安泰空氣凈化有限公司;DMIL LED倒置顯微鏡、DM500 R H三目生物顯微鏡:德國徠卡微系統股份公司。
1.5 方法
1.5.1 急性經口毒性實驗
實驗參考GB 15193.3—2014《食品安全國家標準急性經口毒性試驗》[18]中限量法進行。實驗動物2只同性別一籠,共10籠進行飼養。設定一次灌胃劑量為10.0 g/kg體重,準確配制濃度為0.5 g/mL的ZW3菌液,以20 mL/kg體重劑量對每只大鼠進行灌胃。觀察期14 d,灌胃當天停留0.5 h連續觀察,其余時間每日上、下午各觀察1次大鼠臨床體征,記錄動物中毒癥狀及死亡數,并對異常情況作詳細記錄;實驗前后測量并記錄動物體重;分別在給予受試物前,給予受試物后1、24、48、72 h及實驗結束時,對所有動物各測量1次肛溫;在適應性喂養期、給藥后24 h和實驗結束時,對所有存活的動物進行尾靜脈采血并測量血液學指標;最后,頸椎脫位處死動物,收集并觀察動物各組織器官情況。
1.5.2 細菌回復突變實驗
實驗參考GB 15193.4—2014《食品安全國家標準細菌回復突變試驗》[19]進行測定。實驗設置3個對照組,即自發回變對照組、陰性對照組(1和2,1為蒸餾水,2為DMSO)、陽性對照組(敵克松、疊氮鈉、2-氨基芴、1,8-二羥基蒽醌)。準確配制濃度為 50、20、8、3.2 和1.28 mg/mL的ZW3菌液;將0.1 mL各劑量ZW3菌液和0.5 mL S9(需要活化時)加入測試平板頂部瓊脂中,混合并倒入底層培養基平板上,制備出5個劑量組的測試平板,每個劑量組均設含或不含S9代謝活化系統的兩個組別。每個菌株測試組和每個對照組在每個濃度下做3組平行,且在相同條件下重復整個測試一次。以上所有平板均在37℃下孵育48 h~52 h,計算每個培養皿中回變的菌落數并進行結果分析。
1.5.3 哺乳動物紅細胞微核實驗
實驗參考GB15193.5—2014《食品安全國家標準哺乳動物紅細胞微核試驗》[20]進行。實驗設置陰性對照組、陽性對照組和高、中、低劑量組。對小鼠進行適應性喂養3 d后,隨機分成5組,每組雌雄各5只,同性別5只一籠進行飼養。實驗開始前,給動物稱重,并排除疾病或其他異常跡象;準確配制濃度為500、250、125 mg/mL的ZW3菌液,供高、中、低劑量灌胃使用;通過管飼法,對每組小鼠進行兩次灌胃,兩次灌胃間隔24 h,小鼠灌胃容量均為20 mL/(kg體重/次),陰性對照組給予無菌蒸餾水,陽性對照組給予40 mg/kg體重的環磷酰胺溶液,高、中、低劑量組分別給予 10、5.0、2.5 g/kg 體重的ZW3菌液;第二次灌胃后6 h處死動物,取動物股骨骨髓,按照標準要求制片、觀察、統計數據并分析,實驗結果以P<0.05被判定為具有顯著性差異。
1.5.4 體外哺乳類細胞染色體畸變實驗
實驗參考GB 15193.23—2014《食品安全國家標準體外哺乳類細胞染色體畸變試驗》[21]進行。實驗設置高、中、低3個測試劑量組(ZW3濃度分別為5 000、2 500、1 250 μg/mL),陰性對照組(等量無血清培養液),陽性對照組1(終濃度為15 μg/mL的環磷酰胺)和陽性對照組2(終濃度為0.8 μg/mL的絲裂霉素C),其中各劑量組及陰性對照組均分別設置加和不加S9代謝活化系統的組別,而陽性對照組1為加S9、陽性對照組2為不加S9的情況下測試。中國倉鼠卵巢細胞CHO-K1經48 h培養(37℃,5%CO2)后,棄其培養液,各組分別暴露于受試物(或對照),培養4 h后棄上清,用生理鹽水洗滌3次,加入5 mL含10%胎牛血清的培養液,培養24h。在收獲前4 h,加入秋水仙素(終濃度為1 μg/mL),按常規方法消化、低滲、固定、制片、染色。每劑量組選200個分散良好的中期分裂相細胞,觀察記錄染色體畸變類型及畸變數目,計算細胞畸變率(裂隙和多倍體單獨記錄不作為畸變率統計),計算公式如下。

1.6 數據處理
急性經口毒性實驗數據采用Microsoft Excel軟件建立數據庫,計量資料采用t檢驗,計數資料采用非參數統計法,并按動物性別分別統計。其他實驗數據采用SPSS軟件建立數據庫,采用卡方檢驗對數據進行統計。
2 結果與討論
2.1 大鼠急性經口毒性實驗結果
實驗前后動物體重見表1,大鼠肛溫檢測結果見表2,血常規指標檢測結果見表3。

表1 大鼠急性經口毒性實驗結果Table 1 Summary of acute oral toxicity test results in rats
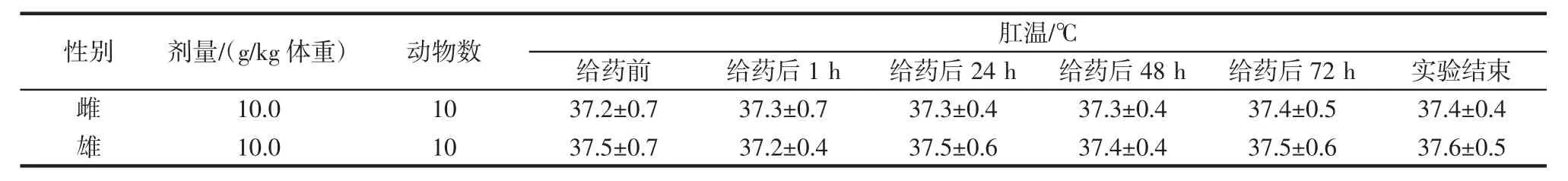
表2 大鼠肛溫檢測結果Table 2 Rat anal temperature test results
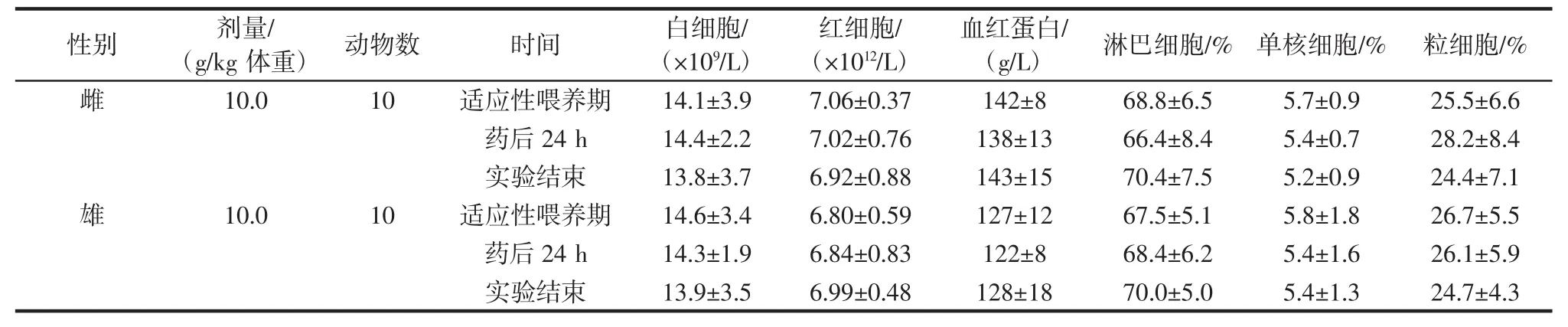
表3 大鼠血常規指標檢測結果Table 3 Rat blood routine index test results
由表1可知,雌雄大鼠體重變化情況符合動物正常生長規律。由表2可知,雌性和雄性大鼠灌胃ZW3前后直腸溫度相似,差異不明顯。由表3可知,雌雄大鼠灌胃ZW3前后白細胞、紅細胞、血紅蛋白、淋巴細胞、單核細胞、粒細胞值,均無明顯差異,且動物灌胃ZW3后的血液學指標與其他益生菌如M1[22]、唾液乳桿菌REN[23]、發酵乳桿菌HM3和布氏乳桿菌FD2[24]的相關研究結果相似。在整個14 d的觀察期內,未見受試動物死亡或出現明顯中毒反應癥狀,運動活動、呼吸、消化和神經系統表現正常,皮膚、毛發、眼睛、口腔等均未見異常,水分和飼料攝取量正常。處死實驗動物后檢查胸腹部主要臟器,包括心臟、肺、肝、脾、腎、胃腸和生殖器,均無任何明顯的病理改變。上述結果表明在本實驗條件下,馬乳酒樣乳桿菌馬乳酒樣亞種ZW3的大鼠急性經口毒性LD50大于10.0 g/kg體重,按照急性毒性分級標準,屬于實際無毒級。
2.2 細菌回復突變實驗結果
細菌回復突變第一次及重復實驗陽性對照物結果見表4和表5。細菌回復突變第一次及重復實驗結果見表6和表7。

表4 細菌回復突變實驗第一次實驗陽性對照物結果Table 4 Positive control result for the first experiment of Ames test

表5 細菌回復突變實驗重復實驗陽性對照物結果Table 5 Positive control result for the repeat test of Ames test
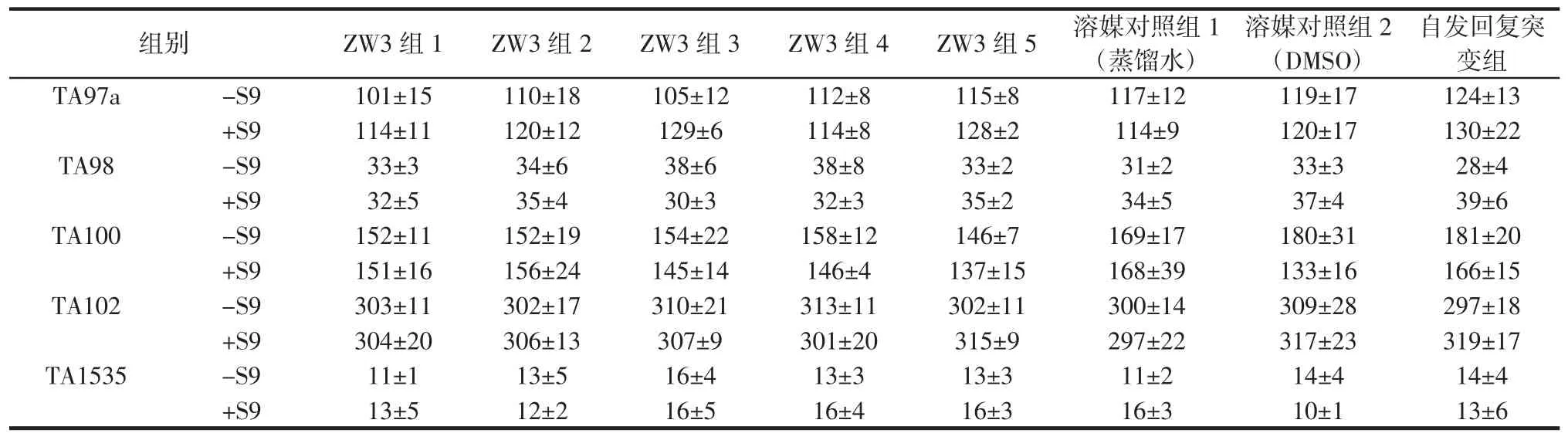
表6 細菌回復突變實驗第一次實驗結果Table 6 First test results of Ames test
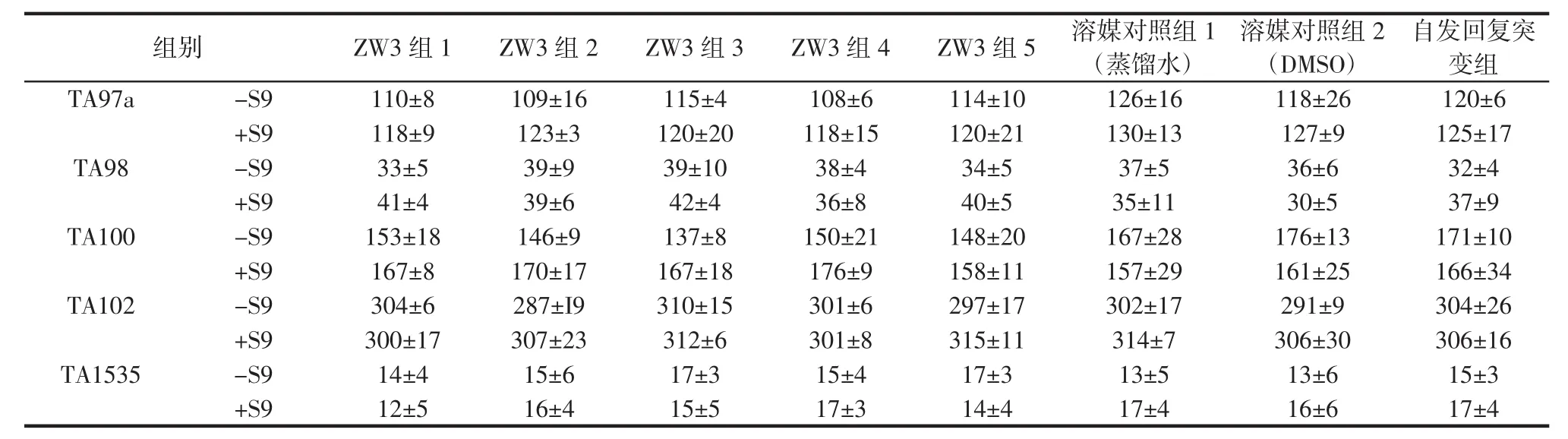
表7 細菌回復突變實驗重復實驗結果Table 7 Repeat test results of Ames test
由表4可知,所有的陽性對照劑在含或者不含S9代謝活化系統中均誘導了回復突變菌落的大幅成倍增加,而由表6可知,添加不同劑量的ZW3,在任何含或者不含S9代謝活化系統及不同測試菌株的組別中,測得的回復突變菌落計數數值,與蒸餾水、DMSO和自發回復突變對照組的數值相似。由表5及表7可知,重復實驗結果與第一次實驗結果相似。
馬乳酒樣乳桿菌馬乳酒樣亞種ZW3對5株實驗菌株,在含或者不含S9代謝活化系統時,以及設置的各劑量組中,均未產生明顯抑菌作用,且各劑量組回變菌落數均未超過溶媒對照組菌落數2倍,且無劑量-反應關系,判定ZW3的細菌回復突變實驗結果為陰性。
2.3 小鼠紅細胞微核實驗結果
小鼠骨髓紅細胞微核實驗結果見表8。
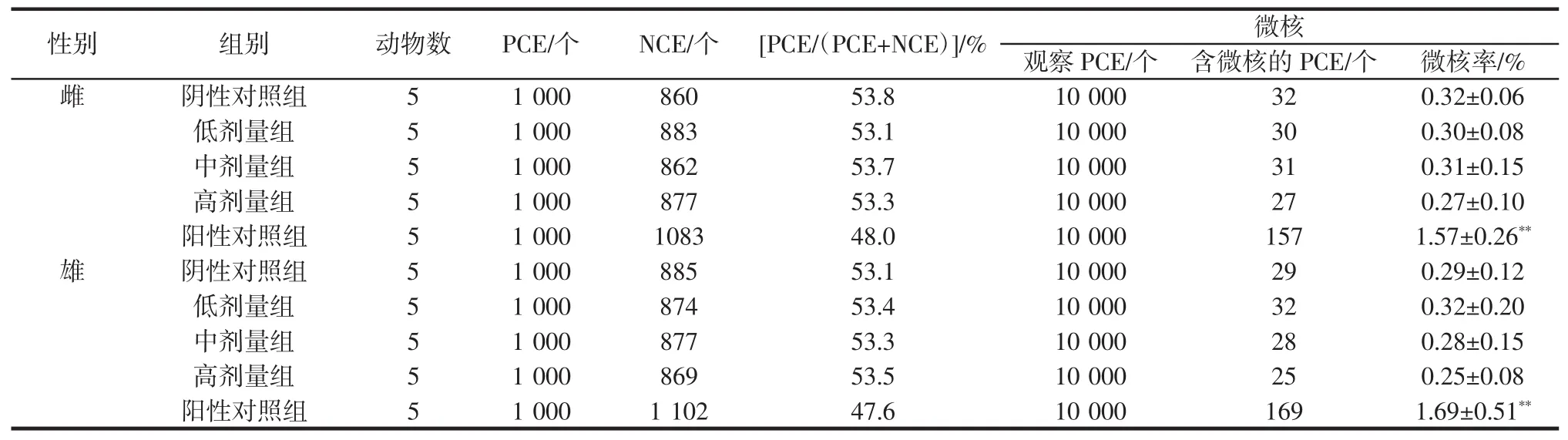
表8 小鼠骨髓細胞微核實驗結果Table 8 Micronucleus test results of mouse bone marrow cells
由表8可知,ZW3的各個劑量組中,嗜多染紅細胞與紅細胞總數的比率[PCE/(PCE+NCE)]均不少于陰性對照組的20%,實驗動物及觀察樣本符合要求。陽性對照組的雌性和雄性小鼠的微核率分別為(1.57±0.26)%和(1.69±0.51)%,均與陰性對照組的微核率有極顯著性差異(P<0.01);相比之下,ZW3各劑量組的雄性和雌性小鼠的微核率,與陰性對照組的微核率無顯著性差異,且均正常值范圍內。表明ZW3不會導致哺乳動物嗜多染紅細胞含微核細胞率增加,不具有誘導細胞變異的風險。
2.4 體外哺乳類細胞染色體畸變實驗
馬乳酒樣乳桿菌馬乳酒樣亞種ZW3對CHO-K1細胞的毒性見表9。
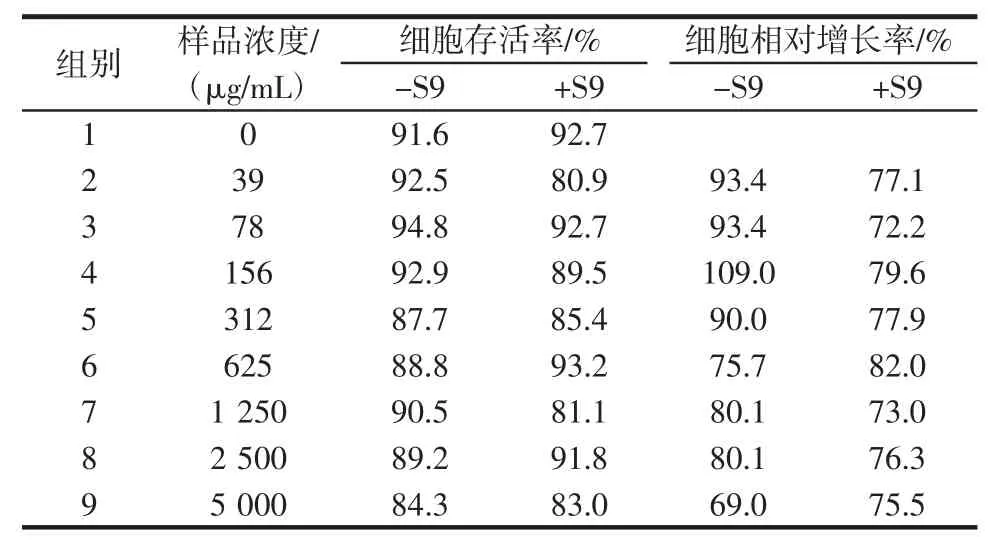
表9 馬乳酒樣乳桿菌ZW3對CHO-K1細胞的毒性Table 9 Cytotoxicity of L.kefiranofaciens ZW3 on CHO-K1 cells
由表9可知,當ZW3濃度達到5 000 μg/mL時,在含或不含S9的體系中CHO-K1細胞存活率分別為84.3%和83.0%,細胞相對增長率分別為69.0%和75.5%,且ZW3在5 000 μg/mL濃度下有少量沉淀,因而設置ZW3在體外細胞染色體畸變實驗中的最大劑量為 5 000 μg/mL。
ZW3體外哺乳類細胞染色體畸變實驗結果見表10。
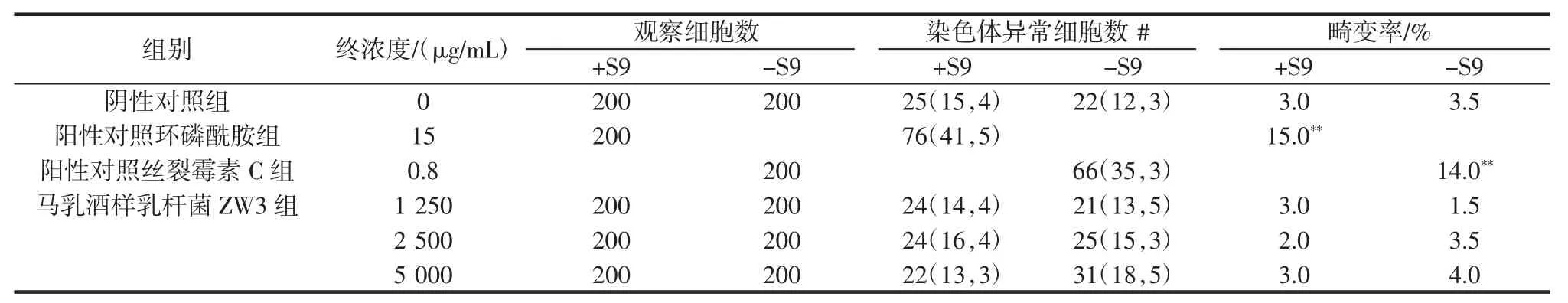
表10 ZW3體外哺乳類細胞染色體畸變實驗結果Table 10 In-vitro mammalian cell chromosome aberration test results of ZW3
由表10可知,陰性對照組有25個(+S9)和22個(-S9)染色體異常細胞,染色體畸變率分別為3.0%(+S9)和3.5%(-S9);陽性對照環磷酰胺組有76個染色體異常細胞,絲裂霉素C組有66個,染色體畸變率分別為 15.0%(+S9)和 14.0%(-S9),極顯著高于陰性對照組(P<0.01)。而ZW3的不同劑量組(-S9和+S9),染色體異常細胞和染色體畸變率均與陰性對照組沒有顯著性差異。表明馬乳酒樣乳桿菌ZW3體外哺乳類細胞染色體畸變實驗結果為陰性。
3 結論
本文通過大鼠急性經口毒性實驗、細菌回復突變實驗、小鼠紅細胞微核實驗和體外哺乳類細胞染色體畸變實驗對馬乳酒樣乳桿菌馬乳酒樣亞種ZW3進行了全面的毒理學評估,以支持長期食用馬乳酒樣乳桿菌馬乳酒樣亞種ZW3的安全性。結果表明,大鼠急性經口毒性研究中,在單劑量為10 g/kg體重劑量下未觀察到與給藥相關的死亡率、發病率或毒性臨床癥狀。在細菌回復突變實驗、小鼠紅細胞微核實驗和體外哺乳類細胞染色體畸變實驗中,ZW3未表現出致誘變、致裂或基因毒性作用。因此,根據我國食品安全國家標準判斷,馬乳酒樣乳桿菌馬乳酒樣亞種ZW3具有良好的食用安全性,為該菌株后續的功能研究以及其在產品中的應用,提供有力的安全性支持。

