基于網絡藥理學探討柴胡-黃芩治療慢性腎功能衰竭的作用機制*
萬麗莎,李建英
1.山東中醫藥大學,山東 濟南 250014;2.山東中醫藥大學附屬青島市中醫醫院,山東 青島 266033
慢性腎功能衰竭(chronic renal failure,CRF)的主要臨床表現是水、電解質紊亂以及代謝產物和毒物潴留、酸堿平衡失調和全身各系統癥狀[1],在中醫學中可歸為“腎勞” “癃閉”“關格”“溺毒”等范疇。全國第五批名老中醫藥專家學術經驗繼承指導老師、齊魯傷寒流派第三代傳人于俊生教授認為慢性腎衰關乎少陽病變,CRF以和解少陽之法治療時應首選小柴胡湯[2],小柴胡湯以柴胡為君藥,黃芩為臣藥,柴胡疏散退熱、疏肝解郁、升舉陽氣,黃芩清熱燥濕、瀉火解毒、止血、安胎[3],二者配伍能和解少陽,運轉少陽樞機,使之開合有度,邪有出路,是于俊生教授治療CRF臨床常用對藥[4]。前期研究證明,以柴胡、黃芩為主藥的小柴胡湯加減方柴半六合湯可緩解CRF患者的胃腸道癥狀,延緩CRF的進一步發展[5]。以柴胡、黃芩為主藥的治療CRF的經驗方補腎排毒合劑可保護腎功能[6],提高血白蛋白、轉鐵蛋白水平[7]。
網絡藥理學為研究中藥復方作用機制提供了新技術手段,可用于發現藥物靶標,推進中藥新藥研發,有益于中醫藥理論的發展和傳承[8]。本文使用網絡藥理學研究方法探討“和解少陽法”代表藥對“柴胡-黃芩”對CRF的作用機制,以期為后續的研究提供一定的參考。
1 資料與方法
1.1 柴胡、黃芩活性成分及相關靶點的篩選基于中藥系統藥理學數據庫與分析平臺(traditional Chinese medicine systems pharmacology database and analysis platform,TCMSP)[9]檢索柴胡、黃芩的化學成分,根據口服生物利用度(oral bioavailability,OB)≥30%且類藥性(drug-likeness,DL)≥0.18進行初步篩選,獲得柴胡、黃芩的活性成分和其對應的蛋白質靶點,將未找到蛋白質靶點的成分剔除,將蛋白質靶點錄入Uniprot數據庫[10],獲得其標準基因名。
1.2 CRF相關靶點篩選以“chronic renal failure”為關鍵詞,挖掘在線人類孟德爾遺傳數據庫(online mendelian inheritance in man,OMIM)和GeneCards數據庫[11]中CRF的相關靶點。在GeneCards數據庫中,Relevance score值越大表示該靶點與疾病的聯系越密切,如果靶點過多則選擇Relevance score值大于中位數的靶點作為疾病的潛在靶點。將兩個數據庫中得到的靶點合并并刪除重復值后得到CRF的相關靶點。
1.3 蛋白質相互作用(protein-protein interaction,PPI)網絡的構建及核心靶點篩選應用Draw Venn Diagram在線工具將柴胡、黃芩活性成分相關靶點與CRF相關靶點取交集并繪制韋恩圖,得到的交集靶點即為柴胡-黃芩治療CRF的潛在靶點,在EXCEL表格中利用VLOOKUP函數映射出作用于潛在靶點的活性成分,將未映射到潛在靶點的成分剔除,將數據導入Cytoscape 3.8.0軟件,構建“活性成分-潛在靶點”網絡圖。將潛在靶點輸入STRING11.0數據庫[12]進行PPI網絡模型構建,物種設定為“Homo sapiens”,設置minimum required interaction score>0.9,隱藏游離節點,得到PPI網絡,將結果導入Cytoscape 3.8.0進行可視化,并使用Cytohubba插件采用最大集團中心性(maximal clique centrality,MCC)、最大鄰域分量(maximum neighborhood component,MNC)、度(degrees)算法挖掘核心靶點,參數為默認設置,利用 Draw Venn Diagram在線工具取三個結果的交集,交集靶點為柴胡-黃芩作用于CRF的核心靶點。
1.4 潛在靶點的基因本體(gene ontology,GO)功能富集分析和京都基因與基因組百科全書(kyoto encyclopedia of genes and genomes,KEGG)信號通路富集分析將柴胡-黃芩治療CRF的潛在靶點錄入Metascape平臺[13],設置P<0.01,進行GO功能的生物學過程(biological process,BP)富集分析及KEGG信號通路富集分析,并采用Cytoscape 3.8.0軟件構建“潛在靶點-信號通路”網絡圖。
2 結果
2.1 柴胡-黃芩活性成分及相關靶點基于TCMSP初步提取柴胡化學成分349種、黃芩化學成分143種,以OB≥30%且DL≥0.18為標準進行篩選后獲得柴胡活性成分17種、黃芩活性成分36種,其中8種化合物未找到相關靶點,將其剔除后得到柴胡活性成分13種、黃芩活性成分32種,見表1。基于TCMSP獲得柴胡活性成分作用靶點181種,黃芩活性成分作用靶點120種,將兩味中藥活性成分的作用靶點合并,刪除重復值后共獲得216個藥物相關靶點。
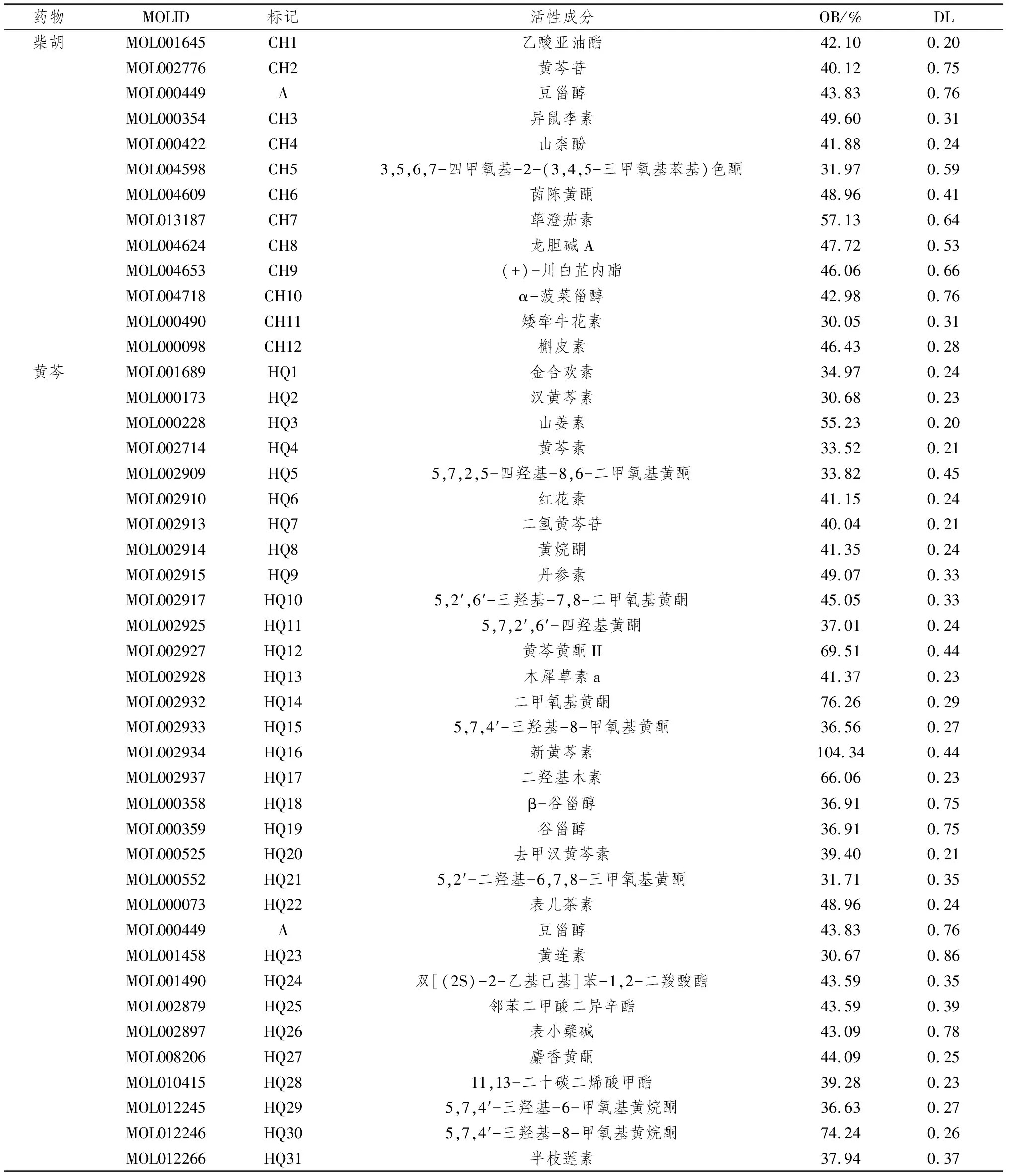
表1 柴胡-黃芩活性成分相關信息表
2.2 CRF相關靶點從GeneCards數據庫中獲得慢性腎功能衰竭靶點8 596個,Relevance score最大值為112.941 818 2,最小值為0.188 800 812,中位數為3.540 131 807,篩選出Relevance score大于中位數的靶點4 298個,靶點仍較多,對篩選后的靶點進行二次篩選,Relevance score最小值為3.540 928 125,中位數為7.813 783 407,篩選出Relevance score大于中位數的靶點2 149個。從OMIM數據庫中獲得慢性腎功能衰竭靶點578個,將兩個數據庫獲得的靶點合并后刪除重復值,最后獲得慢性腎功能衰竭相關靶點2 607個。
2.3 PPI網絡與核心靶點將216個活性成分相關靶點與2 607個CRF相關靶點導入Draw Venn Diagram進行映射,得到137個交集靶點,即為柴胡-黃芩治療CRF的潛在作用靶點,并繪制韋恩圖。11,13-二十碳二烯酸甲酯未映射到潛在靶點,將其剔除,將數據導入Cytoscape 3.8.0軟件,構建“活性成分-潛在靶點”網絡圖,其中粉色矩形代表潛在靶點,圓形代表活性成分,圖形大小、顏色按照degree值大小形成,degree值越大,節點越大、顏色越深,說明該成分與潛在靶點越重要,分析可知槲皮素、山柰酚、漢黃芩素在柴胡-黃芩治療CRF中發揮重要作用。將潛在靶點輸入STRING11.0數據庫構建PPI網絡,并將結果導入Cytoscape 3.8.0進行可視化,圖中節點代表潛在靶點,邊代表靶點間的互作關系,degree值越大,節點越大、顏色越深。使用Cytohubba插件中的MCC、MNC、Degrees算法挖掘核心靶點,將三種算法得出的核心靶點取交集并繪制韋恩圖,得出JUN、RELA、白細胞介素-6(interleukin-6,IL-6)、腫瘤蛋白p53(tumor protein p53,TP53)、絲裂原活化蛋白激酶1(mitogen activated protein kinase 1,MAPK1)和腫瘤壞死因子(tumor necrosis factor,TNF)6個靶點為柴胡-黃芩作用于CRF的核心靶點。見圖1—圖7。
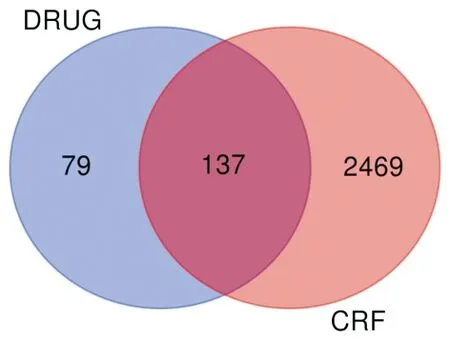
注:DRUG:柴胡-黃芩相關靶點;CRF:慢性腎功能衰竭相關靶點
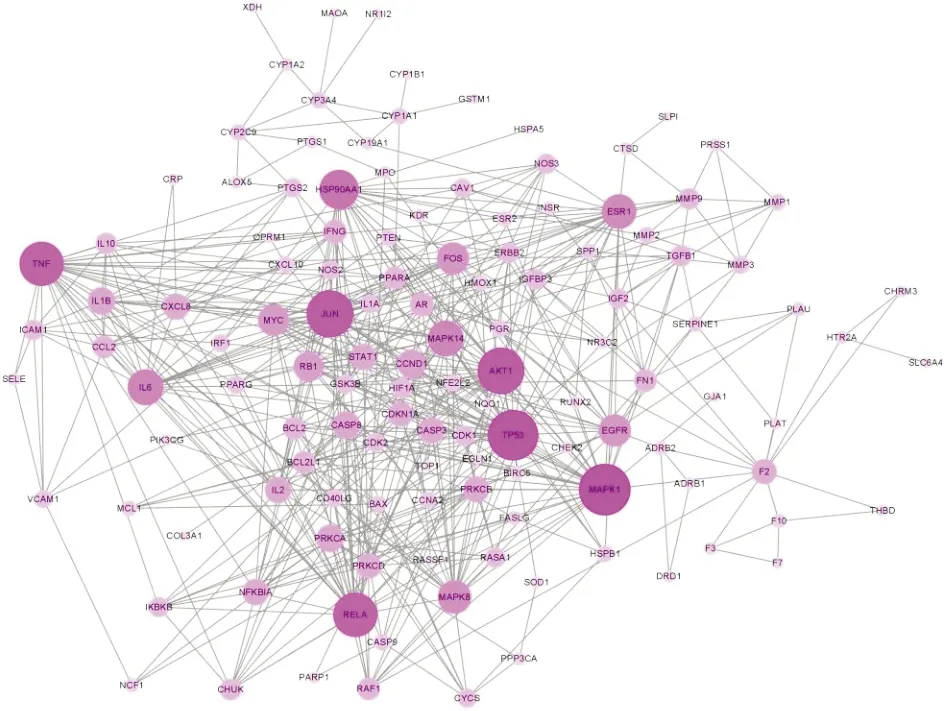
圖3 潛在靶點PPI網絡圖
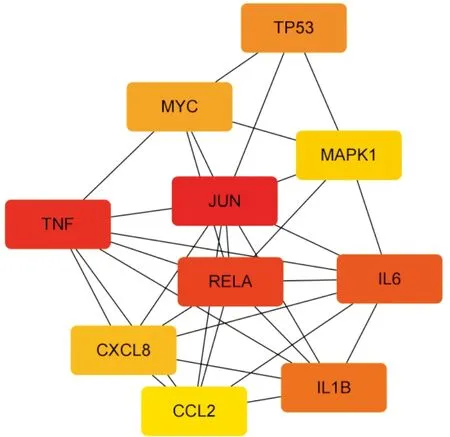
圖4 MCC算法分析結果
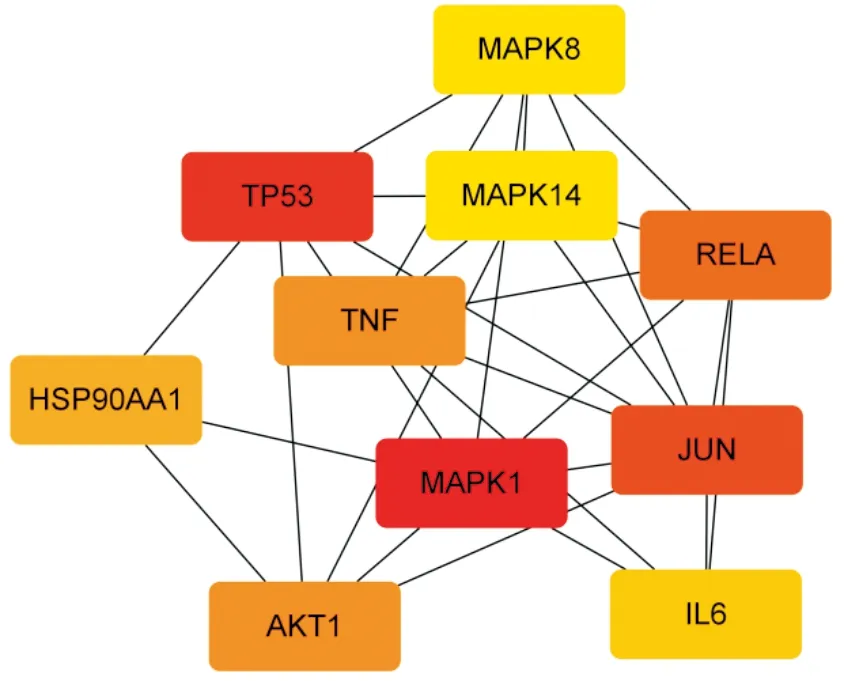
圖5 MNC算法分析結果
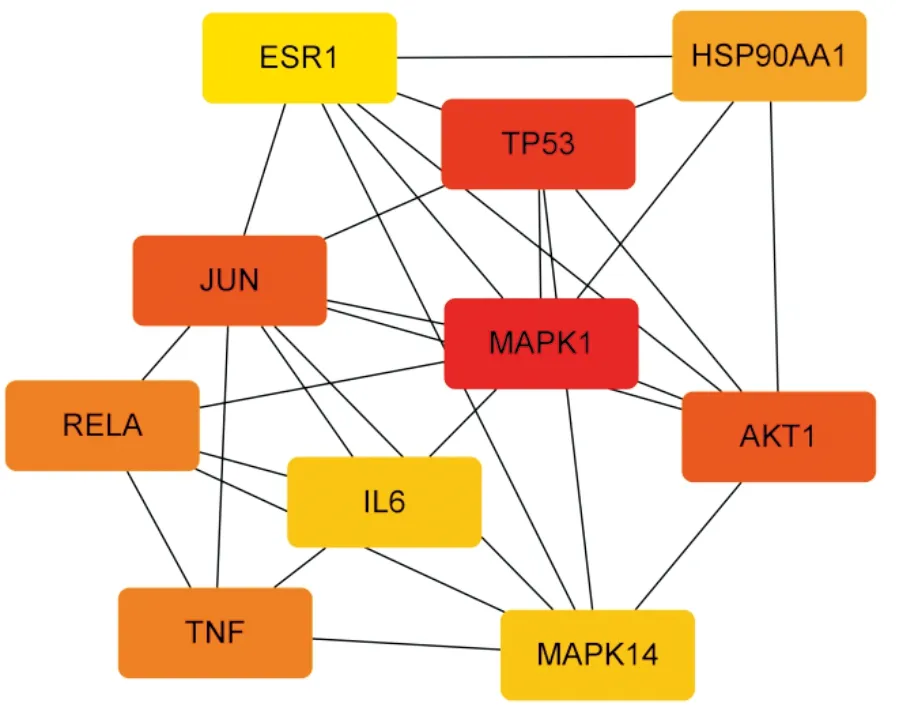
圖6 Degrees算法分析結果
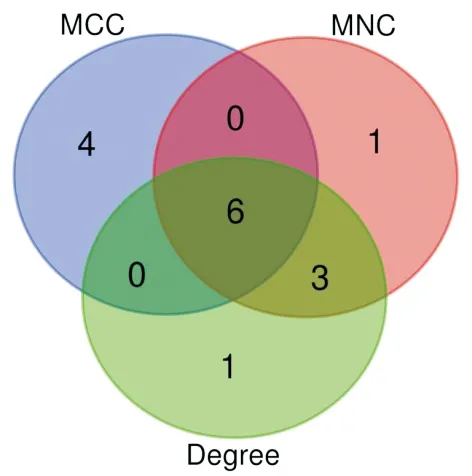
圖7 三種算法核心靶點韋恩圖
2.4 GO功能富集分析和KEGG信號通路富集分析GO功能富集分析共得到5437個BP條目,主要包括對無機物的應答(response to inorganic substance)、對損傷的應答(response to wounding)、對脂多糖的應答(response to lipopolysaccharide)等,設置P<0.01,根據P值排序后,選取排名前20位的條目繪制條形圖。KEGG信號通路富集分析篩選得到434條信號通路,主要涉及腫瘤相關通路(pathways in cancer)、IL-17信號通路(IL-17 signaling pathway)、TNF信號通路(TNF signaling pathway)、細胞凋亡(apoptosis)和PI3K-Akt 信號通路(PI3K-Akt signaling pathway)等,設置P<0.01,根據P值排序后,選取排名前20位的條目繪制氣泡圖。采用 Cytoscape 3.8.0軟件構建“潛在靶點-信號通路”網絡圖,圖中黃色矩形代表靶點,粉色三角形代表通路,連線代表靶點與通路之間的關系,通過該網絡圖可知柴胡-黃芩可通過多條通路的協調作用發揮治療CRF的作用。見圖8—圖10。
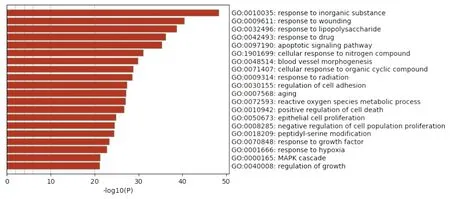
圖8 GO功能富集分析-BP
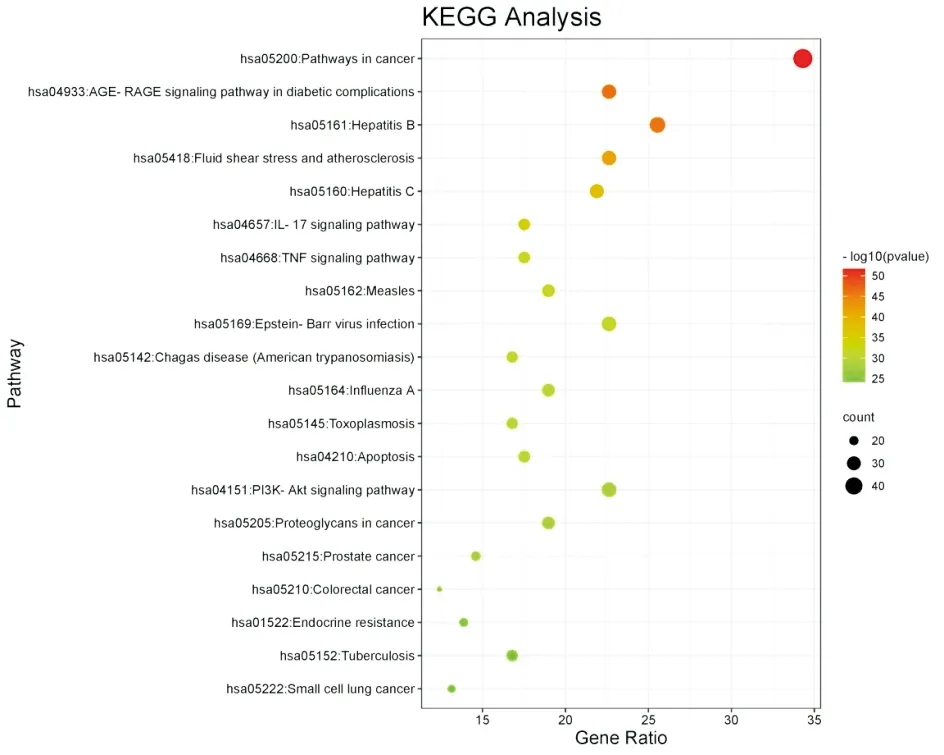
圖9 KEGG信號通路富集分析
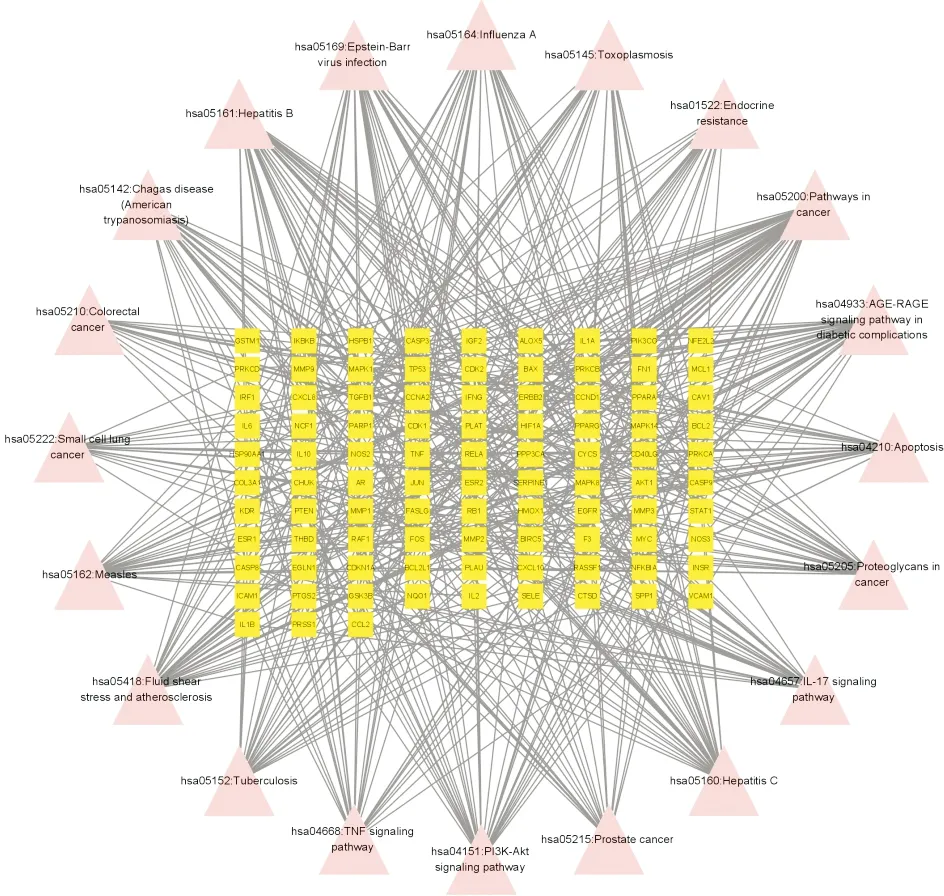
圖10 “潛在靶點-信號通路”網絡圖
3 討論
在我國,慢性腎臟病患病率達10.8%[14],且患病率逐年升高[15],CRF是各種慢性腎臟病發展至后期的一種臨床綜合征,目前CRF的西醫診治方案為治療原發病、控制CRF進展的危險因素和防治并發癥[16],若發展至終末期則需選擇腎臟替代治療,嚴重影響患者的生存質量,對家庭和社會也產生巨大的經濟負擔[17]。在此背景下,如何更好的防治CRF成為亟需解決的問題,而中醫藥不僅可以緩解CRF患者的近期癥狀,還能提高患者的生活質量,為CRF的診療提供了更多的思路[18]。
CRF本虛在脾腎,標實為痰濕瘀毒,脾腎之水液代謝,以三焦為通道,若少陽三焦樞機不利,則氣滯血瘀,痰濕不化,清濁不分,濁毒不排,故臨床治療應重視和解少陽[19-20]。柴胡-黃芩為和解之法的經典藥對,二者共奏通調少陽樞機之功,在臨床上應用于多種系統疾病中[21],既往研究顯示其有抗炎、抗氧化、抗凋亡等藥理作用[22]。
本研究得出柴胡-黃芩治療CRF的潛在作用靶點137個,發揮重要作用的活性成分有槲皮素、山柰酚和漢黃芩素等,篩選出6個核心靶點,包括JUN、RELA、IL-6、TP53、MAPK1和TNF。已有研究表明,TNF和IL-6與腎小球損害和硬化密切相關[23]。李玲等[24]研究顯示,TNF通過促進腎間質成纖維細胞增殖促使腎間質纖維化。IL-6是重要的炎癥參與因子,以自分泌及旁分泌兩種方式促進腎小球系膜細胞增殖,進而造成腎小球損害[25]。Zhang等[26]研究顯示,CRF患者腎臟中 IL-6 表達水平顯著增加,可直接誘導腎臟中纖維化基因表達和前內皮素原1mRNA表達。RELA是 NF-κB 家族的亞單位之一,可通過多種翻譯后修飾包括磷酸化、乙酰化、甲基化和泛素化等調節 NF-κB 的活性和功能[27],而NF-κB 信號通路在腎間質纖維化中起重要的作用[28]。由此推測,柴胡-黃芩主要通過緩解腎臟炎癥和腎纖維化達到改善腎功能的目的。
GO功能富集分析發現,BP主要涉及對無機物的應答、對損傷的應答、對脂多糖的應答等生物學過程。KEGG富集分析發現,與炎癥相關的通路 IL-17 信號通路、TNF信號通路、PI3K-Akt 信號通路等參與了柴胡-黃芩對CRF的治療作用。已有研究表明,TNF可促進血管緊張素Ⅱ的生成,從而導致細胞外基質的過度沉積,最終促進腎纖維化[29]。P13K-Akt 信號通路可通過介導足細胞凋亡調節細胞增殖、生長和代謝等,另外PI3K 可和下游分子 Akt 結合,導致炎癥反應的發生,加快腎纖維化進程[30]。
綜上所述,柴胡-黃芩中一種成分可以調控不同的作用靶點,同一靶點可以干預不同的信號通路,體現了柴胡-黃芩多成分、多靶點、多通路聯合作用的特點,且柴胡-黃芩主要通過調控炎癥相關靶點和通路發揮抗炎、抗纖維化作用從而改善腎功能。其中一些靶點和通路已在前期研究中得到驗證,為臨床運用“柴胡-黃芩”藥對治療CRF提供了科學依據。不足的是本研究未將柴胡-黃芩煎煮后的化學成分和其活性成分在體內的代謝物納入研究,之后將在此基礎上進一步實驗和臨床研究以闡明柴胡-黃芩治療慢性腎功能衰竭的具體機制。

