稽留流產絨毛組織中IGF-1、E-cadherin、微血管密度表達與藥物治療結果的相關性研究
劉 競,張 蘭,曾 利,馬 麗
(巴中市中心醫院產科,四川 巴中 636000)
稽留流產指胚胎死亡或發育停止后稽留于宮腔內未能及時自然排出者[1]。流行病學研究發現,稽留流產發病率從2013年的24.14%上升到2018年的30.50%[2]。稽留流產受遺傳、免疫缺陷、內分泌異常、感染等多因素影響,但病因仍不清楚[3]。胰島素樣生長因子-1(insulin-like growth factor-1,IGF-1)是具有促進滋養細胞增殖或侵蝕作用的細胞因子,對胚胎植入、發育有調控作用[4];E-鈣黏附蛋白(E-cadherin)是一種調節細胞與細胞、細胞與基質間黏附作用的跨膜糖蛋白,對維持正常子宮功能有重要意義[5];微血管密度(microvessel density,MVD)降低可造成胎盤微循環障礙,嚴重時引起胚胎死亡[6]。稽留流產可引起宮壁粘連,宮內組織機化,纖維組織水腫變性,孕囊不易完全排出,臨床上多采用米非司酮片配伍米索前列醇片序貫治療稽留流產,但仍存在完全流產率低、陰道出血多等不足[7]。本研究通過檢測IGF-1、E-cadherin和MVD在進行米非司酮配伍米索前列醇治療的稽留流產和正常早孕患者絨毛組織中的表達情況,分析研究其表達與藥物治療結局的相關性。
1資料與方法
1.1研究對象
收集2019年9月至2021年8月在巴中市中心醫院婦產科收治的,進行米非司酮配伍米索前列醇治療的稽留流產患者95例為研究組,正常早孕患者108例為對照組。納入標準:①研究組均符合《婦產科學》中稽留流產診斷標準[8];②對照組血清人絨毛膜促性腺激素檢測陽性,B型超聲檢查可見胚芽或(和)心管搏動以證實胚胎存活;妊娠囊大小與停經天數相符合;③年齡在20~40歲之間;④妊娠時間在6~10周之間;⑤自愿參與試驗并簽署同意書。排除標準:①對本研究治療藥物過敏或有其他禁忌證者;②生殖道結構畸形、月經周期不規律、生殖道感染等;③妊娠期有毒物、藥物、射線接觸史、家族遺傳史等。
1.2藥物治療
所有患者均采用米非司酮配伍米索前列醇的統一藥物方案進行治療,即第一天口服米非司酮25mg/次(國藥準字H10950003,規格:25mg),早晚各一次,第二天早上50mg,第三天晨空腹口服米索前列醇0.6mg(國藥準字H20000668,規格:0.2mg);患者服用藥物3h后,觀察宮縮情況,如未出現宮縮則再給予0.4mg米索前列醇口服,或將0.2mg米索前列醇置于陰道后穹窿處,據患者陰道出血情況及胚胎排出情況判斷是否進行清宮術。
1.3實驗方法
1.3.1標本采集
收集兩組患者藥物治療后自行排出的絨毛組織,用生理鹽水反復沖洗干凈后,進行固定、脫水、包埋,制成切片,進行免疫組化染色檢測。
1.3.2免疫組織化學法檢測絨毛組織中IGF-1、E-cadherin和MVD的表達
取上述石蠟切片進行脫蠟、水化,利用磷酸鹽緩沖液(phosphate-buffered saline,PBS)洗3次,分別加入IGF-1、E-cadherin和CD34抗體(北京博奧森生物技術有限公司)過夜孵育,PBS洗3次后分別加入辣根過氧化物酶(horseradish peroxidase,HRP)標記的山羊抗兔抗體(北京博奧森生物技術有限公司)室溫孵育1h,PBS洗2次后加3,3′-二氨基聯苯胺(3,3′-diaminobenzidine,DAB)孵育10min;復染5min,水洗分化、藍化,最后脫水封片后由2名高年資病理醫師采用雙盲法獨立觀察染色情況,判讀免疫組織化學結果。
結果判定:①IGF-1、E-cadherin免疫組織化學結果判定[9]:隨機選取高倍視野5個,聯合染色的強度和陽性細胞百分比進行計分,其中染色強度不著色計0分、淺黃色計1分、棕黃色計2分及棕褐色計3分;其中陽性細胞所占視野內細胞的百分比<5%計0分、5%~<25%計1分、25%~50%計2分、>50%計3分;然后取兩者得分乘積為最終分數,判定0分為陰性(-),1~2分為(+),3~4分為(++),5~6分為(+++),后3者均視為陽性表達;②MVD免疫組織化學結果判定:用CD34的表達量代表MVD。CD34分布于細胞質,以細胞質內出現棕黃色顆粒為陽性。微血管計數參考1992年Weidner等計數的標準:凡標記清晰,著色強,與背景明顯有別的單個染色的血管內皮細胞、管腔直徑小于8個紅細胞的血管或血管內皮細胞簇,不論是否形成管腔或管腔內是否有紅細胞,只要不和臨近的微血管、細胞及其他結締組織相連,就作為一個微血管。管壁有平滑肌的血管不予計數。先在低倍鏡下尋找新生血管最密集區,然后在200倍視野下選取5個視野,計數微血管染色數目,其平均值即該病例的MVD。
1.4療效評價標準
藥物治療后效果評價標準[10]:藥物治療效果分為完全流產、不完全流產和治療失敗。①完全流產:接受藥物治療24h內出現宮縮等癥狀,陰道出血量在正常范圍內,妊娠物完全排出,經B超檢查確認宮腔內無組織殘留物;②不完全流產:接受藥物24h內排出部分妊娠物,陰道出血量較大,B超檢查發現宮腔內仍有部分殘留物,需要進行清宮術;③治療失敗:患者接受藥物治療后發生腹痛,出現少量陰道出血但無妊娠物排出,經B超檢查確認宮腔內存在妊娠物,需進行清宮術。
1.5統計學方法
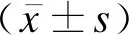
2結果
2.1兩組患者一般資料比較
研究組平均年齡(26.45±4.17)歲,孕周(8.29±1.45)周;對照組平均年齡(26.56±3.98)歲,孕周(8.35±1.58)周;兩組患者的年齡、孕周、體質量指數(body mass index,BMI)、痛經比例間差異均無統計學意義,具有可比性(P>0.05),見表1。
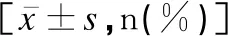
表1 兩組患者的一般資料比較
2.2兩組患者絨毛組織中IGF-1、E-cadherin和MVD的表達情況
兩組患者絨毛組織中均有IGF-1、E-cadherin、MVD的表達,見圖1;研究組絨毛組織中IGF-1的陽性表達率(3.16%)低于對照組(11.11%),差異有統計學意義(χ2=4.67,P=0.03);研究組絨毛組織中E-cadherin的陽性表達率(75.79%)低于對照組(96.30%),差異有統計學意義(χ2=18.43,P<0.01);研究組絨毛組織中MVD的相對表達量(7.56±0.62)低于對照組(13.78±1.16),差異有統計學意義(t=46.71,P<0.01),見表2。
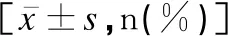
表2 兩組患者絨毛組織中IGF-1、E-cadherin和MVD的表達情況
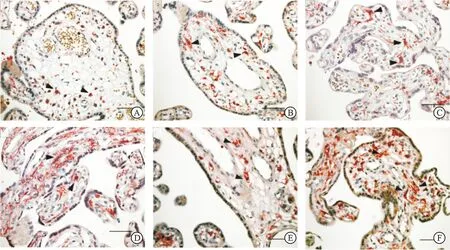
注:(A:研究組,B:對照組)為IGF-1的表達;(C:研究組,D:對照組)為E-cadherin的表達;(E:研究組,F:對照組)為MVD的表達;箭頭為陽性表達區域;(標尺=100μm)。
2.3兩組患者接受藥物治療后的不同結局發生情況
兩組患者接受藥物規范治療后,發生完全流產共165例(81.28%),不完全流產38例(18.72%),無治療失敗病例發生;研究組患者不完全流產發生率(28.42%)高于對照組(10.19%),差異有統計學意義(χ2=11.05,P<0.01),見表3。
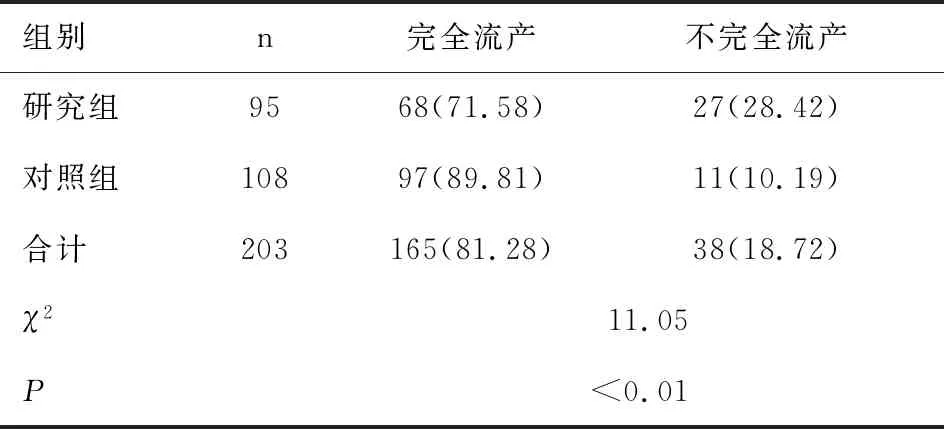
表3 兩組患者接受藥物治療后不同結局發生情況比較[n(%)]
2.4影響藥物治療后發生不完全流產的單因素分析
單因素分析結果顯示,藥物治療后不完全流產患者年齡及BMI偏大(t=5.05,P<0.01;t=5.62,P<0.01)、痛經比例偏高(χ2=17.78,P<0.01)、絨毛組織中E-cadherin陽性表達率較低(χ2=33.64,P<0.01)、MVD的表達量也低于完全流產患者(t=5.27,P<0.01),見表4。
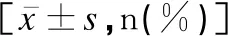
表4 影響藥物治療后發生不完全流產的單因素分析
2.5影響藥物治療后發生不完全流產的多因素Logistic回歸分析
以藥物治療后是否發生不完全流產為因變量,以單因素分析中有統計學差異的因素為自變量進行二分類多因素Logistic回歸分析,結果顯示,痛經(OR=2.24,95%CI:1.36~3.71,P<0.01)是藥物治療后發生不完全流產的獨立危險因素;絨毛組織中E-cadherin的表達(OR=0.69,95%CI:0.55~0.70,P<0.01)和MVD的表達(OR=0.72,95%CI:0.68~0.78,P<0.01)均為患者接受藥物治療后發生不完全流產的獨立保護因素,見表5。
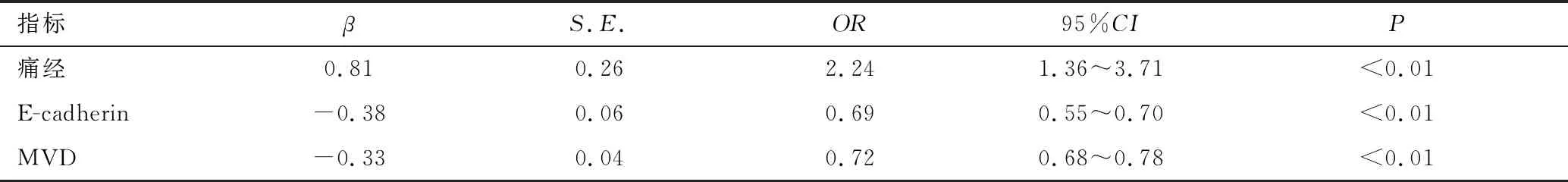
表5 影響藥物治療后發生不完全流產的多因素Logistic回歸分析
3討論
3.1稽留流產絨毛組織中IGF-1、E-cadherin、MVD表達及相關性
胎盤血管網的建立對胚胎的正常生長發育、保障胎兒獲取其生長所需的血液灌注量至關重要。胚胎發育早期,機體絨毛膜的一部分細胞分化為胎盤,另一部分分化為胎盤血管網,對子宮螺旋動脈進行重塑,建立起母體與胎兒之間的聯系,使胎兒能夠通過母體血液獲取自身發展所需要的營養[11]。若胎盤血管網建立受到阻礙,造成胎盤微循環障礙,則胎兒通過母體血液攝取必需物質(充足的氧氣、免疫因子和營養物質等)接收不足,造成發育不良,甚至引發胎兒死亡[12]。本研究結果也顯示,稽留流產患者絨毛組織中MVD的相對表達量明顯低于對照組,提示稽留流產患者胎盤血管網發育不良。胎盤血管網的建立由多種生長因子與基因共同協調參與,若其表達過高或過低,都會對胎盤血管網的發育造成消極影響,使得胎盤功能不全,造成胎兒生長發育受限,最終導致流產或死胎等不良結局。
IGF-1對維持子宮內膜正常分泌與增殖有重要意義,其在妊娠早期通過局部組織分泌產生,發揮調控滋養細胞的增殖、分化等過程,對于胚胎的生長發育至關重要。有研究發現,IGF-1能夠增強體外孕早期滋養細胞的生物活性,調節胎盤血流動力學,改善胎盤生理功能,促進胎兒的生長發育[13]。本研究結果顯示,稽留流產患者絨毛組織中IGF-1表達低于正常流產患者,提示IGF-1低表達與稽留流產的發生存在相關性。其可能原因是由于IGF-1的表達對于滋養細胞的黏附作用有積極影響,可與整合素相互作用,對胚胎著床的信號轉導發揮其介導作用。稽留流產患者體內IGF-1表達過低,致使其信號轉導功能障礙,進而阻斷胚胎著床信號傳導,影響胚胎組織的正常生長分化[14]。E-cadherin是一種鈣依賴性跨膜糖蛋白,其在同型細胞的相互黏附中有重要作用。既往研究表明E-cadherin表達水平異常升高時會使細胞間黏附增強,降低細胞浸潤與遷移能力,對腫瘤的復發與轉移有較強的抑制作用[15]。妊娠期間,E-cadherin在母胎蛻膜上皮細胞與滋養細胞中表達廣泛,并在受精卵著床到胎盤浸潤子宮等多個環節中均有參與[16]。在本研究中,研究組患者E-cadherin陽性率明顯低于對照組,與既往研究結果基本一致,究其原因可能是E-cadherin表達下降,使其介導的細胞連接與黏附受到影響,進而造成滋養細胞黏附與浸潤能力降低,子宮螺旋動脈的形成出現障礙,血管重塑被阻斷,使胎盤血管網的建立被抑制,導致胚胎發育停止,造成稽留流產結局。
3.2米非司酮配伍米索前列醇治療后發生不完全流產的影響因素
稽留流產因其特殊性,在臨床研究中日益受到重視,以往臨床治療多以清宮術為主,雖然效果較好,但易引起感染、宮頸粘連等多種并發癥,甚至導致患者繼發性不孕,使患者生理、心理受到極大創傷。藥物治療作為一種簡單方便、效果較好、患者易于接受的治療方式,在臨床治療中亦有一定的應用價值[17]。米非司酮為抗孕酮類藥物,與孕酮受體結合,表現出高度的受體和組織選擇性,阻斷絨毛組織供血,促進子宮收縮,使胎盤、胎膜與子宮壁發生剝離,且可擴張、軟化宮頸,促進胚胎排出。米索前列醇為前列腺素衍生物,可誘發子宮平滑肌收縮,與米非司酮協同作用,能使宮頸結締組織中的膠原纖維溶解,促進宮頸軟化成熟和擴張,使孕囊排出,應用于終止早孕及小孕周的中期妊娠,取得較好臨床效果[18]。
本研究結果也顯示,藥物治療后發生不完全流產率約為18.72%,稽留流產患者不完全流產發生率高于正常早孕患者。稽留流產的發生機制尚不明確,目前認為可能與母胎之間的免疫平衡失調、孕酮分泌不足、染色體異常、社會環境及各種感染等多種因素共同作用有關。對于米非司酮配伍米索前列醇治療后發生不完全流產的影響因素亦不明確[19]。本研究結果發現,藥物治療后不完全流產的發生率在不同年齡和BMI之間存在差異,多因素分析結果也發現,痛經是藥物治療后發生不完全流產的獨立危險因素,絨毛組織中E-cadherin的表達和MVD的表達均為患者接受藥物治療后發生不完全流產的獨立保護因素,提示稽留流產患者存在痛經史,則其接受藥物治療后發生不完全流產的風險較高,而其E-cadherin表達水平越高,MVD越大,則發生治療后不完全流產的風險越低。
綜上所述,稽留流產患者絨毛組織中IGF-1、E-cadherin表達和MVD含量較低,接受藥物治療后完全流產患者IGF-1、E-cadherin與MVD均高于不完全流產患者,E-cadherin表達水平越高,MVD越大,則出現不完全流產的風險越低。

