基于ACE2受體探討玉屏風散預防新型冠狀病毒肺炎的網絡藥理學機制?
王 登,王 娣,曹 青,閆抗抗△
1 西北大學附屬醫院/西安市第三醫院,陜西 西安 710018; 2 陜西省中醫藥研究院,陜西 西安 710016
中醫藥學是一個動態辨證論治和整體觀念指導的醫學體系,抗擊疫病具有上千年的臨床經驗,在各個時期都發揮著無法替代的積極作用。“治未病”是中醫藥預防疫病的特色,新型冠狀病毒肺炎(Corona Virus Disease 2019,COVID-19)疫情發生后,各地根據“三因制宜”相繼出臺了多個中藥預防方案。本課題組前期通過對各地診療方案用藥規律進行數據挖掘,發現各地發布的預防類處方中,玉屏風散的使用頻次最高[1]。《新型冠狀病毒肺炎中醫診療手冊》也提到對于未能明確診斷的輕型患者,時邪犯表證使用蔥豉湯合玉屏風散加味[2]。可見玉屏風散對COVID-19具有一定的預防作用。
血管緊張素轉化酶2(angiotensin converting enzyme 2,ACE2)受體在肺組織中主要分布于Ⅱ型肺泡細胞,嚴重急性呼吸綜合征冠狀病毒2(severe acute respiratory syndrome coronavirus 2,SARS-CoV-2)可能利用宿主細胞ACE2受體,使用其刺突蛋白進入靶細胞,從而感染宿主[3]。所以ACE2相關基因是干預COVID-19的重要靶點。已有研究證實,玉屏風散的主要成分黃芪,對代謝綜合征大鼠腎臟ACE2 mRNA的表達具有一定調節作用[4]。提示玉屏風散可能介導ACE2受體預防COVID-19,但是鑒于中藥復方多成分、多靶點、多通路等作用特點,目前玉屏風散預防COVID-19的作用機制尚未完全闡明。本研究借助網絡藥理學的研究方法,對玉屏風散介導ACE2受體預防COVID-19的有效成分、作用靶點及信號通路進行探索,利用GO(gene ontology)和KEGG(kyoto encyclopedia of genes and genomes)信號通路富集分析其潛在作用機制,以期為其臨床應用提供新的依據。
1 資料與方法
1.1 玉屏風散活性成分的篩選及靶點基因預測玉屏風散由黃芪、白術、防風3味中藥組成。利用中藥系統藥理數據庫和分析平臺(traditional Chinese medicine systems pharmacology database and analysis platform,TCMSP)數據庫(http://tcmspw.com/tcmsp.php)檢索3味藥材所有活性成分,并利用口服生物利用度(oral bioavailability,OB)和類藥性(drug likeness,DL)兩個藥物動力學參數對所有活性成分進行篩選,設置條件為OB≥30%和DL≥0.18,將篩選后的化合物作為候選成分。采用TCMSP數據庫檢索玉屏風散所有活性成分潛在的蛋白靶點,并使用Uniprot數據庫(https://www.uniprot.org)中的UniprotKB搜索功能,通過輸入查詢到的靶蛋白名稱,并限定物種為“Homo sapiens”,剔除非人源靶點,獲取活性成分靶點的標準基因名稱。
1.2 COVID-19靶點的檢索及相互靶點Venn分析本研究利用WANG等[5]對結腸上皮細胞測序結果識別到的與ACE2共表達的5556個基因,與玉屏風散活性成分對應的基因進行Venn分析,得到共同的交集基因。
1.3 構建 “中藥-活性成分-靶點-疾病”網絡圖將交集基因采用網絡圖像化軟件Cytoscape 3.7.2構建“中藥-活性成分-靶點-疾病”網絡圖。“中藥-活性成分-靶點-疾病”網絡圖的核心架構是網絡,每個節點(node)是基因、蛋白質或分子等,節點與節點之間的連接(edge)代表這些生物分子之間的相互作用[6]。本次網絡中節點(node)表示中藥、活性成分、基因靶點、疾病。
1.4 蛋白質-蛋白質相互作用關系(proteinprotein interaction,PPI)網絡圖構建將交集基因在線導入STRING數據庫(https://string-db.org),限定物種人,進行蛋白相互作用分析,設置交互作用可信度等級為高可信度(≥0.7),構建蛋白質-蛋白質相互作用關系網絡圖,尋找靶點和靶點間的作用關系。并將結果導入Cytoscape軟件進行網絡圖優化,其中節點大小和顏色設置用于反映度值的大小,邊的粗細和顏色設置用于反映結合率評分的大小[6]。使用度值、介數中心性篩選關鍵靶點。
1.5 GO與KEGG通路富集分析使用DAVID生物學信息注釋數據庫(https://david.ncifcrf.gov)對網絡合并后獲得的交集基因進行GO富集分析和KEGG信號通路富集分析。將交集靶點導入DAVID數據庫,Select identifier設置為OFFICIAL GENE SYMBOL,List Type設置為GeneList,限定物種為人,對作用靶點進行基因本體(gene ontology,GO)分析和KEGG通路分析,P<0.05為差異有統計學意義。富集分析GO生物學過程包括:生物過程、分子功能、細胞組成分3個模塊繪制條形圖[7],KEGG分析結果做氣泡圖。
2 結果
2.1 玉屏風散活性成分的篩選及靶點基因預測從TCMSP數據庫中搜索組成玉屏風散的3味中藥的化合物成分,得到結果:黃芪87個,白術55個,防風173個。根據OB>30%及DL≥0.18要求,刪去重復的化合物,最終選定44個化合物,其中白術7個,黃芪20個,防風18個,白術與黃芪有1個共同成分。通過TCMSP數據庫檢索得到黃芪對應的蛋白靶點218個,白術19個,防風70個,刪去重復靶點,并在Uniprot數據庫檢索其對應“人”的基因名稱,最終得到基因靶點197個。
2.2 COVID-19靶點的搜集及靶點Venn分析通過文獻獲得與ACE2共表達的5556個基因,將ACE2相關靶點基因與活性成分對應的靶點基因取交集進行韋恩分析,共得到56個靶點。表明這56個靶點可能是玉屏風散介導ACE2預防COVID-19的關鍵靶點。基因維恩分析如圖1所示,交集基因靶點如表1所示。
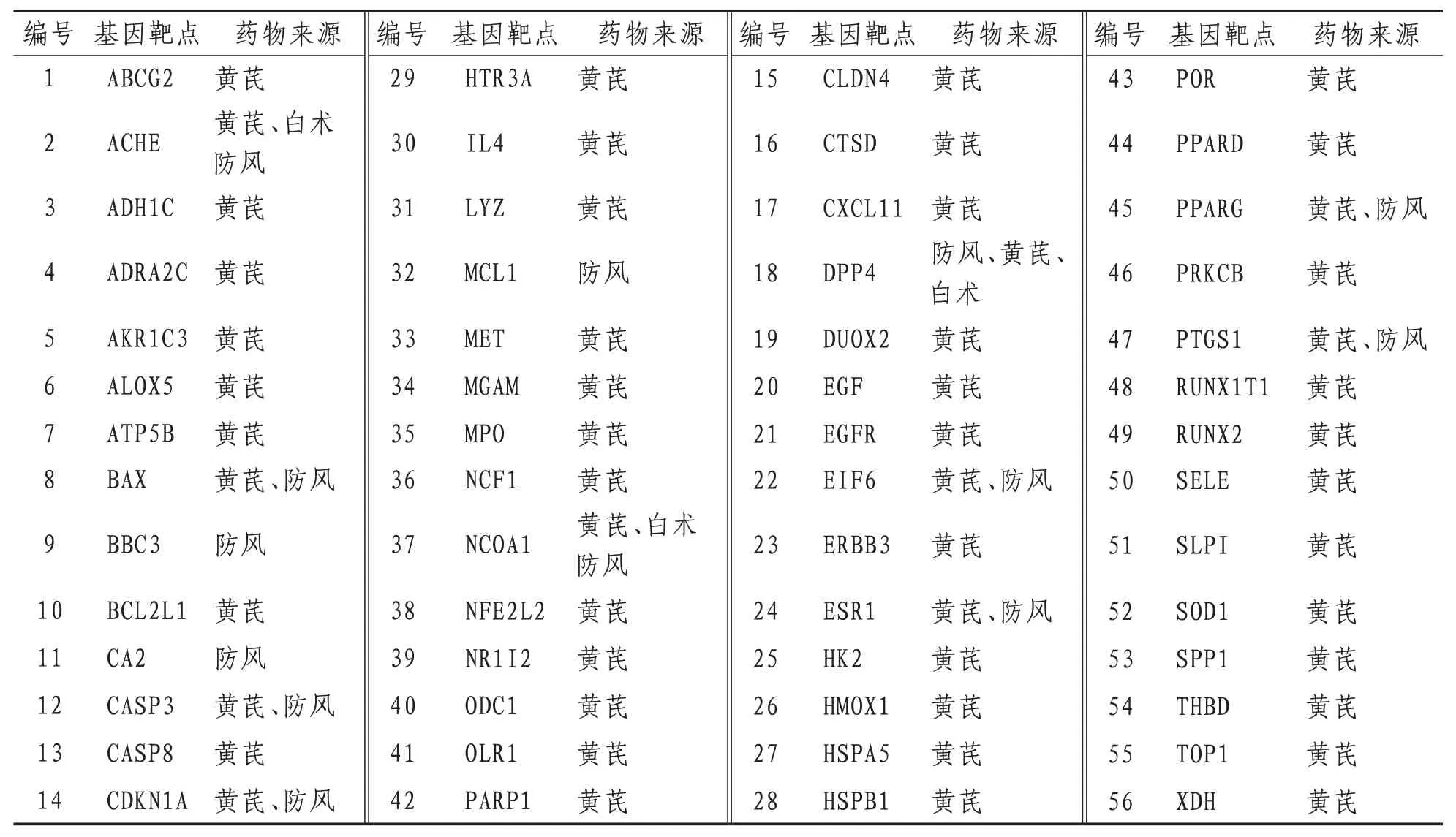
表1 玉屏風散介導ACE2預防COVID-19的關鍵靶點
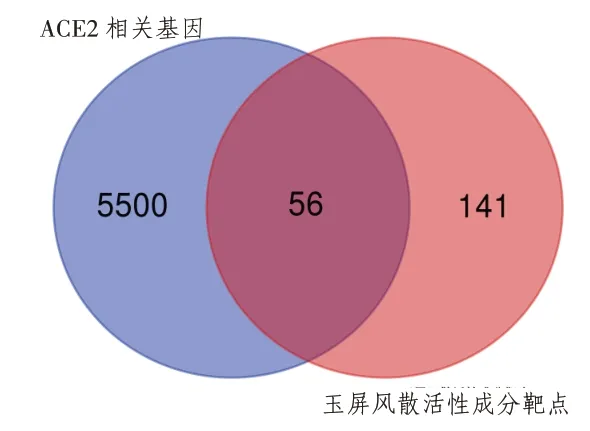
圖1 玉屏風散成分靶基因與ACE2相關靶點基因維恩分析圖
2.3 構建“中藥-活性成分-靶點-疾病”網絡圖將獲得的56個關鍵靶基因映射所屬成分,發現44種有效成分中有26種成分參與對關鍵靶基因的調控,構建成分靶點關系對文件,使用Cytoscape 3.7.2軟件構建“中藥-成分-靶點-疾病”網絡關系圖,網絡關系圖見圖2。

圖2 玉屏風散“中藥-活性成分-靶點-疾病”網絡
2.4 PPI網絡構建采用STRING數據庫構建蛋白相互作用網絡,結果導入Cytoscape 3.7.2軟件構建可視化網絡關系圖,見圖3。結果共涉及65個節點,78條邊。選擇度值≥5,介數中心性≥0.1的節點作為主要靶點,則相互作用的主要靶點為天冬氨酸特異性酶切半胱氨酸蛋白酶3(Caspase-3,CASP3)、表皮生長因子受體(epidermal growth factor receptor,EGFR)、β型蛋白激酶C(protein kinase C beta type,PRKCB)、雌激素受體(estrogen receptor,ER)、表皮生長因子前體(proepidermal growth factor,EGF)等相互作用。
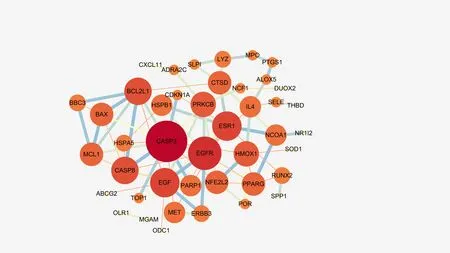
圖3 玉屏風散介導ACE2受體預防COVID-19靶標蛋白互作網絡圖
2.5 關鍵基因靶點Go富集分析對篩選得到的56個關鍵靶點進行GO分析,設定閾值P<0.05,共富集到156條生物學過程,其中生物過程(biological process,BP)條目105個,細胞組成(cellular component,CC)條目20個,分子功能(molecular function,MF)條目31個,分別占67.31%、12.82%、19.87%。篩選P值較小的生物學過程繪圖,見圖4—6。BP主要涉及缺乏配體時的體外凋亡信號通路、凋亡過程負調控、凋亡線粒體的變化、藥物反應、氧化還原過程等。CC涉及細胞外間隙、Bcl-2家族蛋白復合物、膜筏、線粒體外膜、細胞外外泌體、胞質等。MF涉及蛋白結合、酶結合、蛋白質同源二聚化活性、BH3域結合、RNA聚合酶Ⅱ轉錄因子活性等。
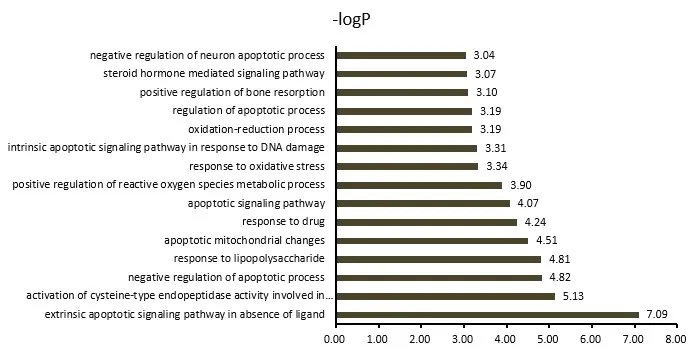
圖4 玉屏風散介導ACE2受體預防COVID-19關鍵靶點的BP富集分析
2.6 通路KEGG富集分析KEGG富集分析篩選到27條通路,其中18條具有顯著意義(P≤0.05),結果見表2。KEGG功能注釋富集分析提示,玉屏風散可能作用包括癌癥通路、HIF-1信號通路、癌癥中的轉錄失調、p53信號通路、PI3K-Akt信號通路、細胞凋亡等通路。這些表明玉屏風散可通過多個通路介導ACE2受體發揮預防COVID-19的作用。進一步對KEGG富集分析結果進行可視化處理,圖形化結果見圖7。
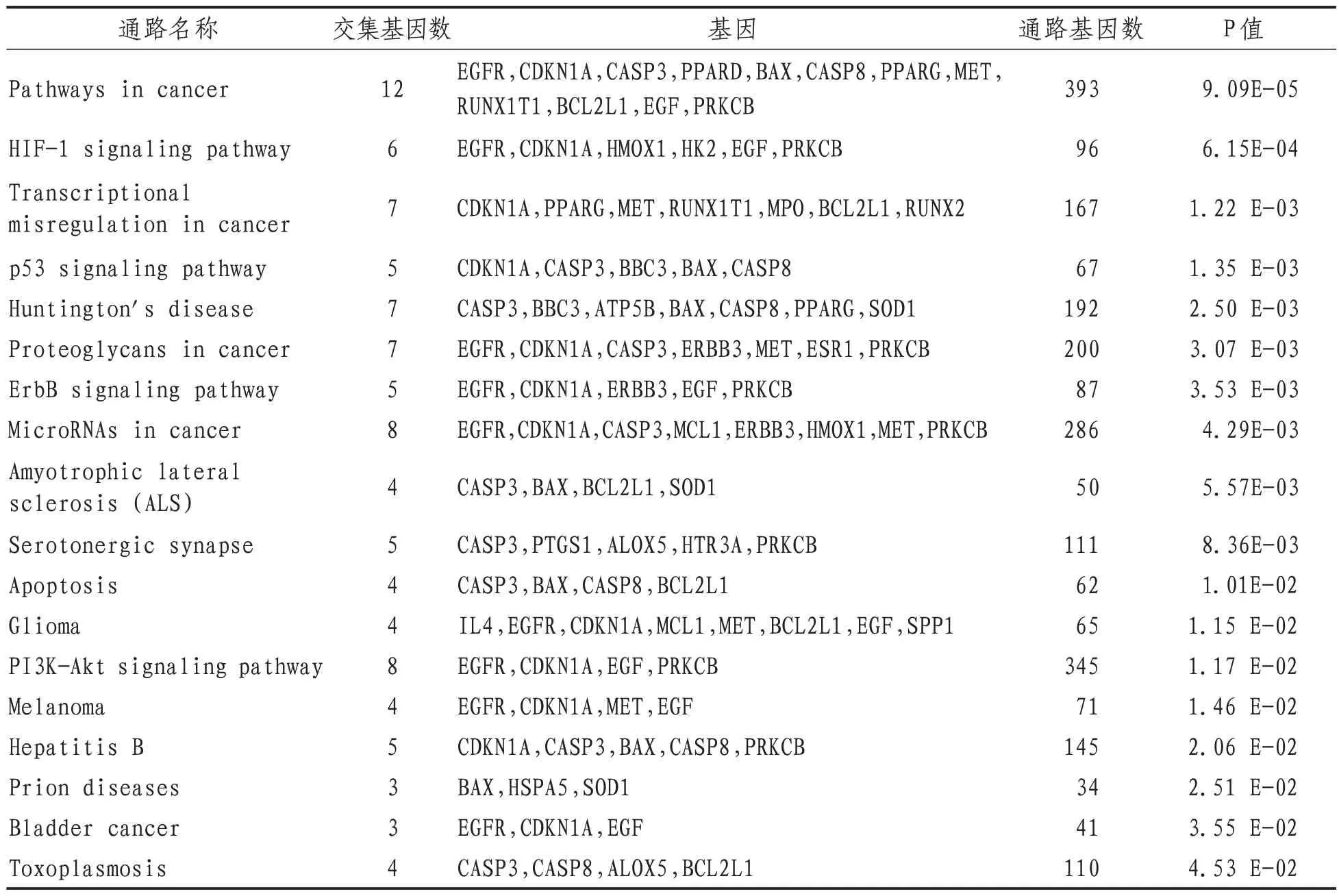
表2 玉屏風散介導ACE2關鍵靶點KEGG富集信號通路
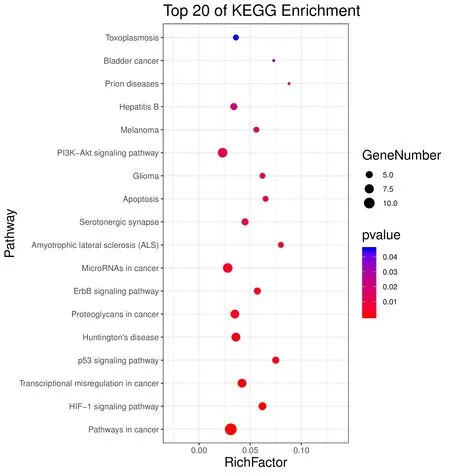
圖7 玉屏風散介導ACE2預防COVID-19潛在核心靶點的KEGG富集分析

圖5 玉屏風散介導ACE2受體預防COVID-19關鍵靶點的CC富集分析
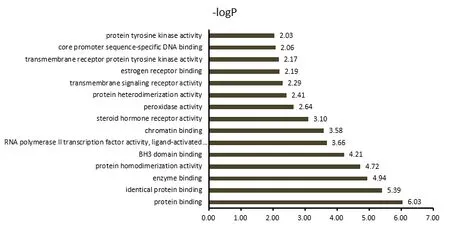
圖6 玉屏風散介導ACE2受體預防COVID-19關鍵靶點的MF富集分析
3 討論
玉屏風散具有益氣固表止汗的功用,用于治療表虛自汗[8]。臨床廣泛用于呼吸道疾病,如反復上呼吸道感染、流行性感冒、難治性支原體肺炎、支氣管哮喘等[9]。最新研究發現,玉屏風散發酵多糖具有雙向免疫調節作用,可增強進淋巴細胞增殖[10]。另外,研究發現玉屏風散具有抑制病毒復制的作用。動物實驗研究發現,加味玉屏風散可抑制預處理小鼠病毒融合受體ICAM-1的表達,抑制病毒附著、病毒滲透,降低細胞對病毒入侵的敏感性,可以預防流感病毒和人呼吸道合胞病毒引起的呼吸道病毒感染[11]。在2003年非典型肺炎流行期間,北京中醫藥大學東直門醫院姜良鐸、周平安教授推薦的預防處方和上海漢殷藥業生產的扶正祛邪口服液中均包含玉屏風散[12]。本次疫情期間中醫藥防治方案中也大多推薦玉屏風散加減方作為預防用藥[13]。可見,玉屏風散對COVID-19具有一定的預防作用,但其具體作用機制尚不明確。
研究發現,ACE2受體蛋白是SARS-Cov-2入侵人體細胞的關鍵,SARS-Cov-2表面的S蛋白與人體細胞表面的ACE2蛋白結合,再通過細胞的胞吞作用進入細胞,感染組織。所以,若能阻斷SARSCov-2與ACE2的結合,便可能阻止病毒感染[13]。黃芪是玉屏風散的重要組成藥物,研究發現黃芪對代謝綜合征大鼠腎臟ACE2 mRNA的表達具有一定調節作用[4]。黃芪的水和甲醇提取物對禽流感H9病毒具有一定的抑制作用[14]。所以,玉屏風散可能通過調控ACE2相關靶點,而發揮預防COVID-19的作用。網絡分析的結果顯示,玉屏風散的3味藥物共含44種不同的化合物,對應197個靶點,其中56個靶點為ACE2相關基因的交集靶點。可見,玉屏風散可能對機體ACE2受體相關表達具有一定的調控作用。
蛋白質相互作用結果顯示玉屏風散的有效成分可能是通過CASP3、EGFR、PRKCB、ESR1、EGF等藥物-疾病共有靶點網絡起作用。研究發現,ACE2與Caspase家族密切相關,ACE2基因敲除小鼠主動脈血管平滑肌細胞活性氧和凋亡明顯增加,同時裂解caspase-3和裂解caspase-8水平升高[15]。病毒感染機體除引起氧化應激損傷和炎癥反應外,還可誘導宿主細胞發生凋亡,凋亡信號傳導以Caspase激活開始,其中Caspase-3是Caspase家族中最重要的凋亡執行者,是引發細胞凋亡的關鍵酶,可降解細胞內的結構蛋白及維持基因組穩定和對細胞周期起調控作用,導致細胞發生凋亡[16]。所以,CASP3可能通過與ACE2相互影響而作用于病毒感染。在呼吸道,EGFR廣泛表達于上皮細胞,EGFR活化后能夠募集中性粒細胞,產生黏蛋白,促進分泌抗菌多肽并清除病原微生物等[17]。研究發現,ACE2表達與EGFR密切相關,EGFR突變的原發性肺腺癌中,ACE2的表達水平遠高于正常肺上皮細胞[18]。所以,EGFR可能是玉屏散介導ACE2預防COVID-19的關鍵靶點。
GO分析結果顯示,BP分析可見玉屏風散的生物過程主要涉及缺乏配體時的體外凋亡信號通路、凋亡過程負調控、凋亡線粒體的變化、藥物反應、氧化還原過程等。研究發現,黃芪注射液具有明顯的抗流感病毒活性,可以提高被感染細胞的存活率,同時提高流感病毒對感染后細胞周期的阻斷作用[19]。CC分析可見玉屏風散靶點主要涉及細胞外間隙、Bcl-2家族蛋白復合物、膜筏、線粒體外膜、細胞外外泌體、胞質等。病毒進入人體后,最外層的刺突蛋白通過與人的呼吸道上皮細胞表面特異性受體(ACE2蛋白)結合,再通過細胞的胞吞作用進入細胞,冠狀病毒進入細胞后直接以病毒基因組RNA為翻譯模板,表達出病毒RNA聚合酶[20]。再利用這個酶完成負鏈亞基因組RNA的轉錄合成、各種結構蛋白mRNA的合成,以及病毒基因組RNA的復制,這些都在細胞質內進行。MF分析可見玉屏風散的靶點主要涉及蛋白結合、酶結合、蛋白質同源二聚化活性、BH3域結合、RNA聚合酶II轉錄因子活性等分子功能。SARS-Cov-2是一種單鏈RNA正鏈包膜β冠狀病毒,其基因組編碼結構蛋白刺突糖蛋白,刺突蛋白與ACE2蛋白結合,再通過細胞的胞吞作用進入細胞。另外,冠狀病毒感染細胞是一個復雜的過程,需要ACE2受體結合和刺突糖蛋白的蛋白水解過程的協同作用來促進病毒-細胞融合。在宿主細胞感染病毒之后,宿主的蛋白酶對S蛋白進行蛋白水解,產生兩個功能亞單位,即S1和S2。S1亞單位包括受體結合區,S2錨定在病毒膜上促進病毒細胞融合。因此,刺突糖蛋白被認為是開發抗病毒藥物的重要靶標[21]。
KEGG通路分析結果顯示,玉屏風散預防COVID-19主要涉及癌癥通路、HIF-1信號通路、癌癥中的轉錄失調、p53信號通路、PI3K-Akt信號通路、細胞凋亡等通路。HIF-1α是HIF-1的亞單位組成,是缺氧狀態下激活的關鍵轉錄因子,在缺氧條件下可穩定表達,是維持細胞內氧環境穩定的核心轉錄因子。研究發現,HIF-1α是肺部炎性損傷的關鍵因子[22]。在缺氧條件下HIF-1α可抑制ACE2的表達,而ACE催化的ANGⅡ的積累是HIF-1α下調ACE2的關鍵中介物[23]。另外PI3K/AKT通路與呼吸系統疾病發生發展密切相關[24]。研究發現,PI3K/AKT信號通路在ACE2促進內皮細胞eNOS活性中發揮重要作用[25]。提高的ACE2可通過AT1受體-PI3K/AKT途徑減弱小鼠系膜細胞血管緊張素Ⅱ誘導的膠原生成,改善促纖維化作用[26]。可見,ACE2與PI3K/AKT通路可能存在一定的交互作用,PI3K/AKT通路可能介導ACE2參與玉屏風散對COVID-19預防。
綜上所述,本研究采用網絡藥理學方法對玉屏風散主要有效成分作用于ACE2相關基因進行分析,初步探索其潛在預防COVID-19的分子機制,結果表明,玉屏風散是可能通過多成分、多靶點、多通路介導ACE2來發揮預防COVID-19的作用,其中CASP3、EGFR等基因可能為其作用關鍵靶點,HIF-1信號通路、PI3K-Akt信號通路等通路可能參與其中,但其具體機制有待進一步研究。

