早產兒視網膜病變患兒致病危險因素及不同分期發病率的探究
趙 翠
信陽市眼科醫院眼科,河南 信陽 464000
視網膜是由大腦向外伸延的視覺神經末梢組織,其結構十分復雜且脆弱,早產兒視網膜病變(retinopathy of prematurity,ROP)是指胎齡在36 周以下、出生時體重過輕、需要長時間氧療的早產兒由于其未血管化的視網膜發生纖維化增生、收縮,并進一步引起牽拉性視網膜脫離和失明[1-2]。通常胎兒的視網膜血管會在胚胎發育至36周時發育到達胎兒鼻側邊緣,胚胎發育至40周時到達顳側緣,而早產兒視網膜未完全血管化,暴露于高濃度的氧環境下,對氧產生血管的收縮和增殖現象,從而引起毛細血管內皮細胞損傷、血管閉塞,刺激纖維血管組織增生,有嚴重的致盲性,其失明占比在所有失明兒童中高達6%~8%[3-4]。對ROP致病危險因素及不同分期發病率進行分析有助于提高臨床診斷篩查率,提高ROP 患兒預后質量[5-6]。本研究對信陽市眼科醫院收治的138 例早產兒臨床資料展開回顧性分析,以探討早產兒發生ROP的獨立危險因素及不同分期發病率,為臨床預防ROP提供參考。
1 資料與方法
1.1 一般資料
回顧性分析2019 年10 月—2021 年1 月信陽市眼科醫院收治的130 例早產兒臨床資料,將出生胎齡為30~36 周的早產兒設置為A 組(n=89),將出生胎齡小于30 周的早產兒設置為B 組(n=41)。納入標準:(1)胎齡<36 周,出生時體重過低、需要長時間氧療的早產兒。(2)檢查報告完整,臨床資料齊全。(3)于我院接受產檢與分娩。(4)無先天性體表畸形疾病。(5)監護人自愿參與。排除標準:(1)眼部結構發育異常。(2)眼部先天畸形。(3)凝血功能障礙。(4)嚴重代謝平衡紊亂。 本研究在患兒家屬知情同意下開展,并經醫院醫學倫理委員會批準通過。
1.2 方法
所有早產兒均于出生4周后接受眼底篩查,檢查前半小時使用復方托吡卡胺滴眼液(沈陽興齊眼藥股份有限公司;國藥準字:H20055546;規格:5 mL/支),滴入早產兒眼部,使其瞳孔充分擴散(共3~4 次,每間隔5 min 重復散瞳1 次,直至雙側瞳孔散大到7~8 mm);在檢查時使用鹽酸奧布卡因滴眼液(山東博士倫福瑞達制藥有限公司;國藥準字:H20056587;規格:0.5 mL:2.0 mg)對早產兒眼球表面進行麻醉,使用開瞼器分開眼瞼,后用間接眼底鏡和屈光度20~30 D的透鏡進行眼底檢查,檢查同時時刻檢測早產兒的各項生命體征,防止發生眼心反射所致的心動過緩,檢查后0.5~2 h 即可進食,體重越輕的早產兒禁食時間越長,期間要注意防止早產兒發生低血糖;ROP診斷及分期標準均參照《早產兒視網膜病變特點和篩查指南》[7]。對早產兒及其母親的臨床資料進行分析,統計產婦信息(年齡、既往是否有生育史、母體宮內感染、妊娠期高血壓、妊娠期糖尿病、胎兒宮內窘迫等)及胎兒/新生兒信息(胎兒胎齡、性別、出生時體質量、氧療時間、出生時是否有呼吸暫停現象、是否有肺炎等),同時結合眼底篩查結果分析各因素與早產兒發生ROP 的相關性。
1.3 觀察指標
(1)分組情況及兩組早產兒基線資料對比:對比兩組不同胎齡早產兒性別及分娩方式。(2)兩組早產兒ROP發病率及其分布規律:結合眼底篩查結果對比不同胎齡早產兒ROP 發病率及不同分期的對應人數。(3)早產兒ROP發病率的單因素分析。(4)早產兒ROP 發病率的多因素分析。
1.4 統計學方法
采用SPSS 22.0 軟件進行統計分析。計數資料以例數和百分比(%)表示,組間比較采用χ2檢驗。計量資料以均數±標準差(±s)表示,組間比較采用t 檢驗。等級資料采用秩和檢驗,采用多因素logistic 回歸模型進行分析早產兒發病率的影響。以P<0.05為差異有統計學意義。
2 結果
2.1 兩組早產兒基線資料情況
臨床資料顯示,130例早產兒中胎齡≥30周的共89例(A 組),<30 周的共41 例(B 組);兩組早產兒基線資料對比,差異無統計學意義(P>0.05),見表1。
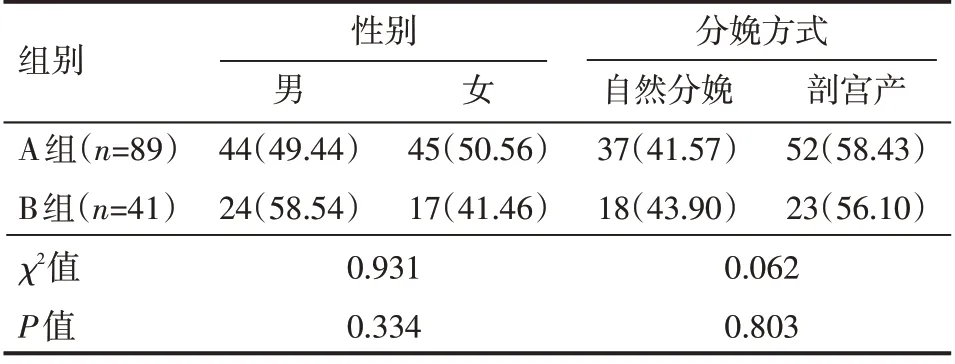
表1 兩組早產兒基線資料情況 例(%)
2.2 兩組早產兒ROP發病率及其分布情況
兩組早產兒眼底篩查結果顯示,A 組ROP 檢出率50.48%(30/89)低于B組的87.80%(36/41),差異有統計學意義(χ2=32.865,P<0.05);B 組ROP 患兒纖維形成期(Ⅰ度、Ⅱ度、Ⅲ度)人數占比高于A 組,差異有統計學意義(P<0.05),見表2。
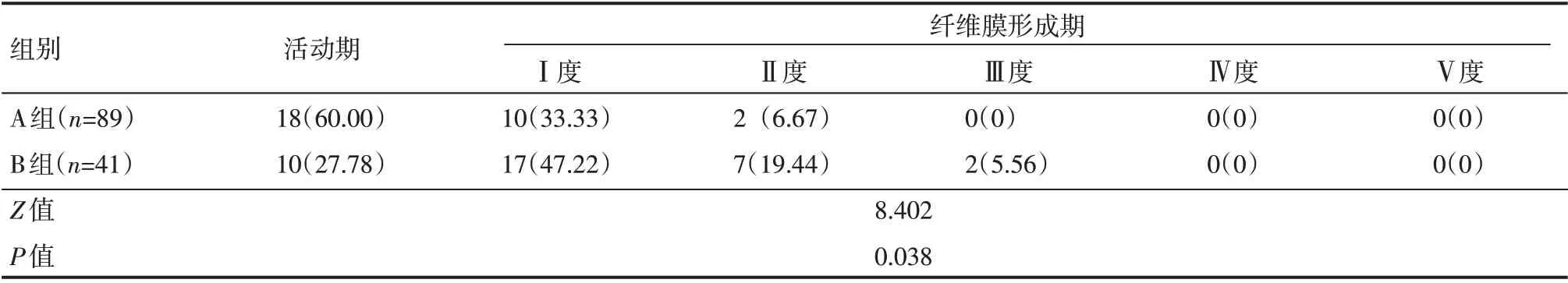
表2 兩組早產兒ROP發病率及其分布情況 例(%)
2.3 早產兒ROP發病率的單因素分析情況
早產兒ROP發病率的單因素分析結果顯示,不同產婦年齡、早產兒性別、產婦既往生育史的ROP發病率,差異無統計學意義(P>0.05),不同呼吸暫停、肺炎、母體宮內感染、妊娠期高血壓、妊娠期糖尿病、胎兒宮內窘迫、胎齡、出生體重、氧療時長的ROP發病率,差異有統計學意義(P<0.05),見表3。
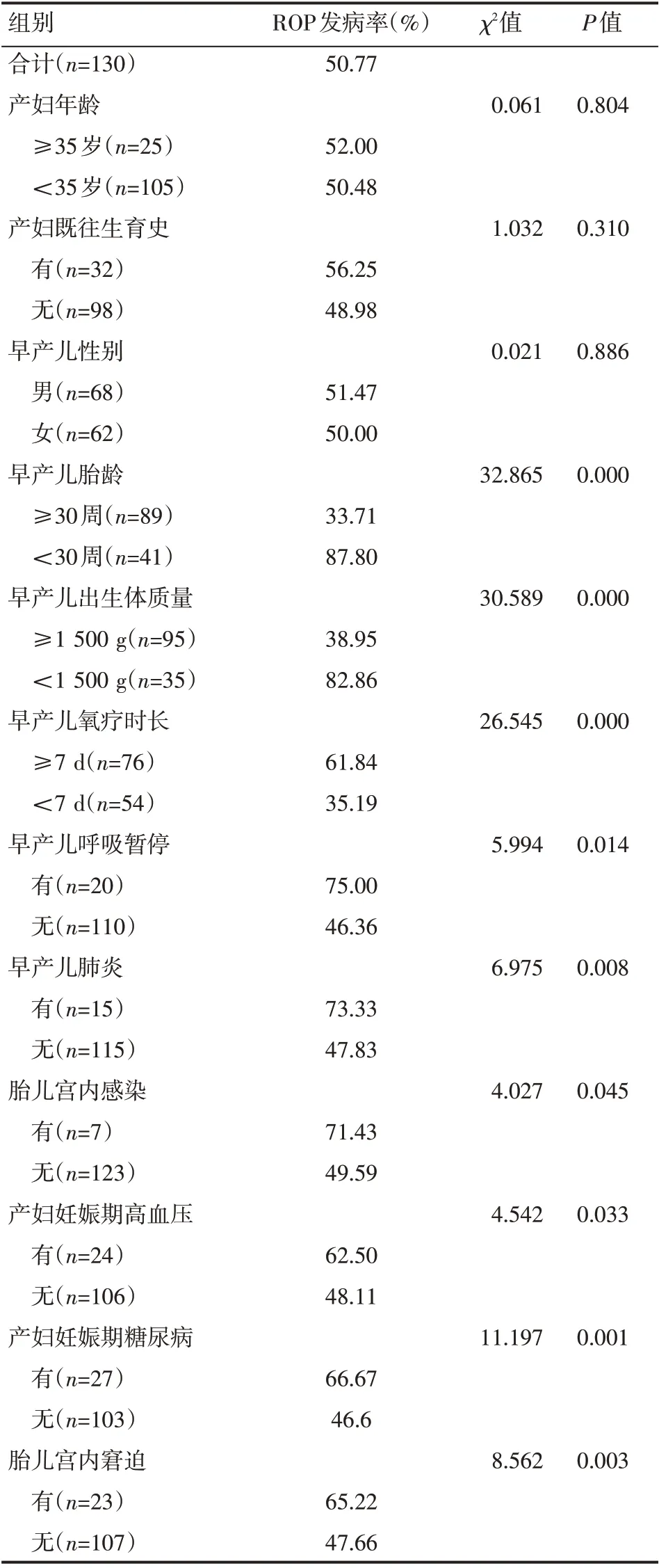
表3 早產兒ROP發病率的單因素分析情況
2.4 logistic回歸分析早產兒ROP發病的危險因素
logistic多因素回歸分析顯示,早產兒胎齡、出生體質量、氧療時長是早產兒ROP發病的危險因素,差異有統計學意義(P<0.05),見表4。
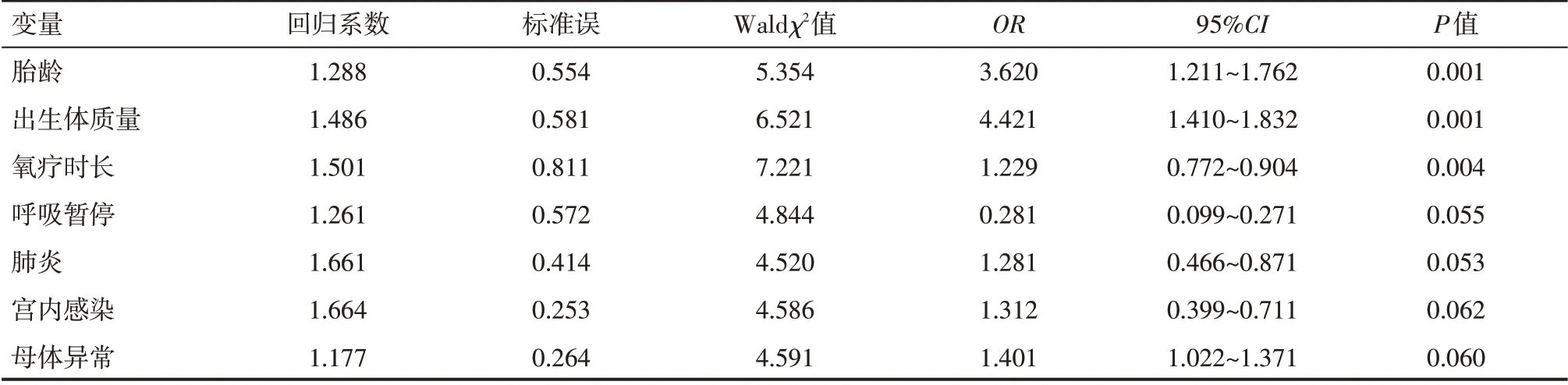
表4 logistic回歸分析早產兒ROP發病的危險因素
3 討論
臨床上ROP常見于早產兒出生后的3~6周,主要分為活動期和纖維膜形成期,ROP的活動期病程一般為3~5個月,若早產兒在活動期病情未自行消退則最終會由于瘢痕化而形成纖維膜[8-10]。ROP的發病進展較快,一旦發生后其可治療的時間相對很短,因此對胎齡小于36周的早產兒出生后應該及時予以篩查,對ROP的高危者也應該加大檢查頻率[11-12]。若早產兒發生ROP后,一般進入Ⅱ~Ⅲ期后就可以采取激光或冷凍治療,將患兒無血管區進行凝固,防止惡化,進入Ⅳ~Ⅴ期后則可以采取玻璃體切除術將增殖的纖維血管組織予以切除,同時進行光凝治療,以此挽救早產兒的視力[13-14]。近年來臨床對ROP的治療已經取得了一定進展,但其發病率卻仍未得到有效控制,因此對ROP 的預防比治療更加重要。對早產兒限制用氧是預防ROP的有效措施之一,若早期發現早產兒有ROP病變風險及時采取冷凝、或激光治療也可有效阻止ROP 進一步惡化,對ROP活動嚴重的患兒可增加散瞳頻率以避免其虹膜后粘連而導致繼發性青光眼發生[15-16]。王亮等[17]指出,早產兒視網膜發生病變與多種因素相關,孕齡小于30周的早產兒發生ROP的風險較高,而出生時體重越輕發病率也會隨之升高。本研究結果也顯示孕齡小于30周、出生體質量小于1 500 g 是早產兒發生ROP 的危險因素。除此之外,早產兒出生時由于身體內各項組織器官都還未發育完整,因此早產兒通常需要進入NICU 進行氧療,以維持其生命體征,而氧療也是造成ROP的重要因素之一,早產兒若長期進行氧療也有可能導致其他嚴重的并發癥[18-19]。陳金國等[20]在研究中指出,ROP 組與正常眼底組早產兒在胎齡、出生體重吸氧時間>7 d、吸氧濃度>40%、呼吸暫停、孕期激素使用顱內出血、貧血、輸血、機械通氣等危險因素具有顯著差異,其中孕周小于27周的早產兒全部出現早產兒視網膜病變。本研究結果也顯示,早產兒發生ROP受多種因素共同影響,其中胎兒在分娩期間出現呼吸暫停、肺炎感染等癥狀可增加ROP發病率,同時若胎兒母體存在高血壓、糖尿病、宮內窘迫等也會一定程度上增加新生兒患ROP的風險,與陳金國等[20]的研究對應。本研究結果還顯示,胎齡小于30 周、出生體質量小于1 500 g、氧療時長>7 d 的早產兒ROP 發病率顯著高于其他早產兒。出生體重及胎齡是公認的ROP發生的兩個重要危險因素,與ROP 呈明顯負相關,本研究表明出生體質量輕或低齡發生ROP的發生率明顯增加,可能由于出生體重低、胎齡較小者發育尚未成熟,伴隨全身并發癥較多,同時需長時間以及高濃度給氧療。以上數據均充分說明早產兒的胎齡、出生時體質量及其對應的氧療時長均為其發生ROP的高危風險因素,因此臨床應對存在上述情況的早產兒及時進行眼底篩查并采取對癥干預。本研究由于樣本數量和觀察時間有限,研究結果不足以代表所有的早產兒視網膜病變情況,針對患兒相關致病危險因素及不同分期發病率還需要進一步實驗與探索。
綜上所述,早產兒胎齡短、出生體質量過輕、氧療時間過長是ROP 的危險因素,胎齡短于30 周的ROP 患兒纖維膜形成期占比高于胎齡長于30周的患兒,臨床應對存在上述情況的早產兒采取積極的治護措施,以提高母嬰生活質量。

