基于抑菌作用機制的金蓮花系列制劑再評價研究
田佩靈 劉睿鵬 鄧妍 鐘林江 雷詩懿 伍利華
摘要:目的 研究金蓮花口服液、片、膠囊及顆粒制劑的抗菌活性及作用機制。方法 采用牛津杯法初步摸索金蓮花系列制劑的抑菌活性;采用二倍稀釋法進一步測定金蓮花口服液、片、膠囊、顆粒對金黃色葡萄球菌和枯草芽孢桿菌的最小抑菌濃度(MIC)和最小殺菌濃度(MBC),并通過測定菌體的生長曲線、胞外核酸相對含量和胞外可溶性蛋白質含量研究金蓮花系列制劑對金黃色葡萄球菌的抗菌機制。結果 4種金蓮花制劑對金黃色葡萄球菌和枯草芽孢桿菌的抑菌活性按由強到弱為膠囊、口服液、片、顆粒。4種金蓮花制劑對金黃色葡萄球菌菌體生長均顯著的抑制效果,其作用機制相同,可增加菌體胞外核酸相對含量和胞外可溶性蛋白質含量趨勢,均通過對細菌細胞膜造成損傷改變其通透性,影響細菌生長,使胞內大量滲出,從而起到抑制細菌生長的作用。結論 4種金蓮花制劑的抗菌活性不同,對金黃色葡萄球菌的抑菌機制相同,為金蓮花系列制劑的質量再評價提供一定參考。
關鍵詞:金蓮花系列制劑;抗菌;抗菌活性;抑菌機制;再評價研究;金黃色葡萄球菌
中圖分類號:R978.1+9 ? ? ? ? 文獻標志碼:A ? ? ? ? 文章編號:1001-8751(2023)04-0263-06
Study on Antibacterial Activity and Antibacterial Mechanism of
Chinese globeflower Series Preparations
Tian Pei-ling1, Liu Rui-peng2,Deng Yan 1, ?Zhong Lin-jiang 1, Lei Shi-yi1,Wu Li-hua1
(1 Chengdu University School of Pharmacy, ? ? Chengdu ? ? 610106;
2 Chengdu University of Traditional Chinese Medicine, ? ?Chengdu ? ?610106)
Abstract:Objective To study the antibacterial activity and mechanism of Jinlianhua oral liquid, tablets, capsules and granules. Methods The Oxford cup method was used as a preliminary investigation of the antibacterial activity of the Jinlianhua series preparations. The minimum inhibitory concentration (MIC) and minimum bactericidal concentration (MBC) of Jinlianhua oral liquid, tablets, capsules and granules against Staphylococcus aureus and Bacillus subtilis were further determined by double dilution method. The antibacterial mechanism of Jinlianhua series preparations against Staphylococcus aureus was studied by measuring the growth curve of bacteria, the relative content of extracellular nucleic acid, and the content of extracellular soluble protein. Results The antibacterial activities of 4 kinds of Trollius chinensis Bunge preparations against Staphylococcus aureus and Bacillus subtilis were capsule, oral liquid, tablet and granule from strong to weak. In order of strength to weakness, the four different Trollius chinensis Bunge preparations have antibacterial activities against Staphylococcus aureus and Bacillus subtilis. Four kinds of Trollius chinensis preparations have significant inhibitory effects on the growth of Staphylococcus aureus. The mechanism of action is the same, which can increase the relative content of extracellular nucleic acid and the trend of extracellular soluble protein content. All of them alter the permeability of bacterial cell membranes by damaging them, impairing bacterial growth, and causing huge amounts of body fluid to exude, which prevents bacterial growth. Conclusion The antibacterial activities of the four kinds of Trollius chinensis Bunge preparations are different, and the antibacterial mechanism against Staphylococcus aureus is the same, which provides a reference for the quality reevaluation of Trollius chinensis Bunge preparations. The antibacterial activities of the four Trollius chinensis Bunge preparations were different and the inhibition mechanisms against Staphylococcus aureus were the same, providing some reference for the quality re-evaluation of Trollius chinensis Bunge of preparations.
Key words:Jinlianhua series preparations; ? antibacterial; ? antibacterial activity; ? antibacterial mechanism; ? ? ? re-evaluation research; ? Staphylococcus aureus
目前收載于《中國藥典》2020年版一部中的金蓮花系列制劑包括金蓮花口服液、片、膠囊及顆粒等,均由金蓮花一味中藥制得,文獻研究發現[1-5],這4種金蓮花制劑的適應癥均為上呼吸道感染,但其中金蓮花口服液和金蓮花膠囊在臨床中多用于治療口腔炎癥。上呼吸道感染是一種常見的臨床疾病,而金黃色葡萄球菌是導致患者上呼吸道感染的一種重要病原菌,常定植于人群鼻腔中。金蓮花對金黃色葡萄球菌(Staphylococcus aureus,SA)、枯草芽胞桿菌(Bacillus subtilis,BS)及大腸埃希菌(Escherichia coli,EC)具有一定的抑菌作用,但未對其作用機制進行研究。由于SA、BS及EC為常見細菌,金蓮花該味藥材抗菌譜較廣,因此,本文選取這3種細菌,研究金蓮花系列制劑對其抑菌作用機制。
本課題組前期通過綜合譜效相關性對金蓮花系列制劑的抑菌活性差異進行初步研究,結果表明,金蓮花系列制劑因其制備工藝不同,對4種制劑的藥效物質作用發揮有一定影響[6]。為探究金蓮花4種制劑的制備工藝的差異是否會對其抑菌活性造成影響,本研究以已上市的4種金蓮花制劑為研究目標,選用金黃色葡萄球菌、枯草芽胞桿菌及大腸埃希菌為實驗菌種,探索4種金蓮花制劑的抑菌活性及其作用機制,對金蓮花系列制劑進行再評價,為其4種制劑的臨床使用和質量控制提供參考。
1 材料與儀器
1.1 材料和試劑
所有產品均購自市場,金蓮花口服液(批號03211214),A廠家;金蓮花片(批號2111047),B廠家;金蓮花膠囊(批號20210902),C廠家;金蓮花顆粒(批號2111157),D廠家;SA、EC、BS菌株由成都大學附屬醫院贈送;蛋白胨購自北京奧博星生物技術有限責任公司,酵母浸出粉、氯化鈉、瓊脂粉及考馬斯亮藍G-250購自成都市科隆化學品有限公司等;自制LB液體培養基、LB固體培養基等。
按照《中國藥典》2020年版一部金蓮花制劑項下制備方法,計算金蓮花口服液、金蓮花片、金蓮花膠囊及金蓮花顆粒的原藥材生藥量分別為0.4500 g/mL,4.8387 g/g,2.8571 g/g,0.4255 g/g,取膠囊、片劑及顆粒劑樣品,用適量的純水配制成相同生藥量的藥液,紫外滅菌后使用,口服液直接使用。
1.2 試驗器材
手提式壓力蒸汽滅菌器(型號 XFS-280,浙江新豐醫療器械有限公司);紫外可見分光光度計(型號 TU-1810,北京普析通用儀器有限責任公司);空氣浴振蕩器(型號 HZQ-C,哈爾濱市東聯電子技術開發有限公司);電熱恒溫培養箱(型號 DH3006A,西安禾普生物科技有限公司);離心機(型號TG20G,天津廣豐科技公司);超凈工作臺(型號 JJ-CJ-2FD,蘇州市金凈凈化設備科技有限公司)。其他儀器包括96孔一次性細胞培養板、移液槍、比濁管等。
2 方法
2.1 菌株活化
將細菌分別接種在LB液體培養基中,在搖床中以37 ℃、120 r/min的條件下活化培養細菌12~24 h,制得菌懸液,用高溫滅菌后冷卻至室溫的無菌水將菌懸液濃度稀釋至1×106~1×107 CFU/mL,備用[6]。
2.2 抗菌活性研究
2.2.1 牛津杯法
金蓮花系列制劑功能主治相同,且4種金蓮花制劑除金蓮花口服液外均為固體制劑,為排除溶劑選擇對抗菌活性實驗造成的誤差,選用金蓮花口服液作為抗菌活性研究對象。
將配制好的固體培養基、純水、試管、培養皿、牛津杯等放入高壓滅菌鍋中滅菌1h左右取出,將固體培養基分別倒入培養皿中冷卻待凝固后使用,用移液管分別移取菌懸液(金黃色葡萄球菌、枯草芽孢桿菌、大腸埃希菌)1 mL置于固體培養基上使菌液布滿整個培養皿,接著均勻擺放6個牛津杯,并向牛津杯中分別加入150 ?L金蓮花口服液,在37 ℃條件下恒溫培養12~24 h后取出觀察。
2.2.2 最小抑菌濃度(MIC)的測定
取無菌96孔一次性細胞培養板,采用二倍稀釋法[6],在B~H號孔中預先加入100 ?L培養基溶液,在A號孔分別加入100 ?L樣品溶液(金蓮花口服液、金蓮花片、金蓮花膠囊、金蓮花顆粒),平行設立2組,A號孔再加入100 ?L樣品溶液混勻后吸取100 ?L至B號孔,依次進行倍比稀釋至F號孔,最后A~G孔均加入10 ?L,1×106~1×107 CFU/mL菌懸液,混勻,且G號孔培養液加相應菌懸液,H號孔只加入培養液作空白對照,待加入菌液接種后,將無菌96孔一次性細胞培養板置于37 ℃恒溫培養24 h,培養完成取出觀察,若A~F號孔內澄清即視為細菌生長受到了抑制,澄清小孔中所對應的最低藥物濃度為對該菌的最低抑菌濃度,同時G號孔中應有細菌生長呈現渾濁狀態,而H號孔目的是排除培養液等因素對實驗造成的影響應無細菌生長。
2.2.3 最小殺菌濃度(MBC)測定
倒入滅菌后的固體培養基制備好瓊脂平板,再將上述實驗組中各澄清小孔中的液體分別接種涂布于瓊脂平板上,經37 ℃恒溫培養12~24 h后觀察結果[7],若瓊脂平板上無菌落生長則視為細菌100%被殺滅,此最低藥物濃度值為其MBC值。
2.3 抑菌機制研究
2.3.1 抑菌曲線的繪制
調整LB液體培養基中各制劑樣液質量濃度為MIC和1/2MIC,然后分別接入500 ?L1×106~1×107 CFU/mL菌懸液,在37 ℃、120 r/min條件下連續培養15 h,每隔1 h取樣1 mL,加入無菌水稀釋10倍后測定其在600 nm波長處的吸光度,以A600值表示,以不含樣品溶液的空白培養基為對照,繪制細菌的生長曲線,每組設2個重復[7]。
2.3.2 胞外核酸相對量的測定
配制樣品溶液,使藥物質量濃度為MIC和2倍MIC,將500 ?L菌懸液分別加入樣品溶液,在37 ℃、120 r/min條件下培養8 h,以空白培養基作對照,每隔1 h定時分別取樣500 ?L,加入無菌水稀釋10倍后4000 r/min離心10 min,取其上清液于260 nm 波長處測定吸光度,以 A260值表示核酸相對量,每組設2個重復[7]。
2.3.3 胞外可溶性蛋白的測定
配制樣品溶液,使藥物質量濃度為MIC和2倍MIC,將500 ?L菌懸液分別加入樣品溶液,在37 ℃、120 r/min條件下培養8 h,以空白培養基作對照,每隔1 h定時分別取樣1 mL,加入無菌水稀釋3倍后4000 r/min離心10 min,取其上清液1 mL加入考馬斯亮藍試劑2 mL,靜置10 min,于595 nm波長處測定吸光度,以A595值表示胞外蛋白相對量,每組設2個重復[7]。
3 結果
3.1 牛津杯法
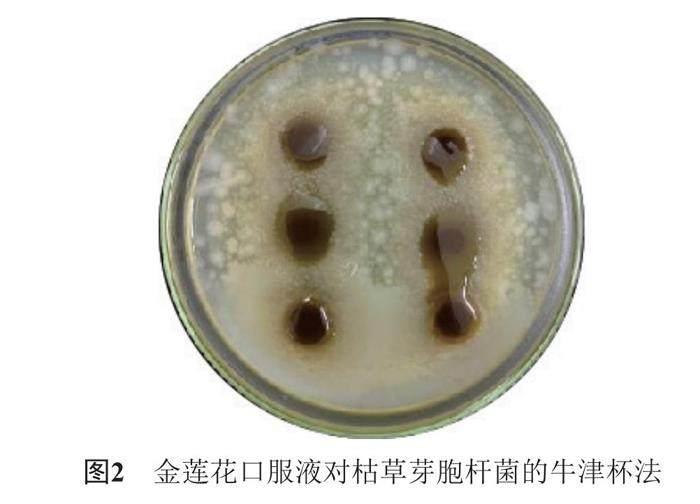
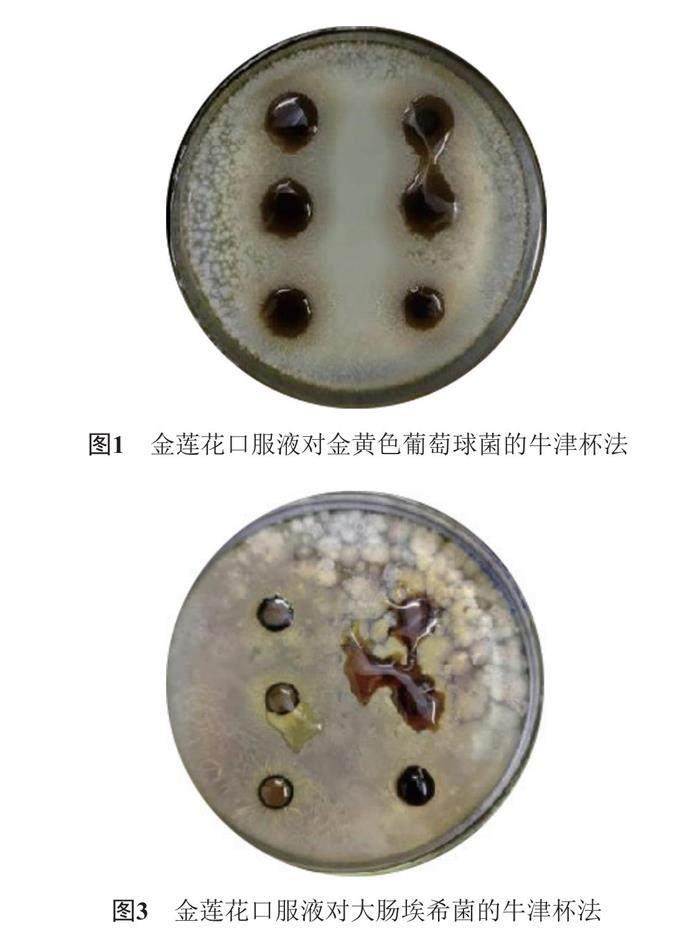
實驗發現,金蓮花口服液對金黃色葡萄球菌和枯草芽孢桿菌有明顯抑菌圈,表現出良好的抑菌效果和一定的殺菌能力,而金蓮花口服液在同一條件下對大腸埃希菌并未顯示出抑菌性,見圖1~3。已知金黃色葡萄球菌是導致人體上呼吸道感染的一種重要病原菌,而金蓮花系列制劑主要治療上呼吸道感染,同時金蓮花中有相關化學成分能有效抑制枯草芽孢桿菌的生長[8],故選取金黃色葡萄球菌和枯草芽孢桿菌對4種金蓮花制劑進行后續機制研究。
3.2 金蓮花系列制劑的MIC、MBC測定
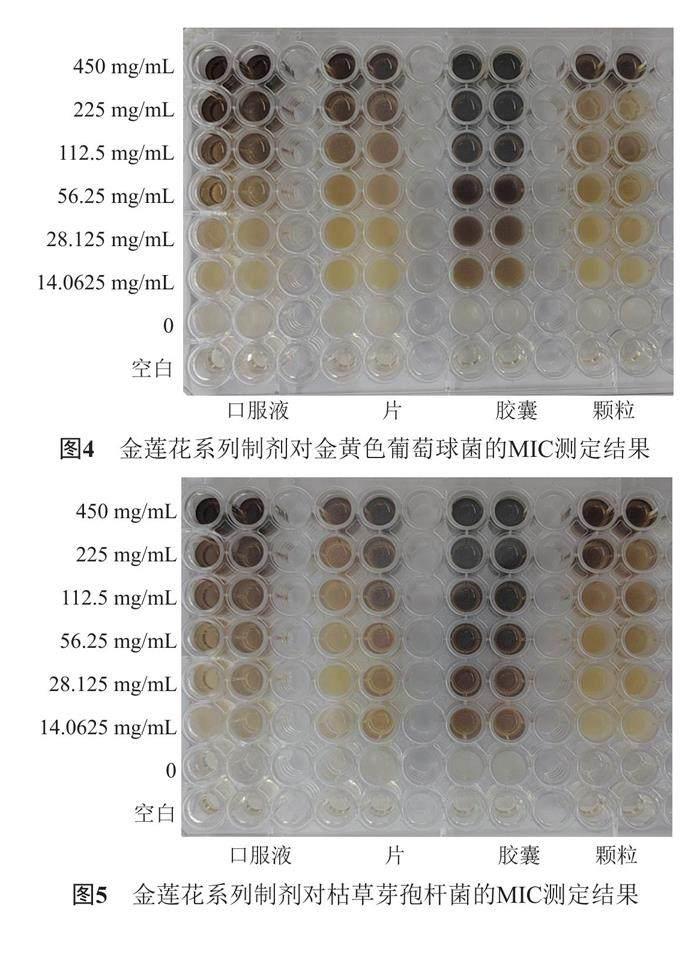
本研究采用二倍稀釋法測定了金蓮花口服液、金蓮花片、金蓮花膠囊、金蓮花顆粒對金黃色葡萄球菌和枯草芽胞桿菌的抗菌活性。圖4可見,金蓮花片濃度≥225 mg/mL,金蓮花膠囊濃度≥56.25 mg/mL,金蓮花顆粒濃度≥450 mg/mL,金蓮花口服液濃度≥ 56.25 mg/mL時的金黃色葡萄球菌溶液澄清;圖5可見,金蓮花片濃度≥56.25 mg/mL,金蓮花膠囊濃度≥14.062 5 mg/mL,金蓮花顆粒濃度≥225 mg/mL,金蓮花口服液濃度≥28.125 mg/mL時的枯草芽孢桿菌溶液澄清。
上述可得4種金蓮花系列制劑對2種試驗菌的最小抑菌濃度和最小殺菌濃度均不同(表1),說明在相同生藥量情況下,不同金蓮花制劑具有不同的抑菌效果,也就是不同制劑在服用生藥量相同的情況下,其抑菌活性有異。金蓮花系列制劑對金黃色葡萄球菌和枯草芽孢桿菌均能顯示出較強的抑菌活性,但基于金蓮花系列制劑的功效,選取導致人體上呼吸道感染的重要病原菌即金黃色葡萄球菌進行后續作用機制研究。
3.3 金蓮花系列制劑對金黃色葡萄球菌的抗菌機制
3.3.1 對細菌生長曲線的影響
4種金蓮花制劑作用后的金黃色葡萄球菌與不含樣品溶液的空白對照組相比生長顯著減緩,且隨著質量濃度的升高,對SA的抑制效果更為明顯,當培養液中各金蓮花制劑濃度為MIC時,培養液中細菌生長速率明顯減緩,表明各金蓮花制劑對SA的生長具有明顯的抑制效果,結果見圖6~9。
3.3.2 對細菌胞外核酸相對含量的影響
由圖10可知,金蓮花口服液、金蓮花片、金蓮花膠囊、金蓮花顆粒作用后,培養液中SA的胞外核酸相對含量逐漸增加,表示細菌的細胞膜遭到破壞,因為細胞膜是細菌的保護屏障之一,當藥液與細菌直接接觸作用后細菌遭到破壞,細胞膜的通透性發生改變,可能使正常狀態下在細菌細胞中的DNA、RNA等大分子物質穿過細胞膜泄漏到培養液中,導致培養液在260 nm處的吸光度值增大,即胞外核酸相對含量增大。
3.3.3 對細菌胞外可溶性蛋白的影響
由圖11可見,4種金蓮花制劑分別作用后,各試驗組培養液中的胞外可溶性蛋白含量均顯著增加,說明金蓮花系列制劑可以通過改變細胞膜的通透性使胞內的蛋白質大分子通過細胞膜泄漏到細胞外,培養液中胞外可溶性蛋白含量增加導致在595 nm處的吸光度增大,這一結果與上述4種金蓮花制劑對金黃色葡萄球菌胞外核酸相對含量的測定結果相似,進一步說明了金蓮花系列制劑可以影響細菌的細胞膜通透性,對細菌造成一定的破壞,導致細胞內的大分子物質穿過細胞膜泄漏到胞外,從而達到抑菌效果。
4 結論
本研究通過牛津杯法得到4種金蓮花制劑對3種致病菌的抑菌活性從強到弱為枯草芽孢桿菌、金黃色葡萄球菌、大腸埃希菌。通過96孔板法得出4種金蓮花制劑對金黃色葡萄球菌和枯草芽孢桿菌的最小抑菌濃度(MIC)各不相同,按由強到弱為膠囊、口服液、片、顆粒。說明在相同生藥量情況下,制備工藝的不同會對金蓮花本身抑菌的效果產生差異性影響,與本課題組前期研究結果相同[6]。
在對金蓮花系列制劑主要起作用的金黃色葡萄球菌的作用機制研究中,實驗通過細菌生長曲線得到4種金蓮花制劑作用后的SA與空白組相比生長速度均顯著減緩,說明4種金蓮花制劑對金黃色葡萄球菌均有良好的抑制作用。胞外核酸相對含量與胞外可溶性蛋白的測定結果相似,且隨著4種金蓮花制劑質量濃度的增加,細菌胞外核酸相對含量和胞外可溶性蛋白含量均逐漸增加,在抑菌作用機制研究中發現,金蓮花系列制劑作用后,細菌的細胞膜通透性被影響,導致細菌胞內維持生命體征的代謝物質外流或對細菌有害的藥液內流,進而影響細菌的生長,達到抑菌效果[7],且在金蓮花等中藥材抗菌過程中是否還存在其他抑菌作用機制,如影響細胞壁、菌體結構、蛋白和核酸的合成等,還需要進一步深入研究[9-10]。
5 討論
金蓮花系列制劑收載于《中國藥典》2020年版一部中,制備工藝參數不同,質量標準有異,但其標識的功效卻完全相同,需對其合理性進行再評價研究。目前,現有的質量再評價主要包括薄層鑒別、含量測定、指紋圖譜等方法,不能真實地表征其藥物的臨床屬性。本研究采用抑菌作用機制對四種制劑進行再評價研究,從細菌的生長曲線、胞外核酸相對含量和胞外可溶性蛋白的測定等方面評價其質量,通過抗菌活性和其抑菌作用機制的對比,可為具有抗菌活性的中成藥系列制劑的再評價提供參考。
在實驗過程經過預試驗發現輔料均不影響細菌生長的物質,因此在正式實驗中未考察輔料的影響,本研究結果表明金蓮花膠囊和金蓮花口服液的抑菌活性明顯強于金蓮花片和金蓮花顆粒,一定程度上證明不同的制備工藝會對其抑菌活性造成影響,可能導致各制劑的臨床療效不同,由于4種制劑對金黃色葡萄球菌的抑菌作用機制相同,表明其活性成分相差不大。后期實驗將通過LC-MS技術進行高通量篩選明確化學成分,確定早期干預靶點,篩選作用于藥效物質基礎[11-13];開展生物活性檢定,確定質量標志物,研究其量效關系,為下一步化學評價指標的選擇提供參考,從而進一步全面評價4種金蓮花制劑的質量[14-15]。
參 考 文 獻
林琦琪, 趙楠, 孫琦, 等. 金蓮花制劑治療上呼吸道感染臨床療效的Meta分析[J]. 中國藥物警戒, 2022, 19(8): 893-896+907.
劉然, 張晉瑋, 田野. 金蓮花口服液聯合替硝唑治療牙周炎的臨床研究[J]. 現代藥物與臨床, 2020, 35(11): 2224-2227.
李英. 金蓮花口服液治療牙周炎有效性及安全性Meta分析[J]. 山西醫藥雜志, 2021, 50(15): 2342-2344+2377.
張建麗, 胡杰, 劉翠峰. 金蓮花膠囊聯合大蒜素膠囊治療復發性口腔潰瘍的臨床研究[J]. 現代藥物與臨床, 2019, 34(4): 1120-1124.
賀澤民, 賀宇, 薛雅榮, 等. 金蓮花黃色素抗氧化與抑菌活性 的研究[J]. 中國食品添加劑, 2016, 151(09):68-72.
伍利華, 鐘林江, 楊俊莉, 等. 基于體外抑菌作用的金蓮花系列制劑譜-效關系研究[J].中國測試, 2019, 45(11): 51-56.
汪曉輝, 郭溶, 聶曉彬, 等. 佛手抗菌活性及其藥效成分橙皮苷對金黃色葡萄球菌的作用機制研究[J]. 中國抗生素雜志, ?2021, 46(05): 437-441.
賀澤民, 賀宇, 薛雅榮, 等. 金蓮花黃色素抗氧化與抑菌活性的研究[J]. 中國食品添加劑, 2016, (9): 68-72.
楊慧, 劉曉鳳, 劉錢, 等. Q-marker思路下的黃連花薹抗菌作用及機制研究[J]. 中國抗生素雜志, 2022, 47(6): 550-555.
李亞娜. 中藥抑菌的研究現狀及思考[J]. 國際檢驗醫學雜志, 2014, 35(2): 198-200.
俞鵬, 楊哲君, 石瑞潔, 等. 基于LC-MS技術的急性冠脈綜合征代謝組學研究[J]. 海南醫學院學報: 1-13.
馬焓彬, 賈利軍, 李玉婷, 等. 網絡藥理學研究中“槲皮素類現象”與對策的探討[J]. 成都大學學報(自然科學版), 2021, 40(3): 223-230.
張波, 辛杰, 劉言娟, 等. 生物檢定法在中藥質量評價中的應用研究進展[J].中國中藥雜志, 2022, 47(23):6264-6270.
譚德講, 韓璐, 段麗, 等. 生物活性檢測方法量效關系模型的確立問題探討[J]. 藥物分析雜志, 2022, 42(6): 942-950.
鐘林江, 楊俊莉, 奉梅, 等. 基于數據挖掘的金蓮花系列制劑治療上呼吸道感染的作用機制[J]. 成都大學學報(自然科學版), 2021, 40(01): 1-7+30.

