基于網絡藥理學與數據挖掘的中醫藥治療心力衰竭物質基礎及用藥規律研究
劉 仔,張 麗,鄺惠珍,李俊杰
(東莞市中醫院藥學部,廣東 東莞 523127)
一項基于5000萬人口全國城鎮職工基本醫療保險數據的調查顯示,在我國≥25歲人群中HF的年齡標準化患病率是1.10%,預估現有患病人數達1210萬,每年新發病患者300萬[1]。美國一項對來自254家醫院39982名HF患者進行的風險調整生存分析發現,射血分數下降的心衰(EF≤40%)、射血分數臨界的心衰(EF 41%to 49%)、射血分數保留的心衰HFpEF住院患者5年死亡率分別是75.3%、75.7%、75.7%[2]。降低HF患者死亡率、穩定病情、提高生存質量成為臨床關注的重點和難點。
HF現有治療藥物主要是腎素-血管緊張素系統抑制劑(ACEI/ARB/ARNI)、β受體阻滯劑、醛固酮受體拮抗劑、利尿劑等。雖然心衰治療現代理念和手段在不斷進步,但在西醫治療基礎上,針對不同心衰階段的不同證型加用中醫治療,可有效改善慢性心衰患者臨床癥狀和生活質量,維持心功能,減少再住院率[3]。
本研究以全面系統收集整理HF相關靶點為切入點,基于網絡藥理學和分子對接方法,尋找潛在中藥及活性化合物,構建疾病-靶點-化合物-中藥網絡,探討中醫藥治療HF的藥效物質基礎,以期為臨床治療HF及相關藥學研究提供參考。
1 資料與方法
1.1 心力衰竭相關作用靶點收集
登錄GeneCard、OMIM、DrugBank、DisGeNET數據平臺,以“heart failure”為關鍵詞進行檢索,獲得HF相關{Wang,2021#1}靶點,并使用UniProt匹配靶點全稱。
1.2 候選化合物篩選及靶點-化合物網絡構建
檢索TCMSP(https://old.tcmsp-e.com/tcmsp.php)[4]收集與HF靶點相關的化合物信息。根據ADME參數及Lipinski規則對候選化合物進行篩選。通過查詢文獻對刪除的化合物活性進行逐一確認,補充相關活性化合物。以上所得化合物視為候選化合物。使用Cytoscape 3.8.0構建潛在靶點-候選化合物網絡。
1.3 中藥篩選及靶點-化合物-中藥網絡構建
檢索TCMSP收集含有候選化合物的中藥,構建化合物-中藥網絡,結合靶點-化合物網絡,利用Cytoscape3.8.0構建靶點-化合物-中藥網絡并計算網絡中各節點的拓撲學參數以確定關鍵節點,初步評估中藥及相關化合物對HF的調節作用。
1.4 中藥類別及性味歸經分析
查詢2020版《中華人民共和國藥典》[5]、第3版《全國中草藥匯編》[6]、全國高等中醫藥院校規劃教材第十一版《中藥學》獲取“1.3”項下中藥類別及性味歸經信息,并進行頻數統計分析。在上述資料中無相關信息時不予統計該藥。
1.5 靶點-候選化合物分子對接
選取“靶點-化合物-中藥網絡”中度值排名前5位的核心靶點作為受體,與網絡中的核心成分進行分子對接。
查詢RSCB PDB數據庫(https://www.pdbus.org/),選取5種蛋白的晶體結構。使用AutoDock Tools 1.5.6及PyMOL 2.3對蛋白晶體、化合物進行刪除原始配體、去水、加氫等前處理,保存為.pdbqt格式文件。運用AutoDock Vina 1.1.2進行分子對接,預測蛋白質受體與化合物配體的結合模式和結合能值。
2 結果
2.1 心力衰竭相關靶點
通過GeneCard、OMIM、DrugBank、DisGeNET數據庫分別獲得HF相關靶點54、133、65、109個,將靶點去重處理并經UniProt規范,獲得HF相關靶點323個,查詢TCMSP有對應化合物的靶點有69個,經ADME及Lipinski規則篩選后所得化合物對應的靶點有35個,分別是ADRA2C、ADRB1、ADRB2、PTGS2、SCN5A、CHRM4、KCNH2、IL6、LTA4H、TNF、NR3C2、BIRC5、CXCL2、CYP1A1、CYP3A4、GJA1、HIF1A、HSF1、MAPK1、MMP2、MMP3、PPARG、TP53、XDH、CYP2C9、EDN1、ECE1、BMPR2、CD36、CES1、ACLY、NOX1、FOSL1、OLR1、SLC12A1,將它們定義為潛在靶點。
2.2 候選化合物及靶點-化合物網絡
經檢索TCMSP平臺,323個HF靶點中有69個能關聯到中藥成分,關聯化合物共計4090個。關聯化合物經過ADME參數及Lipinski規則篩選,并通過查詢文獻補充4個活性化合物,共篩選得到891個候選化合物。構建潛在靶點與候選化合物的靶點-化合物網絡,得到度值前9的化合物為槲皮素、丹參酮ⅡA、木犀草素、胡椒堿、卡維丁、異胡椒脂堿、牡丹草堿、育亨賓堿、隱丹參酮,這些化合物可作用于多個HF相關靶點而具有較強活性,可考慮對其進一步深入研究。度值排前9的靶點為PTGS2、SCN5A、ADRB2、KCNH2、NR3C2、CHRM4、ADRA2C、ADRB1、LTA4H,分別對應735、395、267、163、133、87、45、43、35個化合物,與HF發生機制相關性較高,可作為進一步研究的主要靶點。
2.3 匹配中藥及靶點-化合物-中藥網絡
891個候選化合物在TCMSP平臺關聯得到445味中藥,根據關聯關系構建化合物-中藥網絡。其中度值前11的中藥為甘草、丹參、鉤藤、黃芩、延胡索、板藍根、降香、半枝蓮、苦參、白屈菜、苦地丁,分別含候選化合物65、43、29、27、26、22、22、21、21、19、19個。通過候選化合物橋接作用統計關聯靶點數≥24的中藥有21個,分別為銀杏葉、延胡索、白果、半枝蓮、大棗、甘草、紅芪、黃柏、黃連、金盞菊花、沒藥、木蝴蝶、青蒿、沙棘、山楂葉、土茯苓、菟絲子、夏枯草、香附、洋金花、皂角刺,推測這21種中藥對HF有干預作用,可為臨床遣方用藥及試驗研究提供支撐信息。
對關聯靶點數≥24的中藥及其關聯化合物、靶點構建網絡,見圖1。圖中節點大小與度值正相關,圓形代表化合物,菱形代表靶點,六邊形代表中藥。
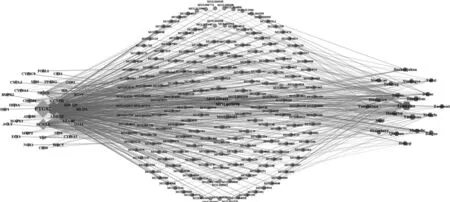
圖1 靶點-化合物-中藥網絡圖(中藥關聯靶點數≥24)
2.4 中藥類別及性味歸經
對445味中藥的類別及性味歸經進行頻數統計分析。結果顯示潛在可干預HF的中藥類別以清熱藥(17.3%)、補虛藥(11.6%)、化痰止咳平喘藥(10.6%)、解表藥(8.5%)、利水滲濕藥(7.9%)、活血化瘀藥(7.0%)、理氣藥(7.0%)為主,上述七類中藥累計占比69.9%。藥味頻率較高者為苦、辛、甘,藥性寒溫并重。歸經方面,肝經占比最高(47.0%),其次為肺經(38.0%)、胃經(30.8%),具體頻次見圖2。
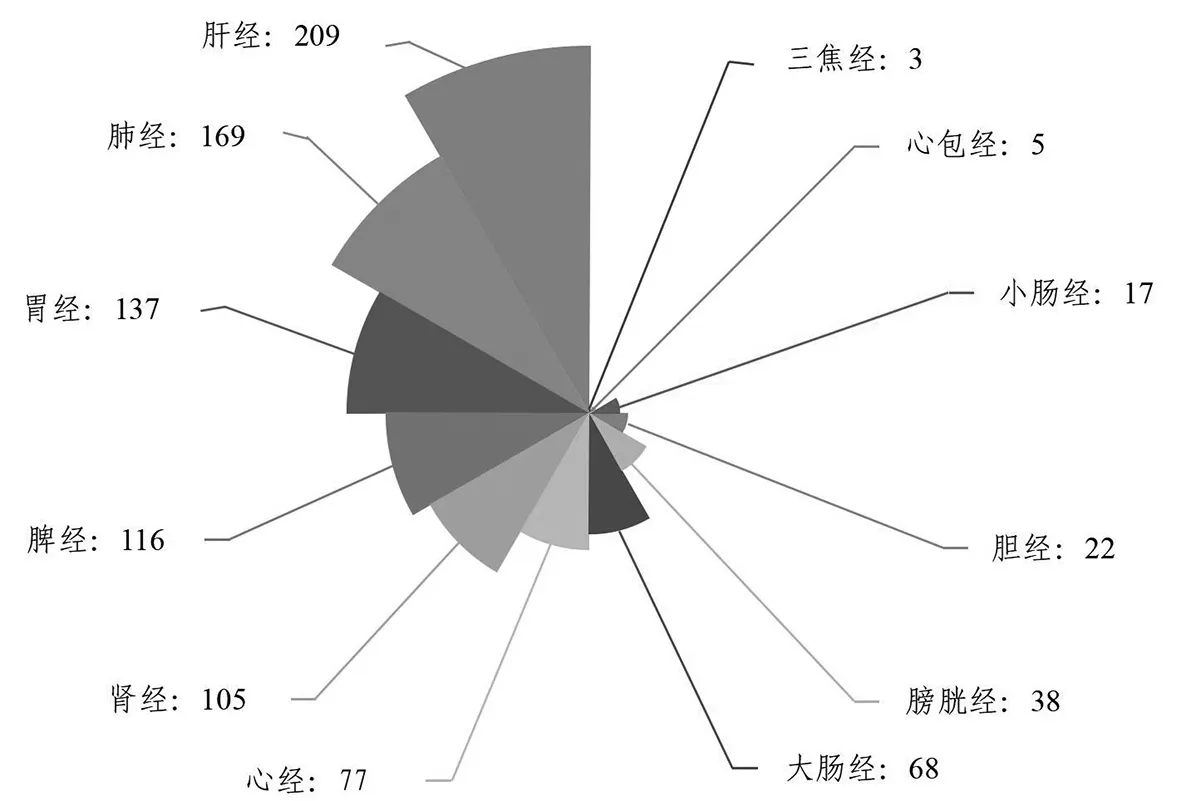
圖2 干預心力衰竭中藥歸經分布
2.5 分子對接結果
30個核心成分(Degree≥6)與5個核心靶點PTGS2(PDB ID:5IKQ)、SCN5A(PDB ID:4DCK)、ADRB2(PDB ID:6PS2)、KCNH2(PDB ID:6SYG)、NR3C2(PDB ID:3VHV)的對接得分見對接得分熱圖3。
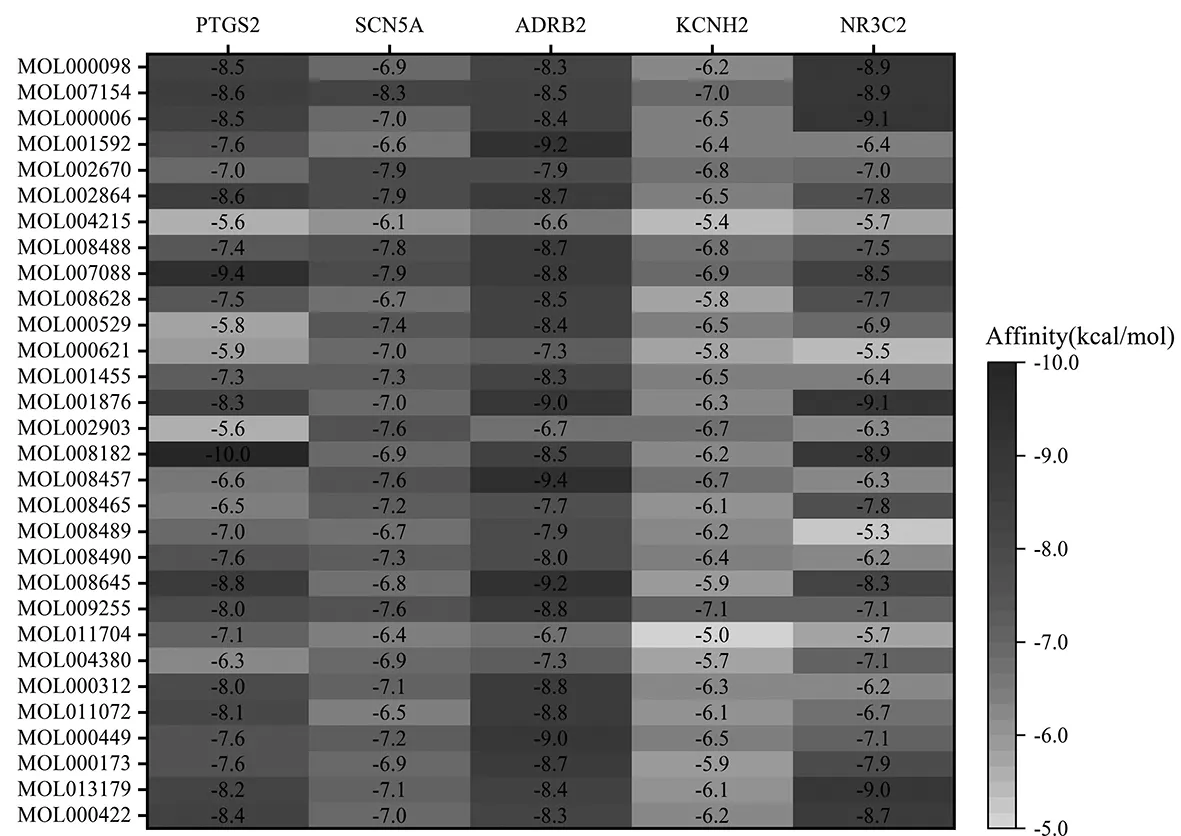
圖3 干預心力衰竭潛在核心成分與核心靶點分子對接得分熱圖
150組對接組合中,有99組為靶點-化合物網絡中的組合,其中有60組Affinity<-7.0 kcal/mol,對接得分最高的是PTGS2-alpha-berbine(-10.0 kcal/mol),得分最低的是KCNH2-leonticine(-5.4 kcal/mol),網內99個組合平均對接得分-7.5 kcal/mol,表明潛在核心成分與核心靶點之間可能有較好的對接活性。51組網外組合中,有20組Affinity<-7.0 kcal/mol,Affinity前3位的是NR3C2-luteolin(-9.1 kcal/mol)、NR3C2-6-Methoxyflavone(-9.1 kcal/mol)、NR3C2-fisetin(-9.0kcal/mol)。
綜合考慮分子對接Affinity值及成分在網絡中的度值,選擇其中4組進行可視化展示,見圖4。
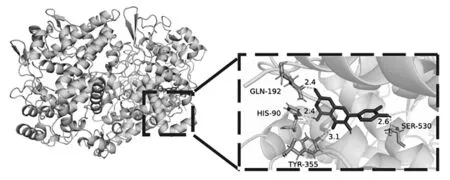
A:PTGS2與quercetin分子對接模型
3 討論
中醫用藥講究臨證化裁,加上中藥成分具有復雜性,對人體疾病的調節往往是多靶點、多通路的,網絡藥理學可系統、整體、高效的分析疾病與藥物涉及靶點的相關性,有助于揭示中醫藥治療心衰的藥效物質基礎和作用機制。
本文對HF靶點進行了較為全面的收集整理,篩選出35個潛在靶點,其中能關聯較多候選化合物的靶點有PTGS2、SCN5A、ADRB2、KCNH2、NR3C2、CHRM4、ADRA2C、ADRB1等,已有研究表明這些靶點與HF之間存在相關性。例如由PTGS2編碼的環氧合酶2(COX2)在非缺血性HF患者中具有高表達水平[7]。SCN5A編碼的電壓門控鈉離子通道(Nav1.5)是心臟中表達的主要電壓門控鈉通道,該通道通過產生快速鈉內流啟動心臟動作電位,Nav1.5功能障礙與包括HF在內的多種先天性或獲得性心臟病相關[8]。
本研究在全面收集整理HF靶點的基礎上,篩選出能作用于較多HF靶點的化合物有槲皮素、丹參酮ⅡA、木犀草素、隱丹參酮等。有研究表明,槲皮素可能通過SIRT5促進IDH2的去琥珀酸化,維持線粒體穩態,保護炎癥狀態下的小鼠心肌細胞,并改善心肌纖維化,從而降低HF的發生率[9]。丹參酮ⅡA通過抑制細胞凋亡和激活AMPK-mTOR信號通路誘導自噬保護心肌細胞并改善心臟功能,抑制氧化應激改善HF大鼠的心功能障礙和纖維化[10]。
為更深一步評估上述核心靶點及成分之間的結合活性,本研究利用計算機分子對接技術做了進一步驗證。所選取的度值排名靠前的核心靶點與核心成分的分子對接結果顯示,大多數靶點-化合物網絡內的成分和靶點之間有著強結合力,進一步驗證了本文構建的靶點-化合物網絡具有一定的預測意義,可為進一步研究中藥治療HF的有效成分提供參考。
通過構建靶點-化合物-中藥網絡,得到了能映射較多HF靶點的銀杏葉、延胡索、白果、半枝蓮等21種中藥,推測這些中藥對HF具有干預作用。
在中藥類別分析部分有意思的是,頻次靠前中藥還出現了清熱藥、解表藥,并且清熱藥占比最高,這些清熱藥、解表藥在治療HF方面是否真正具有臨床應用價值及如何讓HF患者獲益尚值得進一步研究。性味歸經方面,潛在可干預HF的中藥藥味以苦、辛、甘為多,歸經以肝、肺經為主。性味歸經頻數分析結果與中醫治療HF時使用益氣養陰或益氣溫陽固本,活血、利水、化痰治標的治療大法相一致,可為進一步解釋中醫藥治療HF的作用機制提供參考。
綜上所述,本研究基于網絡藥理學、數據挖掘及分子對接等研究方法,較為系統的探討了中醫藥治療HF可能的物質基礎及用藥規律,可為臨床治療HF及相關藥學研究提供參考。但因為本研究數據基本來源于網絡數據庫及通過軟件計算所得,后續可嘗試選取映射靶點多的中藥,通過實驗對其發揮抗HF作用的物質基礎、藥理作用、量效關系等作進一步研究。

