度拉糖肽藥品不良反應個案文獻分析*
周 楊,蔣偉豪
(1. 四川省成都市第五人民醫院,四川 成都 611130; 2. 西南醫科大學,四川 瀘州 646000)
度拉糖肽屬胰高血糖素樣肽-1受體激動劑(GLP-1RA)[1],于2019 年在我國獲批上市,常見藥品不良反應(ADR)主要為胃腸道反應[2]。目前關于其ADR 的個案報道較少,本研究中以國內外已有個案報道為基礎,旨在分析該ADR 發生、發展的特點,為臨床安全用藥提供參考。
1 資料與方法
1.1 資料來源
檢索中國知網、萬方、維普數據庫、PubMed、Web of Science。中文檢索詞為“度拉糖肽”“不良反應”“病例報道”;英文檢索詞為“dulaglutide”“adverse reaction”“case report”。檢索時限為2014年9月至2022年3月,剔除表述不清晰、重復病例的文獻,得到符合條件的文獻共11篇(涉及患者11例),均為國外文獻[3-13]。
1.2 方法
統計患者的性別、年齡、合并基礎疾病、用藥劑量、用藥情況,以及ADR 的發生時間、臨床表現、處理與轉歸等信息,并按《藥品不良反應報告和監測管理辦法》的相關要求判斷該ADR與用藥的關聯性。
2 結果
2.1 患者基本情況
患者的性別與年齡分布情況見表1;基礎疾病均有糖尿病,同時合并丙型肝炎、高血壓、焦慮癥、肥胖、慢性阻塞性肺疾病、冠狀動脈疾病、充血性心力衰竭、阻塞性睡眠呼吸暫停、高脂血癥等。度拉糖肽給藥劑量為每周0.75~1.5 mg;聯合用藥品種1~4種,主要為降糖藥、降壓藥、調脂藥和抗血小板藥。其中降糖藥為二甲雙胍、磺酰脲類降糖藥和胰島素,降壓藥為氨氯地平、比索洛爾,調脂藥為辛伐他汀和瑞舒伐他汀,抗血小板藥主要為阿司匹林。參考上述聯用藥物的藥品說明書,其與度拉糖肽未見明顯相互作用。但在使用度拉糖肽時,應考慮維持或逐步減少胰島素劑量,若減量或停藥過快,可增加糖尿病酮癥酸中毒風險。
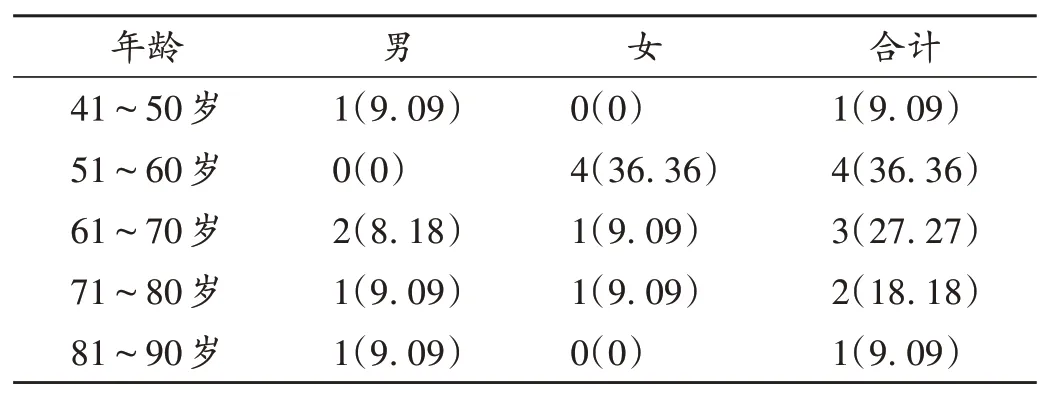
表1 患者性別與年齡分布[例(%),n=11]Tab.1 Distribution of the patients′ gender and age[case(%),n=11]
2.2 ADR 發生特點
ADR 發生時間為用藥后0(立即發生且伴隨全過程)~16 個月,以用藥后2 個月內較多(72.73%),詳見表2。ADR 累及器官/系統及臨床表現見表3。11例患者中,10 例停藥和對癥支持治療后均有好轉,1 例嚴重過敏反應患者預后不良,出現缺血性腦損傷。ADR 的表現、處理及轉歸詳見表4。

表3 ADR累及器官/系統及臨床表現(n=11)Tab.3 Organs/systems involved in ADRs and their clinical manifestations(n=11)
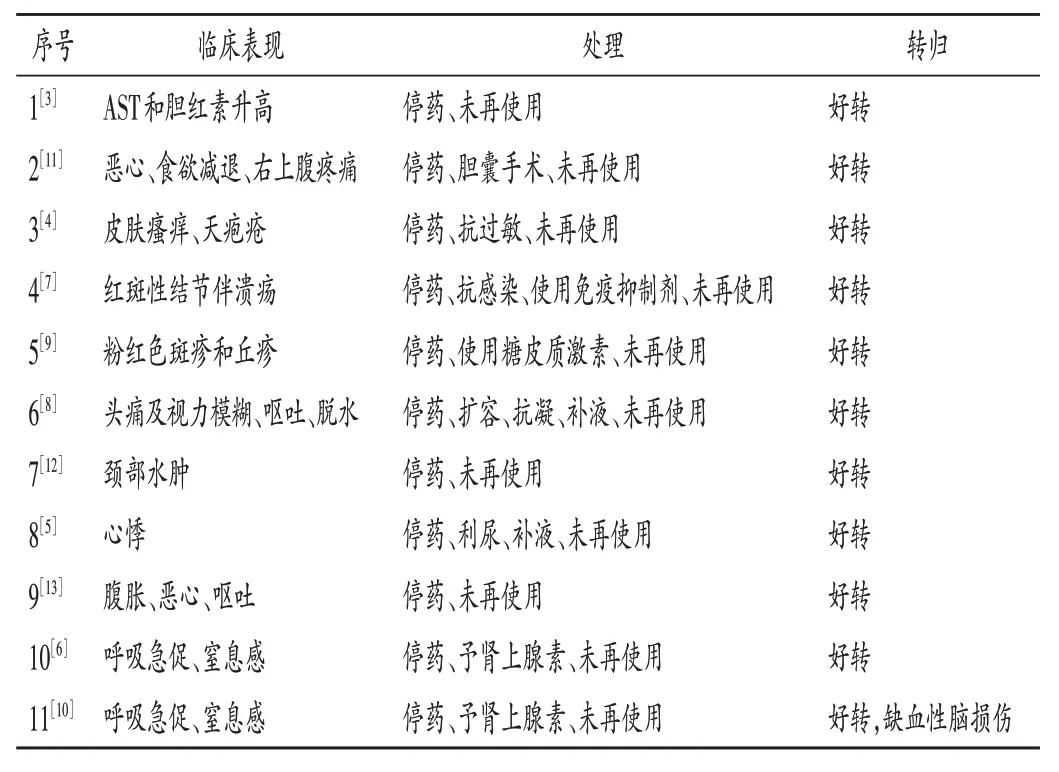
表4 ADR的臨床表現、處理及轉歸Tab.4 Clinical manifestation,treatments and outcomes of ADRs
2.3 關聯性評價
按《藥品不良反應報告和監測管理辦法》評價,11 例ADR與使用度拉糖肽的相關性均為“可能”。
3 討論
3.1 ADR 類型
度拉糖肽藥品說明書中常見ADR 為胃腸道反應,包括惡心、嘔吐和腹瀉。此外還有低血糖、急性胰腺炎、心率增快、過敏反應等。膽囊炎、房顫加重在其藥品說明書中有明確記載,考慮為一般ADR。而涉及皮膚系統的壞疽性膿皮病、麻疹樣藥疹、大皰性類天皰瘡,以及消化系統的藥物性肝損傷在其藥品說明書中未見收載,應為新的ADR,其中壞疽性膿皮病和大皰性類天皰瘡發生程度較嚴重,延長了患者的住院時間,故考慮為新的嚴重ADR。
3.2 ADR 與性別、年齡及用藥劑量、時間的關系
本研究中納入ADR 病例的性別差異不明顯,年齡以50 歲以上較多(90.91%),與2 型糖尿病的常見發病年齡相符。同時,隨著年齡的增加,老年人機體功能減退,肝腎代謝能力下降,這也是ADR增多的因素之一。
本研究中11例患者的用藥劑量為每周0.75~1.5 mg,屬常規用法用量。雖然近期有研究發現,患者大劑量(每周3.0 mg 和4.5 mg)使用度拉糖肽后的ADR 發生率與使用1.5 mg 時并無顯著差異[14],但仍建議按藥品說明書規定使用,不應隨意增加劑量。
本研究結果發現,度拉糖肽的ADR 發生時間跨度相對較大。故在開始應用度拉糖肽時就要密切監測患者情況,加強用藥監護與教育,及時處理ADR。
3.3 ADR 累及系統及臨床表現
皮膚及附件:有資料顯示,二肽基肽酶4(DPP-4)抑制劑與大皰性類天皰瘡有一定相關性[15]。且由于胰高血糖素樣肽1(GLP-1)受體在皮膚成纖維細胞和角質形成細胞中表達,GLP-1 RA 也可能會損傷皮膚[16]。因此GLP - 1 RA 與DPP - 4 抑制劑造成皮膚及附件ADR 可能有相似的機制,建議用藥前需特別詳細詢問患者的既往用藥史和過敏史。
循環系統:GLP - 1 受體在人類胰腺、腸道和心臟中均有發現[17]。動物實驗表明,自主神經系統GLP - 1受體的激活增強了交感神經系統的活性,減弱了副交感神經系統的活性。有學者認為,心肌GLP - 1 受體的過度激活可能會增加陣發性房顫患者的房顫加重風險[18]。另外,關于腦靜脈血栓的形成可能和患者惡心嘔吐所致脫水有關。度拉糖肽的循環系統ADR 雖發生率較低,但仍需重視,對于既往有心律失常的患者應慎用。
消化系統:胃腸道反應是度拉糖肽最常見的ADR類型。根據國內的一項調查,胃腸道反應在治療前2 周最顯著[19],度拉糖肽藥品說明書中也提到分別使用度拉糖肽0.75 mg 和1.5 mg(均為每周)時,累積報告104 周的胃腸道不良事件發生率,包括惡心(12.9% 和21.2%)、腹 瀉(10.7% 和13.7%)和 嘔 吐(6.9% 和11.5%),多為輕度或中度。本研究中收集到的患者用藥后出現的胃輕癱,考慮目前度拉糖肽尚未在重度胃腸道疾病患者中應用,因此用藥前需評估患者胃腸道疾病情況。另外,該藥會延緩胃排空和延長膽囊收縮的時間,可能增加膽囊相關并發癥的風險。
3.4 藥學監護建議
結合本研究收集的案例情況和臨床應用實際,建議醫務人員從小劑量開始使用度拉糖肽,使用前關注患者既往用藥史和過敏史,發現ADR 時及時處理。通常肝功能損害患者無須調整用藥劑量,但結合本研究中使用藥物后出現藥物性肝損傷的案例,使用期間仍需加強肝腎功能的監測。此外,既往有心律失常、急慢性腎功能損傷的患者應慎用該藥。若懷疑發生了胰腺炎,應逐步停用。對確診但未確定由其他原因引起的胰腺炎,不應再次使用度拉糖肽。
綜上所述,度拉糖肽作為新型降糖藥,為糖尿病的治療提供了新選擇,但其ADR 不容忽視。本研究中納入度拉糖肽引起的ADR 累及多個系統,部分ADR 在其藥品說明書中未收載,隨著該藥國內上市后的廣泛使用,可能會有更多未知ADR 的出現,醫務人員需不斷加強對度拉糖肽ADR 的認識,尤其加強對合并多種疾病患者的用藥監護。同時,關于度拉糖肽ADR 的發生機制還有待進一步研究。

