腹腔鏡直腸癌全系膜切除術后排尿功能障礙的危險因素分析
李朝劍, 芶 勇, 蔡美煌, 謝 宇
(1. 四川省彭州市中醫醫院 胃腸/胸外科, 四川 彭州, 611930;2. 四川省中西醫結合醫院 骨科, 四川 成都, 610000)
直腸癌是常見的消化系統惡性腫瘤,具有較高的發病率,患病人群主要集中在中老年人群[1]。近年來,中國直腸癌的發病情況呈逐年上升化、年輕化的趨勢,這可能是由脂肪攝入量不斷上升造成的[2]。研究[3]表明不良的飲食習慣和錯誤的飲食結構是導致直腸癌發生的重要原因。腹腔鏡手術因具有創傷小、術后疼痛輕、術后恢復快等優點而被廣泛應用于臨床治療,腹腔鏡直腸癌全系膜切除術結合了微創手術的優越性,因此被定義為直腸癌手術治療的金標準[4-5]。然而,患者術后排尿功能障礙等相關并發癥會給手術的治療效果及術后恢復造成不良影響[6]。本研究分析腹腔鏡直腸癌全系膜切除術后排尿功能障礙的危險因素,現報告如下。
1 資料與方法
1.1 一般資料
回顧性分析2018年10月—2022年10月收治的92例直腸癌患者的臨床資料,其中男49例,女43例,年齡33~71歲,平均(56.73 ±7.68)歲,平均體質量指數(BMI)為(24.74±3.35) kg/m2。采用隨機數字法將患者以3∶1的比例分為訓練集69例和驗證集23例,分別用于構建術后排尿功能障礙的預測模型和模型驗證。訓練集患者平均年齡(56.34±7.25)歲,平均BMI為(24.98±3.51) kg/m2, 根據術后膀胱殘余尿量情況又分為排尿功能障礙組22例和排尿功能正常組47例。驗證集患者平均年齡(57.12±7.81)歲,平均BMI為(24.50±3.11) kg/m2。訓練集與驗證集患者一般資料比較,差異無統計學意義(P>0.05)。納入標準: ① 符合直腸癌診斷標準者[7]; ② 采用腹腔鏡直腸癌全系膜切除術治療者; ③ 術前排尿功能正常者。排除標準: ① 中轉開腹的患者; ② 合并其他惡性腫瘤的患者; ③ 腫瘤遠端轉移并侵犯臨近臟器的患者。
1.2 方法
1.2.1 手術方法: 手術采取傳統5孔法進行,即臍上(觀察孔),左、右腹直肌外(操作孔),左側麥氏點(牽引結腸)以及右側麥氏點處(主操作孔); 建立人工氣腹,根據直腸癌全系膜切除術原則分離腸系膜,期間注意保護神經叢和輸尿管,將Denonvilliers筋膜與腫瘤病灶全部切除,切除范圍不低于腫瘤遠端直腸系膜5 cm。
1.2.2 觀察指標: 收集患者的一般資料,包括性別、年齡、BMI、病程、是否患有高血壓及糖尿病,術前是否進行放療、是否存在淋巴結轉移、直腸前壁分離,同時記錄腫瘤位置、腫瘤直徑、病理類型、病理分期、淋巴結切除數量、盆腔自主神經受損情況、手術方式、術中視野、出血量、手術時間、術后拔尿管時間以及是否發生吻合口瘺。
1.2.3 排尿功能評價: 術后2周時,依據膀胱殘余尿量評估患者排尿功能[8]。殘余尿量<50 mL為排尿功能正常,殘余尿量≥50 mL為排尿功能障礙。
1.3 統計學分析
采用SPSS 23.0統計軟件進行數據分析,計量資料以均數±標準差表示,組間比較采用t檢驗; 計數資料采用[n(%)]表示,組間比較采用χ2檢驗。采用多因素Logistic回歸模型確定患者術后排尿功能障礙的獨立風險預測因子。構建列線圖模型,采用受試者工作特征(ROC)曲線和校準曲線對列線圖預測模型進行檢驗。采用遞歸分割分析(RPA)法建立危險分層系統,并通過不同手術方式進行亞組分析。在不同手術方式內,采用Kaplan-Meier法繪制排尿功能障礙發生率曲線,并采用Log-rank檢驗對排尿功能障礙發生率曲線進行比較。檢驗水準α=0.05,P<0.05為差異有統計學意義。
2 結 果
2.1 臨床資料比較
訓練集69例患者中, 22例(31.88%)術后排尿功能障礙; 分析結果顯示,術后排尿功能障礙與性別、年齡、糖尿病、術前放療、腫瘤位置、淋巴結切除數量、盆腔自主神經受損情況、手術方式有相關性(P<0.05)。見表1。
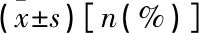
表1 訓練集中排尿功能障礙與正常患者的臨床資料的單因素分析
2.2 多因素分析
將單因素分析中有統計學意義的指標納入多因素分析,結果顯示性別、年齡、糖尿病、術前放療、腫瘤位置、淋巴結切除數量、盆腔自主神經受損情況、手術方式均是患者術后排尿功能障礙的獨立影響因素(P<0.05), 見表2。
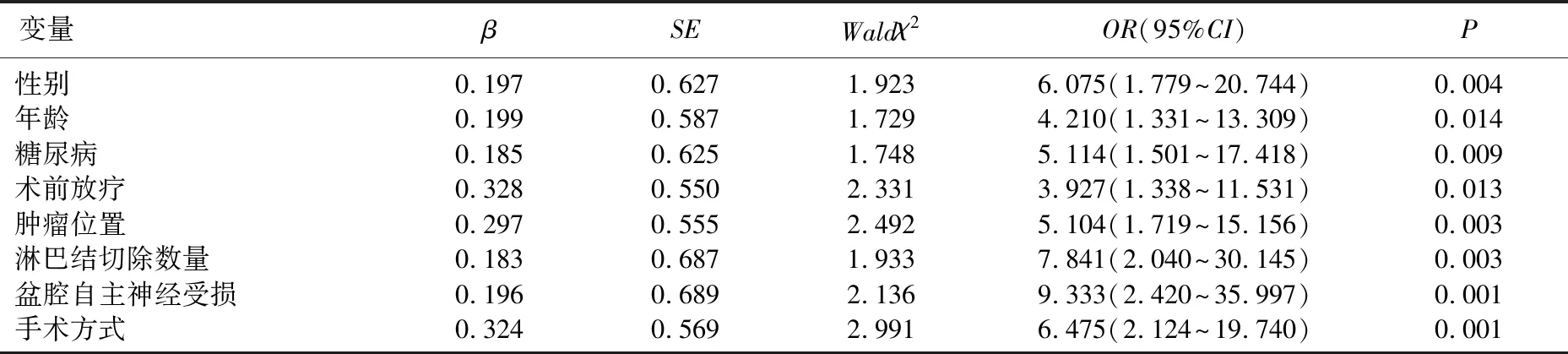
表2 多因素Logistic回歸分析
2.3 模型構建
將多因素Logistic回歸分析中有統計學意義的變量納入列線圖預測模型,通過每個變量對應得分,計算個體風險評分總分,并預測個體患者術后排尿功能障礙發生概率,見圖1。例如,某例患者為男性、年齡>55歲、未合并糖尿病、術前未接受放療、腫瘤位置為低位、淋巴結切除數量較少、盆腔自主神經受損、手術方式為Dixon術,對應的總分為18+15+0+0+52+0+79+0=164分,列線圖風險預測值約為78%。

圖1 列線圖預測模型
2.4 模型評價
2.4.1 區分度評價: 訓練集和驗證集的曲線下面積(AUC)分別為0.843(95%CI: 0.788~0.898,P<0.001)和0.801(95%CI: 0.740~0.862,P<0.001), 曲線的特異度分別為92.94%、92.56%, 敏感度分別為92.37%、91.86%, 表明本模型的區分度良好,見圖2。
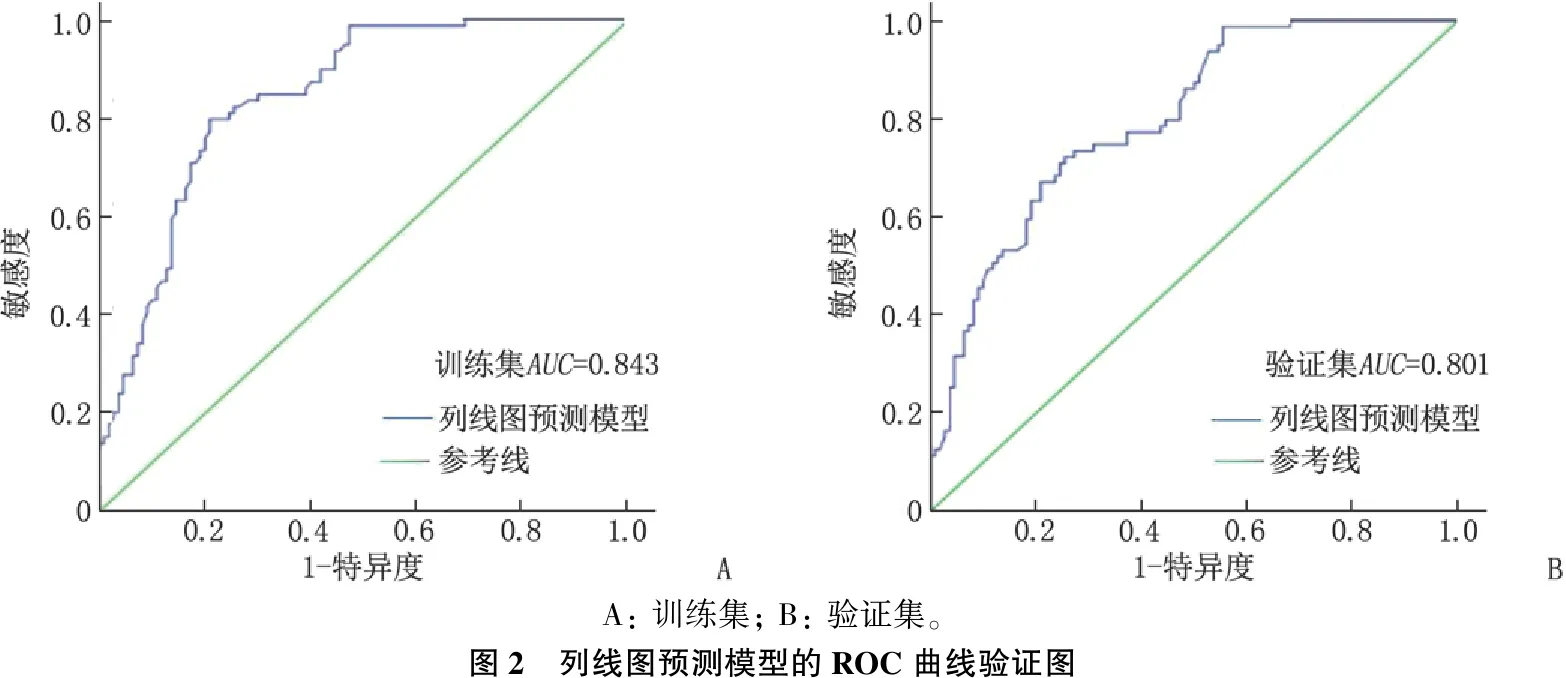
A: 訓練集; B: 驗證集。圖2 列線圖預測模型的ROC曲線驗證圖
2.4.2 校準度評價: 繪制校正曲線,結果顯示訓練集和驗證集的一致性指數(C-index)分別為0.896(95%CI: 0.841~0.944,P<0.001)和0.874(95%CI: 0.819~0.923,P<0.001), 見圖3。
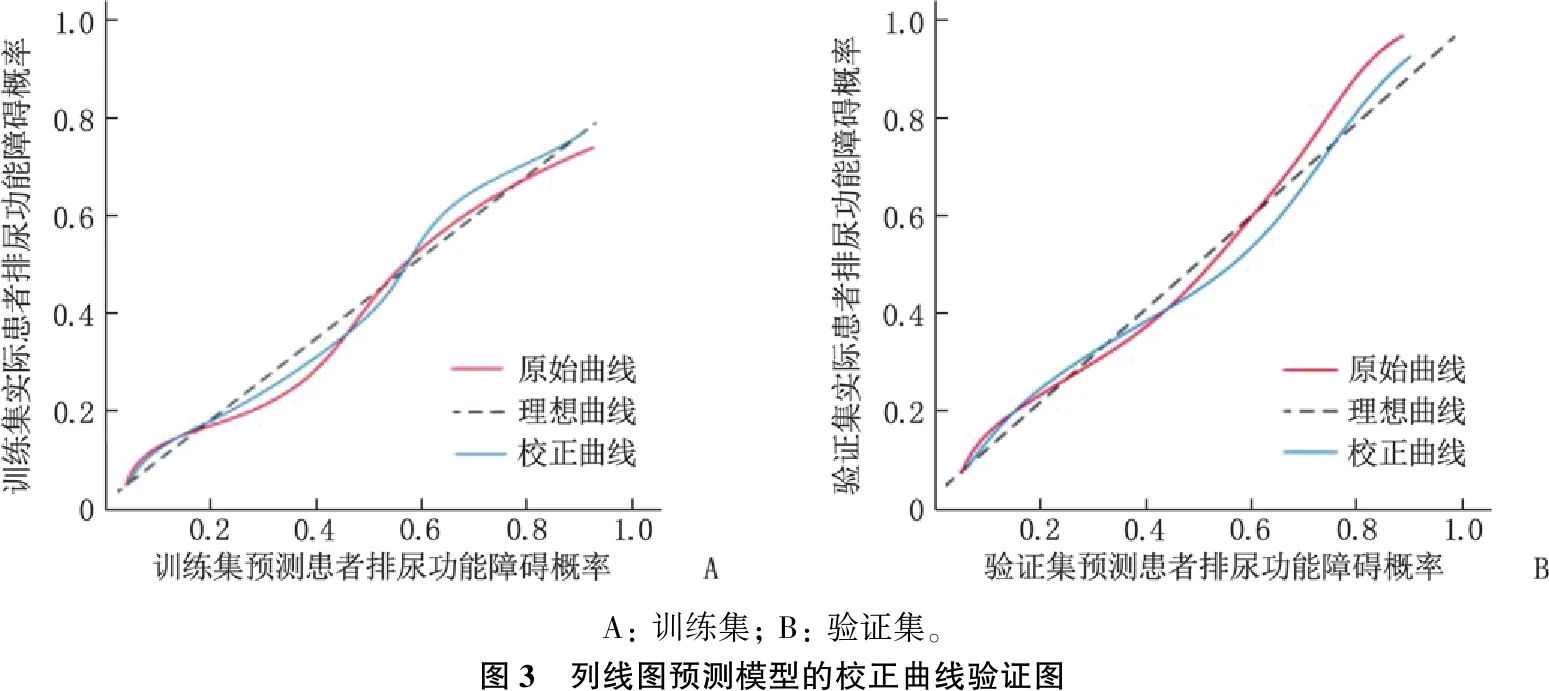
A: 訓練集; B: 驗證集。圖3 列線圖預測模型的校正曲線驗證圖
2.5 危險分層系統
采用RPA以產生樹型結構模型,樹形算法在建模隊列中展開,將所有患者分為4個危險分組: 極低風險組(總分<138分)、低風險組(總分138~<216分)、中風險組(總分216~<274分)和高風險組(總分≥274分),見圖4。在不同手術方式中驗證該危險分層系統,結果顯示在2種手術方式內,該危險分層系統均能對患者術后排尿功能障礙概率進行區分(P<0.05), 見圖5。
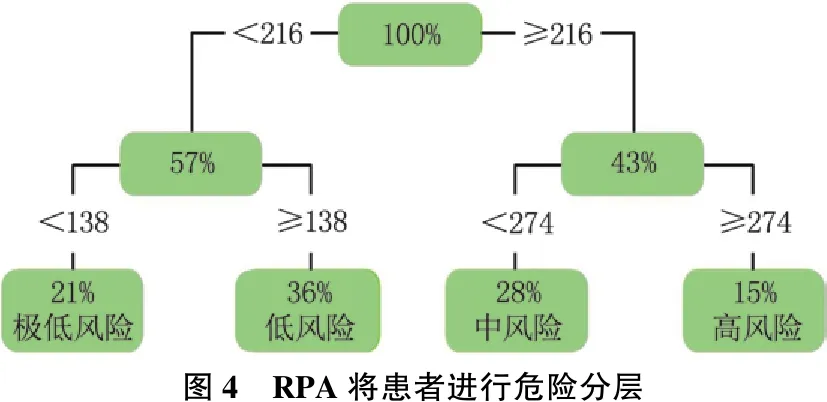
圖4 RPA將患者進行危險分層
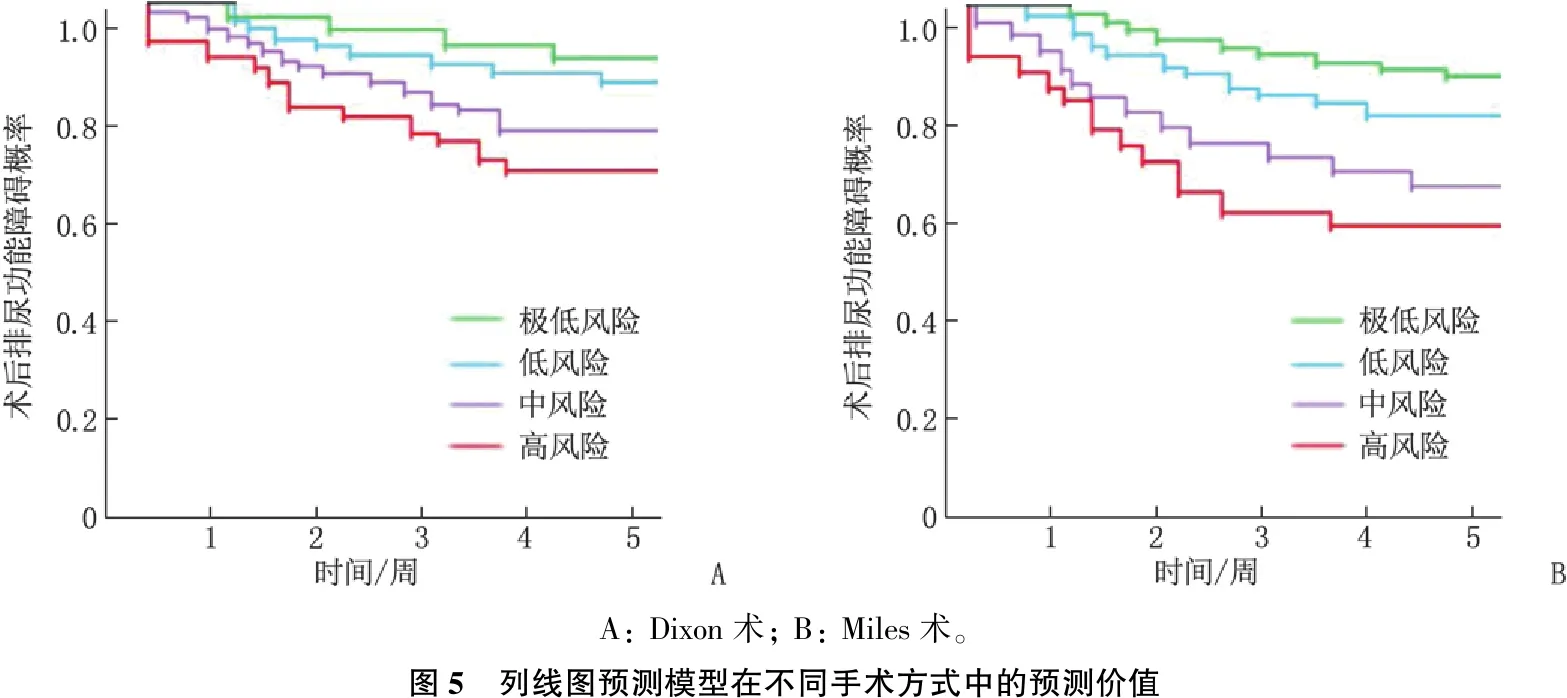
A: Dixon術; B: Miles術。圖5 列線圖預測模型在不同手術方式中的預測價值
3 討 論
直腸癌的發生發展與不健康的生活方式、不良飲食習慣、肥胖及遺傳等因素密切相關[9], 其早期臨床癥狀不明顯,當發生腫瘤感染或破裂時,會出現便血等臨床表現[10]。若不及時接受手術治療,會嚴重威脅患者的身體健康和生命安全。腹腔鏡直腸癌全系膜切除術是目前臨床上治療直腸癌的首選方案[11], 但術后極易引發排尿功能障礙等并發癥,而長期排尿功能障礙則會引起患者腎臟病變,不利于患者術后康復[12]。
本研究結果顯示,性別、年齡、是否患有糖尿病、術前是否進行放療、腫瘤位置、淋巴結切除數量、盆腔自主神經受損情況、手術方式均是影響患者術后排尿功能障礙的獨立危險因素。與女性盆腔相比,男性盆腔更狹窄,且盆叢神經更接近直腸,手術操作難度更大,術中造成盆叢神經損傷的風險更高,因而術后排尿功能障礙的發生率高于女性[13-14]。隨著患者年齡的增長,機體排尿功能發生退行性改變,從而導致術后排尿功能障礙的發生率上升,同時高齡患者免疫力減弱,術后發生并發癥的概率更高[15]。有研究[16-19]指出,合并糖尿病的直腸癌患者術后發生排尿功能障礙的風險明顯升高,其原因可能是糖尿病造成的機體高血糖狀態容易對盆腔神經組織造成損傷,降低盆腔自主神經敏感性,而盆腔自主神經受損又會造成患者排尿感知減退,是導致患者術后排尿功能障礙的主要原因。研究[20-22]表明,放療會導致膀胱、前列腺、尿道括約肌等組織纖維化,對患者排尿功能產生不良影響。術中淋巴結清掃數量多、范圍大也是導致盆腔自主神經損傷的重要原因[23]。腫瘤位置也是影響患者術后排尿功能的重要因素,腫瘤位置越低,手術切除范圍越靠近盆底,對盆叢神經造成損傷的可能性越大,同時腫瘤位置也是決定手術方式的重要因素,腫瘤位置距離肛緣較遠的患者一般可以采用Dixon術進行保肛治療,以減輕對盆腔自主神經的損傷[24-25]。與Miles術相比, Dixon術可較好地保留完整肛管、會陰,對患者排尿反射系統影響較小,盡可能減少對盆腔自主神經功能的損傷,以降低排尿功能障礙的發生率[26-28]。
本研究在單因素、多因素分析的基礎上,針對上述危險因素建立列線圖預測模型。ROC曲線以及校準曲線分析結果顯示,該預測模型的區分度和準確度均較高,可為臨床預測患者術后排尿功能障礙情況提供幫助。危險分層系統將所有患者分為4個危險分組,即極低風險組(總分<138分)、低風險組(總分138~<216分)、中風險組(總分216~<274分)和高風險組(總分≥274分)。不同手術方式對危險分層系統區分度的驗證結果顯示,該危險分層系統區分度良好,對預測患者術后排尿功能障礙有積極作用,并且對臨床上采取相應措施保護患者正常的排尿功能具有一定的指導作用。
本研究也有不足之處,例如影響直腸癌全系膜切除患者術后排尿功能障礙的因素較多,本研究納入的影響因素尚不全面,得到的結果也可能因為樣本量不足而產生偏差,還需擴大樣本量并納入更多的可能影響因素以進行更為全面的分析。
綜上所述,性別、年齡、是否患有糖尿病、術前是否進行放療、腫瘤位置、淋巴結切除數量、盆腔自主神經受損情況、手術方式是腹腔鏡直腸癌全系膜切除術后排尿功能障礙的影響因素。本研究建立的列線圖預測模型能有效預測直腸癌全系膜切除患者術后排尿功能障礙的情況,且基于該模型的危險分層系統對區分患者術后排尿功能障礙情況具有一定的臨床價值。

